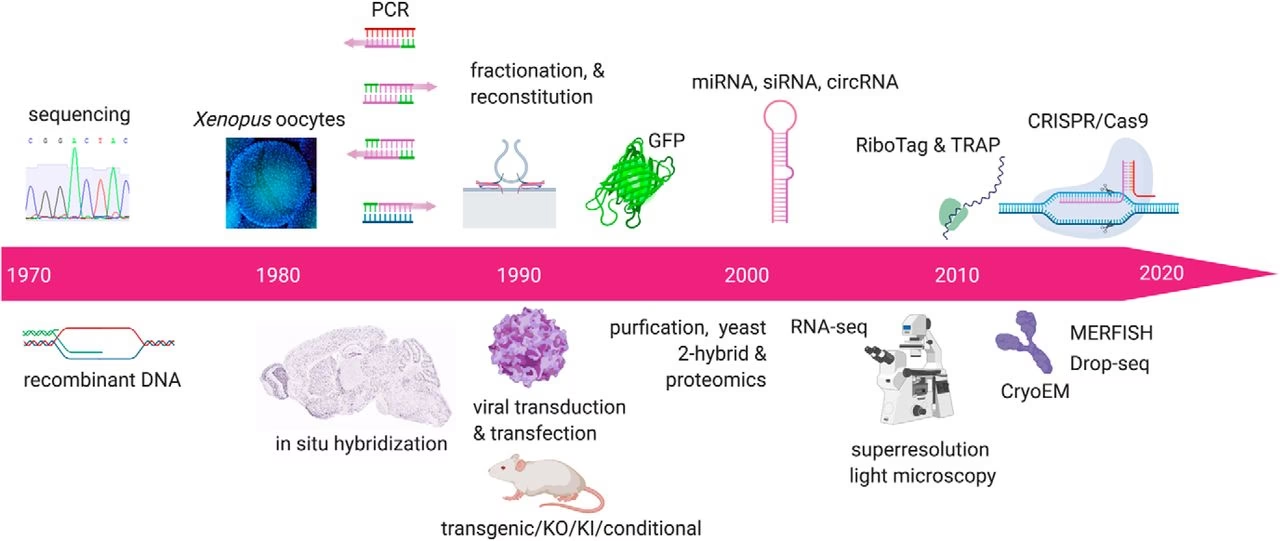
La Neurociencia Molecular es un campo apasionante que busca comprender el funcionamiento del sistema nervioso a su nivel más fundamental: el de las moléculas. Estudia los procesos moleculares que subyacen a la estructura, función y plasticidad de las neuronas y las sinapsis. Desde la síntesis y liberación de neurotransmisores hasta la compleja cascada de eventos que ocurren cuando una señal es recibida por otra neurona, cada paso está orquestado por intrincadas interacciones moleculares.
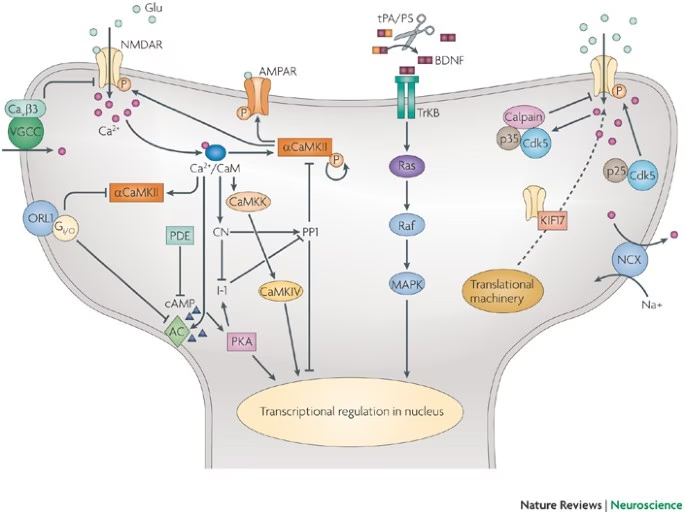
Este campo abarca una amplia gama de temas, cada uno contribuyendo a nuestra comprensión global de cómo funciona el cerebro. Analizar la localización de neurotransmisores, la función de canales iónicos y receptores, el proceso dinámico de liberación de neurotransmisores, la expresión génica en las neuronas y cómo las disfunciones moleculares pueden llevar a enfermedades neurodegenerativas, nos brinda una perspectiva detallada y profunda sobre la base de nuestros pensamientos, emociones y acciones.
Localización de Neurotransmisores
Uno de los primeros pasos para entender la comunicación neuronal es identificar dónde se encuentran los mensajeros químicos, los neurotransmisores. Estos compuestos son sintetizados en la neurona, a menudo en el soma o en la terminal axónica, y luego almacenados en vesículas. Técnicas moleculares y bioquímicas permiten a los científicos mapear la distribución de diferentes neurotransmisores dentro del cerebro, así como estudiar las enzimas responsables de su síntesis y degradación, y los transportadores que los recapturan o los empaquetan en vesículas. Comprender su localización es crucial para descifrar los circuitos neuronales específicos y sus funciones.
Canales Iónicos Dependientes de Voltaje
La excitabilidad neuronal, la capacidad de las neuronas para generar y transmitir impulsos eléctricos (potenciales de acción), depende en gran medida de los canales iónicos dependientes de voltaje. Estas proteínas transmembrana actúan como compuertas que se abren o cierran en respuesta a cambios en el potencial eléctrico a través de la membrana celular. Al controlar el flujo de iones como sodio (Na+), potasio (K+), calcio (Ca2+) y cloruro (Cl-) a través de la membrana, estos canales determinan la polaridad de la neurona y la propagación de las señales eléctricas. La diversidad de tipos de canales iónicos y sus propiedades cinéticas y de conductancia específicas son fundamentales para las distintas propiedades eléctricas de las diferentes poblaciones neuronales.
Receptores Neuronales
Una vez que un neurotransmisor es liberado en la hendidura sináptica, necesita ser detectado por la neurona postsináptica. Esta detección es mediada por los receptores neuronales, que son proteínas especializadas ubicadas principalmente en la membrana postsináptica. Los receptores se unen específicamente a un neurotransmisor particular y, al hacerlo, desencadenan una respuesta en la célula postsináptica. Existen dos clases principales de receptores: los receptores ionotrópicos, que son canales iónicos que se abren directamente al unirse el neurotransmisor, y los receptores metabotrópicos, que están acoplados a proteínas G e inician una cascada de señalización intracelular más compleja. La interacción entre neurotransmisores y receptores es altamente específica y determina si la señal transmitida será excitatoria o inhibitoria, modulando la actividad de la neurona postsináptica.
Liberación de Neurotransmisores: El Mecanismo Clave de la Sinapsis
El proceso de liberación de neurotransmisores es central para la comunicación sináptica. Ocurre en la terminal axónica de la neurona presináptica y permite que la señal eléctrica de un potencial de acción se convierta en una señal química que puede cruzar la hendidura sináptica y afectar a la neurona postsináptica. Los neurotransmisores se almacenan en pequeñas estructuras membranosas llamadas vesículas sinápticas.
Existen dos tipos principales de vesículas en la terminal axónica:
- Pequeñas Vesículas Sinápticas (SSVs): Con un diámetro de aproximadamente 40-60 nm. Se derivan de endosomas. Almacenan neurotransmisores clásicos de molécula pequeña como acetilcolina, glutamato, GABA y glicina.
- Grandes Vesículas de Núcleo Denso (LDCVs): Con un diámetro de aproximadamente 120-200 nm. Se derivan del aparato de Golgi. Almacenan neurotransmisores peptídicos y aminas biogénicas más grandes como las catecolaminas.
La liberación de neurotransmisores desde la terminal axónica hasta las dendritas de otra neurona a través de una sinapsis ocurre en paquetes discretos conocidos como cuantos, identificados al microscopio electrónico como estas vesículas sinápticas.
El proceso de liberación sigue una secuencia de pasos coordinados:
- Movilización/Reclutamiento: Las vesículas sinápticas son movilizadas desde una reserva unida al citoesqueleto hacia la zona activa de la terminal presináptica.
- Anclaje (Docking): Las vesículas se unen físicamente a la membrana presináptica en los sitios de liberación.
- Cebado (Priming): Un paso relativamente lento en el que las vesículas ancladas sufren modificaciones moleculares dependientes de ATP que las preparan para la fusión.
- Fusión y Exocitosis: La vesícula cebada se fusiona con la membrana presináptica, liberando su contenido de neurotransmisores en la hendidura sináptica. Este proceso se llama exocitosis.
- Unión a Receptores: Los neurotransmisores liberados difunden a través de la hendidura sináptica y se unen a receptores específicos en la membrana postsináptica.
- Inicio o Inhibición de Potencial de Acción: La unión del neurotransmisor al receptor postsináptico causa cambios en la permeabilidad iónica de la membrana postsináptica. Si el neurotransmisor es excitatorio (ej. glutamato), causa despolarización y facilita la generación de un potencial de acción. Si es inhibitorio (ej. GABA), causa hiperpolarización o previene la despolarización, inhibiendo la actividad neuronal.
La Dependencia del Calcio en la Liberación
Un descubrimiento crucial en la neurociencia molecular fue la dependencia de la liberación de neurotransmisores del suministro externo de iones Ca2+. Los iones de calcio entran en las terminales axónicas a través de canales de calcio dependientes de voltaje. Cuando un potencial de acción llega a la terminal, despolariza la membrana, abriendo estos canales de calcio. La entrada de Ca2+ crea gradientes locales de alta concentración de calcio cerca de los sitios de liberación vesicular. Estos iones Ca2+ actúan como una señal intracelular que desencadena la maquinaria molecular responsable de la fusión vesicular con la membrana presináptica. La movilización de nuevas vesículas desde la reserva para someterse a esta fusión también es inducida por los iones de calcio. Este mecanismo fue elegantemente demostrado en los axones gigantes del calamar.
La reducción de los niveles intracelulares de Ca2+ tiene un efecto inhibidor directo sobre la liberación de neurotransmisores, subrayando la importancia crítica de este ión en el proceso sináptico.
Después de la liberación, las membranas vesiculares son recicladas para su posterior uso, un proceso conocido como endocitosis, que asegura un suministro continuo de vesículas para la liberación.
Es importante notar que los canales de calcio pueden variar dependiendo de su ubicación. Los canales presentes en las terminales axónicas difieren de los canales de calcio típicos encontrados en el cuerpo celular de las neuronas u otras células. Incluso dentro de las terminales axónicas, pueden existir diferentes tipos de canales de calcio, como los canales de tipo P encontrados en la unión neuromuscular, lo que sugiere una especialización molecular adaptada a las necesidades funcionales de cada sinapsis.
Expresión Génica Neuronal
La identidad, función y plasticidad de cada neurona están intrínsecamente ligadas a los genes que expresa. La expresión génica neuronal es el proceso mediante el cual la información codificada en el ADN se transcribe en ARN y luego se traduce en proteínas. Este proceso está finamente regulado y es esencial para el desarrollo del sistema nervioso, la formación de circuitos neuronales y la adaptación a nuevas experiencias (plasticidad sináptica). Factores de transcripción, mecanismos epigenéticos, procesamiento de ARN y transporte de proteínas son solo algunos de los niveles de control molecular que aseguran que cada neurona produzca las moléculas necesarias en el momento y lugar adecuados. Cambios en la expresión génica pueden alterar la síntesis de neurotransmisores, la composición de canales iónicos y receptores, o la formación de sinapsis, impactando directamente la función neuronal y la conducta.
Mecanismos Moleculares de Enfermedades Neurodegenerativas
Finalmente, la neurociencia molecular juega un papel crucial en la comprensión de las enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la Esclerosis Lateral Amiotrófica (ELA). Estas enfermedades se caracterizan por la pérdida progresiva de neuronas y la disfunción de los circuitos neuronales. A nivel molecular, a menudo implican la acumulación de proteínas mal plegadas, disfunción mitocondrial, estrés oxidativo, inflamación y alteraciones en el transporte axonal. Estudiar los mecanismos moleculares subyacentes a estas patologías es fundamental para identificar posibles dianas terapéuticas y desarrollar tratamientos que puedan ralentizar o detener la progresión de estas devastadoras enfermedades. Por ejemplo, entender cómo se agrega la proteína beta-amiloide en el Alzheimer o la alfa-sinucleína en el Parkinson, o cómo mutaciones genéticas específicas afectan la función neuronal, son áreas activas de investigación en la neurociencia molecular.
Comparativa de Vesículas Sinápticas
| Característica | Pequeñas Vesículas Sinápticas (SSVs) | Grandes Vesículas de Núcleo Denso (LDCVs) |
|---|---|---|
| Diámetro aproximado | 40-60 nm | 120-200 nm |
| Origen principal | Endosomas | Aparato de Golgi |
| Contenido típico | Neurotransmisores de molécula pequeña (acetilcolina, glutamato, GABA, glicina) | Neurotransmisores peptídicos, catecolaminas |
| Velocidad de liberación | Rápida, en respuesta a potenciales de acción únicos o de baja frecuencia | Lenta, requiere trenes de potenciales de acción de alta frecuencia |
| Sitio de liberación | Zona activa (sitios de anclaje) | Fuera de la zona activa |
Preguntas Frecuentes sobre Neurociencia Molecular
¿Qué son los neurotransmisores excitatorios e inhibitorios?
Los neurotransmisores excitatorios, como el glutamato, aumentan la probabilidad de que la neurona postsináptica genere un potencial de acción al causar despolarización. Los neurotransmisores inhibitorios, como el GABA, disminuyen esta probabilidad al causar hiperpolarización o estabilizar el potencial de membrana.
¿Por qué es tan importante el calcio para la liberación de neurotransmisores?
El calcio actúa como el principal sensor de la llegada de un potencial de acción a la terminal presináptica. La entrada de iones Ca2+ desencadena la fusión de las vesículas sinápticas con la membrana presináptica, liberando los neurotransmisores en la hendidura sináptica.
¿Cómo se reciclan las vesículas sinápticas?
Después de liberar su contenido por exocitosis, la membrana de la vesícula se recupera de la membrana presináptica mediante un proceso llamado endocitosis. Esta membrana recuperada se utiliza para formar nuevas vesículas.
¿Pueden los problemas en los canales iónicos causar enfermedades?
Sí, las mutaciones o disfunciones en los canales iónicos pueden llevar a diversas canalopatías, que afectan la excitabilidad neuronal y muscular, causando desde epilepsia y migrañas hasta arritmias cardíacas.
¿La neurociencia molecular estudia solo las neuronas?
Aunque las neuronas son centrales, la neurociencia molecular también estudia otras células del sistema nervioso, como las células gliales (astrocitos, oligodendrocitos, microglia), que desempeñan roles cruciales en el soporte, la modulación sináptica y la respuesta inmune, todos con bases moleculares importantes.
En resumen, la neurociencia molecular nos proporciona las herramientas y el conocimiento para desentrañar los complejos procesos que permiten la comunicación y el funcionamiento del sistema nervioso a nivel fundamental. Desde las finas interacciones moleculares en la sinapsis hasta la influencia de nuestros genes, este campo continúa revelando los secretos del cerebro.
Si quieres conocer otros artículos parecidos a Neurociencia Molecular: Desvelando la Sinapsis puedes visitar la categoría Neurociencia.