En el vasto y complejo campo de la neurociencia, la búsqueda de comprender las enfermedades que afectan al cerebro y al sistema nervioso, así como el desarrollo de tratamientos efectivos, dependen en gran medida de herramientas fundamentales. Una de estas herramientas esenciales son los modelos animales. Estos modelos son organismos vivos, desde invertebrados simples hasta mamíferos más complejos, que se utilizan para estudiar aspectos de las enfermedades humanas debido a que comparten similitudes genéticas, fisiológicas o conductuales con los humanos.
https://www.youtube.com/watch?v=2020-11-23-youtube-modelos-animales-en-neurociencia
La modelización animal de enfermedades humanas constituye una piedra angular tanto para los estudios científicos básicos sobre los mecanismos de las enfermedades como para los estudios preclínicos de posibles terapias. El rápido progreso en la modelización animal ha permitido avances significativos en la comprensión de los mecanismos fundamentales de muchos trastornos del sistema nervioso central (SNC). Estos avances han proporcionado conocimientos básicos, nuevas perspectivas sobre las enfermedades humanas y la base para ensayos preclínicos de terapias novedosas.

- El Propósito de Desarrollar Modelos Animales en Neurociencia
- Desafíos y Críticas en la Modelización Animal
- Principios Generales de Modelización
- Ejemplos de Modelos Animales en Neurociencia
- Comparación de Algunos Modelos Animales
- Evaluación Crítica Continua
- Preguntas Frecuentes sobre Modelos Animales en Neurociencia
El Propósito de Desarrollar Modelos Animales en Neurociencia
El propósito principal de crear y utilizar modelos animales de enfermedades neurológicas es doble. Por un lado, buscan desentrañar los mecanismos subyacentes a la patología. Al recrear aspectos de la enfermedad en un sistema controlable, los investigadores pueden investigar cómo se inician y progresan los daños neuronales, identificar las células y vías moleculares involucradas y comprender las respuestas del sistema nervioso a la lesión o disfunción. Por otro lado, estos modelos son plataformas cruciales para la prueba preclínica de compuestos y enfoques terapéuticos candidatos. Antes de que una terapia pueda ser probada en humanos, debe demostrar seguridad y eficacia potencial en modelos animales relevantes.
Estos modelos idealmente deberían generar conocimientos básicos, ofrecer nuevas visiones de la enfermedad humana y facilitar los ensayos preclínicos de terapias innovadoras. Se ha logrado mucho progreso en esta dirección, contribuyendo a nuestra comprensión de procesos como la muerte celular inicial y la reparación posterior en el accidente cerebrovascular, las patologías motoras y no motoras en la enfermedad de Parkinson, y la regeneración axonal en lesiones de nervios periféricos y ópticos, entre muchos otros.
Desafíos y Críticas en la Modelización Animal
A pesar de su importancia, la modelización animal de enfermedades neurológicas no está exenta de controversias y desafíos. Las críticas a menudo provienen de fallas en la aplicación de un modelo animal a las pruebas preclínicas de moléculas terapéuticas candidatas. Por ejemplo, en el campo del accidente cerebrovascular, aproximadamente 500 terapias neuroprotectoras que tuvieron éxito en modelos de roedores posteriormente fracasaron en alguna etapa de traslación a humanos, con solo un tratamiento emergiendo como una nueva terapia aprobada.
Similarmente, en la esclerosis lateral amiotrófica (ELA), un modelo de ratón específico ha sido la plataforma para probar cientos de terapias candidatas, resultando en que solo una (riluzol) llegue a la práctica clínica con un beneficio funcional modesto. Incluso, metaanálisis de datos de tratamiento con este modelo llevaron a predicciones de éxito para una terapia que, en un ensayo clínico posterior, empeoró a los pacientes.
Es importante señalar que muchos de estos fracasos pueden estar relacionados con el diseño experimental y el análisis de datos más que con los propios modelos. Sin embargo, el uso de modelos con una relevancia mecánica incierta para la enfermedad humana también puede llevar a resultados decepcionantes en ensayos clínicos. Un ejemplo es la dependencia de modelos basados en toxinas para modelar la enfermedad de Parkinson y el fracaso de los fármacos que muestran neuroprotección en estos modelos en proporcionar beneficios a los pacientes.
Está claro que es necesario un estudio cuidadoso de la modelización animal a medida que estos modelos se incorporan al proceso traslacional del desarrollo neuroterapéutico y las pruebas preclínicas de fármacos.
Principios Generales de Modelización
Aunque las revisiones específicas pueden centrarse en áreas particulares, como la epilepsia pediátrica o las neuropatías periféricas, se discuten principios que se aplican de manera más general a un modelo animal de enfermedad del SNC. Estos principios buscan asegurar que el modelo sea lo más relevante posible para la condición humana, considerando no solo la patología progresiva sino también factores como el desarrollo cerebral temprano y las diferencias en los cronogramas de desarrollo entre especies, como roedores y humanos. La evaluación cuidadosa de las medidas de resultado y su paralelismo entre estudios en animales y humanos es fundamental.
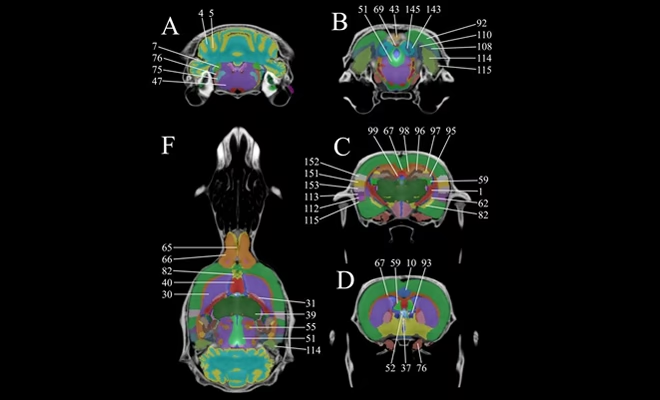
Ejemplos de Modelos Animales en Neurociencia
La diversidad de enfermedades neurológicas exige una variedad de modelos animales y estrategias de modelización. Los investigadores han desarrollado enfoques ingeniosos para abordar los desafíos monumentales de modelar trastornos humanos de manera significativa.
Modelos Genéticos en Ratones: En enfermedades monogénicas (causadas por una única mutación), los modelos de ratón transgénico a menudo parecen ofrecer una plataforma ideal para imitar molecularmente la condición causal. Por ejemplo:
- En la enfermedad de Huntington, donde se conoce la etiología genética de una expansión de repeticiones CAG en el gen huntingtina, se han creado modelos que expresan ampliamente la mutación. Estos han sido herramientas útiles para comprender la fisiopatología y probar fármacos, aunque enfoques genéticos más sofisticados también se utilizan para preguntas mecánicas sobre poblaciones celulares específicas.
- En la enfermedad de Machado-Joseph (ataxia espinocerebelosa tipo 3), las variaciones en la expansión de nucleótidos triplete y las isoformas del producto génico llevan a una presentación clínica compleja. Se han desarrollado estrategias transgénicas distintas que varían el promotor del gen, las repeticiones triplete, la isoforma y la expresión condicional para modelar fenotipos de alta, intermedia y baja severidad.
- Aunque la enfermedad de Parkinson es en gran parte no genética, raras mutaciones genéticas (como en la alfa-sinucleína) han proporcionado una ventana inesperada para su comprensión. Algunos modelos genéticos de ratón basados en la sobreexpresión de alfa-sinucleína reproducen una amplia gama de déficits similares a la enfermedad de Parkinson, ofreciendo una herramienta relevante para pruebas preclínicas en un modelo de la forma esporádica de la enfermedad.
- Incluso en trastornos monogénicos como la distonía focal, que son difíciles de modelar completamente con solo genética, se han utilizado enfoques farmacogenéticos. Un modelo válido de distonía se logró mediante la infusión de un antagonista de un sistema génico específico (inhibidor de la ATPasa de sodio/potasio, oubaina) en regiones cerebrales de un ratón genéticamente modificado, recapitulando así aspectos de la enfermedad humana con múltiples etiologías.
Modelos de Lesión Aguda en Ratones: Para eventos patológicamente complejos como la lesión cerebral traumática (LCT), que no tienen predilección genética, se utilizan modelos de lesión. La aplicación de análisis molecular serial con ratones transgénicos en modelos de LCT ha producido resultados mecánicos en estudios de muerte celular y neuroplasticidad.
Modelos para Rasgos Conductuales Complejos: En rasgos conductuales complejos como la adicción o los comportamientos afectivos, los estudios gen por gen en modelos de ratón son muy limitantes. Se emplean enfoques de genética y genómica integrativa, utilizando el mapeo genético cuidadoso de híbridos de cepas endogámicas para determinar regiones genéticas y patrones de expresión génica que subyacen a estos fenotipos conductuales complejos. Esto combina la genética de ratón recientemente comprendida con el procesamiento bioinformático para obtener información sobre las bases moleculares de los rasgos conductuales y las enfermedades psiquiátricas.
Modelos de Accidente Cerebrovascular de Sustancia Blanca en Roedores: Aunque las diferencias en la sustancia blanca entre humanos y roedores son profundas, con una orientación precisa, la sustancia blanca del ratón puede servir como locus para un modelo de accidente cerebrovascular focal que imita en muchos aspectos el accidente cerebrovascular de sustancia blanca subcortical humana. Estos modelos han demostrado que los eventos celulares desencadenados por un accidente cerebrovascular de sustancia blanca son distintos de los observados en los modelos más comunes de accidente cerebrovascular en la materia gris.
Modelos en Animales Grandes: La cuestión del tamaño y la complejidad del cerebro es recurrente. Las diferencias neuroanatómicas entre humanos y roedores, particularmente en la estructura de la sustancia blanca y la organización de los sistemas de proyección cortical, dificultan la modelización de algunas enfermedades del SNC solo en roedores. La cantidad de sustancia blanca cerebral en humanos es significativamente mayor que en el ratón. Para enfermedades centradas en la sustancia blanca o que involucran un desarrollo cerebral complejo, se requieren modelos animales más grandes:
- Modelo de Oveja Fetal Instrumentada: Para la lesión de sustancia blanca perinatal, que lleva a la parálisis cerebral, un modelo de oveja fetal instrumentada proporciona una plataforma relevante. Este modelo captura no solo una estructura de sustancia blanca subcortical compleja y grande, sino también un cronograma de desarrollo de la sustancia blanca que se asemeja mucho más a la progresión humana que la del roedor. Permite estudios de imagen, fisiopatología y ensayos terapéuticos.
- Modelos en Primates No Humanos: Estos modelos se aproximan más a los modelos de enfermedades del SNC humano. Aunque requieren recursos sustanciales, los beneficios en la modelización de la biodistribución y la imitación de la complejidad anatómica del cerebro y la médula espinal humanos pueden justificar el gasto. Se han desarrollado nuevos modelos de accidente cerebrovascular en primates, permitiendo sincronizar estudios de imagen, análisis de tejido y resultados conductuales a largo plazo.
Modelos de Lesión Medular en Primates No Humanos: El campo de la lesión medular ha visto muchos modelos en ratones y ratas. Sin embargo, varias características de la médula espinal humana no se observan en roedores, como la ubicación del tracto corticoespinal o el grado de inervación de las motoneuronas y el control muscular. La médula espinal de primate contiene extensos colaterales axonales bilaterales que contribuyen al control de la función de las extremidades, lo cual no está presente en roedores. Un modelo novedoso de lesión medular cervical y control del miembro anterior en primates no humanos proporciona una base para estudios de regeneración y recuperación funcional del control del brazo y la mano.
Modelos en Invertebrados Inferiores: Extendiendo la cuestión del tamaño del cerebro hacia abajo en el orden filogenético, incluso organismos con "cerebros pequeños" o grupos conectados de neuronas pueden ser modelos valiosos. Aunque carecen de las complejas interacciones centrales de un cerebro real, los modelos animales de enfermedades en vertebrados inferiores o invertebrados proporcionan pruebas manejables de interacciones neuronales, gliales y vasculares dentro de una red conectada y funcional. El gusano Caenorhabditis elegans ha proporcionado información crucial sobre el envejecimiento normal y patológico, la caracterización molecular rápida de sistemas de genes candidatos y resultados conductuales registrados. Se utiliza para modelar trastornos del movimiento y para la detección de fármacos de alto rendimiento, posicionando al modelo de gusano por encima del cultivo celular: un sistema in vivo para el descubrimiento de fármacos. Los estudios en C. elegans ilustran cómo los estudios rápidos de ganancia y pérdida de función en múltiples vías moleculares de un sistema de genes candidatos, realizados en serie y en paralelo, pueden determinar la interacción causal en la patología de la enfermedad.
Comparación de Algunos Modelos Animales
La elección del modelo animal depende de la pregunta de investigación, la enfermedad estudiada y los recursos disponibles. Aquí una comparación simplificada basada en la información proporcionada:
| Organismo | Complejidad Cerebral | Ventajas Típicas (en Neurociencia) | Limitaciones Típicas (en Neurociencia) | Ejemplos de Uso (según texto) |
|---|---|---|---|---|
| C. elegans (Gusano) | Red neuronal simple | Genética rápida, alto rendimiento, sistema in vivo simple, bajo costo | Falta de complejidad cerebral y anatómica de mamíferos | Trastornos del movimiento, envejecimiento, detección de fármacos |
| Ratón/Rata | Cerebro pequeño de mamífero | Modelos genéticos (transgénicos), modelos de lesión, herramientas moleculares avanzadas, costo y manejo intermedio | Diferencias significativas en tamaño cerebral, estructura (sustancia blanca, tractos), cronograma de desarrollo, plasticidad post-lesión comparado con humanos | Huntington, SCA3, Parkinson (modelos genéticos), Distonía (farmacogenética), LCT, Adicción/Comportamiento, ACV sustancia blanca |
| Oveja | Cerebro grande de mamífero | Tamaño cerebral y estructura de sustancia blanca más cercana, cronograma de desarrollo relevante | Mayor costo y complejidad de manejo, menos herramientas genéticas disponibles que en roedores | Lesión de sustancia blanca perinatal |
| Primates No Humanos | Cerebro grande y complejo, más cercano al humano anatómicamente y funcionalmente | Biodistribución, complejidad anatómica (cerebro, médula), resultados conductuales complejos a largo plazo, imagenología | Alto costo y complejidad de manejo, consideraciones éticas | Accidente cerebrovascular, Lesión medular cervical |
Evaluación Crítica Continua
Es fácil criticar los modelos individuales por su incapacidad para reproducir todas las facetas de la enfermedad humana, pero esto es de esperar. La pregunta más importante es si los modelos son útiles para comprender mejor los mecanismos que llevan a las manifestaciones de las enfermedades neurológicas, validar dianas terapéuticas y proporcionar la confianza necesaria de que un compuesto o enfoque terapéutico finalmente beneficiará a los pacientes.
La evaluación crítica de los modelos sigue siendo primordial. Cada modelo tiene sus fortalezas y debilidades, y la elección y el diseño experimental deben ser cuidadosamente considerados para que los resultados sean significativos y traslacionales. A pesar de los desafíos, el progreso se logra a diario, impulsado por la ingenuidad de los investigadores para abordar estos complejos problemas.

Preguntas Frecuentes sobre Modelos Animales en Neurociencia
Aquí respondemos algunas preguntas comunes sobre este tema:
¿Qué es un modelo animal en el contexto de la neurociencia?
Un modelo animal en neurociencia es un organismo vivo que se utiliza para imitar o estudiar aspectos de enfermedades neurológicas humanas. Estos modelos permiten investigar los mecanismos de la enfermedad y probar la eficacia y seguridad de posibles terapias en un sistema biológico complejo antes de pasar a ensayos en humanos.
¿Por qué son necesarios los modelos animales para estudiar las enfermedades cerebrales?
Las enfermedades cerebrales son extremadamente complejas y a menudo involucran interacciones entre diferentes tipos de células, circuitos neuronales y sistemas corporales. Estudiar estos procesos directamente en humanos es limitado por razones éticas y prácticas. Los modelos animales ofrecen sistemas controlables donde se pueden manipular variables, observar la progresión de la enfermedad a lo largo del tiempo y probar intervenciones de manera rigurosa. Son esenciales para desentrañar mecanismos básicos y realizar pruebas preclínicas.
¿Son los modelos animales réplicas perfectas de las enfermedades humanas?
No, rara vez lo son. Las enfermedades humanas son multifacéticas y a menudo influenciadas por una combinación compleja de factores genéticos, ambientales y de estilo de vida. Los modelos animales generalmente imitan solo ciertos aspectos de la enfermedad humana (por ejemplo, una mutación genética específica, un tipo de lesión, o un síntoma particular). Las diferencias biológicas inherentes entre especies también limitan la replicación exacta. La clave está en que el modelo sea relevante para la pregunta de investigación específica y el aspecto de la enfermedad que se estudia.
¿Qué tipos de animales se utilizan como modelos en neurociencia?
Se utiliza una amplia gama de organismos, desde invertebrados simples como el gusano C. elegans, pasando por roedores como ratones y ratas, hasta mamíferos más grandes como ovejas y primates no humanos. La elección depende de la complejidad de la enfermedad, los mecanismos a estudiar y la pregunta específica. Por ejemplo, los ratones son útiles para modelos genéticos, mientras que los primates pueden ser necesarios para estudiar la complejidad anatómica y conductual de enfermedades como el accidente cerebrovascular o la lesión medular que afectan estructuras no presentes de manera similar en roedores.
¿Cuáles son las principales limitaciones de usar modelos animales?
Las limitaciones incluyen las diferencias biológicas fundamentales entre especies que pueden afectar cómo se manifiesta una enfermedad o cómo responde a un tratamiento. La falta de traducción exitosa de terapias prometedoras de modelos animales a ensayos clínicos en humanos es una limitación importante. Además, los modelos pueden no capturar la complejidad total de una enfermedad humana, que a menudo involucra factores ambientales y sociales que son difíciles de replicar en un laboratorio. También existen desafíos en el diseño experimental y el análisis de datos que pueden llevar a resultados engañosos.
¿Se utilizan diferentes modelos animales para diferentes enfermedades neurológicas?
Sí, absolutamente. No existe un único modelo animal que sirva para todas las enfermedades neurológicas. La elección del modelo se adapta a la enfermedad específica y a los mecanismos que se desean investigar. Por ejemplo, modelos transgénicos en ratones son comunes para enfermedades genéticas como Huntington o SCA3, mientras que modelos de lesión se utilizan para estudiar el accidente cerebrovascular o la lesión cerebral traumática. Para aspectos que involucran estructuras cerebrales grandes o cronogramas de desarrollo específicos, pueden ser necesarios modelos en ovejas o primates.
En resumen, los modelos animales son herramientas indispensables en la investigación de las enfermedades neurológicas. A pesar de sus desafíos y la necesidad de una evaluación continua, han sido y siguen siendo fundamentales para desentrañar los mecanismos patológicos y avanzar en el desarrollo de nuevas terapias que, con suerte, beneficiarán a los pacientes.
Si quieres conocer otros artículos parecidos a Modelos Animales en Neurociencia puedes visitar la categoría Neurociencia.
