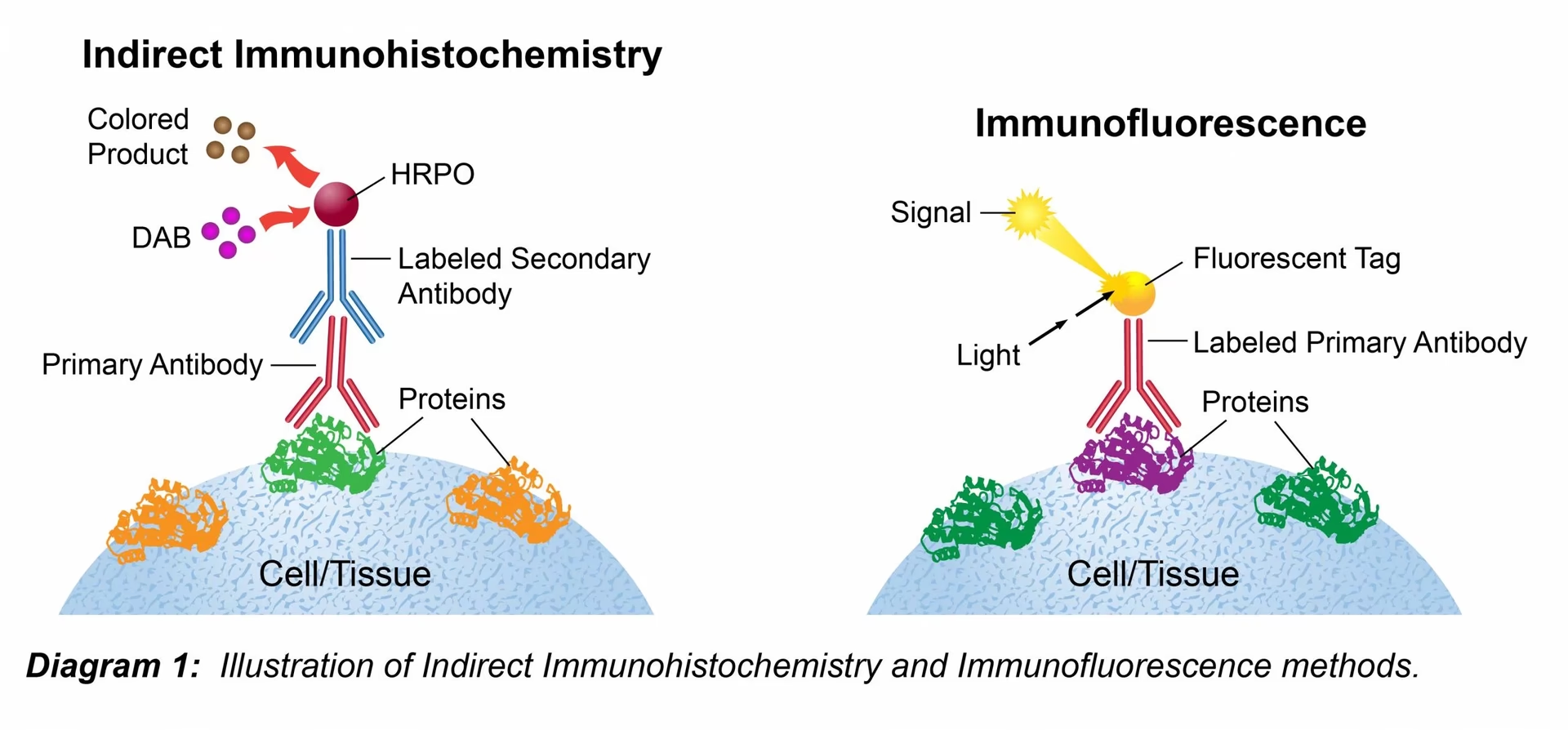
La neurociencia moderna se apoya en una variedad de técnicas sofisticadas para desentrañar los complejos mecanismos del cerebro. Entre ellas, la inmunohistoquímica (IHC) destaca como un método fundamental, a menudo considerado un estándar de oro, para visualizar la localización subcelular de proteínas específicas dentro del tejido cerebral. Esta técnica ofrece una ventana invaluable para comprender dónde y cómo operan las moléculas clave que gobiernan la función neuronal y la patología.
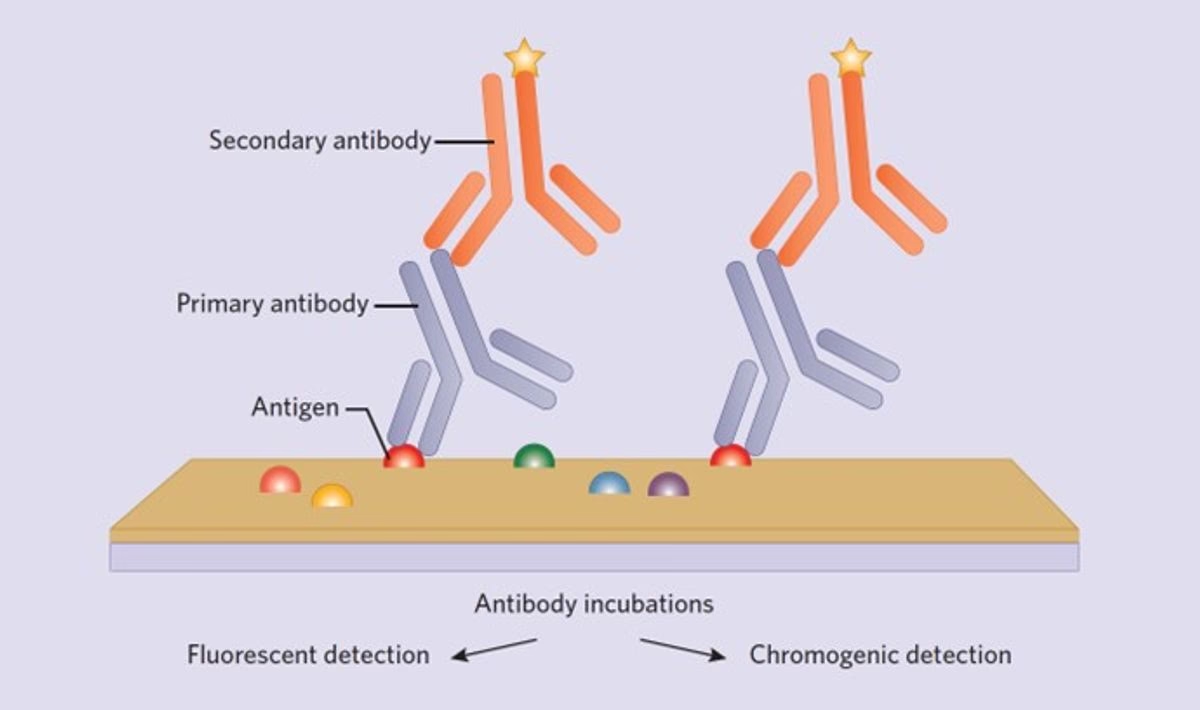
En esencia, la inmunohistoquímica se basa en un principio biológico fundamental: la interacción altamente específica entre un antígeno (la proteína de interés) y un anticuerpo. Al utilizar anticuerpos que han sido desarrollados para reconocer de forma selectiva una proteína particular, los investigadores pueden 'etiquetar' esa proteína dentro de una sección de tejido. Una vez que el anticuerpo se ha unido a su objetivo, esta interacción antígeno-anticuerpo se visualiza mediante diversas técnicas de tinción.
Históricamente, el principio detrás de la IHC existe desde la década de 1930, pero fue en 1941 cuando Coons y sus colegas realizaron el primer estudio reportado, utilizando anticuerpos marcados con isotiocianato de fluoresceína (FITC) para localizar antígenos de neumococo. Desde entonces, la técnica ha evolucionado enormemente con la introducción de diversos marcadores de visualización, como enzimas (peroxidasa, fosfatasa alcalina), elementos radiactivos y oro coloidal, además de una amplia gama de fluoróforos. El objetivo siempre ha sido lograr la detección más sensible y específica posible, minimizando el daño al tejido y la cantidad de anticuerpo necesaria.
- El Principio Fundamental: Antígeno y Anticuerpo
- Aplicaciones Específicas en Neurociencia
- Inmunofluorescencia: Una Variante Clave de la IHC
- Limitaciones de la Inmunohistoquímica en Neurociencia
- Alternativas y Enfoques Complementarios
- Preguntas Frecuentes sobre Inmunohistoquímica en Neurociencia
- Conclusión
El Principio Fundamental: Antígeno y Anticuerpo
El corazón de la inmunohistoquímica reside en la especificidad de la interacción antígeno-anticuerpo. Un antígeno es típicamente una molécula (en este caso, una proteína de interés) que puede ser reconocida por el sistema inmune. Un anticuerpo es una proteína producida por el sistema inmune que se une de manera muy selectiva a una región específica del antígeno, llamada epítopo.
El proceso general implica la preparación del tejido (generalmente fijación y corte en secciones finas), la incubación de estas secciones con un anticuerpo primario que se une a la proteína de interés, y luego la visualización de dónde se ha unido este anticuerpo. La visualización se logra uniendo un marcador detectable (como un fluoróforo o una enzima que produce un precipitado coloreado) directamente al anticuerpo primario (método directo) o, más comúnmente, utilizando un anticuerpo secundario marcado que se une al anticuerpo primario (método indirecto). El método indirecto a menudo proporciona una amplificación de la señal, ya que múltiples anticuerpos secundarios pueden unirse a un solo anticuerpo primario.
Aplicaciones Específicas en Neurociencia
La inmunohistoquímica es una herramienta indispensable en la investigación del sistema nervioso. Permite a los científicos determinar no solo si una proteína está presente en una región cerebral particular, sino también en qué tipos de células se encuentra (neuronas, glía) y en qué compartimentos subcelulares (núcleo, citoplasma, dendritas, axones, sinapsis).
Sus aplicaciones en neurociencia son variadas y profundas:
- Mapeo de la Localización de Proteínas: Es quizás la aplicación más fundamental. Permite visualizar la distribución de canales iónicos, receptores, enzimas, proteínas estructurales y otras moléculas clave en diferentes áreas cerebrales, lo cual es crucial para entender su función.
- Estudio de Enfermedades Neurodegenerativas: La IHC juega un papel vital en la investigación de trastornos como el Alzheimer, Parkinson, Huntington y otras. Permite detectar y localizar acumulaciones anormales de proteínas, como la beta amiloide, alfa sinucleína, tau fosforilada, ubiquitina o huntingtina, que son características distintivas de estas patologías. Cuantificar estas proteínas anormales en tejidos humanos post-mortem o en modelos animales es central para comprender la progresión de la enfermedad.
- Análisis del Desarrollo Neuronal: Durante el desarrollo del cerebro, las proteínas se expresan y localizan de manera dinámica. La IHC permite rastrear estos cambios, revelando patrones de migración neuronal, diferenciación celular y formación de circuitos.
- Investigación del Trauma Cerebral: La detección inmunohistoquímica de proteínas como la proteína precursora amiloide beta (APP) se ha validado como un método sensible para detectar la lesión axonal incluso horas después de un traumatismo craneoencefálico, lo cual es útil en contextos de investigación y médico-legales.
- Estudio de Trastornos Neuromusculares: Aunque técnicamente no es solo neurociencia, la IHC en biopsias musculares es crucial para diagnosticar distrofias musculares y otras miopatías, identificando anormalidades en proteínas musculares (distrofina, sarcoglicanos, etc.) que a menudo tienen implicaciones neurológicas o genéticas importantes.
- Detección de Agentes Infecciosos: En ciertos casos de neuroinfecciones, la IHC puede usarse para detectar directamente antígenos virales o bacterianos en el tejido cerebral o meníngeo.
- Validación de Modelos Animales: En la investigación preclínica, la IHC es esencial para validar modelos animales de enfermedades neurológicas, confirmando que expresan las características moleculares y patológicas de la enfermedad humana.
Además de estas aplicaciones específicas en neurociencia, la IHC es ampliamente utilizada en patología diagnóstica, especialmente en oncología (identificación de tipos tumorales, marcadores pronósticos), hematopatología y para detectar infecciones en diversos tejidos.
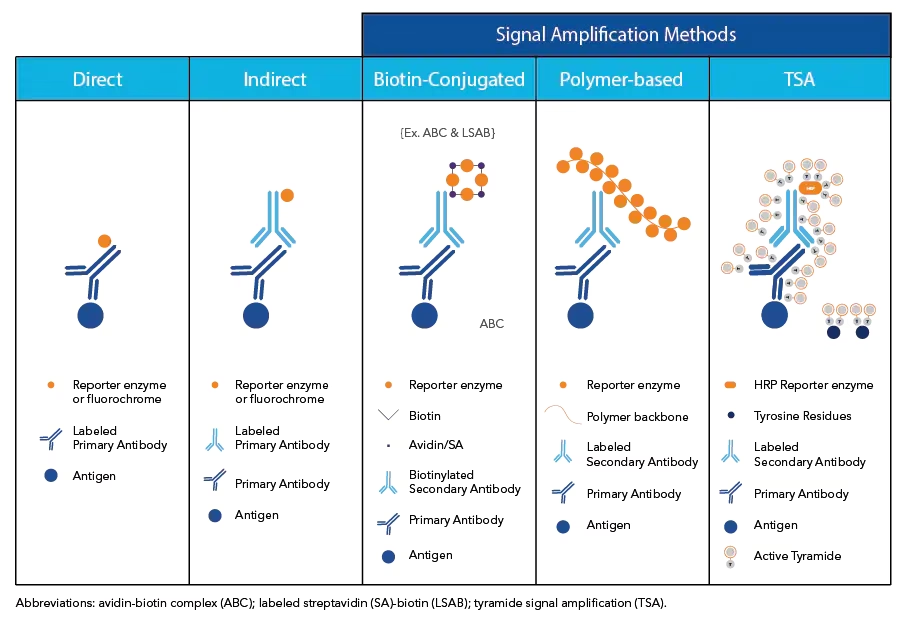
Inmunofluorescencia: Una Variante Clave de la IHC
La inmunofluorescencia (IF) es una aplicación particularmente importante de la inmunohistoquímica, especialmente en investigación. En lugar de utilizar enzimas que producen un precipitado coloreado visible con luz blanca, la IF emplea fluoróforos, que son moléculas que emiten luz de una longitud de onda específica cuando son excitadas por luz de otra longitud de onda (generalmente ultravioleta o visible). La visualización se realiza con microscopios de fluorescencia o confocales, que permiten obtener imágenes de alto contraste de estructuras fluorescentes sobre un fondo oscuro.
La IF se realiza típicamente en secciones de tejido congelado, aunque también es posible en tejido incluido en parafina con ciertas preparaciones. Permite la detección de antígenos con gran sensibilidad y, a menudo, se combina con otros marcadores fluorescentes (como el DAPI para teñir núcleos) para visualizar múltiples estructuras o proteínas simultáneamente en diferentes colores (IF multicolor).
Existen dos enfoques principales en inmunofluorescencia:
| Característica | Inmunofluorescencia Directa | Inmunofluorescencia Indirecta |
|---|---|---|
| Anticuerpos utilizados | Un solo anticuerpo primario marcado con fluoróforo | Anticuerpo primario sin marcar + Anticuerpo secundario marcado con fluoróforo (que se une al primario) |
| Número de pasos de tinción | Menos pasos | Más pasos |
| Complejidad del protocolo | Menor | Mayor |
| Sensibilidad | Menor | Mayor (debido a la amplificación de la señal) |
| Amplificación de señal | No | Sí (múltiples secundarios se unen a un primario) |
| Fondo inespecífico | Generalmente menor (menos anticuerpos) | Potencialmente mayor (más pasos, posible reactividad del secundario) |
| Flexibilidad | Menor (cada primario necesita conjugación directa) | Mayor (un secundario marcado puede usarse con múltiples primarios de la misma especie) |
La IF indirecta es más sensible debido a la amplificación de la señal, lo que la hace ideal para detectar antígenos poco abundantes. La IF directa es más rápida y tiene menos potencial de fondo inespecífico relacionado con el anticuerpo secundario, pero requiere que cada anticuerpo primario sea conjugado directamente al fluoróforo.
Limitaciones de la Inmunohistoquímica en Neurociencia
A pesar de ser una técnica poderosa y ampliamente utilizada, la IHC presenta ciertas limitaciones, particularmente en el contexto de la investigación neurocientífica:
- Disponibilidad y Especificidad de Anticuerpos: Obtener anticuerpos de alta calidad y especificidad contra una proteína de interés puede ser difícil. La reactividad cruzada de un anticuerpo con otras proteínas puede llevar a una tinción inespecífica y resultados engañosos.
- Acceso Estérico al Antígeno: En estructuras densas y complejas del cerebro, como la densidad postsináptica (PSD), el acceso físico de los anticuerpos al epítopo del antígeno puede estar limitado. Esto puede impedir la detección eficiente de algunas proteínas, incluso si están presentes.
- Dificultad para la Imagen de Célula Única de Alto Contraste: Dado que los anticuerpos tiñen todas las células donde se encuentra el antígeno, obtener imágenes de alto contraste de proteínas en células individuales, lo cual es crucial para mapear con precisión la localización subcelular en neuronas individuales, puede ser desafiante con la IHC convencional.
- Incompatibilidad con la Imagen en Vivo: El proceso de inmunohistoquímica requiere que el tejido esté fijado, lo que mata las células. Por lo tanto, la IHC no es compatible con la obtención de imágenes en células o tejidos vivos, lo que impide el estudio de la dinámica proteica en tiempo real.
Alternativas y Enfoques Complementarios
Para superar algunas de estas limitaciones, especialmente la imposibilidad de la imagen en vivo y los problemas de especificidad/accesibilidad de los anticuerpos, se han desarrollado enfoques alternativos o complementarios:
- Sobreexpresión de Proteínas Marcadas con Proteínas Fluorescentes: Introducir genéticamente una proteína de interés fusionada a una proteína fluorescente (como GFP o mCherry) permite visualizar la proteína fusionada directamente por su fluorescencia. Esta técnica es compatible con la imagen en vivo, permitiendo estudiar el tráfico, recambio e interacción de proteínas en tiempo real en células vivas. Sin embargo, la sobreexpresión puede llevar a niveles de expresión no fisiológicos, lo que a veces causa localización anormal o efectos secundarios en la función celular.
- Ratones Knock-in con Etiquetas (Tag-knockin mice): Estos ratones modificados genéticamente expresan la proteína de interés endógena fusionada a una pequeña etiqueta de epítopo o una proteína fluorescente. Esto permite visualizar la proteína en sus niveles de expresión fisiológicos, mitigando los problemas de sobreexpresión. Se pueden generar ratones knock-in globales o condicionales (donde la etiqueta se expresa solo en tipos celulares específicos o en momentos determinados, como con el sistema Cre- recombinasa ENABLED). Aunque ofrecen condiciones más fisiológicas y permiten la imagen de proteínas endógenas, generar estas líneas de ratones es costoso y requiere mucho tiempo. Además, algunas estrategias de knock-in tienen limitaciones técnicas, como ENABLED, que no es adecuada para etiquetar el extremo N-terminal de las proteínas.
Si bien estas técnicas complementarias abordan ciertas limitaciones de la IHC, cada una tiene sus propios inconvenientes. La inmunohistoquímica sigue siendo una técnica esencial y a menudo el primer paso para validar la presencia y localización de una proteína en tejido cerebral fijado debido a su robustez y la capacidad de trabajar con secciones de tejido preservado.
Preguntas Frecuentes sobre Inmunohistoquímica en Neurociencia
¿Qué es la inmunohistoquímica (IHC) en neurociencia?
Es una técnica de laboratorio utilizada para visualizar la localización de proteínas específicas dentro de secciones de tejido cerebral, basándose en la unión de anticuerpos a estas proteínas y su posterior detección.
¿Cómo funciona la IHC?
Funciona incubando secciones de tejido con anticuerpos que se unen de forma específica a la proteína de interés (el antígeno). La ubicación donde se unen los anticuerpos se visualiza utilizando marcadores detectables, como fluoróforos o enzimas que producen un color.

¿Para qué se utiliza la IHC en la investigación del cerebro?
Se utiliza para mapear la distribución de proteínas en diferentes regiones cerebrales y tipos celulares, estudiar cambios en la expresión o localización de proteínas en enfermedades neurológicas (como las neurodegenerativas) y validar hallazgos en modelos animales.
¿Cuáles son las principales limitaciones de la IHC en neurociencia?
Las limitaciones incluyen la dificultad de obtener anticuerpos específicos, el acceso restringido de los anticuerpos a los antígenos en estructuras cerebrales densas, la dificultad para obtener imágenes de alto contraste de proteínas en células individuales y, crucialmente, que no es compatible con la obtención de imágenes en tejido vivo.
¿Se puede utilizar la IHC para ver proteínas en células cerebrales vivas?
No, la inmunohistoquímica requiere que el tejido esté fijado (preservado), lo que significa que las células están muertas. Para ver proteínas en células vivas, se utilizan técnicas como la sobreexpresión de proteínas fusionadas a proteínas fluorescentes o los ratones knock-in.
¿Cuál es la diferencia entre inmunohistoquímica e inmunofluorescencia?
La inmunofluorescencia es un tipo de inmunohistoquímica que utiliza fluoróforos como marcadores detectables y microscopios de fluorescencia o confocales para la visualización, en contraste con la IHC cromogénica que utiliza enzimas que producen un precipitado coloreado visible con microscopios de luz blanca.
Conclusión
La inmunohistoquímica sigue siendo una técnica pilar en la investigación neurocientífica. Su capacidad para visualizar con precisión la localización de proteínas en el tejido cerebral fijado proporciona información esencial para comprender la función normal del sistema nervioso y los mecanismos subyacentes de las enfermedades neurodegenerativas y otras patologías. Aunque presenta limitaciones, especialmente en lo que respecta a la imagen en vivo y el acceso en estructuras complejas, a menudo se complementa con otras técnicas genéticas y de imagen para obtener una imagen más completa. La evolución continua de los anticuerpos y las tecnologías de visualización asegura que la IHC seguirá siendo una herramienta indispensable para los neurocientíficos que buscan desentrañar los misterios del cerebro.
Si quieres conocer otros artículos parecidos a Inmunohistoquímica en Neurociencia puedes visitar la categoría Neurociencia.