El cerebro, esa compleja red de miles de millones de neuronas, se comunica a través de señales eléctricas. Comprender cómo se generan y propagan estos impulsos nerviosos ha sido uno de los mayores desafíos de la neurociencia. A mediados del siglo XX, un trabajo pionero arrojó luz sobre este enigma, sentando las bases de nuestra comprensión moderna de la electrofisiología neuronal.
Sir Andrew Fielding Huxley, un distinguido fisiólogo inglés, fue una figura central en este avance. En 1963, compartió el Premio Nobel de Fisiología o Medicina con otros dos notables fisiólogos, John Eccles y Allan Hodgkin. El premio reconoció sus descubrimientos fundamentales sobre los mecanismos iónicos que subyacen a la excitación y la inhibición en las porciones periféricas y centrales del sistema nervioso. Su trabajo se centró en desentrañar cómo el movimiento de partículas cargadas, los iones, a través de la membrana celular genera las rápidas fluctuaciones de voltaje que constituyen la señal nerviosa.
El Nacimiento de una Teoría: El Modelo Hodgkin-Huxley
El corazón de la contribución de Andrew Huxley, junto con Allan Hodgkin, es el modelo que lleva sus nombres: el Modelo Hodgkin-Huxley. Este modelo es una descripción matemática de cómo el potencial de acción, la señal eléctrica fundamental de las neuronas, se inicia y se propaga a lo largo del axón. Sus experimentos cruciales se llevaron a cabo en el axón gigante del calamar, una preparación ideal debido a su tamaño, que permitía la inserción de electrodos y la manipulación experimental.
A través de cuidadosas mediciones, Hodgkin y Huxley identificaron tres tipos principales de corrientes iónicas que cruzan la membrana del axón:
- Corriente de Sodio (Na+): Responsable de la fase de despolarización rápida del potencial de acción.
- Corriente de Potasio (K+): Responsable de la fase de repolarización que devuelve el potencial de membrana a su estado de reposo.
- Corriente de Fuga (Leak): Una corriente más general, compuesta principalmente por iones Cl-, que contribuye al potencial de reposo y a la estabilidad de la membrana.
La clave de su modelo fue reconocer que el flujo de estos iones no es constante, sino que está controlado por canales iónicos específicos incrustados en la membrana celular. Lo más importante es que la conductancia (la facilidad con la que los iones pueden pasar) de los canales de sodio y potasio depende del voltaje a través de la membrana. Es decir, la propia señal eléctrica (el voltaje) controla la apertura y el cierre de los canales que generan esa señal.
La Analogía Eléctrica
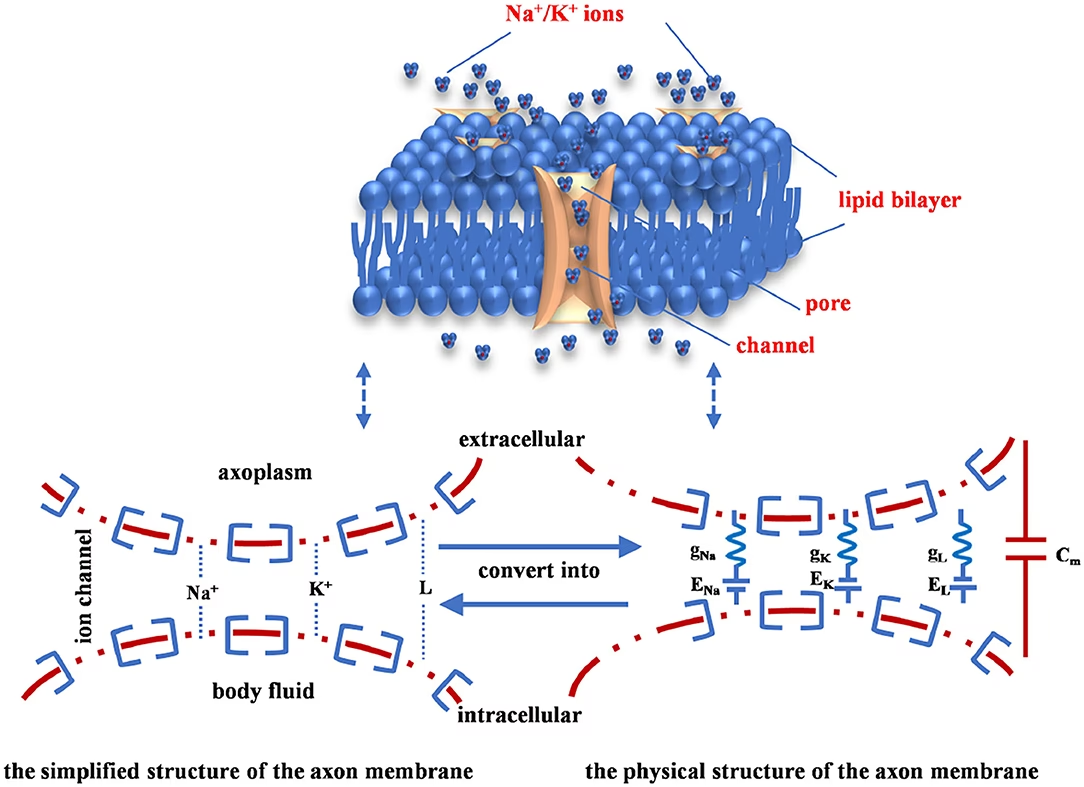
Para describir matemáticamente estos fenómenos, Hodgkin y Huxley utilizaron una analogía con un circuito eléctrico simple. En este modelo:
- La membrana celular semipermeable actúa como un condensador, capaz de almacenar carga eléctrica y separar el interior del exterior de la célula.
- Cada tipo de canal iónico (Sodio, Potasio, Fuga) se representa como una resistencia variable. La flecha diagonal sobre el símbolo de la resistencia indica que su valor no es fijo, sino que cambia.
- Las diferencias en la concentración de iones entre el interior y el exterior de la célula generan un potencial eléctrico (conocido como potencial de Nernst o potencial de reversión). Esto se representa en el circuito por una batería para cada tipo de ión (E_Na, E_K, E_L), con un voltaje específico determinado por las concentraciones iónicas.
La ley fundamental que rige este circuito es la conservación de la carga eléctrica. Una corriente total aplicada a la membrana (I(t)) se divide en una corriente capacitiva (I_C) que carga el condensador de la membrana y las corrientes iónicas (I_k) que pasan a través de los canales:
I(t) = I_C(t) + Σ I_k(t)
La corriente capacitiva es proporcional a la velocidad de cambio del voltaje a través de la membrana (I_C = C * du/dt), donde C es la capacitancia de la membrana y u es el voltaje. Reorganizando, obtenemos la ecuación central que describe cómo cambia el voltaje de la membrana:
C * du/dt = - Σ I_k(t) + I(t)
La suma de las corrientes iónicas (Σ I_k(t)) representa el flujo neto de iones a través de la membrana. Para el modelo estándar de Hodgkin-Huxley, esta suma incluye las corrientes de Sodio, Potasio y Fuga:
Σ I_k(t) = I_Na(t) + I_K(t) + I_L(t)
Conductancias Variables y Variables Compuerta
La corriente de fuga es la más simple; se describe por una conductancia constante (g_L = 1/R) y sigue la Ley de Ohm: I_L = g_L * (u - E_L), donde (u - E_L) es la diferencia de voltaje a través de la resistencia de fuga.
Sin embargo, las conductancias de sodio y potasio son dependientes del voltaje y del tiempo. Hodgkin y Huxley introdujeron el concepto de "variables compuerta" o "gating variables" (m, n y h) para modelar la probabilidad de que un canal esté abierto en un momento dado. Estas variables, que varían entre 0 y 1, representan diferentes "puertas" dentro de los canales iónicos que se abren o cierran en respuesta al voltaje.
- Los canales de Sodio están controlados por dos tipos de compuertas: una compuerta de activación (m) y una compuerta de inactivación (h). La conductancia efectiva del sodio se modela como g_Na * m³ * h. El factor cúbico (m³) y el factor simple (h) se derivaron empíricamente para ajustar los datos experimentales.
- Los canales de Potasio están controlados por una compuerta de activación (n). La conductancia efectiva del potasio se modela como g_K * n⁴, con el factor a la cuarta potencia (n⁴) también ajustado a los datos.
Así, las corrientes iónicas se expresan finalmente como:
I_Na(t) = g_Na * m³ * h * (u - E_Na)
I_K(t) = g_K * n⁴ * (u - E_K)
I_L(t) = g_L * (u - E_L)
Donde g_Na, g_K y g_L son las conductancias máximas cuando todos los canales están abiertos, y E_Na, E_K y E_L son los potenciales de reversión (los voltajes a los que la corriente iónica neta para ese ión es cero).
La Dinámica de las Compuertas
Las variables compuerta (m, n, h) no cambian instantáneamente con el voltaje, sino que evolucionan con el tiempo según ecuaciones diferenciales de primer orden. Para una variable genérica x (que representa m, n o h):
dx/dt = (x₀(u) - x) / τₓ(u)
Esta ecuación significa que la variable x tiende hacia un valor de equilibrio dependiente del voltaje (x₀(u)) con una constante de tiempo también dependiente del voltaje (τₓ(u)). Hodgkin y Huxley determinaron empíricamente las funciones específicas para x₀(u) y τₓ(u) para cada variable compuerta ajustando sus modelos a los datos de corrientes iónicas medidos bajo diferentes voltajes de membrana.
Experimentos Fundamentales
Para deducir estas complejas relaciones, Hodgkin y Huxley emplearon una técnica llamada "fijación de voltaje" (voltage clamp). Esta técnica les permitía mantener el voltaje de la membrana en un valor fijo y medir la corriente iónica necesaria para mantener ese voltaje. Al aplicar "pasos de voltaje" (cambios repentinos del voltaje de la membrana a un nuevo valor fijo) y bloquear selectivamente los canales iónicos (por ejemplo, bloqueando los canales de sodio para estudiar solo los de potasio), pudieron medir las corrientes de sodio y potasio por separado a lo largo del tiempo y a diferentes voltajes.
A partir de estas mediciones de corriente y conociendo el potencial de reversión de cada ión, pudieron calcular la conductancia dependiente del tiempo y del voltaje. Luego, ajustaron sus modelos matemáticos (incluyendo la forma de las funciones de las variables compuerta y sus exponentes) a estos datos experimentales. Un ejemplo notable es cómo dedujeron el exponente de cuatro para la conductancia de potasio (n⁴) basándose en la cinética de la corriente de potasio observada.
El Legado del Modelo
El Modelo Hodgkin-Huxley fue un logro monumental. Fue la primera descripción cuantitativa exitosa de los mecanismos que generan un potencial de acción. Demostró que las propiedades eléctricas de las neuronas pueden ser explicadas por las propiedades de los canales iónicos dependientes del voltaje incrustados en la membrana. Este modelo no solo explicó el impulso nervioso en el axón del calamar, sino que se convirtió en la base para comprender la excitabilidad eléctrica en una amplia variedad de células, incluidas las neuronas humanas, las células musculares y las células cardíacas.

Aunque se han desarrollado modelos más complejos y detallados desde entonces, el Modelo Hodgkin-Huxley sigue siendo fundamental. Es la piedra angular de la neurociencia computacional y la electrofisiología, y su estructura conceptual (capacitancia de membrana, conductancias iónicas dependientes del voltaje y el tiempo, potenciales de reversión) es esencial para cualquier estudio de la excitabilidad celular. Su impacto se extiende desde la investigación básica hasta la comprensión de enfermedades neurológicas y cardiovasculares.
Una Nota Aclaratoria: Andrew Huxley vs. Thomas Henry Huxley
Es importante no confundir a Sir Andrew Fielding Huxley (el neurofisiólogo del siglo XX) con su abuelo, Thomas Henry Huxley (el biólogo del siglo XIX). Aunque ambos fueron científicos ingleses prominentes, sus campos de estudio y contribuciones fueron muy diferentes.
| Característica | Andrew Fielding Huxley | Thomas Henry Huxley |
|---|---|---|
| Época Principal | Siglo XX | Siglo XIX |
| Campo Principal | Neurofisiología, Biofísica | Biología General, Paleontología, Educación |
| Contribución Famosa | Modelo Hodgkin-Huxley (impulso nervioso) | Defensor de Darwin ("Bulldog de Darwin"), Agnosticismo, estudio de invertebrados marinos |
| Premio Nobel | Sí (1963, Fisiología o Medicina) | No |
| Relación Familiar | Nieto | Abuelo |
Thomas Henry Huxley fue un apasionado defensor del evolucionismo de Charles Darwin, ganándose el apodo de "el bulldog de Darwin". Sus trabajos sobre anatomía comparada, sus estudios de invertebrados marinos (como medusas y anémonas) y su activismo por la educación científica y el agnosticismo dejaron una marca indeleble en la historia de la ciencia, pero no se centraron en los mecanismos iónicos del impulso nervioso como lo hizo su nieto Andrew.
Preguntas Frecuentes sobre el Modelo Hodgkin-Huxley
¿Qué es un potencial de acción?
Es una señal eléctrica rápida y transitoria que se propaga a lo largo de la membrana de una célula excitable, como una neurona o una célula muscular. Es la forma principal de comunicación a larga distancia en el sistema nervioso.
¿Por qué usaron el axón gigante del calamar?
Su tamaño excepcionalmente grande (hasta 1 mm de diámetro) permitió a Hodgkin y Huxley insertar electrodos dentro del axón para medir el voltaje de la membrana y controlar la corriente iónica con una precisión que era imposible en axones más pequeños en ese momento.
¿Qué son las variables compuerta (m, n, h)?
Son variables matemáticas introducidas en el modelo para representar el estado (abierto o cerrado) de las "puertas" dentro de los canales iónicos de sodio y potasio. Su valor (entre 0 y 1) puede interpretarse como la probabilidad de que una compuerta particular esté en un estado abierto, o como la fracción de compuertas que están abiertas en un momento dado.
¿El modelo Hodgkin-Huxley es universal?
Es un modelo fundamental y conceptualmente muy potente. Sin embargo, las propiedades exactas de los canales iónicos (como las funciones de las variables compuerta y las constantes de tiempo) varían entre diferentes tipos de neuronas y diferentes especies. Por lo tanto, el modelo se adapta a menudo ajustando sus parámetros o añadiendo más tipos de canales para describir con precisión la excitabilidad de células específicas.
¿Sigue siendo relevante el modelo hoy en día?
Absolutamente. Aunque hay modelos neuronales más complejos, el Modelo Hodgkin-Huxley sigue siendo la base conceptual para entender la bioelectricidad. Se utiliza ampliamente en la enseñanza, en simulaciones computacionales de redes neuronales y como punto de partida para desarrollar modelos más detallados de la excitabilidad celular en la investigación.
Conclusión
El trabajo de Andrew Huxley y Allan Hodgkin, culminado en el Modelo Hodgkin-Huxley, transformó nuestra comprensión del impulso nervioso. Al explicar cómo el flujo controlado de iones a través de canales dependientes del voltaje genera el potencial de acción, proporcionaron un marco cuantitativo que ha sido la base de la electrofisiología moderna. Este logro, merecedor del Premio Nobel, subraya la importancia de comprender los mecanismos iónicos subyacentes a las funciones biológicas y continúa siendo una fuente de inspiración en la neurociencia.
Si quieres conocer otros artículos parecidos a El Modelo Hodgkin-Huxley: Clave del Impulso Nervioso puedes visitar la categoría Neurociencia.

