La comunicación en el sistema nervioso se basa en señales eléctricas rápidas conocidas como potenciales de acción. Durante décadas, el mecanismo preciso de cómo estas señales se generan y propagan fue un misterio. Fue el trabajo pionero de Alan Hodgkin y Andrew Huxley en la década de 1950, utilizando el axón gigante del calamar, el que proporcionó una explicación cuantitativa y detallada de este fenómeno fundamental. Su investigación culminó en un modelo matemático que no solo describió con precisión los potenciales de acción, sino que también sentó las bases de lo que hoy conocemos como neurociencia computacional, un logro por el cual fueron galardonados con el Premio Nobel en 1963.
- La Base Experimental: El Axón de Calamar y el Clamp de Voltaje
- El Modelo Eléctrico de la Membrana Neuronal
- Los Canales Iónicos Clave: Sodio y Potasio
- La Dinámica de las Compuertas: Las Ecuaciones de Gating
- Generación del Potencial de Acción Según el Modelo
- Otros Componentes del Modelo: Canales de Fuga y Bombas
- Extensiones y Aplicaciones del Modelo
- Legado e Impacto en la Neurociencia
- Preguntas Frecuentes sobre el Modelo Hodgkin-Huxley
- Conclusión
La Base Experimental: El Axón de Calamar y el Clamp de Voltaje
Para desentrañar los mecanismos iónicos subyacentes al potencial de acción, Hodgkin y Huxley emplearon una técnica experimental crucial: el clamp de voltaje. Esta técnica les permitió fijar el potencial eléctrico a través de la membrana neuronal a un valor deseado y medir las corrientes iónicas que fluían a través de ella en respuesta. El axón gigante del calamar era ideal para estos experimentos debido a su gran tamaño, que facilitaba la inserción de electrodos.
Al variar sistemáticamente el voltaje de la membrana y observar las corrientes resultantes en presencia y ausencia de iones específicos (sodio y potasio), pudieron deducir las propiedades de los canales iónicos responsables. Descubrieron que la permeabilidad de la membrana al sodio y al potasio no era constante, sino que dependía tanto del voltaje de la membrana como del tiempo.
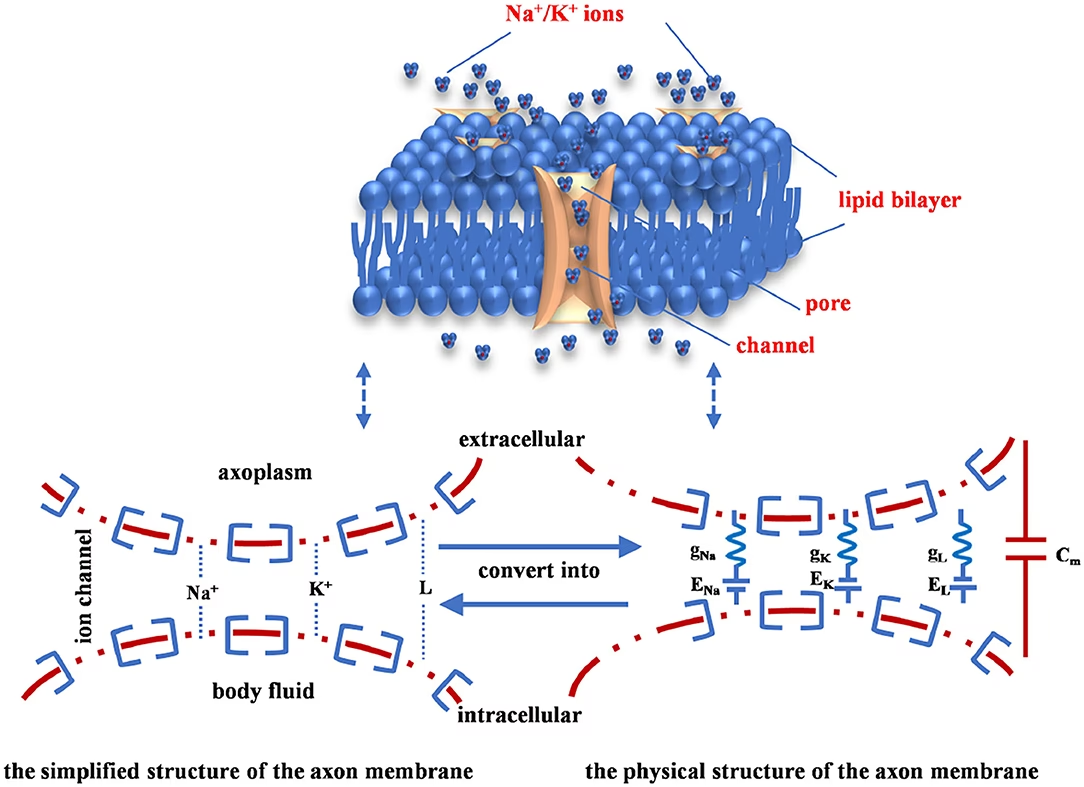
El Modelo Eléctrico de la Membrana Neuronal
Hodgkin y Huxley concibieron la membrana neuronal como un circuito eléctrico. En este modelo, la bicapa lipídica actúa como un capacitor (Cm), capaz de almacenar carga eléctrica. Los canales iónicos, que permiten el paso de iones específicos a través de la membrana, se representan como conductancias (g) en paralelo con baterías, donde cada batería representa el potencial de equilibrio o potencial de reversión (Vrev) para un ion particular (como VNa para el sodio y VK para el potasio), determinado por sus gradientes de concentración.
La corriente total (I) que atraviesa la membrana por unidad de área se considera la suma de la corriente que carga el capacitor (corriente capacitiva) y las corrientes que fluyen a través de los distintos canales iónicos (corrientes iónicas). La corriente capacitiva es proporcional a la tasa de cambio del voltaje de la membrana (dVm/dt), mientras que la corriente a través de cada canal iónico es el producto de su conductancia (g) y el potencial de arrastre (Vm - Vrev), que es la diferencia entre el voltaje actual de la membrana y el potencial de reversión del ion.
La ecuación fundamental que describe esta relación es:
I = Cm (dVm/dt) + Iiónica total
Los Canales Iónicos Clave: Sodio y Potasio
El modelo de Hodgkin-Huxley se centró principalmente en los canales de sodio (Na+) y potasio (K+) dependientes de voltaje, ya que son los principales responsables del potencial de acción rápido en el axón del calamar. También incluyeron una corriente de fuga (Il) para representar la permeabilidad pasiva de la membrana a otros iones.
Las conductancias de los canales dependientes de voltaje (gNa y gK) no son constantes. Hodgkin y Huxley descubrieron que estas conductancias dependen del voltaje de la membrana (Vm) y del tiempo (t). Para describir esta dependencia, introdujeron variables de compuerta (o variables de gating), que son probabilidades adimensionales entre 0 y 1:
- m: Probabilidad de activación de las subunidades del canal de sodio. Aumenta rápidamente con la despolarización.
- h: Probabilidad de inactivación de las subunidades del canal de sodio. Disminuye lentamente con la despolarización.
- n: Probabilidad de activación de las subunidades del canal de potasio. Aumenta lentamente con la despolarización.
La conductancia total para un tipo de canal dependiente de voltaje se modela como el producto de una conductancia máxima (ḡ) y una combinación de estas variables de compuerta elevadas a ciertas potencias. Estas potencias (m3, h1, n4 en el modelo original) representan el número de "compuertas" hipotéticas dentro del canal que deben estar en el estado correcto (abierto/cerrado) para que el canal sea conductor. Por ejemplo, el canal de potasio se modeló como si tuviera cuatro subunidades (n4) que deben estar activadas.
Las corrientes iónicas dependientes de voltaje se expresan entonces como:
INa = ḡNa m³ h (Vm - VNa)
IK = ḡK n⁴ (Vm - VK)
La corriente de fuga es más simple, con una conductancia constante:
Il = ḡl (Vm - Vl)
Así, la ecuación principal del modelo combinando todas las corrientes es:
I = Cm (dVm/dt) + ḡK n⁴ (Vm - VK) + ḡNa m³ h (Vm - VNa) + ḡl (Vm - Vl)
La Dinámica de las Compuertas: Las Ecuaciones de Gating
La parte innovadora del modelo reside en cómo describieron la evolución temporal de las variables de compuerta (m, h, n). Postularon que la tasa de cambio de cada variable de compuerta dependía del voltaje de la membrana. Esto se formuló mediante un conjunto de tres ecuaciones diferenciales ordinarias:
dm/dt = αm(Vm)(1 - m) - βm(Vm)m
dh/dt = αh(Vm)(1 - h) - βh(Vm)h
dn/dt = αn(Vm)(1 - n) - βn(Vm)n
Donde α (alfa) y β (beta) son coeficientes de tasa (con unidades de 1/tiempo) que dependen únicamente del voltaje de la membrana (Vm). α representa la tasa de transición de la compuerta al estado "abierto" (o activado), y β representa la tasa de transición al estado "cerrado" (o inactivado). Por ejemplo, para la variable m, αm rige la transición de cerrado a abierto, y βm rige la transición de abierto a cerrado.
Estas ecuaciones implican que cada variable de compuerta tiende hacia un valor de estado estacionario (x∞) con una constante de tiempo (τx) que también dependen del voltaje. Los experimentos de clamp de voltaje fueron cruciales para determinar las funciones matemáticas específicas que describen cómo α y β (y, por lo tanto, x∞ y τx) cambian con el voltaje.

Generación del Potencial de Acción Según el Modelo
El verdadero poder del modelo de Hodgkin-Huxley radica en su capacidad para simular la secuencia completa de eventos que dan lugar a un potencial de acción en respuesta a un estímulo. Partiendo de un potencial de membrana en reposo (donde los canales de fuga están predominantemente abiertos, y los canales de Na y K dependientes de voltaje están cerrados o inactivados), un estímulo despolarizante desencadena el proceso:
- Despolarización inicial: Un estímulo (como una inyección de corriente) despolariza ligeramente la membrana, aumentando Vm.
- Activación rápida de Na+: El aumento en Vm incrementa rápidamente αm, haciendo que la variable m aumente rápidamente. Esto abre los canales de sodio (gNa aumenta), permitiendo una rápida entrada de iones Na+ (corriente despolarizante). Este influjo de carga positiva despolariza aún más la membrana, creando un ciclo de retroalimentación positiva.
- Pico del potencial de acción: La rápida entrada de Na+ lleva el potencial de membrana hacia VNa.
- Inactivación de Na+ y Activación de K+: A medida que la membrana se despolariza, dos procesos más lentos se ponen en marcha. La variable h (inactivación de Na+) comienza a disminuir (aumenta βh), cerrando los canales de sodio. Simultáneamente, la variable n (activación de K+) comienza a aumentar (aumenta αn), abriendo los canales de potasio (gK aumenta).
- Repolarización: El cierre de los canales de sodio y la apertura de los canales de potasio llevan a una disminución en el influjo de Na+ y a un aumento en el eflujo de K+ (corriente repolarizante). La salida de carga positiva repolariza la membrana, devolviéndola hacia su potencial de reposo.
- Hiperpolarización (Undershoot): Los canales de potasio se cierran más lentamente que los de sodio se inactivan. Esto puede llevar a que la membrana se hiperpolarice temporalmente, volviéndose más negativa que el potencial de reposo, ya que la conductancia al potasio es transitoriamente más alta que en reposo.
- Retorno al Reposo: Finalmente, los canales de potasio se cierran completamente y el potencial de membrana vuelve a su estado de reposo, mantenido por la corriente de fuga y la acción de las bombas iónicas (aunque las bombas no están explícitamente modeladas en la dinámica rápida del potencial de acción en la formulación original, son esenciales para mantener los gradientes iónicos a largo plazo).
El modelo captura esta compleja interacción de conductancias dependientes de voltaje y tiempo con notable precisión.
Otros Componentes del Modelo: Canales de Fuga y Bombas
Además de los canales de sodio y potasio dependientes de voltaje, el modelo incluye una corriente de fuga (Il). Estos canales de fuga representan la permeabilidad basal de la membrana a varios iones (principalmente potasio y cloruro en muchas neuronas) que no depende significativamente del voltaje en el rango fisiológico. Su conductancia (gl) se considera constante. La corriente de fuga ayuda a establecer el potencial de membrana en reposo.
Aunque no se incluyeron explícitamente en las ecuaciones dinámicas rápidas del potencial de acción, es importante mencionar que las bombas iónicas (como la bomba de sodio-potasio) son cruciales para mantener los gradientes de concentración iónica a través de la membrana a largo plazo. Estas bombas transportan iones activamente contra sus gradientes electroquímicos, contrarrestando el movimiento neto de iones durante los potenciales de acción y restaurando las concentraciones iónicas intracelulares y extracelulares. Su función es más lenta que la dinámica de los canales iónicos dependientes de voltaje.
Extensiones y Aplicaciones del Modelo
El modelo original de Hodgkin-Huxley se basó en un "parche" de membrana (asumiendo que el voltaje es uniforme en toda la extensión). Para modelar la propagación del potencial de acción a lo largo de un axón, se debe incorporar la teoría de cables. Esto implica añadir un término que represente la corriente longitudinal que fluye a lo largo del axón, lo que convierte el conjunto de ecuaciones diferenciales ordinarias en un conjunto de ecuaciones diferenciales parciales, donde el voltaje es una función tanto del tiempo como de la posición espacial.
Además, aunque el modelo original solo consideraba canales de Na+ y K+ dependientes de voltaje y una corriente de fuga, su marco puede extenderse para incluir otros tipos de canales iónicos que se encuentran en diferentes neuronas (como canales de calcio, canales de potasio activados por calcio, etc.). La inclusión de estos canales adicionales permite modelar una variedad más amplia de comportamientos neuronales, como la descarga tónica sostenida o los patrones de descarga en ráfagas (bursting).
El modelo Hodgkin-Huxley, o variaciones del mismo (conocidos como modelos tipo Hodgkin-Huxley), no solo se aplica a neuronas. Ha sido adaptado con éxito para describir la excitabilidad en otras células, como las células musculares cardíacas.
Legado e Impacto en la Neurociencia
El modelo de Hodgkin-Huxley es, sin duda, uno de los logros más significativos en la historia de la fisiología y la neurociencia. Fue uno de los primeros ejemplos exitosos de cómo un modelo matemático cuantitativo podía explicar un fenómeno biológico complejo a nivel molecular y celular. Su publicación en 1952 fue un hito que demostró el poder de combinar la experimentación rigurosa con el modelado matemático.
Su impacto en la neurociencia computacional es incalculable. Proporcionó el andamiaje conceptual y matemático para construir modelos de neuronas individuales y, posteriormente, de redes neuronales completas. Aunque hoy existen modelos más simplificados (como el modelo FitzHugh-Nagumo o el modelo Izhikevich) o modelos más detallados que incluyen una miríada de tipos de canales y la compleja morfología dendrítica, el modelo de Hodgkin-Huxley sigue siendo la base fundamental para entender los mecanismos biofísicos de la excitabilidad neuronal.
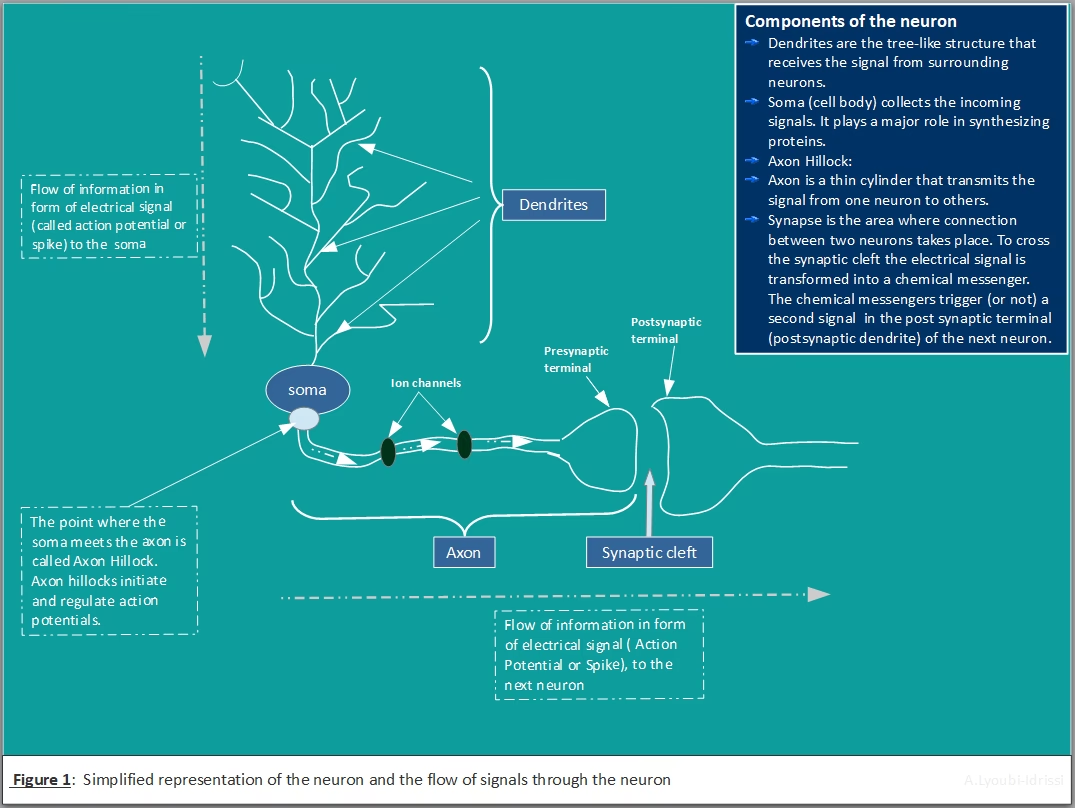
Su relevancia perdura no solo en la investigación básica para entender cómo las neuronas procesan información, sino también en aplicaciones más aplicadas, como el diseño de estimuladores neuronales o la comprensión de enfermedades neurológicas que afectan la función de los canales iónicos (canalopatías). El modelo sigue siendo una herramienta invaluable para la enseñanza y la investigación, demostrando cómo la física y las matemáticas pueden iluminar los misterios de la biología.
| Componente | Analogía Eléctrica | Función Biológica Principal | Representación en el Modelo |
|---|---|---|---|
| Membrana Celular | Capacitor (Cm) | Almacena carga eléctrica | Término Cm (dVm/dt) |
| Canales de Sodio (Na+) Dependientes de Voltaje | Conductancia variable (gNa) en paralelo con una batería (VNa) | Generan la fase de despolarización rápida del potencial de acción | Término ḡNa m³ h (Vm - VNa) con dinámica de m y h |
| Canales de Potasio (K+) Dependientes de Voltaje | Conductancia variable (gK) en paralelo con una batería (VK) | Generan la fase de repolarización del potencial de acción | Término ḡK n⁴ (Vm - VK) con dinámica de n |
| Canales de Fuga | Conductancia constante (gl) en paralelo con una batería (Vl) | Establecen el potencial de membrana en reposo | Término ḡl (Vm - Vl) |
| Variables de Compuerta (m, h, n) | Variables internas que controlan las conductancias | Representan la probabilidad de que los canales estén en estados abiertos/cerrados | Ecuaciones diferenciales que describen su evolución temporal dependiente de Vm |
Preguntas Frecuentes sobre el Modelo Hodgkin-Huxley
Aquí respondemos algunas preguntas comunes sobre este influyente modelo:
¿Qué es exactamente un potencial de acción?
Es un impulso eléctrico rápido y transitorio que se propaga a lo largo de la membrana de una célula excitable (como una neurona o una célula muscular). Es la base de la comunicación rápida en el sistema nervioso.
¿Por qué Hodgkin y Huxley usaron el axón gigante de calamar?
El axón gigante de calamar (Loligo pealeii) tiene un diámetro mucho mayor (hasta 1 mm) que la mayoría de los axones de mamíferos, lo que facilitaba la inserción de electrodos intracelulares y la aplicación de técnicas como el clamp de voltaje para medir corrientes iónicas.
¿El modelo Hodgkin-Huxley es una representación perfecta de una neurona real?
No, es una simplificación. El modelo original se centra en la membrana de un parche de axón e incluye solo los principales canales responsables del potencial de acción rápido en el calamar. Las neuronas reales tienen morfologías complejas (dendritas, soma), muchos más tipos de canales iónicos, bombas, intercambiadores y otras complejidades biofísicas que pueden influir en su comportamiento eléctrico. Sin embargo, es una aproximación muy precisa y poderosa de los mecanismos fundamentales de la excitabilidad.
¿Se sigue utilizando el modelo Hodgkin-Huxley en la investigación actual?
Sí, absolutamente. El modelo original y sus numerosas extensiones y variaciones siguen siendo herramientas fundamentales en la neurociencia computacional para estudiar la dinámica de neuronas individuales, la interacción entre neuronas y la función de los circuitos neuronales. También se utiliza en campos como la electrofisiología cardíaca y la farmacología para entender cómo los fármacos afectan los canales iónicos.
¿Qué significan las variables de compuerta m, h, n?
Representan la probabilidad de que las subunidades o "compuertas" dentro de un canal iónico dependiente de voltaje estén en un estado particular (abierto o cerrado). La conductancia total del canal depende de que todas sus compuertas relevantes estén en el estado "abierto". La despolarización o repolarización de la membrana cambia estas probabilidades con el tiempo.
¿Cómo se determinaron los parámetros del modelo (como las funciones α y β)?
Se determinaron experimentalmente a partir de los datos de corriente iónica obtenidos en experimentos de clamp de voltaje a diferentes potenciales de membrana. Hodgkin y Huxley ajustaron funciones matemáticas (exponenciales y sigmoides) a estos datos para describir la dependencia del voltaje de las tasas de transición de las compuertas.
Conclusión
La teoría de Hodgkin-Huxley es un ejemplo brillante de cómo la investigación experimental y el modelado matemático pueden unirse para desvelar los secretos de la biología. Su modelo no solo explicó el mecanismo del potencial de acción, la señal eléctrica fundamental del sistema nervioso, sino que también proporcionó un marco cuantitativo que ha impulsado décadas de investigación en neurociencia, fisiología y modelado computacional. Su legado perdura como un pilar en nuestra comprensión de cómo las células excitables generan la actividad eléctrica que subyace a funciones vitales como el pensamiento, el movimiento y la sensación.
Si quieres conocer otros artículos parecidos a La Teoría de Hodgkin-Huxley Explicada puedes visitar la categoría Neurociencia.

