La edición genómica, también conocida como edición de genes, representa un conjunto de tecnologías innovadoras que otorgan a los científicos la capacidad de modificar el ADN de un organismo. Estas herramientas permiten añadir, eliminar o alterar material genético en ubicaciones específicas del genoma, abriendo un universo de posibilidades en investigación y terapia.

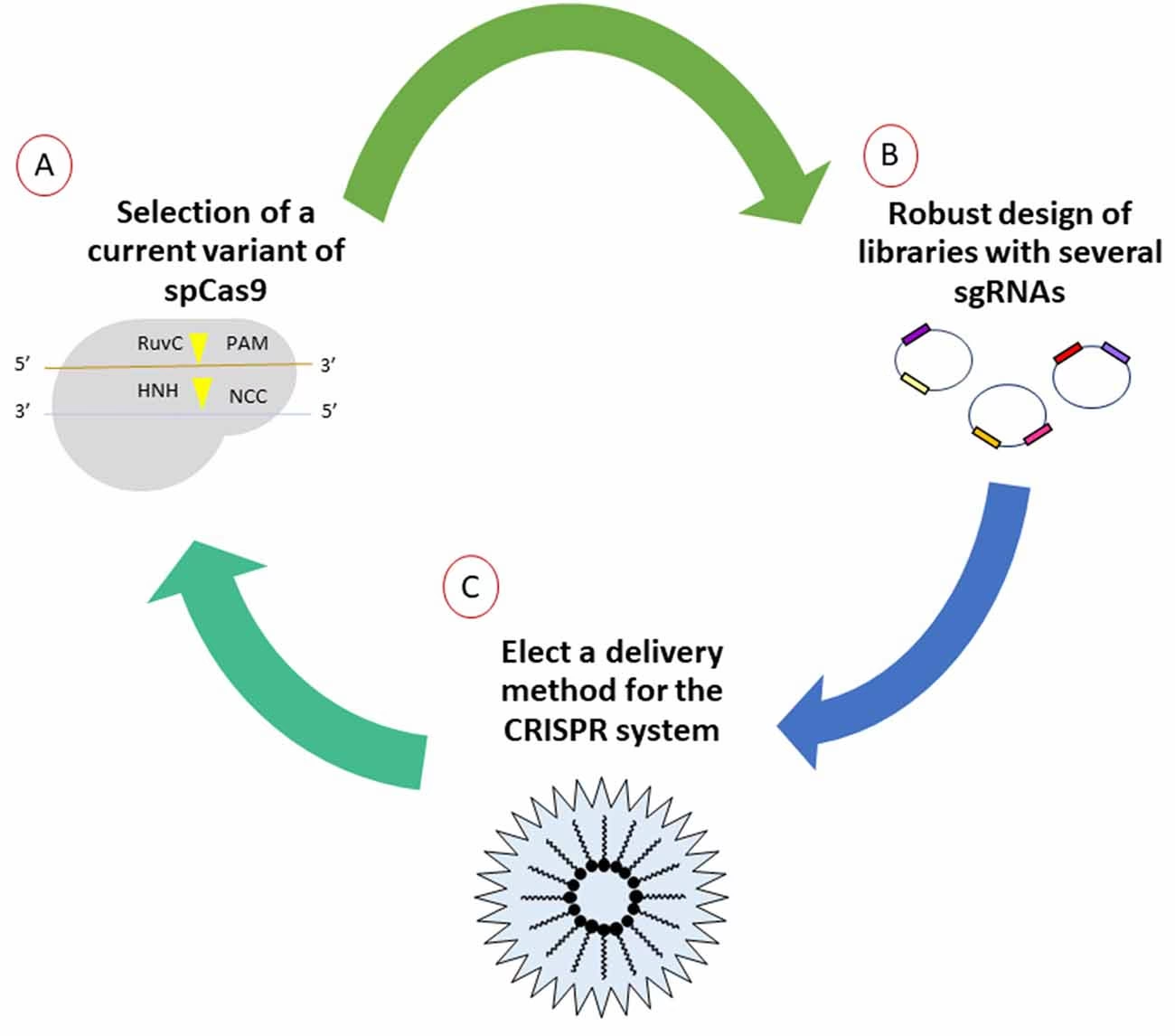
A lo largo de los años, se han desarrollado diversas estrategias para la edición genómica. Entre ellas, destaca de manera prominente el sistema CRISPR-Cas9, cuyo nombre proviene de las repeticiones palindrómicas cortas agrupadas y regularmente espaciadas y la proteína asociada 9. Este sistema ha generado un entusiasmo sin precedentes en la comunidad científica debido a su velocidad, coste reducido, precisión y eficiencia superiores en comparación con métodos anteriores de edición genómica.
CRISPR-Cas9: Un Mecanismo Adaptado de la Naturaleza
El sistema CRISPR-Cas9 fue adaptado de un mecanismo de edición genómica que ocurre de forma natural en las bacterias. Estas bacterias lo utilizan como una defensa inmunitaria ingeniosa contra los virus. Cuando son infectadas, las bacterias capturan pequeños fragmentos del ADN viral y los insertan en su propio ADN siguiendo un patrón específico para crear segmentos conocidos como matrices CRISPR. Estas matrices actúan como una memoria genética, permitiendo a las bacterias reconocer los virus (o virus estrechamente relacionados) si atacan de nuevo.
Si el virus reaparece, las bacterias producen segmentos de ARN a partir de las matrices CRISPR que reconocen y se unen a regiones específicas del ADN viral. Posteriormente, utilizan la enzima Cas9 (o enzimas similares) para cortar el ADN viral, neutralizando así la amenaza. Los investigadores lograron adaptar este sistema de defensa inmunitaria para la edición de ADN. Crean una pequeña molécula de ARN con una secuencia "guía" corta que se une a una secuencia objetivo específica en el ADN de una célula, de manera similar a como los segmentos de ARN bacterianos se unen al ADN viral. Este ARN guía también se asocia con la enzima Cas9. Cuando se introduce en las células, el ARN guía localiza la secuencia de ADN deseada y la enzima Cas9 realiza un corte preciso en esa ubicación, imitando el proceso bacteriano. Aunque Cas9 es la enzima más utilizada, otras enzimas como Cpf1 también pueden emplearse.
Una vez que el ADN es cortado, los científicos aprovechan la maquinaria de reparación de ADN propia de la célula para añadir o eliminar fragmentos de material genético, o para introducir cambios reemplazando un segmento existente por una secuencia de ADN modificada. Este proceso de reparación puede seguir dos vías principales: la unión de extremos no homólogos (NHEJ), que es propenso a errores y a menudo inactiva el gen, o la recombinación homóloga (HR), que utiliza una plantilla de ADN para una reparación precisa.
Aplicaciones Médicas de la Edición Genómica
La edición genómica despierta un enorme interés en la prevención y el tratamiento de enfermedades humanas. Actualmente, esta tecnología se utiliza principalmente en células y modelos animales en laboratorios de investigación para comprender la base molecular y celular de diversas patologías. Los científicos están trabajando arduamente para determinar si este enfoque es seguro y eficaz para su uso en personas.
Se está explorando en ensayos de investigación y clínicos para una amplia variedad de enfermedades, incluyendo trastornos monogénicos causados por mutaciones en un solo gen, como la fibrosis quística, la hemofilia y la anemia de células falciformes. También muestra una promesa considerable para el tratamiento y la prevención de enfermedades más complejas, como el cáncer, las enfermedades cardíacas, las enfermedades mentales y la infección por el virus de la inmunodeficiencia humana (VIH).
Además del tratamiento directo, la edición genómica es fundamental en la creación de modelos celulares y animales de enfermedades. Al modificar el genoma de organismos modelo, los investigadores pueden replicar las condiciones patológicas humanas para estudiar su desarrollo, identificar dianas terapéuticas y probar la eficacia de nuevos tratamientos. Ejemplos notables incluyen modelos de inmunodeficiencia combinada grave (SCID) en titíes, distrofia muscular de Duchenne en ratas y síndrome de Laron en cerdos miniatura.
Esta capacidad de modelado preciso es crucial para avanzar en nuestra comprensión de las enfermedades y desarrollar lo que se ha dado en llamar "medicina precisa", adaptada a las características genéticas individuales de cada paciente.

Evolución de las Terapias Biológicas
La edición genómica no surge en un vacío, sino que representa una evolución significativa en el campo de la terapia biológica. Las primeras incursiones en este ámbito se remontan a la terapia celular, ejemplificada por los trasplantes de médula ósea en las décadas de 1960 y 1970, donde se buscaba reemplazar células dañadas por células sanas. Posteriormente, en la década de 1990, surgió la terapia génica, que consistía en introducir una copia adicional de un gen sano en las células del paciente para restaurar su función. Aunque exitosa en algunos casos, la terapia génica tradicional presenta desafíos como la inserción aleatoria del gen y la respuesta inmunitaria a los vectores virales utilizados.
Más recientemente, la terapia con ARN ha ganado terreno, utilizando oligonucleótidos de ARN para modular la expresión génica, por ejemplo, corrigiendo defectos en el empalme del ARN mensajero, como se ha logrado en el tratamiento de la atrofia muscular espinal (AME).
La edición genómica, y en particular el sistema CRISPR-Cas9, lleva este concepto un paso más allá al permitir la corrección directa de la secuencia de ADN existente en su ubicación original en el genoma, en lugar de simplemente añadir una copia funcional del gen. Esto ofrece la posibilidad de reparaciones genéticas más precisas y potencialmente permanentes.
Desafíos Técnicos en la Aplicación Clínica
A pesar de su inmenso potencial, la aplicación clínica de la edición genómica enfrenta varios desafíos técnicos significativos:
- Mejora de los Mecanismos de Reparación: Para corregir una mutación específica, es necesario inducir el mecanismo de reparación de ADN por recombinación homóloga (HR), que utiliza una plantilla para una reparación precisa. Sin embargo, las células tienden a favorecer la vía de unión de extremos no homólogos (NHEJ), que es más propensa a errores y puede inactivar el gen en lugar de corregirlo. Aumentar la eficiencia de la HR y controlar la vía de reparación son aspectos cruciales de la investigación actual. La tecnología de prime editing surge como una alternativa prometedora que puede realizar ciertos tipos de ediciones sin crear rupturas de doble hebra.
- Entrega a Células Vivas: Hacer llegar los componentes del sistema de edición genómica (como la enzima Cas9 y el ARN guía) al interior de las células diana es un desafío complejo. La entrega puede realizarse ex vivo (modificando células fuera del cuerpo y luego reintroduciéndolas) o in vivo (administrando los componentes directamente al cuerpo). Se están investigando diversas estrategias de entrega, incluyendo vectores virales (como los virus adenoasociados - AAV) y métodos no virales (como la electroporación, liposomas o nanopartículas). Cada método tiene sus pros y contras en términos de eficiencia, seguridad y potencial de respuesta inmunitaria.
- Efectos Fuera de Objetivo (Off-targets): Uno de los riesgos principales es que el sistema de edición genómica corte o modifique el ADN en lugares no deseados del genoma. Estos "off-targets" pueden tener consecuencias celulares impredecibles y potencialmente dañinas. La investigación se centra en diseñar sistemas más específicos y utilizar herramientas bioinformáticas para predecir y minimizar estos efectos. Las nuevas generaciones de herramientas de edición, como los editores de base o los prime editors, buscan reducir o eliminar las rupturas de doble hebra, que son una causa principal de off-targets.
- Viabilidad Celular y Estabilidad de la Corrección: La capacidad de las células editadas para sobrevivir, proliferar y mantener la corrección genética a largo plazo es esencial para un efecto terapéutico duradero. La viabilidad puede depender del gen editado y del impacto de la edición en la célula.
Consideraciones Éticas Fundamentales
El uso de la edición genómica, especialmente en humanos, plantea importantes cuestiones éticas. La distinción clave aquí es entre la edición de células somáticas y la edición de células germinales.
- Edición de Células Somáticas: Implica modificar células que no son óvulos ni espermatozoides. Los cambios genéticos introducidos se limitan a tejidos específicos y no se transmiten a las generaciones futuras. Aunque todavía requiere una cuidadosa evaluación de seguridad y eficacia, la edición de células somáticas para tratar enfermedades graves generalmente se considera éticamente más aceptable, similar a otras formas de terapia génica.
- Edición de Células Germinales y Embriones: Implica modificar el ADN en óvulos, espermatozoides o embriones tempranos. Los cambios resultantes serían hereditarios y se transmitirían a todas las células de las generaciones futuras. Esto plantea una serie de desafíos éticos complejos y profundos, incluyendo la posibilidad de utilizar la tecnología para "mejorar" rasgos humanos normales (como la altura o la inteligencia) en lugar de tratar enfermedades. Debido a estas preocupaciones éticas y de seguridad, la edición del genoma de células germinales y embriones es actualmente ilegal en muchos países, incluyendo Estados Unidos.
El debate sobre la edición de células germinales es intenso y requiere una cuidadosa consideración de los posibles beneficios terapéuticos frente a los riesgos desconocidos y las implicaciones sociales a largo plazo.
Preguntas Frecuentes sobre la Edición Genómica
- ¿Es segura la edición genómica en humanos?
- Actualmente, la edición genómica en humanos está mayormente en etapas de investigación y ensayos clínicos. La seguridad a largo plazo aún se está evaluando, especialmente en relación con los efectos fuera de objetivo y la respuesta inmunitaria. Para la edición de células somáticas, la seguridad está siendo investigada rigurosamente en ensayos para enfermedades específicas. La edición de células germinales se considera insegura e ilegal en muchos lugares debido a los riesgos desconocidos y las implicaciones éticas.
- ¿Qué enfermedades puede tratar la edición genómica?
- Se está investigando para tratar una amplia gama de enfermedades genéticas, incluyendo trastornos monogénicos como la fibrosis quística, la hemofilia y la anemia de células falciformes. También se explora su potencial para enfermedades más complejas como el cáncer, el VIH, enfermedades cardíacas y neurológicas.
- ¿Cuál es la diferencia entre edición genómica y terapia génica tradicional?
- La terapia génica tradicional generalmente introduce una nueva copia funcional de un gen en las células. La edición genómica, en cambio, modifica directamente la secuencia de ADN existente en su ubicación original en el genoma, permitiendo correcciones precisas, eliminación o adición de secuencias.
- ¿Qué es CRISPR-Cas9?
- CRISPR-Cas9 es una de las tecnologías de edición genómica más conocidas. Utiliza una molécula de ARN guía para dirigir la enzima Cas9 a una ubicación específica en el ADN, donde Cas9 realiza un corte. Este sistema es más rápido, económico y fácil de usar que tecnologías anteriores.
El Futuro de la Edición Genómica
El campo de la edición genómica avanza a un ritmo vertiginoso. La investigación continua no solo perfecciona herramientas existentes como CRISPR-Cas9, sino que también descubre y desarrolla nuevas tecnologías con mayor precisión y versatilidad. Superar los desafíos técnicos relacionados con la entrega eficiente y segura a las células diana, minimizar los efectos fuera de objetivo y controlar los mecanismos de reparación del ADN son áreas clave de enfoque.
Aunque el camino hacia la aplicación clínica generalizada es complejo y requiere una cuidadosa navegación de las consideraciones científicas, éticas y regulatorias, el potencial de la edición genómica para transformar la medicina y mejorar la vida de las personas que padecen enfermedades genéticas es innegable. Es un área de la neurociencia y la biotecnología que continuará generando descubrimientos apasionantes y ofreciendo nuevas esperanzas para el futuro de la salud humana.
Si quieres conocer otros artículos parecidos a Edición Genómica: Revolucionando la Medicina puedes visitar la categoría Neurociencia.