Dentro de las profundidades de nuestro sistema digestivo reside una red neuronal vasta y compleja, a menudo referida como el "segundo cerebro". Este es el Sistema Nervioso Entérico (SNE), intrínseco al tracto gastrointestinal y con una capacidad asombrosa para operar de forma independiente del sistema nervioso central (SNC). Aunque modulado por las otras dos divisiones del sistema nervioso autónomo (el simpático y el parasimpático), el intestino delgado y grueso puede funcionar sin la supervisión directa del cerebro y la médula espinal. Esta independencia subraya la sofisticación y la importancia vital de este sistema neuronal para la salud y el bienestar general.

El SNE no es una simple colección de nervios; es un sistema completo con más de 100 millones de neuronas. Esta cifra supera la cantidad de neuronas que se encuentran en toda la médula espinal humana, aunque no llega a ser tan numerosa como las del cerebro. Esta impresionante cantidad de neuronas está incrustada en la pared gastrointestinal y se organiza en dos plexos principales: el plexo submucoso (o de Meissner), situado justo debajo de la mucosa intestinal, y el plexo mientérico (o de Auerbach), más profundo, que se encuentra entre las dos capas de la muscular externa. Estos plexos trabajan en conjunto para orquestar las complejas funciones digestivas.
Funciones Clave del SNE
La función principal del Sistema Nervioso Entérico es controlar el comportamiento del tracto gastrointestinal. Esto incluye la regulación de la secreción de hormonas y, crucialmente, los movimientos musculares del intestino. Dos de los movimientos más importantes que controla son:
- Peristalsis: Contracciones musculares coordinadas que impulsan el contenido luminal a lo largo del tracto digestivo en una dirección.
- Segmentación: Contracciones localizadas que mezclan el contenido luminal con enzimas digestivas.
Estas actividades son finamente coreografiadas por microcircuitos dentro del SNE, que contienen neuronas aferentes primarias intrínsecas (IPANs) capaces de responder a estímulos locales e integrar información para coordinar la respuesta motora. La independencia del SNE en estas funciones motoras es tan vital que, incluso si se cortaran todas las conexiones con el SNC, la motilidad esencial en el intestino delgado y grueso permanecería intacta. Por el contrario, la ausencia de un pequeño segmento del SNE, ya sea congénita (como en la enfermedad de Hirschsprung) o adquirida (como en la enfermedad de Chagas), puede llevar a una pseudo-obstrucción letal, demostrando que el SNE es esencial para la vida.
El SNE y sus Neurotransmisores
Sorprendentemente, la mayoría de los neurotransmisores que se encuentran en el sistema nervioso central también desempeñan roles importantes en el Sistema Nervioso Entérico. Esta similitud neuroquímica es parte de lo que lo hace tan complejo y capaz de una regulación autónoma. Algunos de los actores clave incluyen:
- Serotonina (5-HT): Liberada por las células enteroendocrinas (células enterocromafines) en respuesta a la distensión luminal. Activa las IPANs en el plexo mientérico, que a su vez activan interneuronas ascendentes y descendentes.
- Acetilcolina (ACh): Un neurotransmisor excitatorio importante. Junto con la encefalina, activa las neuronas motoras excitatorias. También puede activar neuronas motoras inhibitorias junto con la serotonina.
- Sustancia P: Implicada en la contracción muscular longitudinal.
- Óxido Nítrico (NO): Un neurotransmisor inhibitorio que causa relajación del músculo longitudinal.
- Péptido Intestinal Vasoactivo (VIP): También un neurotransmisor inhibitorio que causa relajación del músculo longitudinal.
- Encefalina: Neurotransmisor que activa interneuronas ascendentes, las cuales a su vez activan neuronas motoras excitatorias.
Esta compleja red de neurotransmisores permite al SNE modular con precisión la actividad muscular, la secreción y el flujo sanguíneo local en respuesta a las condiciones dentro del lumen intestinal.
El Eje Intestino-Cerebro: Una Comunicación Bidireccional Constante
Aunque el SNE posee una notable independencia, no opera en aislamiento. Existe un intercambio constante y significativo de estímulos entre el cerebro y el SNE, conocido como el eje intestino-cerebro. Es fascinante notar que se estima que el 90% de las fibras en el nervio vago son aferentes, lo que significa que la mayor parte de la información que viaja a través de este nervio va del intestino hacia el sistema nervioso central, no al revés. Esto sugiere que el cerebro está más en el extremo receptor de esta comunicación.
Las señales enviadas desde el intestino al cerebro a través del nervio vago pueden iniciar reflejos vagovagales que regulan patrones de motilidad en el esófago o el estómago. También transmiten sensaciones conscientes como náuseas, hinchazón o saciedad. Sin embargo, gran parte de la información es de naturaleza 'homeostática' y puede no llegar a la conciencia, pero aún así puede influir en el estado de ánimo. La estimulación del nervio vago, que imita la señalización aferente del intestino, se ha utilizado incluso con éxito para tratar la depresión y mejorar el aprendizaje y la memoria en estudios con animales y humanos. Además, el nervio vago es un posible conducto para las señales de la microbiota luminal que afectan el estado de ánimo, el comportamiento y el desarrollo cerebral.
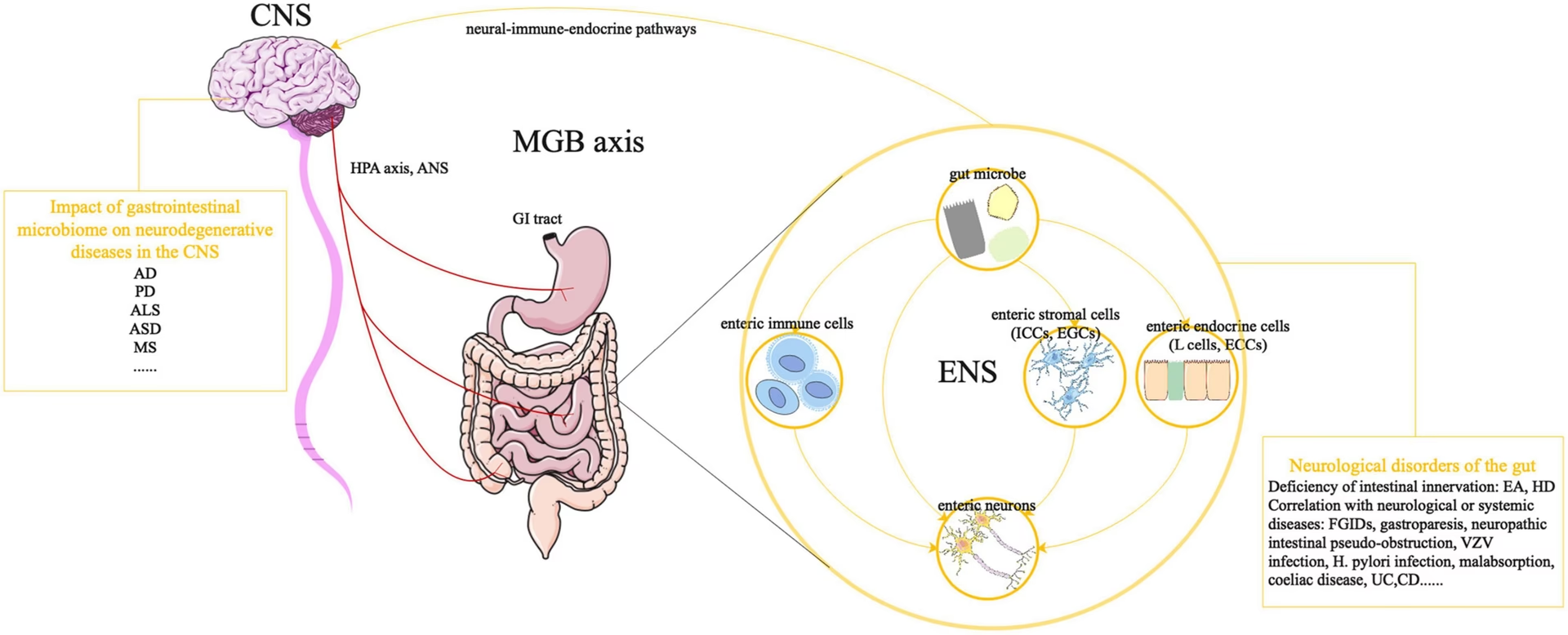
El SNE y su Sorprendente Papel en Trastornos Neurológicos
Dada la importancia, el tamaño y la complejidad del SNE, no sorprende que contribuya a la fisiopatología de los trastornos gastrointestinales. Pero lo que ha ganado una atención creciente es su posible implicación en trastornos primarios del sistema nervioso central. Los mecanismos patofisiológicos que dan lugar a trastornos del SNC podrían también operar en el SNE, ya que comparten muchos neurotransmisores y mecanismos de desarrollo similares. La disfunción del SNE se ha relacionado con un número creciente de trastornos del SNC, desde neurodesarrollo hasta neurodegenerativos, y las manifestaciones gastrointestinales disfuncionales a menudo ocurren incluso antes de que los síntomas del SNC se hagan evidentes.
Enfermedad de Parkinson (EP)
La Enfermedad de Parkinson es un trastorno neurodegenerativo progresivo definido por la disfunción del SNC en regiones específicas. Sin embargo, la identificación de anomalías gastrointestinales en pacientes con EP hace más de 30 años planteó la posibilidad de que el SNE pudiera estar involucrado. Las neuronas dopaminérgicas se encuentran en el SNE y son esenciales para la motilidad gastrointestinal normal. Modelos animales (como la administración de MPTP o la sobreexpresión de alfa-sinucleína) sugieren que el SNE es vulnerable a la degeneración en la EP.
Un hallazgo clave en la EP es la acumulación de agregados resistentes a proteasas de alfa-sinucleína, el componente principal de los cuerpos de Lewy, la lesión patognomónica de la EP. Estos agregados de alfa-sinucleína también se han encontrado en las neuronas del SNE de pacientes con EP. La hipótesis de Braak sugiere que la EP podría ser causada por un patógeno neurotrópico que primero entra en las neuronas entéricas desde el lumen intestinal y luego se mueve por transporte retrógrado a lo largo de las fibras vagales eferentes hacia el núcleo motor dorsal del vago (NMDV) en el tronco encefálico, para finalmente acceder a la corteza cerebral. Estudios en roedores, como la administración intragástrica crónica de pesticidas o la inyección de alfa-sinucleína humana en la pared intestinal, han proporcionado pruebas de principio de que un insulto gastrointestinal puede desencadenar patología del SNC similar a la EP, con acumulación de alfa-sinucleína ascendiendo por el eje intestino-cerebro.
Esto ha llevado a investigar si las biopsias del SNE (obtenidas por colonoscopia) podrían servir como un sitio accesible para el diagnóstico temprano o el seguimiento de la EP, ya que la patología de Lewy puede aparecer en el intestino hasta 20 años antes que los síntomas del SNC. Aunque los hallazgos sobre la especificidad y utilidad diagnóstica de los cuerpos de Lewy en el SNE siguen siendo objeto de debate y se necesitan más estudios, la evidencia de la participación gastrointestinal en la patogénesis y/o fisiopatología de al menos algunos casos de EP es considerable.
Trastorno del Espectro Autista (TEA)
El Trastorno del Espectro Autista es un trastorno del neurodesarrollo común con una prevalencia 3-4 veces mayor de síntomas gastrointestinales en niños afectados que en niños no afectados. Aunque el TEA se diagnostica por el comportamiento, la investigación reciente sugiere que la disfunción del SNE podría ser parte del fenotipo en algunos subtipos genéticamente definidos.
Mutaciones en genes como CHD8 o TCF4, asociados con el TEA, han demostrado causar defectos en la neurogénesis entérica o afectar la motilidad gastrointestinal en modelos animales. Además, niveles elevados de serotonina en sangre, casi enteramente derivada del intestino, se encuentran en aproximadamente un tercio de los pacientes con TEA. Mutaciones de ganancia de función en el gen SLC6A4 que codifica el transportador de serotonina (SERT) también se han asociado con el TEA y, en ratones, resultan en comportamiento similar al TEA y un fenotipo gastrointestinal caracterizado por hipoplasia del SNE y tránsito lento.

La hipótesis del "intestino permeable" en el TEA postula que defectos en la permeabilidad de la barrera epitelial intestinal conducen a una señalización inapropiada por componentes luminales. Aunque los datos son limitados y a veces contradictorios, algunos estudios en humanos y modelos animales (como el modelo de activación inmunitaria materna - MIA) apoyan esta idea. En el modelo MIA, el tratamiento con la bacteria Bacteroides fragilis restauró la integridad de la barrera intestinal y se asoció con una mejora en algunos comportamientos similares al TEA. Dado que las neuronas y la glía entéricas desempeñan papeles importantes en el mantenimiento de la barrera intestinal, la disfunción del SNE podría subyacer a estos defectos de barrera en el TEA, sugiriendo que modular la función del SNE podría ofrecer oportunidades de tratamiento.
Otros Trastornos Neurológicos
La evidencia creciente sugiere que el SNE puede desempeñar un papel, ya sea como portal de entrada o participante activo, en otros trastornos neurológicos. En las encefalopatías espongiformes transmisibles (EET), como la Enfermedad de Creutzfeldt-Jakob, se ha sugerido que el agente patógeno (PrPSc) podría entrar por el intestino y propagarse a través de las vías nerviosas (incluidas las entéricas) y el sistema inmunitario. En la Enfermedad de Alzheimer (EA), aunque los estudios en humanos son escasos, modelos transgénicos de ratón que expresan formas mutantes de la proteína precursora de amiloide (APP), asociada a la EA familiar, desarrollan acumulación de Aβ en las neuronas entéricas, lo que se asocia con una disminución del número de neuronas entéricas y dismotilidad. Esto implica que la disfunción del SNE podría ocurrir en la EA, aunque se necesita mucha más investigación.
Diferencias Clave: SNE, SNC y SNP
El Sistema Nervioso Periférico (SNP) incluye todas las células nerviosas fuera del cerebro y la médula espinal (SNC). Se divide en una división sensorial y una división motora. La división motora incluye el sistema nervioso somático (controla músculos esqueléticos) y el sistema nervioso autónomo. El sistema nervioso autónomo se divide tradicionalmente en tres partes: simpático, parasimpático y entérico.
La principal diferencia que distingue al SNE de otras partes del SNP es su capacidad única para orquestar el comportamiento gastrointestinal de forma independiente de la entrada del SNC. Mientras que la mayoría de las neuronas en los ganglios simpáticos o parasimpáticos reciben inervación directa del SNC, la mayoría de las neuronas entéricas no. El SNE está organizado en microcircuitos con interneuronas e IPANs que pueden iniciar reflejos localmente. Aunque el SNE puede funcionar sin el SNC, normalmente interactúan bidireccionalmente. Existe una clase distintiva de neuronas entéricas llamadas neuronas viscerofugales, que son las únicas que salen de la pared intestinal y activan neuronas simpáticas, que a su vez proyectan de vuelta al intestino para inhibir movimientos. Nuevos datos sugieren que estas vías entero-simpáticas pueden transmitir patrones de disparo sincronizado originados en el SNE, permitiendo un control de motilidad a largo alcance entre diferentes regiones intestinales, una necesidad que va más allá del rango de los circuitos puramente entéricos.
| Característica | Sistema Nervioso Entérico (SNE) | Sistema Nervioso Central (SNC) | Sistema Nervioso Autónomo (SNA - Simpático/Parasimpático) |
|---|---|---|---|
| Ubicación Principal | Pared del tracto gastrointestinal | Cerebro y Médula Espinal | Ganglios y nervios fuera del SNC, controlando órganos internos (incluido el tracto GI) |
| Independencia | Puede funcionar independientemente del SNC para funciones básicas (motilidad, secreción) | Centro de control principal, integra información de todo el cuerpo | Modula la actividad de órganos internos; su control proviene del SNC |
| Número de Neuronas | > 100 millones (más que la médula espinal) | Miles de millones | Menor que el SNE |
| Organización | Plexos mientérico y submucoso, microcircuitos con IPANs e interneuronas | Núcleos, cortezas, tractos, integra información compleja | Ganglios, nervios que proyectan a órganos objetivo |
| Función Principal en GI | Control directo de motilidad, secreción, flujo sanguíneo local | Regulación general, reflejos vagovagales, influencia en partes proximal/distal | Modulación excitatoria (parasimpático) o inhibitoria (simpático) de la función GI |
| Comunicación con SNC | Bidireccional (principalmente aferente vía vago) | Recibe y envía información a todo el cuerpo | Recibe órdenes del SNC para modular órganos periféricos |
Preguntas Frecuentes sobre el SNE
¿Qué significa ENS en neurociencia?
ENS significa Enteric Nervous System, o Sistema Nervioso Entérico en español.
¿Es el SNE realmente un "segundo cerebro"?
Aunque no es un cerebro en el sentido de conciencia o pensamiento, se le apoda así debido a su gran número de neuronas y su notable capacidad para controlar las funciones gastrointestinales de manera autónoma, independientemente del cerebro y la médula espinal.

¿Puede un problema en el SNE causar problemas digestivos?
Sí, la disfunción del SNE está directamente relacionada con muchos trastornos digestivos, ya que es responsable de coordinar la motilidad, la secreción y otras funciones esenciales del tracto gastrointestinal. De hecho, la ausencia de una parte del SNE es letal.
¿Cómo se comunica el SNE con el cerebro?
Se comunican a través del eje intestino-cerebro, principalmente a través del nervio vago. La mayor parte de la comunicación viaja del intestino al cerebro (fibras aferentes).
¿Está el SNE involucrado en la Enfermedad de Parkinson?
La investigación sugiere fuertemente una conexión. Se han encontrado agregados de alfa-sinucleína (cuerpos de Lewy) en las neuronas del SNE de pacientes con Parkinson, a menudo años antes de los síntomas motores. Se investiga si la enfermedad podría comenzar en el intestino y propagarse al cerebro.
¿Tiene el SNE un papel en el Trastorno del Espectro Autista?
Sí, estudios muestran una alta prevalencia de problemas gastrointestinales en el TEA. Investigaciones genéticas y modelos animales vinculan mutaciones asociadas al TEA con disfunciones en el SNE y la barrera intestinal. La microbiota intestinal, que interactúa con el SNE, también parece relevante.
El estudio del Sistema Nervioso Entérico ha abierto nuevas y emocionantes vías en la neurociencia y la medicina. Su complejidad, su independencia funcional y su profunda conexión con el sistema nervioso central a través del eje intestino-cerebro nos recuerdan que la salud de nuestro intestino está intrínsecamente ligada a la salud de nuestro cerebro. Comprender mejor este "segundo cerebro" no solo es clave para tratar los trastornos digestivos, sino que también ofrece perspectivas prometedoras para la comprensión y el tratamiento de una variedad de trastornos neurológicos.
Si quieres conocer otros artículos parecidos a El Sistema Nervioso Entérico: Tu Segundo Cerebro puedes visitar la categoría Neurociencia.