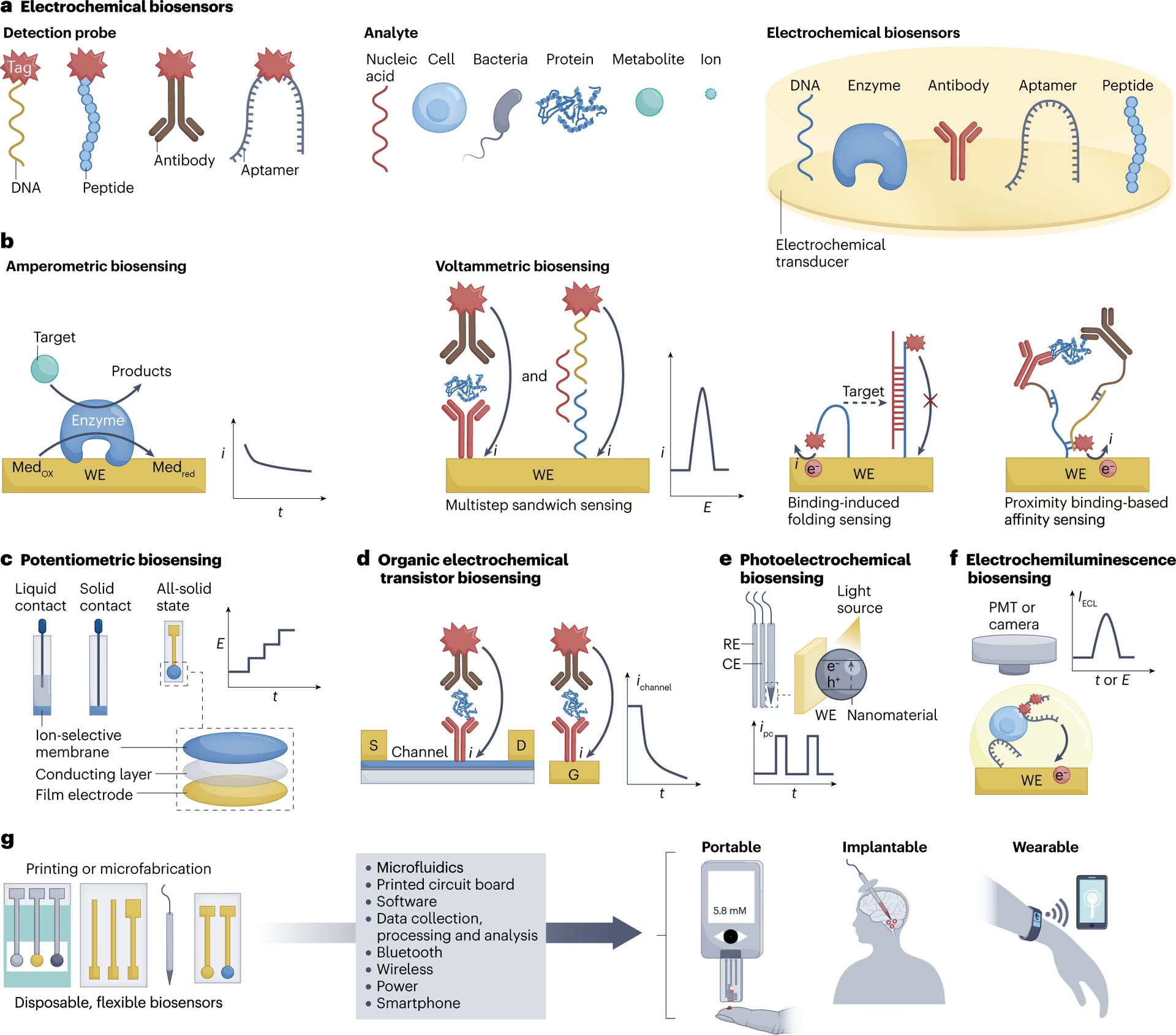
El sistema nervioso, intrínsecamente eléctrico y químico, presenta un campo de estudio natural para las técnicas electroquímicas. Estas herramientas de medición, fundamentadas en la interacción entre la electricidad y la materia, permiten a los neurocientíficos explorar y cuantificar una amplia gama de sustancias químicas clave en el entorno cerebral. Desde iones simples hasta complejos neurotransmisores, la electroquímica ofrece una ventana única para observar los procesos neuronales dinámicos.

- Un Vistazo Histórico y Pilares Fundamentales
- Principios Fundamentales de la Detección Electroquímica
- Técnicas Electroquímicas Clave en Neurociencia
- Tipos de Electrodos y Sensores
- Sustancias Detectables en el Cerebro
- Ventajas y Limitaciones de los Métodos Electroquímicos
- Desarrollos Continuos
- Comparativa: Electroquímica vs. Microdiálisis (en Neurociencia)
- Preguntas Frecuentes sobre Electroquímica en Neurociencia
Un Vistazo Histórico y Pilares Fundamentales
La aplicación de la electroquímica en el estudio del cerebro tiene una historia rica, marcada por hitos significativos. Uno de los avances cruciales fue la invención del microelectrodo de fibra de carbono por Gonon y sus colegas. Estos electrodos, que siguen siendo populares hoy en día, podían ser pretratados electroquímicamente para resolver las corrientes de oxidación registradas en el cerebro en picos distintos a lo largo del eje potencial. Estos estudios pioneros demostraron la viabilidad de desarrollar técnicas de registro electroquímico selectivas.
Otro avance importante fue la introducción de electrodos de carbono recubiertos con Nafion, un material polimérico permselectivo. Nafion es un derivado sulfonado del Teflón que, al ionizarse en ambientes acuosos, crea sitios aniónicos fijos en la membrana. Estos sitios aniónicos limitan la capacidad de las sustancias aniónicas en el cerebro (como el ascorbato, el urato y los metabolitos ácidos de los neurotransmisores monoamínicos) para alcanzar la superficie del electrodo. Esto aumenta significativamente la selectividad de las técnicas electroquímicas para sustancias catiónicas, como los propios neurotransmisores monoamínicos. Además, la naturaleza similar al Teflón de Nafion mejora la biocompatibilidad de la superficie del electrodo y disminuye el ensuciamiento durante los experimentos in vivo.
A Ralph Adams se le atribuye generalmente ser el primero en implantar un microelectrodo de carbono en el cerebro de una rata con el objetivo de medir la concentración in vivo de neurotransmisores catecolamínicos y sus metabolitos en el fluido extracelular. Estos primeros estudios revelaron rápidamente la importancia de la selectividad y la necesidad de identificar y confirmar la fuente química de las corrientes de oxidación registradas, ya que se descubrió que las catecolaminas y sus metabolitos no eran las únicas sustancias cerebrales que se oxidaban en los electrodos de carbono.
A principios de la década de 1980, Mark Wightman y sus colegas idearon las ahora conocidas coloquialmente como las "Cinco Reglas de Oro" de la electroquímica in vivo. Estas reglas son un conjunto de criterios que deben cumplirse para afirmar la identificación certera de la sustancia detectada durante las mediciones electroquímicas in vivo.
Las bases de los métodos amperométricos y voltamétricos empleados en neurociencia hoy en día se encuentran en el trabajo de Jaroslav Heyrovsky, quien recibió el Premio Nobel de Química en 1959 por el descubrimiento y desarrollo de métodos polarográficos de análisis. Heyrovsky descubrió que era posible causar la reducción de moléculas orgánicas en un electrodo de mercurio mediante la aplicación de un voltaje apropiado. La reducción generaba una corriente cuantitativamente relacionada con la concentración de la sustancia que se reducía. Además, la posición y forma de la onda polarográfica (un gráfico de la corriente observada en función del potencial aplicado) era útil para identificar la sustancia. Estos son los principios clave que subyacen al uso de métodos amperométricos y voltamétricos en neurociencia.
Principios Fundamentales de la Detección Electroquímica
En el centro de los métodos electroquímicos se encuentra un electrodo, que proporciona una superficie o interfaz donde ocurre un proceso de transferencia de carga. Este proceso da lugar a potenciales y/o corrientes que pueden medirse y relacionarse, ya sea por teoría o calibración, con la concentración de sustancias en la solución que baña el electrodo. Ampliamente hablando, estos métodos se dividen en dos grupos: mediciones que no implican corriente (métodos potenciométricos) y mediciones que implican el flujo de corriente en un electrodo bajo control de potencial (amperometría, voltametría o polarografía).
Durante una medición electroquímica, la corriente que proporciona información sobre la composición de la solución que baña el electrodo se deriva de la oxidación y reducción de los componentes de la solución en la superficie del electrodo. Cuando una molécula se oxida, los electrones fluyen de la molécula al electrodo, generando corriente. Cuando una molécula se reduce, los electrones fluyen en la dirección opuesta. El factor determinante de si el electrodo actúa como oxidante o reductor es el potencial del electrodo, que está bajo control experimental. Potenciales más negativos hacen que el electrodo sea un agente reductor más fuerte, mientras que potenciales más positivos lo convierten en un agente oxidante.
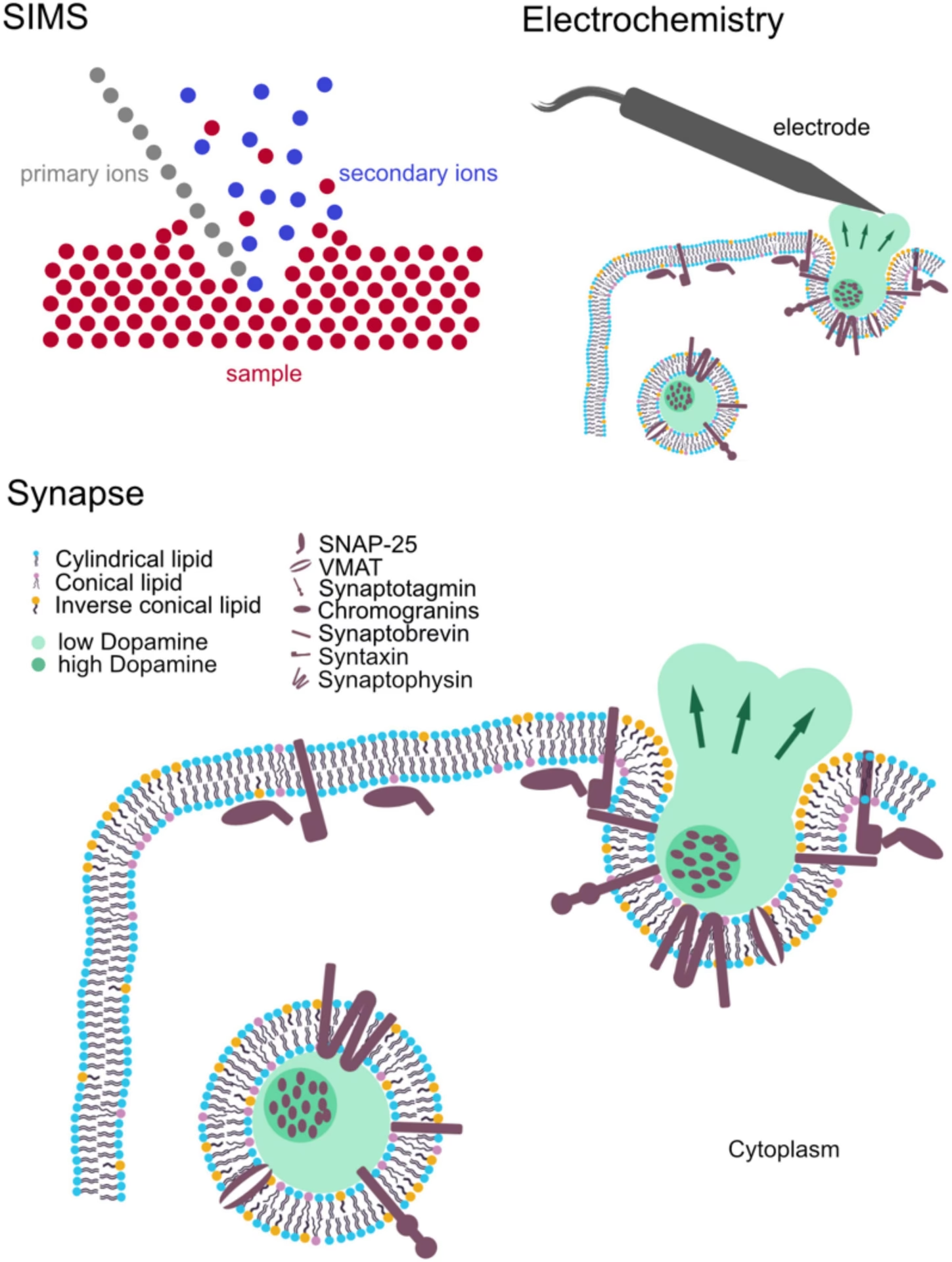
La velocidad a la que las moléculas se difunden hacia el electrodo es un determinante importante en la velocidad de las reacciones electroquímicas. Para reaccionar, las moléculas deben estar en contacto con la superficie del electrodo. La difusión, impulsada por el movimiento aleatorio y los gradientes de concentración, transporta las moléculas desde las regiones de alta concentración hacia la superficie del electrodo, donde su concentración disminuye debido a la reacción. La corriente medida está directamente relacionada con el gradiente de concentración en la superficie del electrodo, el área del electrodo, el número de electrones transferidos por molécula y la constante de Faraday.
Es importante destacar que la corriente total observada puede tener más de una contribución. Además de la corriente Faradaica (asociada a la reacción de oxidación/reducción de la sustancia), existe una corriente de carga asociada al proceso de cambiar el potencial del electrodo. Esta corriente de carga decae típicamente de forma exponencial después de un cambio de potencial. Debido a la corriente de carga, todas las mediciones electroquímicas tienen una señal de fondo distinta de cero. Esto dificulta enormemente el uso de métodos electroquímicos para medir concentraciones estáticas o basales de sustancias, ya que es difícil discriminar la contribución de la sustancia objetivo de la corriente de carga. Por esta razón, los métodos electroquímicos son más adecuados para monitorizar eventos dinámicos, como los cambios rápidos en la concentración extracelular de un neurotransmisor durante la actividad neuronal.
Técnicas Electroquímicas Clave en Neurociencia
Varias técnicas electroquímicas, basadas en diferentes formas de aplicar y variar el potencial del electrodo, se utilizan en neurociencia:
Cronoamperometría
Es uno de los métodos más simples. El potencial del electrodo se mantiene inicialmente en un potencial de reposo que no causa reacción, y luego se cambia bruscamente a un nuevo potencial para iniciar la reacción electroquímica. Se mide la corriente en función del tiempo. A medida que la reacción consume la sustancia en la superficie del electrodo, se crea un gradiente de concentración que impulsa la difusión. Con el tiempo, este gradiente se vuelve menos pronunciado y la corriente disminuye, siguiendo la ecuación de Cottrell (la corriente es proporcional a la inversa de la raíz cuadrada del tiempo). La corriente se mide típicamente después de que la corriente de carga inicial haya decaído.
Voltametría de Pulso Normal (NPV)
Implica la aplicación de una serie de pulsos de potencial, cada uno a un valor secuencialmente diferente. La corriente se mide al final de cada pulso. La gráfica de la corriente versus el potencial aplicado genera un voltagrama de forma sigmoidal. La corriente aumenta desde un valor bajo hasta una meseta una vez que el potencial causa la oxidación o reducción completa de la sustancia objetivo. El potencial donde la corriente alcanza la mitad de su valor máximo es el potencial formal de la sustancia.
Voltametría de Pulso Diferencial (DPV)
Esta técnica ofrece mayor sensibilidad y mejor resolución entre diferentes especies. La forma de onda del potencial es diferente a la de NPV; el potencial entre cada pulso no regresa completamente al potencial de reposo inicial. La corriente se muestrea inmediatamente antes de cada pulso (i_a) e inmediatamente antes de que termine (i_b). Se grafica la diferencia (i_b - i_a) versus el potencial aplicado. DPV produce un voltagrama con picos, lo que mejora los aspectos cualitativos y cuantitativos de la detección.
Voltametría Cíclica (CV)
Ampliamente utilizada en neurociencia, la CV implica barrer el potencial desde un potencial inicial a uno final y luego regresar al potencial inicial, generalmente a la misma velocidad de barrido. La corriente se mide continuamente durante el barrido y se grafica contra el potencial aplicado. Esto proporciona información voltamétrica (corriente vs. potencial) que es útil para la identificación cualitativa, ya que el voltagrama de una sustancia es generalmente único en su posición y forma de pico. Por ejemplo, el voltagrama cíclico de la dopamina se distingue fácilmente del del ascorbato. Con microelectrodos pequeños que se cargan rápidamente, son posibles velocidades de barrido de cientos de voltios por segundo, lo que permite registrar un ciclo completo en milisegundos. Esto hace que la CV sea una técnica voltamétrica muy rápida, crucial para su alta resolución temporal.
Tipos de Electrodos y Sensores
La versatilidad de la electroquímica en neurociencia se ve amplificada por la variedad de diseños de electrodos:
- Microelectrodos de Fibra de Carbono: Pequeños y populares, pueden ser pretratados para mejorar la resolución.
- Electrodos Recubiertos con Nafion: Mejoran la selectividad para cationes (como neurotransmisores monoamínicos) al repeler aniones interferentes (como ascorbato y urato), y mejoran la biocompatibilidad.
- Sensores Enzimáticos: Permiten detectar especies no electroactivas (glucosa, glutamato, lactato, colina) acoplando enzimas oxidasa al electrodo. La enzima reacciona con la sustancia objetivo y produce una especie electroactiva (comúnmente H2O2) que se detecta. A menudo utilizan películas delgadas de enzimas inmovilizadas o polímeros redox para "conectar" la enzima al electrodo.
- Electrodos Iones-Selectivos: Como los electrodos de pH, se pueden miniaturizar para aplicaciones in vivo y medir la concentración de iones específicos.
- Sensores de Moléculas Pequeñas: Electrodos diseñados para detectar O2, NO o H2O2. El sensor de O2 (Clark) se basa en la reducción de O2 en la superficie. Los sensores de NO son similares. La detección de H2O2 a menudo requiere selectividad adicional, a menudo lograda mediante enzimas.
Sustancias Detectables en el Cerebro
El sistema nervioso contiene numerosas sustancias detectables electroquímicamente, lo que explica la utilidad de estos métodos. Incluyen:
- Iones inorgánicos simples
- Neurotransmisores catecolamínicos (dopamina, norepinefrina) e indolamínicos (serotonina) y sus metabolitos. En medios fisiológicos, las catecolaminas se oxidan a orto-quinonas y la porción fenólica de la serotonina se oxida a una cetona.
- Glutamato (a menudo detectado con sensores enzimáticos)
- Óxido nítrico (NO)
- Glucosa (detectada con sensores enzimáticos)
- Lactato (detectado con sensores enzimáticos)
- Ascorbato (ácido ascórbico) y urato. El ascorbato es particularmente interesante. Está presente en altas concentraciones en el cerebro y se oxida a potenciales cercanos a los de la dopamina y norepinefrina, lo que lo convierte en un interferente común. Sin embargo, su interferencia puede controlarse aumentando la velocidad de barrido en voltametría. A pesar de ser un interferente, las mediciones electroquímicas también han revelado el papel del ascorbato como neuromodulador.
- Peróxido de hidrógeno (H2O2)
- Oxígeno (O2)
- pH (medido con electrodos ion-selectivos)
Ventajas y Limitaciones de los Métodos Electroquímicos
Las técnicas electroquímicas ofrecen beneficios significativos para la neurociencia in vivo:
- Tiempo Real: Permiten registros en tiempo real, a menudo en el rango de los microsegundos, capturando eventos neuronales rápidos.
- Alta Resolución Espacial: El uso de microelectrodos minimiza el daño al tejido cerebral durante la implantación.
- Detección de Eventos Dinámicos: Son excepcionalmente adecuadas para monitorizar cambios rápidos en la concentración de sustancias, como la liberación de neurotransmisores provocada o incluso los transitorios espontáneos de dopamina, que son virtualmente invisibles para técnicas más lentas como la microdiálisis debido a la borrosidad temporal asociada a la difusión.
Sin embargo, existen limitaciones:
- Dificultad para Medir Niveles Basales: La señal de fondo de la corriente de carga hace que sea casi imposible medir concentraciones estáticas o basales de sustancias con precisión. Son herramientas para medir cambios de concentración.
- Desafíos de Selectividad: Distinguir la sustancia objetivo de otras especies electroactivas presentes en el cerebro puede ser un desafío, aunque técnicas como el pretratamiento de electrodos, el uso de recubrimientos (Nafion) y las características voltamétricas (forma y posición del pico) ayudan a mitigar esto.
El campo de la neuroquímica in vivo también utiliza la técnica de microdiálisis, que es una técnica de muestreo donde pequeñas moléculas se recuperan del fluido extracelular cerebral. Las muestras de microdiálisis se analizan luego con métodos como cromatografía o electroforesis capilar, a menudo con detección electroquímica, espectroscopia de fluorescencia o espectrometría de masas. La microdiálisis ofrece una tremenda selectividad analítica, pero carece de la alta resolución temporal de las mediciones electroquímicas directas con microelectrodos.

Curiosamente, la electroquímica también se utiliza frecuentemente en neurociencia como detector en línea para dispositivos de muestreo y separación como la microdiálisis y la cromatografía líquida de alta resolución (HPLC), aprovechando su capacidad para medir la concentración de sustancias a medida que eluyen de la columna o membrana.
Desarrollos Continuos
El campo de la electroquímica en neurociencia sigue evolucionando. Se desarrollan continuamente nuevos métodos y diseños de electrodos, produciendo electrodos mejores, más pequeños y más rápidos, mejorando aún más esta técnica ya versátil. Casi 30 años después de los primeros experimentos in vivo de Adams y Gonon, miles de publicaciones demuestran la versatilidad y funcionalidad de la electroquímica para la detección in vivo, y el campo continúa creciendo, expandiéndose y explorando nuevas áreas neuroquímicas.
Comparativa: Electroquímica vs. Microdiálisis (en Neurociencia)
| Característica | Electroquímica (Amperometría/Voltametría) | Microdiálisis |
|---|---|---|
| Resolución Temporal | Alta (Tiempo real, microsegundos) | Baja (Minutos, borrosidad temporal) |
| Resolución Espacial | Alta (Microelectrodos, daño mínimo) | Moderada a Baja (Sonda de diálisis) |
| Selectividad | Moderada (Mejorada con recubrimientos/enzimas, pero desafiante) | Muy Alta (Análisis post-muestreo con cromatografía/MS) |
| Tipo de Evento Medido | Principalmente Dinámico (Cambios rápidos, transitorios) | Basal y Dinámico (Pero eventos rápidos se "desdibujan") |
Preguntas Frecuentes sobre Electroquímica en Neurociencia
¿Qué tipos de sustancias se pueden detectar con electroquímica en el cerebro?
Se puede detectar una amplia gama de sustancias, incluyendo iones inorgánicos, neurotransmisores (como dopamina, norepinefrina, serotonina) y sus metabolitos, glutamato, óxido nítrico (NO), glucosa, lactato, ascorbato, urato, peróxido de hidrógeno (H2O2), oxígeno (O2) y cambios de pH.
¿Por qué se prefieren los métodos electroquímicos para estudiar eventos rápidos en el cerebro?
Los métodos electroquímicos, particularmente las técnicas voltamétricas rápidas como la voltametría cíclica, ofrecen una muy alta resolución temporal (en el rango de los microsegundos a milisegundos) y pueden registrar cambios en la concentración de sustancias en tiempo real, lo que es esencial para capturar la dinámica rápida de la señalización neuronal.
¿Qué es un microelectrodo de fibra de carbono y por qué es importante?
El microelectrodo de fibra de carbono fue un desarrollo clave que permitió las mediciones electroquímicas in vivo en el cerebro. Su pequeño tamaño minimiza el daño al tejido, y su superficie puede ser modificada electroquímicamente o recubierta (por ejemplo, con Nafion) para mejorar la selectividad y la resolución de la señal.
¿Cómo ayuda el recubrimiento de Nafion en los electrodos?
El Nafion es un recubrimiento polimérico que contiene sitios aniónicos fijos. Estos sitios repelen sustancias aniónicas como el ascorbato y el urato, que a menudo interfieren con la detección de neurotransmisores catiónicos como la dopamina. Al repeler estos aniones, el Nafion aumenta la selectividad del electrodo para los neurotransmisores.
¿Pueden los métodos electroquímicos medir la concentración basal (en reposo) de una sustancia en el cerebro?
Es difícil medir con precisión las concentraciones basales con los métodos electroquímicos típicos debido a la presencia de una señal de fondo significativa (corriente de carga). Estas técnicas son inherentemente más adecuadas para medir los cambios dinámicos de concentración que ocurren durante la actividad neuronal o la estimulación.
Si quieres conocer otros artículos parecidos a Electroquímica Aplicada a la Neurociencia puedes visitar la categoría Neurociencia.