El sistema nervioso es una red intrincada que nos permite interactuar con el mundo y sentir nuestro propio cuerpo. Dentro de esta red, los nervios sensoriales desempeñan un papel fundamental al transmitir información desde la periferia hasta el cerebro. Un componente clave en esta vía es el Ganglio de la Raíz Dorsal, o DRG por sus siglas en inglés (Dorsal Root Ganglion).
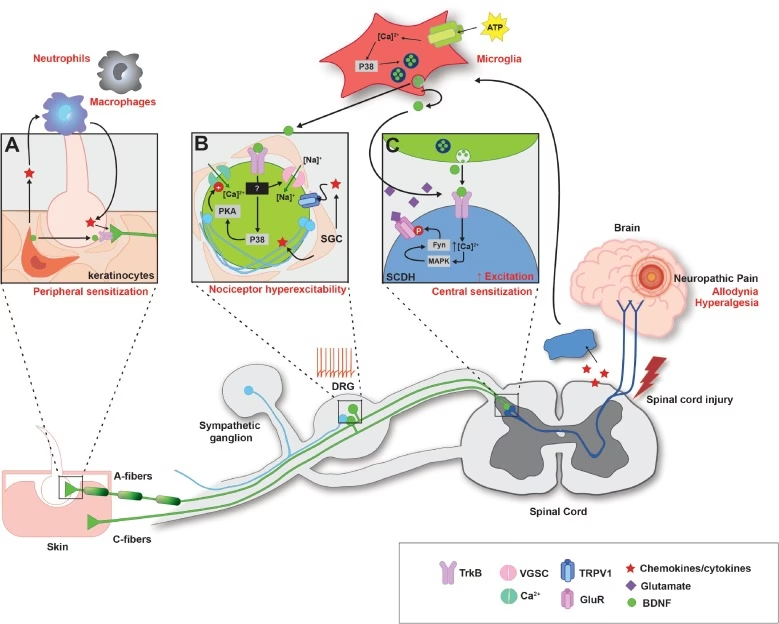
Los ganglios de la raíz dorsal son estructuras vitales del sistema nervioso periférico que actúan como estaciones de relevo para las señales sensoriales. Se originan en la raíz dorsal de los nervios espinales y son los encargados de llevar mensajes neuronales sensoriales, como el dolor, la temperatura, el tacto y la vibración, desde los receptores en la periferia del cuerpo hacia el sistema nervioso central (SNC) para su procesamiento y respuesta. Su ubicación anatómica, justo fuera de la médula espinal y dentro del foramen intervertebral, los convierte en un punto estratégico y, como se ha descubierto en las últimas décadas, un actor crucial en el desarrollo y mantenimiento del dolor crónico.
El Ganglio de la Raíz Dorsal (DRG): Portal Sensorial Clave
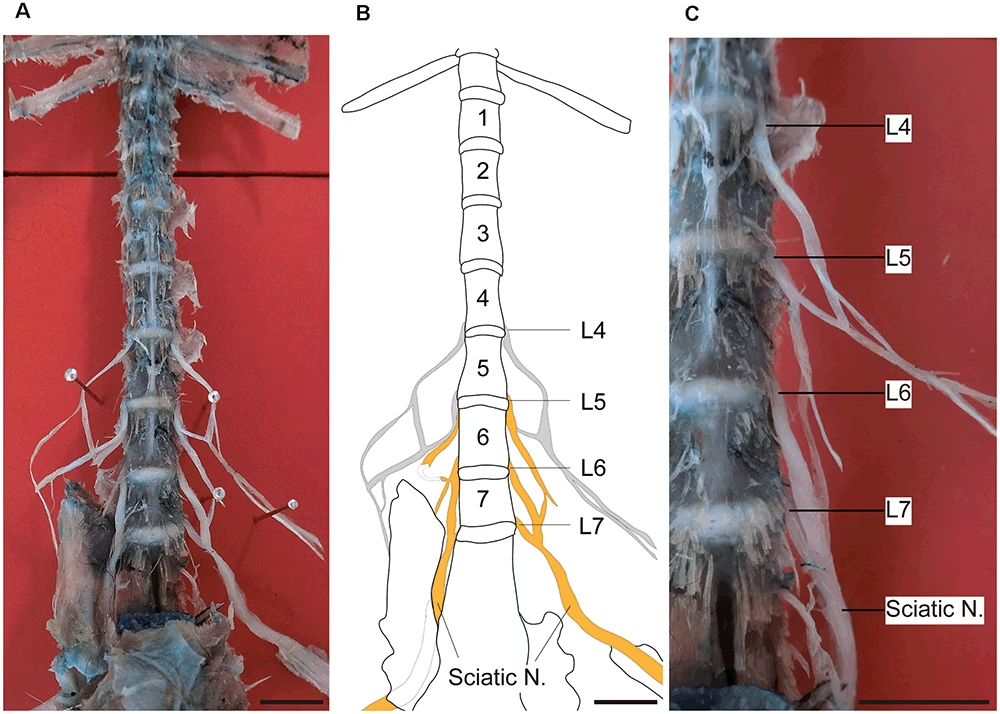
Anatómicamente, el DRG es un ensanchamiento en la raíz dorsal del nervio espinal. Hay un par de DRG (uno a cada lado) en cada nivel vertebral, desde el cuello hasta el sacro. Estas estructuras están alojadas dentro de las estructuras óseas fijas (neuroforamen) y se encuentran dentro de la vaina dural.
Estructura Intrincada para la Sensación
El DRG es fundamentalmente una colección de somas (cuerpos celulares) de las neuronas sensoriales primarias (NSP). En cada DRG pueden encontrarse hasta 15,000 neuronas en los niveles que inervan las extremidades. Los diámetros de estos somas varían considerablemente, desde 20 hasta 150 μm.
Estas neuronas se pueden clasificar históricamente según la tinción y la densidad de neurofilamentos en neuronas "grandes-claras" (generalmente neuronas A, que retransmiten información no nociva, como el tacto ligero y la propiocepción) y neuronas "pequeñas-oscuras" (generalmente neuronas C, que retransmiten señales dolorosas y de temperatura).
Los axones de estas neuronas se agrupan en raíces/nervios que contienen una mezcla de fibras con distinta excitabilidad. Las fibras sensoriales incluyen:
- Fibras Aβ: Mielinizadas, de gran diámetro y alta velocidad de conducción. Transmiten información de bajo umbral, como el tacto y la vibración.
- Fibras Aδ: Ligeramente mielinizadas, de diámetro mediano y velocidad de conducción moderada. Transmiten detalles nociceptivos agudos (temperatura, mecánicos, químicos).
- Fibras C: No mielinizadas, de pequeño diámetro y baja velocidad de conducción. Transmiten input nociceptivo que contribuye a un dolor secundario más difuso y profundo después de una lesión.
Todas estas fibras transportan información sensorial periférica hacia su soma respectivo en el DRG.
Además de las neuronas, los DRG albergan una gran población de células gliales, aproximadamente ocho veces más glía que neuronas. Las células gliales satélite son una forma especializada de glía que envuelve a cada NSP individualmente, creando una unidad funcional independiente y separada físicamente de otros somas neuronales.
Las neuronas del DRG son neuronas pseudo-unipolares. Esto significa que un solo axón emerge del cuerpo celular y luego se bifurca en una unión en forma de T. La porción periférica del axón se extiende hasta las terminaciones receptoras en la periferia y es responsable de la señalización aferente (hacia el SNC). La porción central del axón se extiende hacia el sistema nervioso central, ramificándose considerablemente en la médula espinal y terminando en sinapsis en las neuronas del asta dorsal ipsilateral o contralateral, redes de interneuronas inhibitorias y otros objetivos. Algunas fibras del DRG incluso atraviesan la longitud de las columnas dorsales para llegar a los núcleos de las columnas dorsales en el tronco encefálico. Estas últimas, típicamente axones centrales de gran diámetro de NSP Aβ, son las que se reclutan más comúnmente en la estimulación de la médula espinal (SCS).
Una sola NSP puede, por lo tanto, abarcar una anatomía dramáticamente extensa, conectando la periferia más distante con el tronco encefálico.
Los DRG también están íntimamente conectados con la cadena simpática a través de los nervios rami communicantes. Los rami communicantes blancos sirven como conducto para las aferentes discogénicas, transmitiendo señales de dolor espinal intrínseco al DRG.
La ubicación exacta de los DRG puede variar ligeramente según el nivel vertebral. Estudios de resonancia magnética (MRI) en sujetos asintomáticos han mostrado que la mayoría se encuentran en el foramen intervertebral, aunque un pequeño porcentaje puede estar en regiones intraspinales o extraforaminales (laterales), especialmente en los niveles L1 y L5. Los DRG sacros, a diferencia de los torácicos y lumbares, pueden ser intracanales (mediales) o intraforaminales (laterales).
La estructura interna del DRG, aunque poblada por distintos tipos de neuronas, generalmente no muestra un patrón topográfico organizado claro para la mayoría de las neuronas maduras, aunque se han observado patrones transitorios durante el desarrollo y agrupaciones dispersas de subtipos neuronales.
La Función del DRG: Transmisión y Modulación Sensorial
La función principal de las neuronas sensoriales periféricas en el DRG es conducir potenciales de acción desde las terminaciones sensoriales periféricas hasta las terminales centrales para su transmisión al SNC. Los potenciales de acción implican corrientes iónicas a través de membranas excitables, con despolarización de sodio seguida de repolarización de potasio y un aumento del calcio intracelular, un segundo mensajero crucial para la excitabilidad y la liberación de neurotransmisores.
Normalmente, los potenciales de acción se generan en las terminaciones sensoriales periféricas en respuesta a estímulos. Los axones transducen señales, mientras que los cuerpos celulares en el DRG apoyan el metabolismo y actúan como "guardianes" o generadores de novo de la transmisión de señales. Los potenciales de acción generados periféricamente pueden causar despolarización de los cuerpos celulares del DRG.
Las conexiones dentro del DRG (conexiones DRG-T) normalmente impiden la propagación directa de los potenciales de acción generados periféricamente, actuando como filtros. Sin embargo, las neuronas del DRG tienen propiedades de membrana especializadas y, aunque están separadas por células gliales satélite, casi todas experimentan excitación subumbral que puede activar otros cuerpos celulares cercanos. Esto se conoce como "despolarización cruzada" o "excitación cruzada", donde la estimulación de los axones de neuronas vecinas en el mismo ganglio puede despolarizar hasta el 90% de las neuronas del DRG.
El campo receptivo y la ramificación axonal de las neuronas del DRG son muy detallados. Una sola neurona gelatinosa puede recibir input de hasta 4 raíces dorsales diferentes. A nivel del nervio espinal, antes del DRG, las fibras C y Aδ pueden inervar una sola área de la piel antes de divergir y luego converger nuevamente en una sola neurona gelatinosa.
Desarrollo Embrionario del DRG
El desarrollo embrionario de los ganglios de la raíz dorsal, al igual que gran parte del sistema nervioso periférico, comienza con la formación del tubo neural y el surgimiento de las células de la cresta neural en sus márgenes. Estas células de la cresta neural migran ventralmente a diversas ubicaciones y se diferencian en los componentes del sistema nervioso periférico, incluyendo los DRG.

Las células del DRG se desarrollan aproximadamente a las 4 semanas postconcepción a partir de la migración de la cresta neural. Entre las semanas siete y ocho, comienzan a aparecer las primeras neuronas bipolares. Alrededor de las 11 semanas, empiezan a formarse neuronas unipolares (pseudo-unipolares) con un solo proceso amplio y orgánulos bien desarrollados. La aparición de la capacidad de respuesta refleja desde la piel de la extremidad superior se correlaciona con la aparición de estas neuronas pseudo-unipolares.
Dado que el DRG surge de las células de la cresta neural en lugar del tubo neural, a veces se le considera como materia gris de la médula espinal que ha migrado a la periferia. Los estudios sugieren que las células de la cresta neural requieren una señal del SNC para sobrevivir y diferenciarse en el DRG, incluso en las primeras horas después de iniciar la migración.
Irrigación y Permeabilidad Única
La irrigación sanguínea del DRG proviene de dos plexos arteriales interconectados, superficial y profundo, que surgen de ramas radiculares de las arterias segmentarias. Es notable que el DRG es una excepción a la restricción de permeabilidad que caracteriza a la mayor parte del sistema nervioso periférico. Mientras que la mayoría del SNP tiene una baja permeabilidad entre la sangre y el tejido nervioso, similar a la barrera hematoencefálica, el DRG exhibe una alta permeabilidad debido a su interfaz hemato-nerviosa más laxa.
Esta organización vascular proporciona al DRG humano un suministro sanguíneo robusto, esencial para las neuronas con procesos largos y alta demanda energética necesaria para la producción y el transporte de receptores, canales iónicos y proteínas estructurales. Además, su alta permeabilidad tiene implicaciones clínicas, ya que lo hace susceptible a neurotóxicos de bajo y alto peso molecular, así como a metabolitos tóxicos en neuropatías inducidas por fármacos.
El drenaje venoso se realiza principalmente a través de plexos venosos peri-ganglionares que desembocan en las venas intervertebrales.
Variantes Fisiológicas y Canales Iónicos
El conocimiento sobre las variantes fisiológicas del DRG en humanos es limitado, aunque se han propuesto varios modelos en ratas para explicar estos fenómenos. Las variantes en los canales iónicos dependientes de voltaje SCN9A, Na(v)1.7 y Troy son sitios comunes de investigación actual en ratas. Algunas variantes pueden influir considerablemente en la excitabilidad de las neuronas del DRG.
Por ejemplo, la variante 1739V del canal Na(v)1.7 se ha identificado en algunos pacientes con disfunción autonómica y dolor neuropático, asociándose a una alteración de la inactivación lenta dentro de las neuronas del DRG, lo que lleva a hiperexcitabilidad.
El DRG y el Dolor Crónico: Un Vínculo Crucial
El papel del DRG en el desarrollo y mantenimiento del dolor crónico está bien establecido. Después de una lesión nerviosa periférica, los DRG experimentan cambios drásticos en su fenotipo y función, convirtiéndose a menudo en la fuente de señales de dolor hacia el cerebro.
El DRG como Fuente de Dolor Neuropático
Tras una lesión nerviosa aferente periférica, se inicia una cascada inmune que involucra leucocitos, macrófagos, linfocitos T, células gliales y células de Schwann. Se observa un aumento en el número de linfocitos T y macrófagos en los DRG de nervios periféricos lesionados meses después de la lesión. La infiltración de estas células inflamatorias probablemente resulta en la liberación prolongada de citoquinas excitatorias, contribuyendo al dolor persistente a pesar de la resolución de la lesión original.
Las células gliales, en particular las células gliales satélite, también responden a la lesión nerviosa periférica proliferando y liberando mediadores inflamatorios. La axotomía periférica causa un aumento en la expresión de factores neurotróficos en las células gliales satélite que rodean los somas neuronales sensoriales en el DRG. Estos neutrófilos dentro del DRG pueden inducir alodinia mecánica persistente y causar dolor neuropático después de una lesión nerviosa periférica.
La consecuencia funcional de estos cambios es la sensibilización y la hiperexcitabilidad de las neuronas del DRG, lo que conduce al dolor neuropático. Después de una lesión, las corrientes de calcio dependientes de voltaje de bajo umbral se reducen significativamente. La pérdida de esta corriente de calcio interna y la reducción del desplazamiento extracelular de potasio pueden contribuir a la hiperexcitabilidad post-lesión. Además, la alodinia puede asociarse con niveles elevados de norepinefrina.
Las neuronas del DRG normales generan patrones de oscilación sinusoidal a través de mecanismos sensibles al voltaje, cuya frecuencia aumenta después de una lesión nerviosa. Cuando estas oscilaciones alcanzan un umbral, se generan potenciales de acción. La regulación al alza de los canales de iones de sodio transmembrana y el aumento del transporte de iones de sodio desempeñan un papel significativo en el aumento de las oscilaciones y, por lo tanto, en la descarga ectópica asociada al dolor neuropático crónico.
También se ha demostrado que la lesión del DRG aumenta el número de fibras Aβ que terminan en el asta dorsal de la médula espinal. Se generan potenciales de acción espontáneos en el DRG después de una lesión y daño nervioso periférico. Sin embargo, no ocurren en lesiones proximales al DRG. Muchas descargas ectópicas se originan en fibras Aβ, que normalmente transmiten sensaciones táctiles y vibratorias. Después de una lesión nerviosa, ocurren cambios electrofisiológicos que permiten a estas fibras transmitir dolor. Estas fibras Aβ pueden contribuir significativamente a la sensibilización central.
El DRG como Objetivo Terapéutico
Dado su papel central en la transmisión sensorial y su implicación en el dolor crónico, el DRG se ha convertido en un objetivo terapéutico prometedor. Desde las primeras técnicas de infiltración anestésica, se han desarrollado numerosas intervenciones dirigidas a esta estructura.
Intervenciones Quirúrgicas y de Ablación
Históricamente, se han utilizado técnicas como la rizotomía dorsal o la gangliectomía (extirpación del ganglio) para tratar el dolor. Sin embargo, la gangliectomía, una técnica neuroquirúrgica irreversible, ha demostrado ser menos efectiva a largo plazo y puede incluso producir dolor en otras áreas. La lesión de la zona de entrada de la raíz dorsal (DREZ), aunque adyacente, es un objetivo relacionado.
Actualmente, las técnicas de ablación o modulación del DRG mediante radiofrecuencia son más comunes debido a su enfoque no quirúrgico y mínimamente invasivo. La radiofrecuencia continua térmica y la radiofrecuencia pulsada se utilizan para modular la función neuronal del DRG. La ablación por radiofrecuencia es particularmente útil para áreas de difícil acceso como la parte baja de la espalda o el pie.
Neuromodulación: Estimulación del DRG
En la última década, la estimulación eléctrica del DRG ha surgido como una opción viable y efectiva para la terapia de neuromodulación en el tratamiento del dolor crónico. Los estimuladores eléctricos del DRG implican la colocación de electrodos cerca del ganglio para aplicar impulsos eléctricos a los somas de las neuronas sensoriales primarias.
La estimulación del DRG ha demostrado ser particularmente eficaz para el dolor en áreas como el pie, la ingle, el dolor lumbar axial, el dolor discogénico, el dolor del miembro fantasma, la neuralgia postherpética, el síndrome de dolor regional complejo (CRPS) o causalgia, la neuropatía periférica diabética y el dolor perineal. Estas áreas son a menudo difíciles de tratar eficazmente con la estimulación convencional de la médula espinal (SCS) porque las fibras de las columnas dorsales relevantes pueden ser inaccesibles o requerir amplitudes de estimulación que activan dolorosamente las raíces nerviosas.
El estudio ACCURATE, un ensayo controlado aleatorizado que comparó la estimulación del DRG con la SCS convencional, demostró que los resultados con la estimulación del DRG fueron estadísticamente superiores en alivio del dolor a los 3 meses, y esta superioridad se mantuvo durante 12 meses. La estimulación del DRG ofreció una mayor especificidad de la estimulación para las áreas dolorosas, menor variación en la intensidad de la estimulación con los cambios posturales y, en algunos sujetos, la capacidad de ofrecer analgesia sin parestesias.
Aunque la SCS tiene un lugar establecido en el tratamiento avanzado del dolor, la estimulación del DRG ha mostrado beneficios en afecciones que antes no estaban bien atendidas por la SCS tradicional, ofreciendo un alivio duradero, reportado hasta por 3 años.
Enfoques Farmacológicos Dirigidos
Debido a la alta vascularización del DRG y la ausencia de una barrera protectora similar a la hematoencefálica, los DRG pueden ser fácilmente accesibles mediante enfoques de administración de fármacos sistémicos y locales. Esto abre la puerta a estrategias terapéuticas más seguras que minimicen los efectos secundarios en el SNC.
Actualmente, se están investigando y desarrollando tratamientos que apuntan selectivamente a moléculas involucradas en los mecanismos del dolor que se expresan exclusivamente o están enriquecidos en las neuronas del DRG. Un grupo importante de objetivos son los canales iónicos, como los canales de potencial receptor transitorio (TRP), incluyendo TRPV1 y TRPA1, y los canales de sodio dependientes de voltaje (Nav), especialmente Nav1.7, Nav1.8 y Nav1.9, que son únicos en las neuronas periféricas.
El uso de capsaicina (un agonista de TRPV1) como analgésico tópico es un ejemplo de targeting periférico. Se están desarrollando antagonistas de TRPV1 y TRPA1, buscando superar los efectos secundarios de las primeras generaciones. También se exploran enfoques indirectos, modulando estos canales a través de proteínas de andamiaje (como SHANK3 para TRPV1) o receptores acoplados a proteínas G (GPCRs), utilizando mediadores lipídicos pro-resolución (resolvinas, protectinas) derivados de ácidos grasos omega-3.
La administración local, como las inyecciones perineuronales o intraganglionares, o las inyecciones en los nervios periféricos, ofrecen una especificidad regional mejorada. Los bloqueos nerviosos selectivos, por ejemplo con anestésicos locales como la lidocaína, o la administración de corticosteroides cerca de un DRG lesionado, pueden aliviar el dolor con menos efectos sistémicos.
Un avance notable es la estrategia de bloqueo nervioso selectivo mediante el uso de derivados de anestésicos locales cargados, como QX-314, que solo pueden entrar en neuronas específicas a través de canales activados. Al co-administrar QX-314 con agonistas de canales específicos (como capsaicina para TRPV1 o flagelina para TLR5), se puede lograr un bloqueo selectivo de las neuronas que expresan esos canales, aliviando tipos específicos de dolor (por ejemplo, alodinia mecánica).
Terapia Génica y Celular
Emergen nuevas terapias para el dolor crónico que utilizan terapia génica y celular dirigidas al DRG. La terapia génica, a menudo administrada mediante vectores virales modificados (como AAV, HSV-1 o lentivirus), permite la supresión (knockdown) o inserción (knock-in) estable de genes en neuronas específicas del DRG. Estos enfoques buscan modificar la función neuronal para reducir la hiperexcitabilidad o promover la liberación de sustancias analgésicas.
Existen desafíos, como la capacidad de empaquetamiento limitada de algunos vectores, la transfección de tejidos no deseados y la imprevisibilidad de los efectos a largo plazo. Las estrategias con ARN de interferencia pequeño (siRNA) ofrecen un knockdown temporal de genes, superando las limitaciones de la terapia génica permanente, pero requieren métodos de entrega eficientes para superar la barrera de la membrana celular (usando polímeros, lípidos o péptidos penetrantes de células).
La terapia celular, particularmente el uso de células madre estromales de médula ósea (BMSCs), también muestra un gran potencial. Las BMSCs pueden suprimir el dolor inflamatorio y neuropático y, sorprendentemente, muestran un reclutamiento selectivo hacia los tejidos del DRG lesionados a través de un mecanismo de señalización (eje CXCL12/CXCR4). Una vez allí, sobreviven a largo plazo y ejercen un efecto analgésico persistente, principalmente a través de un papel inmunomodulador y la liberación de factores antiinflamatorios como TGF-β1. Las BMSCs podrían servir como vectores de entrega para otras sustancias analgésicas o antiinflamatorias, ofreciendo un enfoque localizado y de bajo riesgo.
| Tipo de Fibra | Mielinización | Diámetro | Velocidad Conducción | Sensación Principal |
|---|---|---|---|---|
| Aβ | Sí | Grande | Rápida | Tacto, Vibración (No Dolor) |
| Aδ | Parcial | Mediano | Moderada | Dolor Agudo, Temperatura, Mecánica |
| C | No | Pequeño | Lenta | Dolor Difuso/Profundo, Temperatura, Química |
Preguntas Frecuentes (FAQs)
¿Cuál es la función principal del DRG?
La función principal del Ganglio de la Raíz Dorsal es transmitir información sensorial (dolor, temperatura, tacto, vibración, propiocepción) desde los receptores en la periferia del cuerpo hacia el sistema nervioso central (médula espinal y cerebro) para su procesamiento.
¿El DRG forma parte del sistema nervioso autónomo?
No, el DRG forma parte del sistema nervioso sensorial periférico. Está compuesto por neuronas sensoriales primarias. Sin embargo, está íntimamente conectado con la cadena simpática, que es parte del sistema nervioso autónomo, a través de los rami communicantes. Esta conexión permite que las señales, incluyendo las de dolor, interactúen entre ambos sistemas.
¿Por qué el DRG es importante en el dolor crónico?
El DRG es crucial en el dolor crónico porque, después de una lesión nerviosa o tisular, las neuronas del DRG pueden sufrir cambios moleculares y funcionales que las hacen hiperexcitables y capaces de generar señales de dolor espontáneas o exageradas. Actúa como una fuente de señales de dolor que se transmiten al SNC, contribuyendo al mantenimiento del dolor a largo plazo.
¿Qué tratamientos existen dirigidos al DRG?
Existen diversas opciones terapéuticas dirigidas al DRG para tratar el dolor crónico. Estas incluyen intervenciones de ablación (como la radiofrecuencia continua o pulsada), técnicas de neuromodulación como la estimulación eléctrica del DRG, enfoques farmacológicos que apuntan a canales iónicos o receptores específicos en las neuronas del DRG, terapia génica para modificar la expresión de genes relacionados con el dolor y terapias celulares que utilizan células madre para modular la inflamación y promover la analgesia.
En resumen, el Ganglio de la Raíz Dorsal es una estructura sensorial fundamental y compleja. Su papel como puerta de entrada de la información sensorial al SNC y su implicación en el dolor neuropático lo convierten en un área de intensa investigación. Los avances en técnicas como la estimulación del DRG y las terapias dirigidas están abriendo nuevas y prometedoras vías para aliviar el dolor crónico que afecta a millones de personas en todo el mundo.
Si quieres conocer otros artículos parecidos a DRG: El Portal Sensorial y el Dolor Crónico puedes visitar la categoría Neurociencia.
