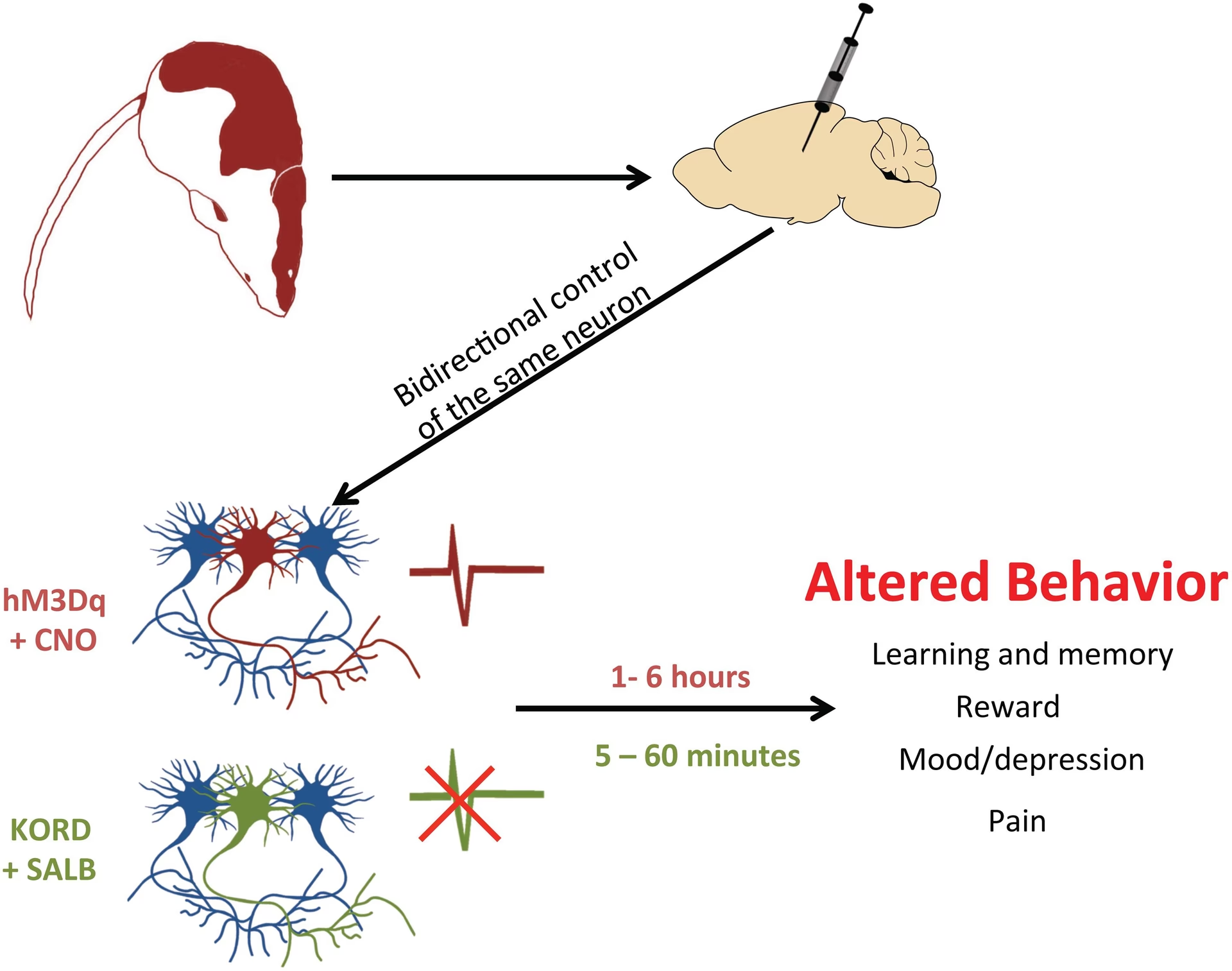
Comprender el funcionamiento del cerebro, tanto en estados normales como patológicos, exige desentrañar cómo la señalización celular dicta sus funciones. En este contexto, las tecnologías chemogenéticas emergen como plataformas invaluable para manipular la transducción de señales neuronales y no neuronales de manera específica para un tipo celular, incluso en animales que se mueven libremente. Entre ellas, las herramientas basadas en DREADDs (Designer Receptors Exclusively Activated by Designer Drugs - Receptores Diseñados Exclusivamente Activados por Fármacos Diseñados) son ampliamente empleadas por neurocientíficos para identificar los circuitos y las señales celulares que subyacen al comportamiento, las percepciones, las emociones, los impulsos innatos y las funciones motoras en una variedad de especies.
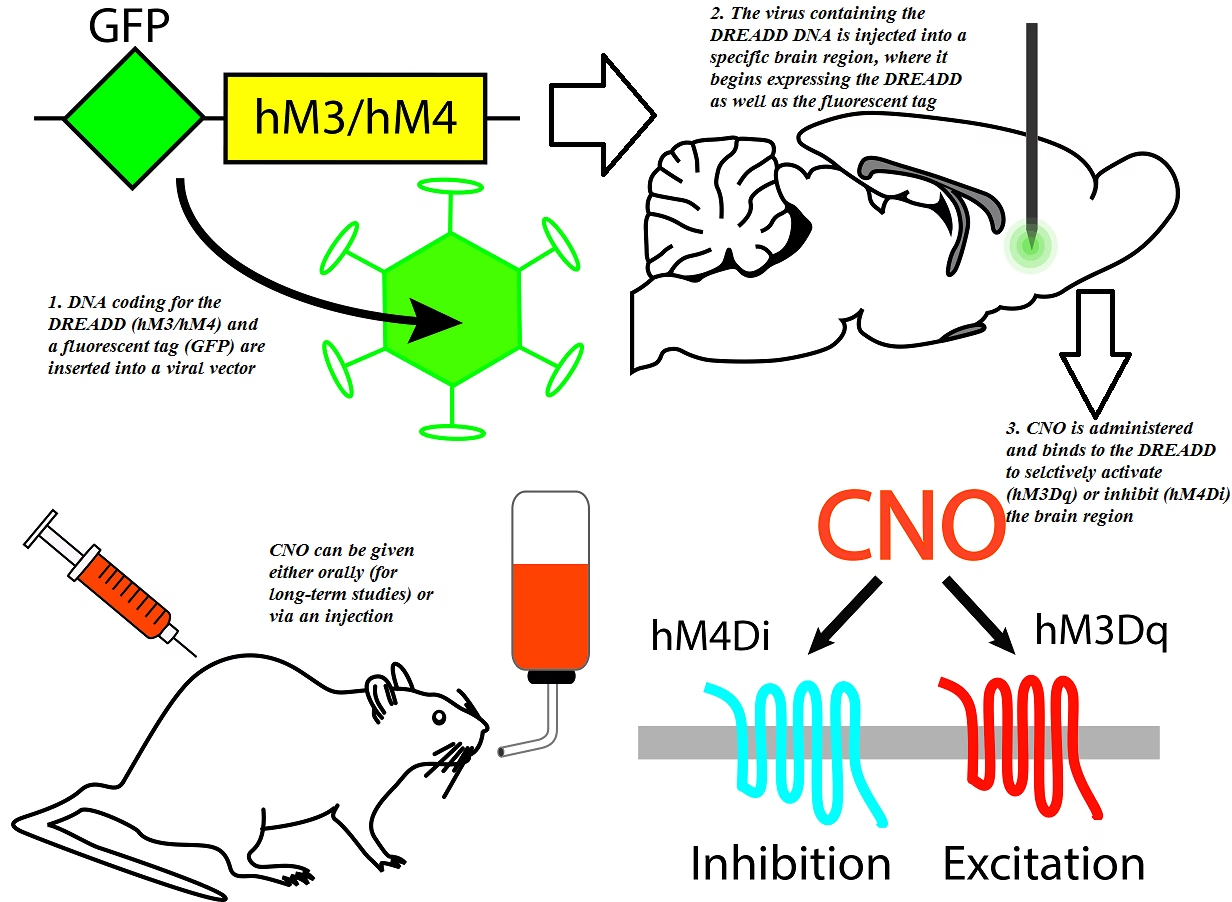
La chemogenética se define como un método mediante el cual se diseñan proteínas para interactuar con actuadores químicos de molécula pequeña previamente no reconocidos. A lo largo de las últimas dos décadas, se han inventado numerosas plataformas chemogenéticas que han demostrado ser útiles para biólogos en general y, de manera destacada, para neurocientíficos. Se han modificado chemogenéticamente diversas clases de proteínas, incluyendo quinasas, enzimas no quinasas, receptores acoplados a proteínas G (GPCRs) y canales iónicos activados por ligando. De estas, las DREADDs, que son GPCRs diseñados, son las más utilizadas hasta la fecha en neurociencia.
Mecanismos de Acción de las DREADDs
Para comprender el uso adecuado de la tecnología DREADD, es fundamental conocer los conceptos básicos de la farmacología molecular y la señalización de los GPCRs. Según los modelos clásicos, los GPCRs existen en múltiples estados dependientes e independientes del ligando, que van desde 'completamente inactivos' hasta 'parcialmente activos', 'completamente activos' y 'complejos de señalización'. Los GPCRs son modulados por ligandos y pueden interactuar tanto con proteínas G heterotriméricas como con β-arrestinas.
Existen múltiples estados inactivos (o 'estado basal') que pueden ser estabilizados por ligandos o incluso ocurrir en ausencia de ligandos. Los iones sodio estabilizan el estado basal ejerciendo una modulación alostérica negativa. Los fármacos que estabilizan estos estados basales funcionan como agonistas inversos. Tanto los agonistas completos como los parciales estabilizan el estado activo y promueven la formación de un complejo de señalización, como el 'complejo ternario', que consta del receptor activo, un agonista y la proteína G heterotrimérica.
Además de la activación e inactivación inducida por ligandos, los GPCRs también pueden isomerizarse espontáneamente a un estado activo en ausencia de ligando. Este estado activo sin ligando se denomina 'actividad constitutiva'. Un GPCR con actividad constitutiva tiene más probabilidades de existir en el estado activo y, por lo tanto, de interactuar espontáneamente con las proteínas G para formar un complejo de señalización en ausencia de ligando.
Los GPCRs también interactúan con las arrestinas para formar complejos de señalización alternativos. Los GPCRs con altos niveles de actividad basal pueden interactuar espontáneamente con β-arrestina en ausencia de agonista. La interacción de los GPCRs con β-arrestina también representa un estado 'desensibilizado' o inactivo para la señalización de la proteína G. A nivel molecular, cuando los GPCRs son activados por agonistas, pueden acoplarse a proteínas G o a arrestinas, pero no a ambas simultáneamente. El sesgo hacia un estado particular depende tanto del contexto celular como del ligando disponible.
Las DREADDs se basan en GPCRs modificados. Las variantes más utilizadas derivan de receptores muscarínicos humanos modificados. Por ejemplo, la hM3Dq es una variante modificada del receptor muscarínico M3 humano acoplado a la proteína Gq. Cuando se activa por su ligando diseñado, la hM3Dq desencadena la cascada de señalización de la proteína Gq, lo que típicamente lleva a la excitación neuronal (aumento del calcio intracelular y disparo en ráfagas). Por otro lado, la hM4Di es una variante modificada del receptor muscarínico M4 humano acoplado a la proteína Gi. Su activación desencadena la cascada de señalización de la proteína Gi, lo que generalmente resulta en la inhibición neuronal (reducción del cAMP y activación de canales de potasio rectificadores de entrada como los GIRKs, así como inhibición de canales de calcio dependientes de voltaje).
Existe también una variante más reciente, la KORD (receptor kappa-opioide DREADD), que es un receptor kappa-opioide modificado acoplado a la proteína Gi. Es insensible a su ligando endógeno (dinorfina) pero se activa exclusivamente por la salvinorina B (SALB), un análogo semisintético inactivo. La activación de KORD por SALB también produce inhibición neuronal, a menudo con una cinética más rápida que la hM4Di activada por CNO.
El Ligando Clave: CNO y Otros
La mayoría de las DREADDs son selectivamente sensibles a compuestos sintéticos. El ligando más común es el CNO (clozapine N-oxide - N-óxido de clozapina). Aunque el CNO es un metabolito del antipsicótico atípico clozapina, se considera biológicamente inerte en roedores y tiene una afinidad despreciable por los blancos nativos relevantes en el sistema nervioso central de estas especies. Tras la administración periférica de CNO, los niveles plasmáticos alcanzan su pico en 30 minutos y disminuyen drásticamente en las 2 horas siguientes. Sin embargo, los efectos conductuales pueden persistir hasta por 6 horas. Esto hace que la tecnología DREADD sea adecuada para estudios que requieren una modulación neuronal prolongada (horas a días).
Es importante señalar que en humanos, primates no humanos y conejillos de indias, una pequeña fracción del CNO puede ser metabolizada de nuevo a clozapina. Esta retroconversión limita el alcance y el potencial translacional de las DREADDs dependientes de CNO en estas especies. La aparición de la KORD, activada por SALB, aborda parcialmente esta limitación al proporcionar un ligando alternativo.
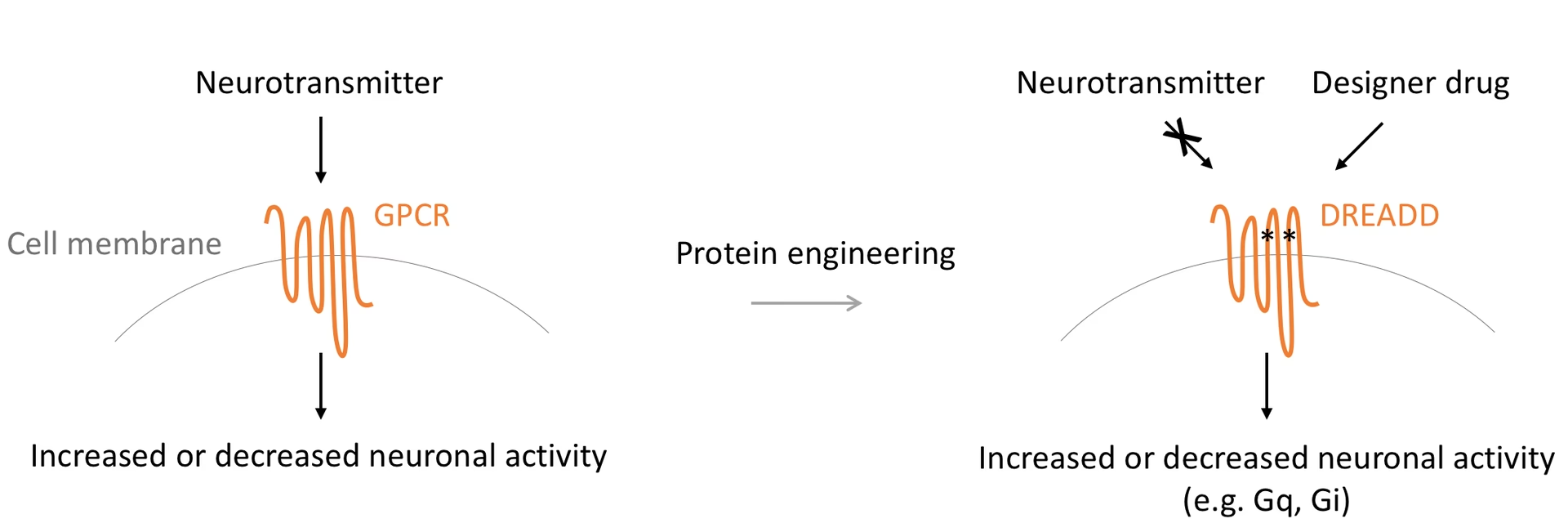
Los ligandos DREADD pueden administrarse de diversas formas: inyección (intraperitoneal, subcutánea, intracraneal), mezclados en la comida o el agua de bebida. La administración por comida o agua es conveniente para estudios a largo plazo, pero menos precisa en cuanto a la dosis ingerida. Las bombas osmóticas implantadas ofrecen una alternativa para una liberación sistémica controlada y prolongada.
Consideraciones Farmacológicas
Una preocupación importante con las tecnologías chemogenéticas es la posibilidad de que altos niveles de expresión de la proteína diseñada tengan efectos en ausencia de activación química (actividad basal constitutiva). Aunque no se han reportado fenotipos basales para las DREADDs más comunes (hM3Dq, hM4Di, GsD) incluso con expresión a niveles altos y de por vida en algunos estudios, es prudente expresar las DREADDs al nivel más bajo compatible con el diseño experimental. Esto se puede lograr usando un menor título viral, un promotor más débil o modificando la expresión post-transcripcional. Según la ley de acción de masas, disminuir la concentración del receptor disminuye la probabilidad de transiciones al estado activo y de señalización en ausencia de ligando.
Otra consideración es la desensibilización y regulación a la baja del receptor tras la dosificación repetida. Los GPCRs nativos pueden desensibilizarse e internalizarse tras la activación por agonistas. La desensibilización depende en gran medida del nivel de sobreexpresión del receptor y de la 'reserva de receptores'. La reserva de receptores implica que se puede lograr una respuesta máxima con una ocupación sub-máxima de los receptores por el agonista. Cuando las DREADDs se expresan a altos niveles, se necesitan concentraciones más bajas del actuador químico para lograr una respuesta máxima, y la respuesta es menos sensible a la desensibilización.
Finalmente, es relevante si los efectos observados se deben a la señalización canónica de la proteína G o a otras vías, como la señalización de β-arrestina. Hasta la fecha, no hay informes que sugieran que las acciones de las DREADDs en la actividad neuronal y las respuestas fisiológicas se expliquen por mecanismos distintos a la alteración del disparo neuronal. La concordancia observada en muchos estudios que comparan DREADDs y optogenética (en términos de valencia y magnitud del efecto, aunque con diferente duración) apoya que las DREADDs primariamente alteran la actividad neuronal a través de las vías de proteína G.
DREADDs vs. Optogenética: Herramientas Complementarias
Tanto las DREADDs como la optogenética son técnicas genéticas que permiten manipular la actividad celular de forma selectiva y han revolucionado la neurociencia al permitir vincular poblaciones celulares específicas con resultados conductuales.
A pesar de compartir el objetivo de manipular circuitos neuronales, difieren significativamente en sus propiedades y aplicaciones:
| Característica | DREADDs | Optogenética |
|---|---|---|
| Resolución Temporal | Minutos a horas (lenta) | Milisegundos a segundos (rápida) |
| Invasividad | Generalmente baja (ligando sistémico), requiere cirugía inicial para el vector | Generalmente alta (fibra óptica implantada), requiere cirugía |
| Duración del Efecto | Prolongada (horas) | Breve y controlable (mientras se aplica luz) |
| Setup Experimental | Más simple (inyección/administración oral) | Más complejo (fuente de luz, fibra óptica, dispositivos de control) |
| Versatilidad Conductual | Alta (permite movimiento libre sin ataduras) | Limitada por la atadura de la fibra óptica |
| Especificidad Celular | Alta (mediante promotores y sistemas Cre-dependientes) | Alta (mediante promotores y sistemas Cre-dependientes) |
Las DREADDs son ideales para estudios donde se necesita modular la actividad neuronal durante períodos prolongados (horas), como durante la adquisición de un comportamiento o un estado emocional duradero. La optogenética es preferible cuando se requiere un control preciso de la actividad en escalas de tiempo rápidas (milisegundos a segundos), como para investigar la contribución de patrones de disparo específicos o la sincronización neuronal.
Aunque la optogenética ofrece una resolución espacial muy alta debido a la colocación precisa de la fibra óptica, un nivel comparable con DREADDs solo es posible mediante la microinyección intracraneal del ligando en un área restringida. Sin embargo, la administración sistémica de ligando DREADD permite modular estructuras cerebrales grandes o alargadas que serían difíciles de alcanzar completamente con fibras ópticas sin causar daño excesivo.
Las DREADDs son generalmente más fáciles de implementar experimentalmente, ya que la administración del ligando sistémico es más sencilla que manejar el equipo de estimulación luminosa y los implantes de fibra óptica. La posibilidad de administrar CNO por inyección, comida o agua aumenta la flexibilidad experimental.
Es crucial considerar estas diferencias al diseñar un experimento. Lejos de ser técnicas competitivas, DREADDs y optogenética son herramientas complementarias que a menudo se utilizan en el mismo diseño experimental para proporcionar líneas de evidencia independientes y convergentes sobre la suficiencia y necesidad de poblaciones neuronales específicas en un comportamiento o función.
Ventajas de las DREADDs en Neurociencia Conductual
Las DREADDs ofrecen ventajas distintivas para estudios de ganancia y pérdida de función en comparación con metodologías convencionales. Su mayor ventaja para la neurociencia conductual es la capacidad de manipular sistemas cerebrales mediante la inyección sistémica del ligando activador, lo que constituye un 'control remoto' de la actividad neural.

Aunque la mayoría de las aplicaciones requieren una cirugía inicial para la entrega intracraneal de constructos virales, el uso de ratones transgénicos que expresan DREADDs en subclases de neuronas elimina incluso este requisito. Una vez que se logra la expresión de DREADDs en el cerebro, la inhibición o activación reversible de las neuronas transfectadas ocurre poco después de la inyección intraperitoneal del ligando diseñado. De esta manera, la dinámica en curso de los sistemas neuronales objetivo puede modularse según requieran las condiciones experimentales con solo un pequeño retraso en el tiempo de inyección.
Además, este procedimiento no requiere necesariamente ninguna atadura o implantes craneales, lo que permite al animal moverse libremente en casi cualquier entorno de tarea. La inyección de CNO es más rápida que las microinyecciones intracraneales tradicionales, lo que ahorra tiempo de personal.
Otro beneficio importante es la repetibilidad de las manipulaciones con DREADDs. Pueden usarse para modular la actividad neuronal de forma transitoria en sesiones de prueba individuales, pero son particularmente adecuadas para estudios en los que un área cerebral debe manipularse repetidamente y de forma transitoria a lo largo de días o semanas. Esto era difícil con lesiones permanentes o microinyecciones que causan daño acumulado.
La evaluación histológica es otra ventaja. El uso de moléculas reporteras (como fluoróforos fusionados o expresados independientemente) permite la localización precisa de las DREADDs en neuronas individuales y en circuitos. Esto es invaluable para interpretar el efecto de las DREADDs en el comportamiento en relación con las áreas cerebrales manipuladas. Las técnicas de inmunohistoquímica permiten confirmar el tipo celular de expresión y, en algunos casos, rastrear las proyecciones axonales de las neuronas objetivo.
La especificidad celular es una ventaja clave de la chemogenética en general y de las DREADDs en particular. Mediante el uso de promotores específicos de tipo celular y sistemas recombinasa-dependientes (como Cre-loxP), es posible restringir la expresión de DREADDs a poblaciones neuronales o no neuronales muy concretas, permitiendo disecar la contribución de estos tipos celulares específicos a funciones complejas.
Aplicaciones de las DREADDs en Neurociencia
La tecnología DREADD se ha aplicado ampliamente en diversas áreas de la neurociencia, particularmente en la disección de los circuitos neuronales que subyacen al comportamiento y en el estudio de modelos animales de enfermedades.
Estudio del Comportamiento
Las DREADDs han sido fundamentales para investigar los mecanismos neuronales de una amplia gama de comportamientos:
- Aprendizaje y Memoria: Se han utilizado para estudiar el aprendizaje asociativo, como el preacondicionamiento sensorial (implicando la corteza retrosplenial) y el error de predicción (implicando la corteza prefrontal medial). También han proporcionado información sobre la codificación (corteza insular, amígdala lateral), consolidación (hipocampo ventral) y reorganización (corteza prefrontal medial) de las trazas de memoria.
- Comportamientos Guiados por Recompensa: Han ayudado a comprender cómo se forman las asociaciones entre estímulos y recompensas (ej. 'sign-tracking' implicando el palidum ventral) y cómo se evalúa la probabilidad de recompensa en la toma de decisiones (implicando la corteza orbitofrontal).
- Alimentación y Gasto Energético: Las DREADDs han sido cruciales para disecar los complejos circuitos hipotalámicos que controlan la ingesta de alimentos y el metabolismo. La activación de neuronas AgRP aumenta la ingesta, mientras que la activación de neuronas POMC la inhibe.
- Estado de Ánimo: Se han aplicado para investigar el papel del sistema serotoninérgico (núcleos del rafe) y de las interneuronas GABAérgicas (corteza prefrontal medial) en la regulación del estado de ánimo, la ansiedad y los efectos de los antidepresivos.
- Dolor: Aunque es un campo más reciente, las DREADDs se han utilizado para estudiar los circuitos espinales (ej. neuronas VGLUT3 en el asta dorsal) y cerebrales (ej. sustancia gris periacueductal, tálamo paraventricular) implicados en la nocicepción y el dolor, incluyendo la modulación descendente del dolor.
Estudio de Enfermedades
Las DREADDs también han demostrado ser valiosas en la investigación de modelos animales de enfermedades neurológicas y psiquiátricas:
- Esquizofrenia: Se han utilizado para investigar la contribución de interneuronas GABAérgicas específicas (PV, GAD65) en el hipocampo ventral y la corteza prefrontal medial a déficits conductuales relevantes para la esquizofrenia.
- Trastorno del Espectro Autista (TEA): La activación de neuronas oxitocinérgicas en el núcleo paraventricular del hipotálamo mediante DREADDs ha demostrado mejorar el comportamiento social en un modelo murino de TEA.
- Enfermedad de Alzheimer: Aunque se han usado otras herramientas chemogenéticas (dirigidas a receptores A2A en astrocitos) para estudiar déficits de memoria en modelos de Alzheimer, las DREADDs también se han aplicado para investigar la enfermedad de Down, asociada a un mayor riesgo de Alzheimer.
- Síndrome de Down: La activación de neuronas noradrenérgicas en el locus coeruleus mediante DREADDs mejoró la memoria de trabajo y redujo la hiperactividad en un modelo murino de Síndrome de Down.
Es importante destacar que las DREADDs no se limitan a las neuronas. También se han utilizado para manipular la actividad de células no neuronales, como células gliales (astrocitos, células gliales entéricas), células cardíacas y células tumorales, ampliando su potencial de aplicación.
Limitaciones y Consideraciones Prácticas
A pesar de sus muchas ventajas, el uso de DREADDs requiere una cuidadosa consideración de posibles limitaciones:
- Actividad Ligando-Independiente: Como se mencionó, la sobreexpresión de DREADDs, especialmente aquellas con actividad constitutiva, podría generar efectos en ausencia de CNO. Además, estudios han demostrado que la expresión de Gi-DREADDs puede causar cambios ligando-independientes en canales iónicos nativos y señalización de segundos mensajeros, lo que podría afectar la excitabilidad celular basal.
- Metabolismo del CNO: La retroconversión a clozapina en especies no roedoras es una limitación importante para la traslación a primates y humanos.
- Cinética del Ligando: La duración prolongada del efecto del CNO, si bien es una ventaja en algunos casos, puede ser una limitación cuando se requiere un control temporal preciso y rápido.
- Controles Experimentales: Es fundamental incluir controles adecuados, como animales que expresan DREADDs pero reciben vehículo en lugar de CNO, o animales control que no expresan DREADDs pero reciben CNO, para descartar efectos inespecíficos del ligando o de la expresión proteica.
Identificar los mecanismos precisos subyacentes a cualquier fenotipo observado tras la activación de DREADDs es esencial, dada la posibilidad de actividad ligando-independiente o efectos no canónicos.
Preguntas Frecuentes sobre DREADDs
¿Qué significa el acrónimo DREADD?
Significa Designer Receptor Exclusively Activated by Designer Drug (Receptor Diseñado Exclusivamente Activado por Fármaco Diseñado).
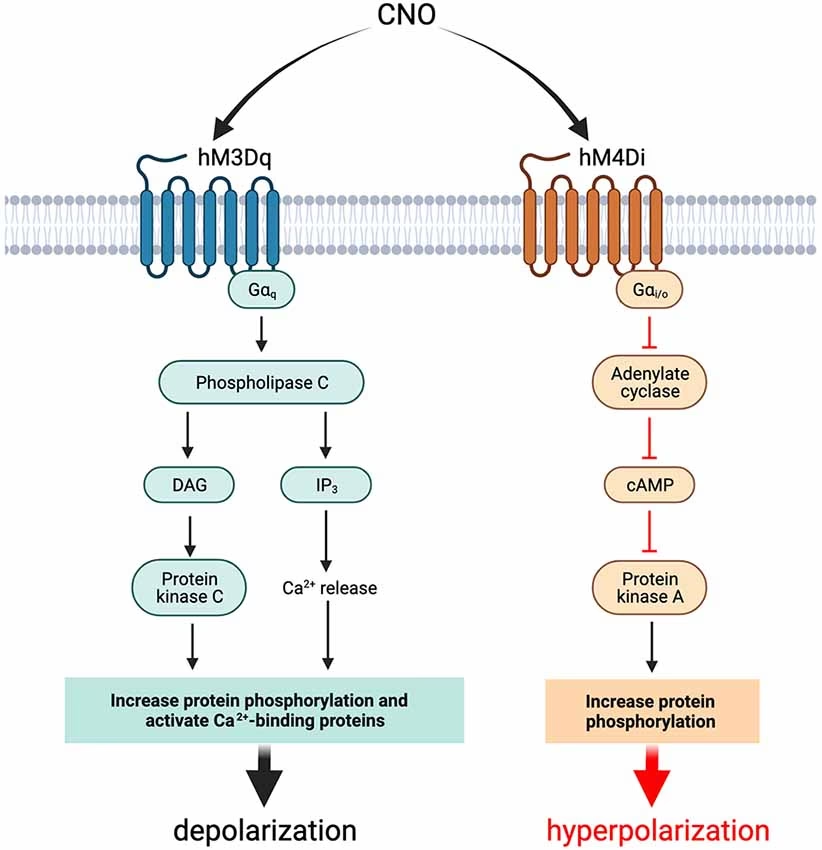
¿Cómo funcionan las DREADDs para controlar la actividad neuronal?
Son receptores acoplados a proteínas G (GPCRs) que han sido modificados genéticamente. Cuando se les administra un fármaco específico (como CNO), se activan y desencadenan cascadas de señalización intracelular (vías Gi, Gq o Gs) que resultan en la inhibición o excitación de la neurona.
¿Cuál es el principal fármaco utilizado para activar las DREADDs?
El más común es el clozapine N-oxide (CNO).
¿Se usan DREADDs en humanos?
Actualmente, las DREADDs son principalmente herramientas de investigación en modelos animales. Existen desafíos para su uso terapéutico en humanos, como la entrega viral segura y eficiente en neuronas adultas y el metabolismo del CNO.
¿Cuál es la diferencia principal entre DREADDs y optogenética?
La diferencia clave es la resolución temporal y el método de activación. Las DREADDs se activan con fármacos (efectos que duran horas) y son menos invasivas. La optogenética se activa con luz (efectos en milisegundos) y requiere la implantación de fibras ópticas.
¿Pueden las DREADDs dirigirse a tipos celulares específicos?
Sí, una de las mayores ventajas de las DREADDs es su especificidad celular. Esto se logra utilizando promotores específicos de tipo celular y sistemas genéticos como Cre-loxP.
¿Las DREADDs solo se dirigen a neuronas?
No, aunque su uso es prominente en neuronas, las DREADDs también se han utilizado para manipular la actividad de células no neuronales, como la glía.
Conclusión
Las técnicas genéticas como las DREADDs están transformando la neurociencia al permitir la manipulación precisa y específica de poblaciones celulares en el cerebro. Han proporcionado conocimientos sin precedentes sobre los circuitos neuronales que controlan una amplia gama de comportamientos y han sido herramientas valiosas para investigar los mecanismos de enfermedades neurológicas y psiquiátricas en modelos animales.
La capacidad de modular la actividad neuronal de forma reversible, repetible y con una invasividad relativamente baja (especialmente con la administración sistémica del ligando) hace que las DREADDs sean una herramienta poderosa y flexible. Aunque presentan limitaciones, como la resolución temporal en comparación con la optogenética y posibles efectos ligando-independientes, el desarrollo continuo de nuevas variantes de DREADDs y ligandos, así como la mejora en las estrategias de entrega y focalización, prometen expandir aún más su utilidad.
La disección de la contribución de tipos celulares específicos a estados patológicos mediante DREADDs podría conducir al desarrollo de terapias más racionales y efectivas en el futuro. Si bien la traducción directa a tratamientos en humanos aún enfrenta desafíos importantes, el potencial de las DREADDs para desentrañar la compleja red del cerebro y sus disfunciones las consolida como una de las herramientas más emocionantes en la neurociencia contemporánea.
Si quieres conocer otros artículos parecidos a DREADDs: Herramientas Clave en Neurociencia puedes visitar la categoría Neurociencia.