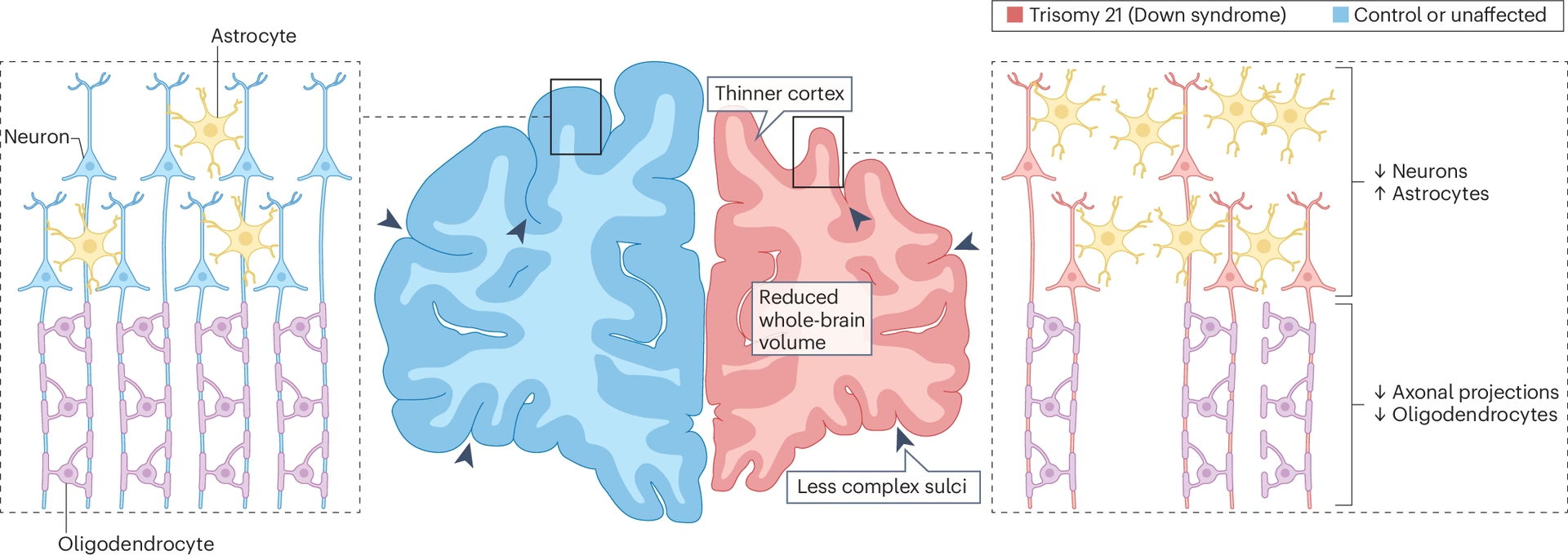
El Síndrome de Down (SD) es la aneuploidía más frecuente en nacidos vivos y la causa genética más común de discapacidad intelectual. Se debe, en la gran mayoría de los casos, a la presencia de una copia extra del cromosoma 21 (Trisomía 21). Este exceso genético no solo afecta rasgos físicos distintivos, sino que tiene un profundo impacto en el desarrollo y funcionamiento del cerebro a lo largo de la vida. Comprender la neurociencia detrás del Síndrome de Down es crucial para abordar sus desafíos cognitivos y neurológicos, y para desarrollar estrategias de apoyo y tratamiento más efectivas.
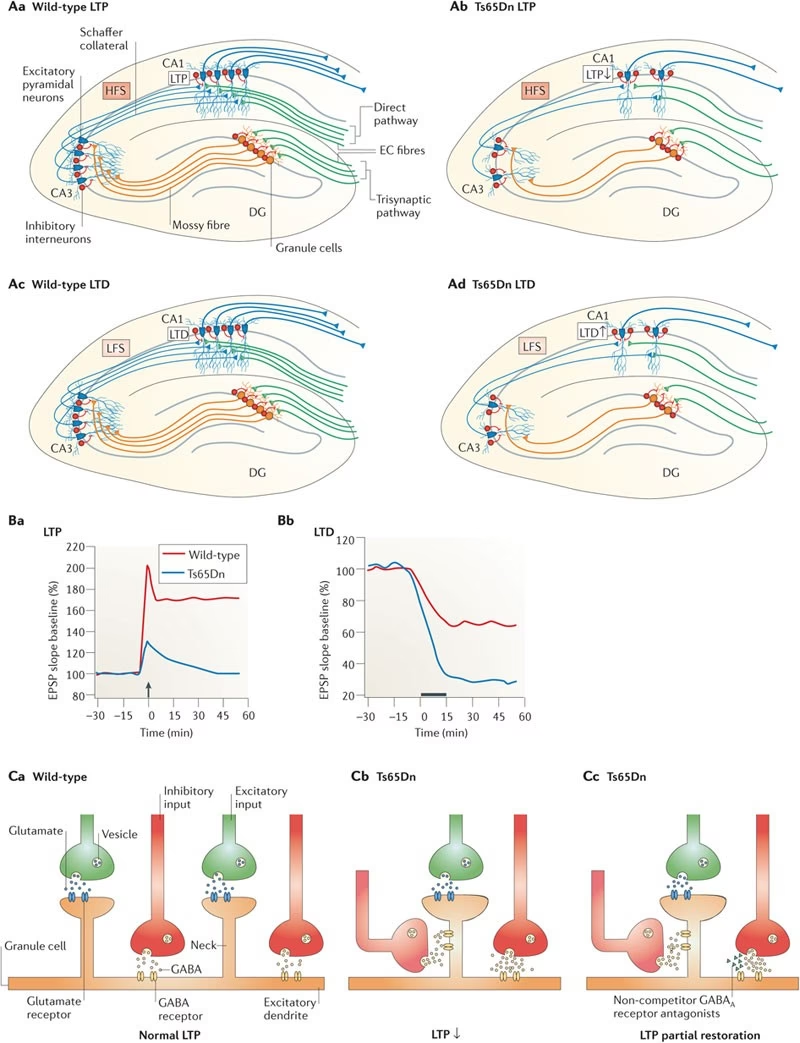
La Trisomía 21 conlleva una desregulación en la expresión de cientos de genes presentes en este cromosoma, lo que a su vez afecta la expresión de genes en otros cromosomas. Esta alteración del equilibrio genético se manifiesta en cada célula del cuerpo, incluyendo las neuronas y otras células cerebrales, desde las primeras etapas del desarrollo embrionario. Aunque la mayoría de los genes del cromosoma 21 muestran una sobreexpresión aproximadamente un 50% mayor de lo normal, el fenotipo variable del SD sugiere que la interacción de factores genéticos, epigenéticos, ambientales y estocásticos contribuye a la diversidad de manifestaciones clínicas.
El Impacto en el Neurodesarrollo
El cerebro de las personas con Síndrome de Down presenta diferencias estructurales notables que comienzan a gestarse en el período fetal. Se observa un volumen cerebral reducido en general, con una disminución desproporcionada en áreas como los lóbulos frontales y temporales, así como el cerebelo. Curiosamente, algunas áreas como los núcleos lenticulares, la materia gris de la corteza parietal posterior y occipital, y el giro parahipocampal (este último, a menudo más grande de lo típico) parecen estar relativamente preservadas o afectadas de manera diferente.
A nivel celular, el neurodesarrollo en el Síndrome de Down se caracteriza por diversas alteraciones. Se han documentado problemas en la laminación cortical, una reducción en la ramificación de las dendritas (las estructuras que reciben señales de otras neuronas) y una disminución en la formación de sinapsis (las conexiones entre neuronas). También hay evidencia de una menor cantidad total de neuronas en varias regiones cerebrales, incluyendo el hipocampo y la neocorteza, lo que sugiere un fallo en la neurogénesis (la creación de nuevas neuronas) y un aumento de la muerte celular durante el desarrollo.
La sobreexpresión de genes en el cromosoma 21 perturba vías moleculares esenciales para la formación y función neuronal. Se están utilizando enfoques de neurociencia de sistemas para identificar las vías impactadas, no solo por los productos directos de los genes del cromosoma 21, sino también por sus interacciones con otras proteínas. Vías como las de los factores de crecimiento nervioso, Sonic Hedgehog (SHH), glucocorticoides, NOTCH y Wnt, así como las cascadas de caspasas involucradas en la apoptosis (muerte celular programada), se ven afectadas. Un pequeño número de proteínas codificadas en el cromosoma 21, como APP, TIAM1, ITSN1, SUMO3, ITGB2 y S100B, parecen tener un impacto significativo en múltiples vías, subrayando la complejidad de la desregulación.
Problemas Neurológicos Específicos
Más allá de la discapacidad intelectual, las personas con Síndrome de Down pueden experimentar una variedad de problemas neurológicos específicos a lo largo de su vida. Estos incluyen:
- Epilepsia y Trastornos Convulsivos: Las convulsiones tienen una distribución bimodal, siendo comunes en la primera infancia (antes del año) y reapareciendo en la edad adulta media. Están asociadas a anomalías estructurales cerebrales y pueden preceder el desarrollo de demencia.
- Trastorno de Regresión del Síndrome de Down: Un fenómeno menos común pero grave donde hay una pérdida significativa de habilidades previamente adquiridas, a menudo asociada a cambios neurológicos o condiciones autoinmunes.
- Trastornos del Movimiento: Pueden incluir hipotonía (tono muscular bajo) en la infancia y, en algunos casos, desarrollar otros trastornos del movimiento con la edad.
- Migrañas y Cefaleas: Dolor de cabeza recurrente.
- Trastornos Cerebrovasculares: Como la enfermedad de Moyamoya, una condición rara que afecta los vasos sanguíneos del cerebro.
- Trastornos del Sueño: Insomnio, apnea obstructiva del sueño, entre otros, que pueden tener un impacto significativo en la función cognitiva y el bienestar general.
- Síncope: Desmayos.
Estos problemas reflejan las alteraciones en la estructura y función cerebral, incluyendo una posible escasez de neuronas inhibitorias y defectos en la laminación cortical.
El Vínculo Inevitable con la Enfermedad de Alzheimer
Uno de los aspectos más estudiados del envejecimiento en el Síndrome de Down es la alta incidencia de la patología de la enfermedad de Alzheimer (EA). Para los 40 años de edad, casi todas las personas con SD desarrollan placas amiloides y ovillos neurofibrilares, las características distintivas de la EA, aunque el inicio y la gravedad de la demencia clínica son variables. Esta conexión se debe, en parte, a que el gen de la proteína precursora amiloide (APP) se encuentra en el cromosoma 21. Tener una copia extra de este gen resulta en una sobreproducción de la proteína APP y, consecuentemente, una mayor acumulación de péptido beta-amiloide en el cerebro.

La demencia en el SD a menudo comienza con síntomas que sugieren disfunción del lóbulo frontal, como cambios en la sociabilidad, el lenguaje emocional y síntomas depresivos. La carga de amiloide parece depositarse primero en las cortezas frontal y entorrinal. Además de la sobreexpresión de APP, otros factores contribuyen a la patología de la EA en el SD, incluido el estrés oxidativo (posiblemente relacionado con mutaciones en el ADN mitocondrial) y alteraciones en el metabolismo energético.
Antes de la aparición evidente de la demencia, se han observado algunos mecanismos compensatorios, como la brotación de neuritas en el hipocampo y un aumento del metabolismo de la glucosa en ciertas estructuras del lóbulo temporal medial. Sin embargo, la trayectoria general es hacia un envejecimiento cerebral acelerado y una mayor vulnerabilidad a la neurodegeneración.
Plasticidad Neuronal y Envejecimiento Cerebral
La plasticidad neuronal, la capacidad del cerebro para cambiar y adaptarse, es fundamental para el aprendizaje y la memoria. En el Síndrome de Down, esta plasticidad parece estar comprometida. Las alteraciones en la formación y función sináptica, así como en la neurogénesis, contribuyen a esta plasticidad reducida. Esto limita la capacidad del cerebro para compensar las anomalías del desarrollo y para recuperarse de lesiones o declive.
El patrón de envejecimiento cerebral en el SD es único. Si bien la patología de la EA es casi universal con la edad, el declive cognitivo no siempre es proporcional. La investigación se centra en identificar biomarcadores (en líquido cefalorraquídeo, plasma o mediante neuroimagen) que puedan predecir el inicio de la demencia, permitiendo intervenciones más tempranas.
Investigación y Modelos de Estudio
La investigación sobre la neurociencia del Síndrome de Down ha avanzado significativamente gracias al desarrollo de nuevos modelos y tecnologías. Estos incluyen:
- Modelos Murinos (Ratones): Modelos como el Ts65Dn o Tc1, que portan un segmento extra del cromosoma murino 16 (ortólogo parcial del cromosoma 21 humano), han sido fundamentales para estudiar los efectos de la trisomía en el cerebro, aunque existen diferencias importantes con el cerebro humano.
- Células Madre Pluripotentes Inducidas (iPSCs): Derivadas de personas con SD, estas células pueden diferenciarse en tipos específicos de células cerebrales (neuronas, astrocitos, oligodendrocitos) en el laboratorio. Permiten estudiar los efectos de la Trisomía 21 en células humanas vivas y en diferentes etapas del desarrollo y maduración.
- Organoides Cerebrales: Estructuras tridimensionales generadas a partir de iPSCs que simulan la organización y el desarrollo de regiones cerebrales humanas. Son herramientas poderosas para modelar el neurodesarrollo y la patología de la EA en un contexto más complejo que los cultivos celulares 2D.
- Tecnologías de Alto Rendimiento: La secuenciación de ARN (RNA-seq) y otras técnicas genómicas y proteómicas permiten analizar la expresión génica y proteica a gran escala en tejidos cerebrales o modelos celulares, identificando las vías moleculares desreguladas.
Estos modelos de investigación están ayudando a desentrañar los complejos mecanismos moleculares y celulares que subyacen a la discapacidad intelectual y otras manifestaciones neurológicas del SD. Se están explorando posibles estrategias terapéuticas, como la modulación de vías de neurotransmisión (por ejemplo, la inhibición GABAérgica, que parece aumentada en el SD) o incluso la silenciamiento de genes extra en el cromosoma 21 utilizando técnicas como la inserción del gen XIST.
Conclusión
La neurociencia del Síndrome de Down es un campo complejo y en evolución. La Trisomía 21 desencadena una cascada de eventos que afectan el desarrollo, la estructura y la función del cerebro a lo largo de la vida. Desde las alteraciones tempranas en la neurogénesis y la sinaptogénesis hasta la vulnerabilidad casi universal a la patología de la enfermedad de Alzheimer en la edad adulta, el cerebro con Síndrome de Down presenta desafíos únicos.

Sin embargo, los avances en la investigación genética, molecular y celular, junto con el uso de modelos innovadores, están abriendo nuevas vías para comprender estos procesos y, en última instancia, desarrollar intervenciones que puedan mejorar la función cognitiva, mitigar los problemas neurológicos y retrasar o prevenir el inicio de la demencia, mejorando así significativamente la calidad de vida de las personas con Síndrome de Down.
Preguntas Frecuentes sobre la Neurociencia del Síndrome de Down
¿Qué causa las diferencias cerebrales en el Síndrome de Down?
Las diferencias se deben principalmente a la presencia de una copia extra del cromosoma 21 (Trisomía 21). Esto lleva a la sobreexpresión de genes en este cromosoma, lo que desregula múltiples vías moleculares esenciales para el desarrollo y funcionamiento normal del cerebro.
¿Las personas con Síndrome de Down tienen el cerebro más pequeño?
Sí, en general, las personas con Síndrome de Down tienen un volumen cerebral reducido. Esta reducción es más pronunciada en ciertas áreas como los lóbulos frontales y temporales, así como el cerebelo.
¿Por qué las personas con Síndrome de Down tienen mayor riesgo de Alzheimer?
El gen que codifica la proteína precursora amiloide (APP), clave en la formación de las placas de Alzheimer, se encuentra en el cromosoma 21. Una copia extra de este cromosoma resulta en más gen APP, más proteína APP y una mayor acumulación de péptido beta-amiloide en el cerebro con la edad.
¿Se pueden tratar los problemas cognitivos en el Síndrome de Down?
Actualmente no existe una cura, pero la investigación activa está explorando tratamientos que modulen las vías moleculares afectadas. Terapias dirigidas a, por ejemplo, la inhibición GABAérgica o el silenciamiento genético son áreas de estudio prometedoras para mejorar la función cognitiva.
¿La plasticidad cerebral es diferente en el Síndrome de Down?
Sí, la plasticidad neuronal, la capacidad del cerebro para cambiar, parece estar comprometida en el Síndrome de Down debido a alteraciones en la formación de sinapsis y la neurogénesis. Esto puede afectar la capacidad de aprendizaje y adaptación.
Comparativa: Características Cerebrales en Síndrome de Down vs. Desarrollo Típico
| Característica | Desarrollo Típico | Síndrome de Down (SD) |
|---|---|---|
| Volumen Cerebral General | Normal para la edad | Reducido (especialmente frontal, temporal, cerebelo) |
| Laminación Cortical | Organización normal en capas | Defectos en la organización |
| Número de Neuronas | Normal | Reducido en varias regiones (hipocampo, neocorteza) |
| Ramificación Dendrítica | Extensa y compleja | Reducida |
| Número y Maduración Sináptica | Densidad pico en la infancia, luego poda. Sinapsis maduras. | Menor densidad, mayor porcentaje de contactos primitivos. |
| Neurogénesis | Activa durante el desarrollo, limitada en adulto (hipocampo) | Impedida durante el desarrollo |
| Plasticidad Neuronal | Alta capacidad de adaptación | Comprometida |
| Patología de Alzheimer | Presente en EA, más común en edad avanzada | Casi universal a los 40 años, inicio de demencia variable |
| Inhibición GABAérgica | Equilibrio normal | Aumentada en algunos modelos |
Si quieres conocer otros artículos parecidos a Neurociencia del Síndrome de Down puedes visitar la categoría Neurociencia.