Los Proteoglicanos de Sulfato de Condroitina, conocidos comúnmente como CSPG (por sus siglas en inglés, Chondroitin Sulfate Proteoglycans), son componentes cruciales de la matriz extracelular en diversos tejidos del cuerpo humano. Sin embargo, su papel en el sistema nervioso central es particularmente significativo y, a menudo, complejo. Estas macromoléculas no solo son fundamentales durante las etapas tempranas del desarrollo neural, guiando el crecimiento y la conexión de las neuronas, sino que también emergen como actores principales en la respuesta del cerebro y la médula espinal a las lesiones y enfermedades.

Su doble faceta, siendo facilitadores de procesos biológicos en condiciones normales y, paradójicamente, inhibidores de la reparación tras un daño, los convierte en un foco de intensa investigación en neurociencia. Comprender la estructura y función de los CSPG es esencial para desentrañar los mecanismos de la recuperación neurológica y desarrollar posibles estrategias terapéuticas.
- ¿Qué son los CSPG y Cuál es su Estructura?
- El Papel de los CSPG en el Neurodesarrollo
- CSPG y la Barrera de la Regeneración Axonal tras Lesiones
- Mecanismos de Regulación y Modulación de los CSPG
- CSPG y su Implicación en Enfermedades Neurológicas
- Enfoques Computacionales y Potenciales Terapias
- Preguntas Frecuentes sobre los CSPG
- Conclusión
¿Qué son los CSPG y Cuál es su Estructura?
Los CSPG pertenecen a una familia de proteoglicanos, que son macromoléculas compuestas por un núcleo proteico al que se unen covalentemente una o más cadenas de glicosaminoglicanos (GAG). En el caso específico de los CSPG, las cadenas de GAG son de sulfato de condroitina.
La estructura básica de un CSPG consta de dos partes principales:
- Núcleo Proteico: Es una proteína, a menudo una glicoproteína, que sirve como ancla para las cadenas de GAG. Existen diferentes tipos de núcleos proteicos que dan lugar a distintos CSPG, como Aggrecan (CSPG1), Versican (CSPG2), Neurocan (CSPG3), CSPG4 (también conocido como NG2), CSPG5, SMC3 (CSPG6), Brevican (CSPG7), CD44 (CSPG8) y Phosphacan. Algunos de estos, como Neurocan, Brevican, Versican y Aggrecan, comparten dominios estructurales similares en sus extremos N y C.
- Cadenas de Sulfato de Condroitina: Son cadenas lineales de polisacáridos compuestas por unidades disacáridas alternantes de ácido urónico y N-acetilgalactosamina. Estas cadenas se unen al núcleo proteico a través de un enlace covalente. La longitud de estas cadenas puede variar según el tipo de CSPG.
Esta estructura modular permite a los CSPG interactuar con una variedad de otros componentes de la matriz extracelular, como laminina, fibronectina, tenascina y colágeno, y desempeñar roles en procesos celulares como la adhesión, el crecimiento, la migración y la unión a receptores.
El Papel de los CSPG en el Neurodesarrollo
Durante las etapas críticas del desarrollo del sistema nervioso, los CSPG desempeñan un papel fundamental como señales de guía para el crecimiento de los axones. Actúan como "señales negativas" o inhibidoras, dirigiendo los conos de crecimiento axonal lejos de ciertas áreas.
Esta función de "evitación" es crucial para establecer los complejos circuitos neuronales. Por ejemplo, estudios en la placa del techo embrionaria de la médula espinal en desarrollo han mostrado que las áreas ricas en CSPG inhiben la elongación axonal, guiando así los axones en otras direcciones. En contraste, las áreas de la placa del techo que atraen la elongación axonal carecen de estos CSPG. Este mecanismo de guía negativa es un aspecto vital del cableado neuronal preciso durante el desarrollo.
CSPG y la Barrera de la Regeneración Axonal tras Lesiones
Uno de los roles más estudiados y perjudiciales de los CSPG en el sistema nervioso central ocurre después de una lesión, como una lesión de la médula espinal (LME) o un traumatismo craneoencefálico (TCE). Tras una lesión, se forma una cicatriz glial en el sitio del daño, compuesta por una acumulación de células gliales (principalmente astrocitos reactivos y microglia) y componentes de la matriz extracelular, incluyendo una marcada sobreexpresión de varios tipos de CSPG.

Esta cicatriz glial, aunque inicialmente puede tener funciones protectoras al contener la extensión del daño, se convierte en una barrera física y molecular que impide la regeneración de los axones cortados. Los CSPG presentes en la cicatriz glial son potentes inhibidores de la elongación y el crecimiento axonal, lo que contribuye significativamente a la falta de regeneración espontánea en el sistema nervioso central de mamíferos adultos.
Estudios han demostrado que los niveles de Neurocan, Brevican, Versican y Phosphacan aumentan drásticamente después de una lesión de la médula espinal. Este aumento se observa tan pronto como un día después de la lesión y los niveles permanecen elevados durante semanas o meses, coincidiendo con el período en que la regeneración axonal es mínima. Se cree que estos cuatro CSPG trabajan en conjunto para crear este ambiente inhibidor.
Upregulación de CSPG tras Lesión Medular
La siguiente tabla ilustra la dinámica de la sobreexpresión de algunos CSPG clave tras una lesión medular, según estudios en roedores:
| CSPG | 1 día post-lesión | 4 semanas post-lesión | 8 semanas post-lesión |
|---|---|---|---|
| Neurocan | 显著 aumentado | Elevado | No especificado |
| Brevican | 显著 aumentado | No especificado | Elevado |
| Versican | 显著 aumentado | Elevado | No especificado |
| Phosphacan | No aumentado | Aumentado | No especificado |
Esta sobreexpresión coordinada y sostenida subraya el papel central de los CSPG en la formación de un ambiente hostil para el crecimiento axonal después de la lesión.
Mecanismos de Regulación y Modulación de los CSPG
Dada su potente capacidad inhibidora, comprender cómo se regulan los CSPG y cómo se pueden modular sus efectos es crucial para el desarrollo de terapias regenerativas. La investigación ha identificado varios mecanismos importantes:
Inhibición del Receptor del Factor de Crecimiento Epidérmico (EGFR)
Se ha sugerido que el EGFR regula la función de los CSPG. La inhibición de EGFR ha demostrado bloquear las actividades de CSPG como Neurocan, Phosphacan, Versican y Aggrecan. Cuando el EGFR está inactivo, los CSPG tienen poco efecto sobre las neuronas, permitiendo una neurogénesis significativamente mayor y el crecimiento de neuronas más largas y numerosas. Esto sugiere que la manipulación del EGFR podría ser una vía para contrarrestar los efectos adversos de los CSPG tras una lesión.
PTP-sigma como Receptor de CSPG
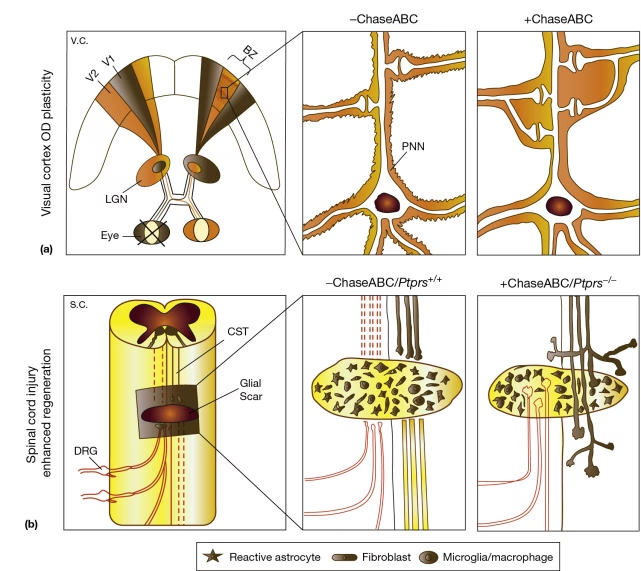
La proteína tirosina fosfatasa transmembrana PTP-sigma ha sido identificada como un receptor funcional de CSPG, uniéndose con alta afinidad a Neurocan y Aggrecan. Estudios en ratones con lesión medular a los que les faltaba PTP-sigma mostraron una regeneración axonal significativamente mayor, a pesar de la presencia normal de CSPG en el sitio de la lesión. Esto indica que la interacción entre CSPG y PTP-sigma es esencial para que los CSPG ejerzan su función inhibidora. Por lo tanto, dirigir la interacción CSPG-PTP-sigma podría ser una estrategia terapéutica.
Interferón-gamma (IFN-gamma)
Este citocina, conocido por su papel en la inmunidad, también ha demostrado ser beneficioso para disminuir la expresión de CSPG después de una lesión medular. El tratamiento con IFN-gamma en ratones lesionados resultó en una reducción significativa de los niveles de CSPG en el sitio de la lesión, sugiriendo que actúa inhibiendo la expresión de ARNm de CSPG.
La Vía Rho/ROCK
Se ha demostrado que la inhibición del crecimiento axonal y la neurogénesis por parte de los CSPG después de una lesión medular está mediada, al menos en parte, por la vía de la proteína cinasa asociada a Rho (ROCK). La activación de la vía ROCK acompaña la inhibición del crecimiento axonal por CSPG. Sin embargo, el uso de inhibidores de la vía ROCK, como C3 transferasa y Y27632, ha mostrado un aumento significativo en la neurogénesis y la longitud de las neuronas. Esto sugiere que bloquear la vía ROCK puede disminuir drásticamente la inhibición de la regeneración axonal mediada por CSPG.
CSPG y su Implicación en Enfermedades Neurológicas
Más allá de las lesiones traumáticas, los CSPG también han sido implicados en la patología de varias enfermedades neurológicas degenerativas y trastornos psiquiátricos.
Enfermedad de Alzheimer
En cerebros post-mortem de pacientes con Alzheimer, se ha encontrado la presencia de CSPG (CSPG-4 y CSPG-6) localizados en el perímetro de los ovillos neurofibrilares (NFT) y las placas seniles (SP), los marcadores distintivos de la enfermedad. También se han encontrado en neuronas distróficas. Dada la capacidad inhibidora de los CSPG, se postula que podrían contribuir a la regresión y disfunción de las neuronas circundantes a estas patologías. Las terapias dirigidas a reducir o modular los CSPG en estas áreas podrían potencialmente aliviar algunos síntomas.
Accidente Cerebrovascular (Ictus)
Tras un ictus, algunos pacientes recuperan parcialmente la función cerebral en las áreas afectadas, un proceso asociado con la plasticidad cerebral. En modelos animales, se ha observado que esta recuperación funcional se correlaciona con una disminución en los niveles de varios CSPG, incluyendo Aggrecan, Versican y Phosphacan, en las regiones cerebrales plásticas. Esto sugiere que la reducción de CSPG podría facilitar la formación de nuevas conexiones neuronales y contribuir a la recuperación funcional. La inducción farmacológica de la reducción de CSPG podría ser una estrategia para mejorar la recuperación después de un ictus.
Epilepsia
En pacientes con epilepsia, se ha observado una disminución de ciertos CSPG, como Phosphacan, en regiones cerebrales afectadas como el lóbulo temporal y el hipocampo. Aunque el mecanismo exacto no está completamente claro, esta alteración en los niveles de CSPG sugiere un papel en la regulación de la plasticidad y el crecimiento axonal en el contexto de la hiperexcitabilidad neuronal característica de la epilepsia.
Trastornos Psiquiátricos
Investigaciones recientes, particularmente estudios de asociación de genoma completo (GWAS), han identificado asociaciones entre variaciones en genes que codifican CSPG (especialmente Neurocan, NCAN) y trastornos psiquiátricos como el trastorno bipolar, la esquizofrenia y el TDAH. Por ejemplo, ciertas variantes de un polimorfismo de nucleótido único (SNP) en el gen NCAN (rs1064395) se han asociado con un mayor riesgo de trastorno bipolar y esquizofrenia. Aunque el mecanismo preciso por el cual estas variantes genéticas de CSPG contribuyen a la patología psiquiátrica aún se está investigando, sugiere un papel de los CSPG en la conectividad neuronal y la función sináptica que es relevante para estos trastornos.

Enfoques Computacionales y Potenciales Terapias
Además de los estudios experimentales, los enfoques computacionales, como las relaciones cuantitativas estructura-actividad (QSAR) y la cristalografía, están proporcionando información valiosa sobre la estructura y función de los CSPG y ayudando a identificar potenciales moduladores. La QSAR, por ejemplo, busca establecer relaciones entre la estructura química de una molécula y su actividad biológica, lo que es útil para diseñar nuevos fármacos o encontrar nuevas aplicaciones para fármacos existentes.
Curiosamente, algunos fármacos antipsicóticos (utilizados para tratar la esquizofrenia y el trastorno bipolar) de la clase de las fenotiazinas (como trifluoperazina, proclorperazina y flufenazina) han demostrado la capacidad de promover el crecimiento de neuritas en presencia de sustratos inhibidores de CSPG (Neurocan, Versican, Aggrecan) en cultivos celulares. Esto sugiere que estos fármacos podrían tener un efecto beneficioso al contrarrestar los efectos inhibidores de los CSPG, lo que podría ser relevante para mejorar la conectividad neuronal en pacientes con esquizofrenia, donde se han observado niveles elevados de CSPG en el cerebro post-mortem.
La cristalografía de rayos X, por su parte, permite determinar la estructura tridimensional de los CSPG o sus dominios proteicos y sus interacciones con otras moléculas, como la tenascina-R (con la que Aggrecan forma estructuras de matriz extracelular como las redes perineuronales). Comprender estas interacciones a nivel atómico es fundamental para diseñar moléculas que puedan interferir selectivamente con las funciones de los CSPG.
Preguntas Frecuentes sobre los CSPG
- ¿Los CSPG son siempre perjudiciales en el cerebro?
- No. Aunque son conocidos por inhibir la regeneración axonal tras una lesión, desempeñan roles cruciales y beneficiosos durante el neurodesarrollo, guiando el crecimiento axonal y la formación de circuitos. Su función se vuelve problemática en el contexto de la lesión o ciertas enfermedades, donde su sobreexpresión crea un ambiente inhibidor.
- ¿Por qué los CSPG impiden que los axones crezcan?
- Los CSPG, particularmente sus cadenas de sulfato de condroitina, interactúan con receptores en la superficie de los conos de crecimiento axonal, como PTP-sigma. Esta interacción activa cascadas de señalización intracelular (como la vía Rho/ROCK) que llevan a la retracción del cono de crecimiento o a la inhibición de su elongación, impidiendo que el axón atraviese la cicatriz glial.
- ¿Se pueden eliminar o bloquear los CSPG para tratar lesiones?
- La investigación está explorando diversas estrategias para neutralizar los efectos inhibidores de los CSPG. Esto incluye el uso de enzimas (como la condroitinasa ABC) para degradar las cadenas de sulfato de condroitina, bloquear los receptores de CSPG (como PTP-sigma) o modular las vías de señalización intracelular (como la vía Rho/ROCK) que median sus efectos. También se buscan enfoques para reducir su sobreexpresión.
- ¿Cómo se relacionan los CSPG con enfermedades como el Alzheimer?
- En la enfermedad de Alzheimer, los CSPG se acumulan alrededor de las patologías características (placas y ovillos). Se cree que su presencia en estas áreas contribuye a la disfunción y pérdida neuronal circundante al crear un ambiente menos propicio para la supervivencia y conectividad neuronal.
- ¿Hay ya terapias basadas en CSPG disponibles?
- Actualmente, no existen terapias clínicas aprobadas que se dirijan directamente a los CSPG para promover la regeneración en lesiones del sistema nervioso central o para tratar enfermedades neurológicas. Sin embargo, es un área activa de investigación preclínica con resultados prometedores que podrían llevar a futuros tratamientos.
Conclusión
Los Proteoglicanos de Sulfato de Condroitina son moléculas multifacéticas con un impacto profundo en el sistema nervioso central. Son esenciales para el cableado neuronal durante el desarrollo, pero se convierten en un obstáculo formidable para la regeneración axonal tras una lesión. Su implicación en diversas enfermedades neurológicas, desde trastornos neurodegenerativos hasta psiquiátricos, resalta su importancia más allá del contexto de la lesión traumática.
La investigación continua sobre su estructura, regulación y mecanismos de acción, utilizando tanto enfoques experimentales como computacionales, es fundamental para desentrañar por completo su complejo papel. Las estrategias dirigidas a modular la expresión o actividad de los CSPG, ya sea mediante la degradación enzimática, el bloqueo de receptores o la modulación de vías de señalización, ofrecen una esperanza considerable para el desarrollo de nuevas terapias que puedan promover la reparación y la recuperación funcional en pacientes con lesiones del sistema nervioso central y posiblemente mitigar la progresión de ciertas enfermedades neurológicas. El desafío reside en encontrar formas de manipular los CSPG para fomentar la plasticidad y la reparación sin comprometer sus funciones beneficiosas.
Si quieres conocer otros artículos parecidos a CSPG: Rol Clave en Cerebro y Lesiones puedes visitar la categoría Neurociencia.

