La neurociencia, el estudio del cerebro y el sistema nervioso, es un campo en constante evolución que busca desentrañar los misterios de la función cerebral en la salud y la enfermedad. Durante décadas, comprender y manipular los elementos genéticos que subyacen a los procesos neuronales ha sido un desafío fundamental. Sin embargo, la llegada de tecnologías de ingeniería genómica ha revolucionado este panorama, ofreciendo herramientas sin precedentes para investigar el intrincado cableado genético del cerebro. Entre estas herramientas, el sistema CRISPR-Cas9 se ha destacado como un verdadero tesoro, transformando la investigación biomédica y, muy especialmente, el campo de la neurociencia.

Descubierto originalmente como un sistema de defensa microbiano contra virus invasores, CRISPR-Cas9 ha sido adaptado y desarrollado para convertirse en una plataforma de edición genética programable, precisa y relativamente asequible. Su capacidad para dirigirse y modificar secuencias específicas de ADN ha abierto un abanico de posibilidades para científicos de todo el mundo, permitiéndoles manipular genes con una eficiencia y facilidad antes inimaginables. Desde células cancerosas hasta modelos animales de enfermedades neurológicas, prácticamente cualquier sistema biológico es ahora susceptible de ser modificado genéticamente, impulsando tanto la investigación fundamental como el desarrollo de nuevas estrategias terapéuticas.
- ¿Qué es CRISPR-Cas9 y cómo funciona en el contexto neurológico?
- Ventajas de CRISPR-Cas9 sobre Otras Herramientas de Edición Genética
- Aplicaciones de CRISPR en la Investigación Neurocientífica
- CRISPR-Cas9 como Herramienta Terapéutica en Trastornos Neurológicos
- Vías de Reparación del ADN: NHEJ vs. HDR
- Desafíos y Limitaciones de CRISPR-Cas9 en Trastornos Neurológicos
- Perspectivas Futuras de CRISPR en Neurociencia
- Preguntas Frecuentes (FAQ)
- Conclusión
¿Qué es CRISPR-Cas9 y cómo funciona en el contexto neurológico?
El acrónimo CRISPR significa "Clustered Regularly Interspaced Short Palindromic Repeats" (Repeticiones Palindrómicas Cortas Agrupadas y Espaciadas Regularmente), que son secuencias de ADN únicas encontradas en bacterias y arqueas. Estas secuencias, intercaladas con "espaciadores" derivados del ADN de virus invasores, forman una especie de memoria genética del sistema inmunitario microbiano.
Cas9 es una enzima endonucleasa asociada al sistema CRISPR. Su función principal es cortar el ADN en sitios específicos dirigidos por moléculas de ARN guía. En el contexto de la edición genética, el sistema CRISPR-Cas9 se compone de dos elementos clave:
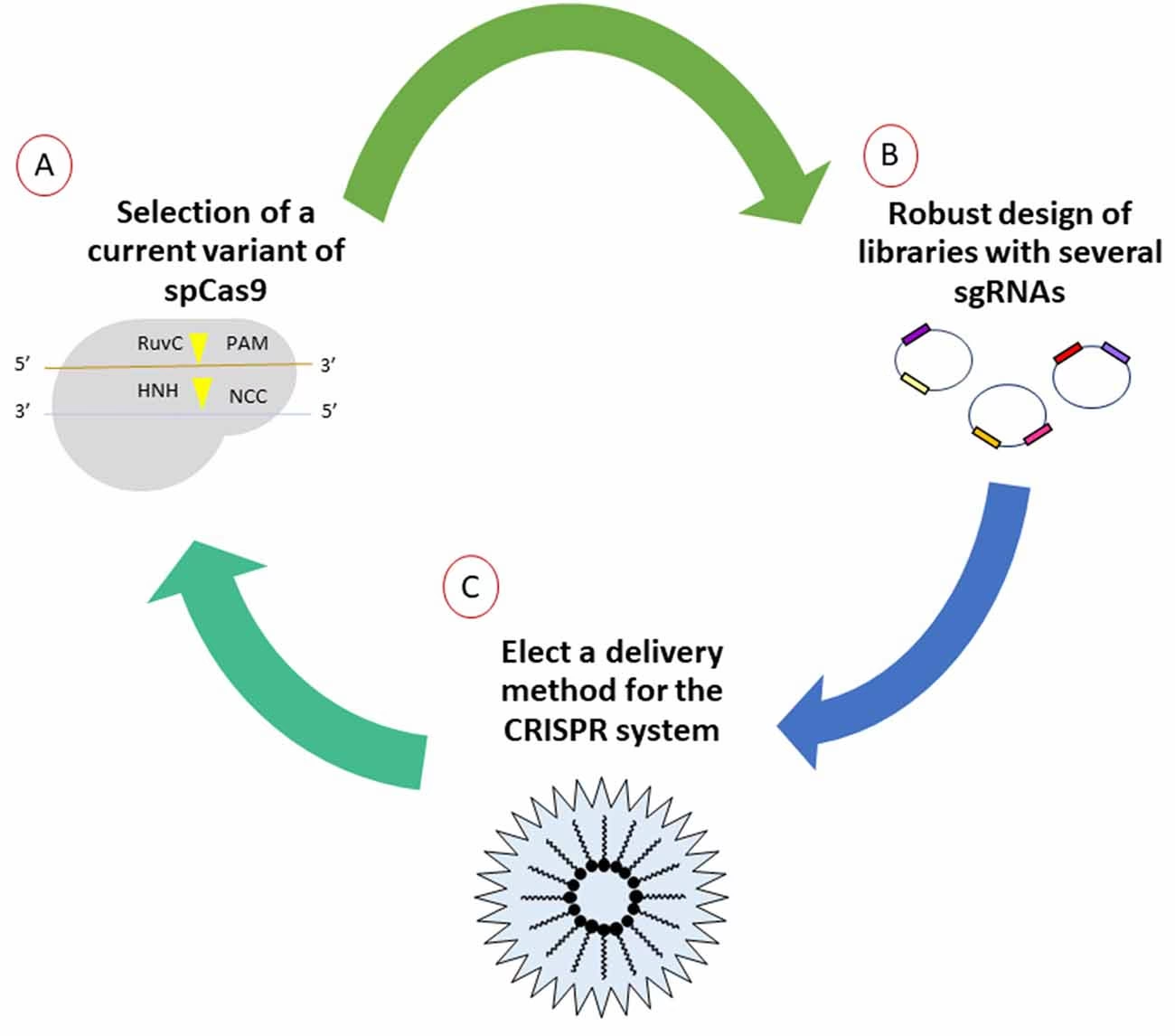
- La enzima Cas9 (o una variante modificada).
- Un ARN guía simple (sgRNA o gRNA).
El sgRNA es una molécula sintética diseñada para imitar el complejo de ARN que guía a Cas9 en la naturaleza. Tiene dos partes: una secuencia "espaciadora" de aproximadamente 20 nucleótidos que es complementaria a la secuencia de ADN objetivo que se desea modificar, y una secuencia "andamio" que se une a la enzima Cas9. Juntos, el sgRNA y Cas9 forman un complejo que navega por el núcleo de la célula hasta encontrar la secuencia de ADN que coincide con la secuencia espaciadora del sgRNA.
Para que Cas9 pueda cortar el ADN, debe encontrar una secuencia corta específica adyacente al sitio objetivo, conocida como PAM (Protospacer Adjacent Motif). La secuencia PAM más común para la enzima Cas9 de Streptococcus pyogenes es 5'-NGG (donde N es cualquier nucleótido). La presencia de la secuencia PAM es esencial para que Cas9 se una al ADN y realice el corte.

Una vez que el complejo sgRNA-Cas9 se une al sitio objetivo y encuentra la secuencia PAM, la enzima Cas9, que posee dos dominios nucleasa (RuvC y HNH), corta ambas hebras del ADN, generando una rotura de doble hebra (DSB, por sus siglas en inglés). Esta DSB activa los mecanismos de reparación del ADN de la propia célula. Los investigadores pueden aprovechar estos mecanismos de reparación para introducir cambios específicos en el genoma.
Existen dos vías principales de reparación que la célula puede utilizar para reparar la DSB:
- Unión de Extremos No Homólogos (NHEJ - Non-Homologous End Joining): Esta es la vía de reparación más común en las células de mamíferos. Es un proceso propenso a errores que a menudo introduce pequeñas inserciones o deleciones (indels) en el sitio de la rotura. Si la DSB ocurre dentro de la región codificante de un gen, estos indels pueden causar un desplazamiento en el marco de lectura, llevando a la inactivación del gen. Esta vía se utiliza a menudo para "noquear" o silenciar genes específicos.
- Reparación Dirigida por Homología (HDR - Homology Directed Repair): Esta vía es menos eficiente en la mayoría de las células, especialmente en neuronas postmitóticas. Requiere una plantilla de ADN homóloga que contenga la secuencia deseada para la reparación. Los investigadores pueden proporcionar una plantilla de ADN sintética con la secuencia modificada (por ejemplo, para corregir una mutación o insertar un nuevo fragmento de ADN) que flanquea el sitio de la rotura. La célula utiliza esta plantilla como referencia para reparar la DSB, incorporando así los cambios deseados de manera precisa.
La elección de la vía de reparación dependerá del objetivo del experimento: NHEJ para inactivar genes, y HDR para correcciones o inserciones precisas.
Ventajas de CRISPR-Cas9 sobre Otras Herramientas de Edición Genética
Antes de CRISPR, existían otras tecnologías de edición genética como las nucleasas con dedos de zinc (ZFNs) y las nucleasas efectoras de tipo activador de la transcripción (TALENs). Si bien estas herramientas fueron importantes avances, CRISPR-Cas9 ofrece varias ventajas significativas:
- Mayor Eficiencia y Precisión: CRISPR-Cas9 generalmente logra tasas de edición más altas y tiene menos efectos fuera del objetivo (cortes no deseados en otros sitios del genoma) en comparación con las tecnologías anteriores.
- Programabilidad y Fácil Diseño: El diseño del sgRNA es relativamente sencillo y se basa en la complementariedad de secuencias, lo que permite dirigirse a prácticamente cualquier sitio del genoma con una secuencia PAM adecuada. El diseño de ZFNs y TALENs era mucho más complejo y costoso.
- Multiplexación: CRISPR-Cas9 permite editar múltiples genes simultáneamente transfectando varios sgRNA dirigidos a diferentes sitios genómicos. Esto es considerablemente más difícil y costoso con ZFNs o TALENs.
- Menor Toxicidad Celular: En general, se ha observado que CRISPR-Cas9 induce menos toxicidad celular en comparación con las tecnologías anteriores.
- Asequibilidad: El diseño y la síntesis de los componentes de CRISPR son mucho más económicos que los de ZFNs y TALENs.
Estas ventajas han hecho de CRISPR-Cas9 la herramienta de elección en la mayoría de los laboratorios de investigación biomédica.
Aplicaciones de CRISPR en la Investigación Neurocientífica
La tecnología CRISPR ha tenido un impacto profundo en la neurociencia, permitiendo a los investigadores abordar preguntas fundamentales y desarrollar modelos de enfermedades con una precisión sin precedentes. Algunas de las aplicaciones clave incluyen:
- Ingeniería de Modelos Animales Transgénicos: CRISPR ha simplificado drásticamente la creación de modelos animales (como ratones, ratas, peces cebra y cerdos) con mutaciones específicas de genes neuronales, ya sean deleciones (knock-outs), inserciones (knock-ins) o mutaciones puntuales. Esto permite estudiar la función de genes específicos en el contexto de un organismo complejo y modelar enfermedades genéticas humanas.
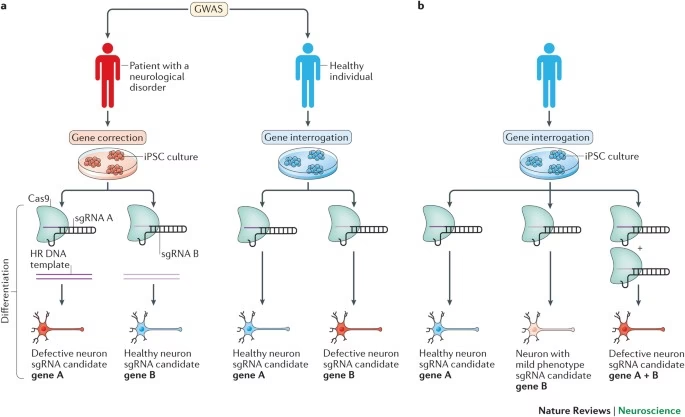
- Modelado de Enfermedades Neurológicas: Utilizando CRISPR en células (incluidas células madre pluripotentes inducidas - iPSCs - derivadas de pacientes) y modelos animales, los investigadores pueden recrear las condiciones genéticas de enfermedades neurodegenerativas y del desarrollo, lo que facilita el estudio de sus mecanismos subyacentes.
- Screening Genómico a Gran Escala: CRISPR permite realizar cribados genéticos de alto rendimiento, inactivando o activando sistemáticamente miles de genes para identificar aquellos que están involucrados en un proceso neuronal particular o en la patología de una enfermedad.
- Programación de Estados Celulares: Se pueden utilizar variantes de Cas9 (como la Cas9 "muerta" o dCas9, que se une al ADN pero no lo corta) fusionadas a dominios activadores o represores para modular la expresión génica de manera específica (CRISPRa para activar, CRISPRi para reprimir), lo que es útil para estudiar la función de genes en tipos celulares neuronales específicos.
- Registro de Linajes Celulares y Procesos Biológicos: CRISPR puede ser empleado para marcar genéticamente células y rastrear sus divisiones, migraciones y diferenciación a lo largo del desarrollo o en respuesta a estímulos, proporcionando información valiosa sobre la formación y plasticidad del sistema nervioso.
- Visualización de Loci Genómicos: La dCas9 puede fusionarse con proteínas fluorescentes para visualizar la ubicación de secuencias de ADN específicas dentro del núcleo de neuronas vivas, permitiendo estudiar la organización del genoma y la dinámica de la cromatina.
- Purificación de Regiones Genómicas y Proteínas Asociadas: Al fusionar dCas9 con etiquetas de afinidad (como biotina), los investigadores pueden aislar secuencias de ADN específicas y las proteínas (como factores de transcripción) unidas a ellas, lo que ayuda a comprender la regulación génica en neuronas.
CRISPR-Cas9 como Herramienta Terapéutica en Trastornos Neurológicos
Uno de los enfoques más prometedores de CRISPR en neurociencia es su uso potencial para corregir mutaciones genéticas que causan enfermedades neurológicas o para modular la expresión de genes relevantes para la patología. Numerosos estudios preclínicos han demostrado el potencial de CRISPR en este ámbito, especialmente en enfermedades neurodegenerativas monogénicas.
Enfermedad de Alzheimer
Si bien la mayoría de los casos de Alzheimer (EA) son esporádicos, las formas de inicio temprano están ligadas a mutaciones en genes como APP, PSEN1 y PSEN2. La acumulación de péptido beta-amilo (Aβ), derivado del procesamiento anormal de la proteína APP por enzimas como BACE1, es una característica clave de la EA. CRISPR ha sido utilizado para:
- Reducir la expresión del gen BACE1 utilizando complejos Cas9-sgRNA administrados mediante nanopartículas en modelos de ratón de EA, logrando una reducción significativa en la acumulación de placas amiloides.
- Eliminar mutaciones suecas en fibroblastos humanos y modelos de ratón para reducir los niveles de proteína APP mutante.
- Corregir mutaciones en PSEN1 y PSEN2 en neuronas derivadas de células madre pluripotentes inducidas (iPSCs) de pacientes, restaurando funciones neuronales y reduciendo la producción de Aβ42/40.
- Crear modelos de ratón con eliminación del gen KIBRA (asociado al rendimiento cognitivo en EA) para investigar su papel neuroprotector.
Enfermedad de Parkinson
La enfermedad de Parkinson (EP) se caracteriza por la pérdida de neuronas dopaminérgicas. Mutaciones en genes como PINK1, SNCA (α-sinucleína) y LRRK2 están implicadas en formas genéticas de EP. CRISPR ha sido utilizado para:
- Reducir la expresión del gen SNCA (cuya proteína α-sinucleína se acumula en los cuerpos de Lewy) utilizando CRISPRi (Cas9 inactiva fusionada a un represor) en líneas celulares neuronales.
- Modular epigenéticamente el intrón 1 del gen SNCA para reducir su expresión en neuronas dopaminérgicas derivadas de iPSCs con múltiples copias del gen.
- Inactivar el gen MCU (canales de calcio mitocondriales) en modelos de pez cebra con EP (deficiencia de PINK1), restaurando la función mitocondrial.
- Crear modelos de iPSCs con genes marcados (como TH-GFP) o mutaciones específicas (como en LRRK2) para estudiar la patología y el desarrollo de terapias.
- Generar modelos porcinos de EP con mutaciones en SCNA para estudiar la progresión de la enfermedad en un organismo superior.
Enfermedad de Huntington
Esta enfermedad autosómica dominante está causada por una expansión de repeticiones CAG en el gen HTT. CRISPR se ha empleado para:
- Eliminar una región de 44 kb que incluye la expansión CAG en el alelo mutante del gen HTT, logrando una inactivación completa de la expresión de la proteína mutante sin afectar el alelo normal.
- Dirigirse a la región 5'-UTR y el límite exón-intrón del gen HTT mutante para interferir con su transcripción en células madre mesenquimales de modelos de ratón.
- Utilizar una nickasa Cas9 (que corta una sola hebra) para intentar reemplazar las repeticiones CAG expandidas por repeticiones normales.
- Administrar Cas9 mediante vectores virales (AAV) directamente en el estriado de modelos de ratón de HD para interrumpir el gen HTT mutante, reduciendo las inclusiones neurotóxicas y mejorando los déficits motores.
Ataxia de Friedreich
Esta enfermedad autosómica recesiva se debe a la expansión de repeticiones GAA en el intrón 1 del gen FXN, que codifica la proteína frataxina. Los niveles bajos de frataxina causan la enfermedad. CRISPR ha sido utilizado para:
- Administrar Cas9 mediante vectores virales en modelos de ratón de la enfermedad, buscando aumentar o disminuir los niveles de frataxina dependiendo del modelo y el objetivo.
- Crear modelos celulares inducibles donde los niveles de frataxina puedan ser controlados mediante edición CRISPR del gen FXN endógeno.
Síndrome del Cromosoma X Frágil
Este trastorno ligado al cromosoma X está causado por una expansión de repeticiones CGG en la región 5'-UTR del gen FMR1, lo que lleva a la hipermetilación y silenciación del gen. CRISPR ha sido utilizado para:
- Excindir las repeticiones CGG patogénicas en células madre embrionarias (ESCs) e iPSCs derivadas de pacientes, logrando la desmetilación espontánea y la restauración de la expresión de la proteína FMRP.
- Utilizar Cas9 fusionada a un activador transcripcional (CRISPRa) para aumentar los niveles de FMRP en modelos de ESCs humanas, incluso en presencia de hipermetilación.
- Administrar complejos Cas9-sgRNA mediante nanopartículas (CRISPR-gold) para dirigirse al gen Grm5 (asociado a la fisiopatología del síndrome) en neuronas de modelos de ratón, reduciendo los niveles de la proteína mGluR5 y normalizando el comportamiento.
Ataxias Espinocerebelosas
Las ataxias espinocerebelosas (SCAs), como SCA2 y SCA3, son trastornos autosómicos dominantes causados por expansiones de repeticiones CAG en los genes ATXN2 y ATX3, respectivamente. CRISPR ha sido utilizado para:
- Generar líneas celulares iPSC corregidas a partir de pacientes con SCA2, reemplazando las repeticiones CAG expandidas por un número normal de repeticiones.
- Eliminar las repeticiones CAG patogénicas en el gen ATX3 en iPSCs derivadas de pacientes con SCA3.
Distrofia Muscular de Duchenne
Aunque no es estrictamente un trastorno primario del sistema nervioso central, afecta gravemente la función neuromuscular. Es una enfermedad ligada al X causada por mutaciones en el gen de la distrofina (DMD). CRISPR ha sido utilizado para:
- Restaurar la función de la proteína distrofina en modelos de ratón (mdx) que portan una mutación en el exón 23, utilizando tanto NHEJ como HDR.
- Lograr una alta restauración de la proteína diana en modelos de ratón que carecen del exón 50, utilizando entrega viral (AAV).
- Emplear nanopartículas (CRISPR-gold) para administrar Cas9 intramuscularmente, mejorando los niveles de distrofina y la fuerza muscular.
- Utilizar nuevas nucleasas como Cpf1 para corregir mutaciones en iPSCs de modelos de ratón.
Distrofia Miotónica
La distrofia miotónica tipo 1 (DM1) es causada por una expansión de repeticiones CTG en el gen DMPK. CRISPR ha sido utilizado para:
- Excindir completamente el gen DMPK en mioblastos, eliminando los focos ribonucleares patogénicos.
- Utilizar dCas9 modificada para eliminar el ARN mutante, reduciendo sus niveles en mioblastos de DM1.
- Administrar dCas9 mediante vectores virales en modelos de ratón de DM1, logrando una mejora en la miotonía.
Potencial en el Trastorno del Espectro Autista
Estudios recientes en modelos animales sugieren que CRISPR podría tener potencial en algunos trastornos del espectro autista (TEA) ligados a genes específicos. En un estudio con ratones adolescentes que portaban una mutación en el gen SCN2A (asociado al autismo), la inyección de una versión modificada de CRISPR (que activa genes en lugar de cortarlos) dirigida al gen SCN2A logró aumentar la expresión de la copia intacta del gen. Esto revirtió déficits neuronales observados en estos ratones, sugiriendo que las mutaciones en este gen podrían ser tratables incluso después de la infancia.
Vías de Reparación del ADN: NHEJ vs. HDR
Comprender cómo la célula repara la rotura de doble hebra inducida por CRISPR es crucial para predecir el resultado de la edición genética. Las dos vías principales, NHEJ y HDR, tienen diferentes características y aplicaciones:
| Característica | Unión de Extremos No Homólogos (NHEJ) | Reparación Dirigida por Homología (HDR) |
|---|---|---|
| Plantilla de ADN | No requiere plantilla | Requiere plantilla de ADN homóloga |
| Precisión | Propensa a errores (indels) | Precisa (introduce el cambio de la plantilla) |
| Eficiencia | Alta en la mayoría de las células | Baja en muchas células (especialmente postmitóticas como neuronas) |
| Resultado Típico | Inactivación del gen (knock-out) | Corrección de mutaciones, inserción de secuencias |
| Fase del Ciclo Celular | Activa durante todo el ciclo | Principalmente activa en fases S y G2 (cuando hay cromátidas hermanas) |
Desafíos y Limitaciones de CRISPR-Cas9 en Trastornos Neurológicos
A pesar de su inmenso potencial, la aplicación de CRISPR-Cas9 en el sistema nervioso central enfrenta varios desafíos:
- Efectos Fuera del Objetivo: Aunque más precisos que las herramientas anteriores, los cortes no deseados en sitios genómicos similares al objetivo siguen siendo una preocupación. Estos efectos fuera del objetivo podrían generar mutaciones no deseadas con consecuencias adversas.
- Entrega In Vivo: Llevar los componentes de CRISPR (Cas9 y sgRNA) de manera segura y eficiente al tipo celular neuronal correcto dentro del cerebro es un obstáculo importante. La barrera hematoencefálica dificulta la entrega. Se están explorando diversas estrategias, como vectores virales (virus adenoasociados - AAV, lentivirus), nanopartículas y lipofectaminas, pero la seguridad a largo plazo y la eficiencia de la entrega específica siguen bajo investigación.
- Eficiencia de HDR en Neuronas: La vía de reparación HDR, esencial para correcciones precisas de mutaciones, es menos activa en células postmitóticas como las neuronas maduras. Esto limita la capacidad de corregir mutaciones de un solo nucleótido o insertar secuencias grandes de manera eficiente en estas células cruciales para la función cerebral.
- Corrección Específica de Alelos: En enfermedades autosómicas dominantes donde solo un alelo está mutado, corregir selectivamente el alelo enfermo sin afectar el alelo sano es un desafío complejo.
- Respuesta Inmune: Cas9 es una proteína de origen bacteriano, y el organismo huésped podría desarrollar una respuesta inmune contra ella, limitando la eficacia de tratamientos de dosis múltiple o la seguridad a largo plazo.
- Edición Irreversible: La edición genética realizada por CRISPR es permanente, lo que subraya la necesidad de una precisión y seguridad extremas antes de su aplicación clínica.
Perspectivas Futuras de CRISPR en Neurociencia
El campo de CRISPR en neurociencia está evolucionando rápidamente, con varias áreas de investigación activas y prometedoras:
- Mejora de la Especificidad y Reducción de Efectos Fuera del Objetivo: Se están desarrollando variantes de Cas9 y nuevos ARN guía para aumentar la especificidad y minimizar los cortes no deseados.
- Nuevas Enzimas de Edición: Se están explorando y optimizando otras enzimas de la familia CRISPR (como Cpf1/Cas12a, CasX) y sistemas de edición sin corte (como la edición de bases y la edición prime) que podrían ofrecer mayor precisión, diferentes requisitos de PAM o la capacidad de editar ADN sin inducir DSBs.
- Optimización de Métodos de Entrega: Se están desarrollando nuevas estrategias de entrega más eficientes, seguras y específicas para el cerebro, incluyendo nuevos tipos de vectores virales, nanopartículas diseñadas para cruzar la barrera hematoencefálica y métodos de entrega física.
- Edición de ARN: Sistemas como CRISPR-Cas13, que se dirigen al ARN en lugar del ADN, están siendo investigados por su potencial para modular la expresión génica de forma reversible, lo que podría ser ventajoso para algunas aplicaciones terapéuticas en el cerebro.
- Modelos de Enfermedad Mejorados: CRISPR continúa siendo una herramienta clave para crear modelos celulares (como organoides cerebrales derivados de iPSCs de pacientes) y animales que recapitulan de manera más precisa las características de las enfermedades neurológicas humanas.
- Investigación de Elementos No Codificantes: CRISPR se está utilizando para investigar el papel de ARN no codificantes (como microARNs y lncRNAs) en la función neuronal y la patología de enfermedades, ya que estos elementos reguladores son cada vez más reconocidos por su importancia.
Preguntas Frecuentes (FAQ)
¿Qué significa CRISPR?
Significa Repeticiones Palindrómicas Cortas Agrupadas y Espaciadas Regularmente, y se refiere a un sistema de defensa bacteriano que ha sido adaptado para la edición genética.
¿Cómo funciona básicamente CRISPR-Cas9?
Un ARN guía (sgRNA) dirige la enzima Cas9 a una secuencia específica de ADN. Cas9 corta el ADN en ese sitio (si hay una secuencia PAM adyacente), y la célula intenta reparar la rotura, permitiendo a los científicos introducir cambios.
¿Se utiliza CRISPR en neurociencia?
Sí, CRISPR es una herramienta fundamental en la neurociencia moderna, utilizada para investigar la función génica en el cerebro, crear modelos de enfermedades neurológicas y desarrollar terapias genéticas potenciales.
¿CRISPR puede revertir el autismo?
La investigación preclínica en modelos de ratón con mutaciones en genes asociados al autismo (como SCN2A) ha mostrado que CRISPR puede revertir algunos déficits neuronales. Sin embargo, esto es investigación temprana en animales y no una cura para el autismo en humanos.
¿Cuál es el principal desafío para usar CRISPR en el cerebro humano?
Los principales desafíos incluyen la entrega segura y eficiente de los componentes de CRISPR a las células cerebrales específicas, evitar efectos fuera del objetivo y superar la respuesta inmune del paciente.
Conclusión
La tecnología CRISPR-Cas9 ha abierto una nueva era en la neurociencia. Su precisión, facilidad de uso y capacidad de multiplexación la han convertido en una herramienta indispensable tanto para la investigación básica como para el desarrollo de enfoques terapéuticos para trastornos neurológicos. Hemos visto cómo está siendo aplicada para desentrañar los complejos mecanismos de enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la enfermedad de Huntington, así como para explorar el potencial tratamiento de trastornos como el síndrome del Cromosoma X Frágil o incluso el autismo en modelos preclínicos.
A pesar de los notables avances, existen desafíos significativos que deben abordarse antes de que CRISPR pueda ser ampliamente utilizado en la clínica para tratar enfermedades del sistema nervioso. La entrega segura y eficiente al cerebro, la minimización de los efectos fuera del objetivo y la superación de las respuestas inmunes son áreas de intensa investigación. Sin embargo, con el rápido desarrollo de nuevas enzimas, métodos de entrega mejorados y estrategias de edición más sofisticadas, el futuro de la edición genética en neurociencia parece increíblemente prometedor. CRISPR no es solo una herramienta; es una puerta de entrada para comprender y, en última instancia, corregir los fallos genéticos que afectan a la mente humana.
Si quieres conocer otros artículos parecidos a CRISPR: Editando el Código Cerebral puedes visitar la categoría Neurociencia.

