El cerebro humano es una red intrincada de señales químicas y eléctricas que orquestan cada aspecto de nuestra existencia, desde los pensamientos más complejos hasta las respuestas más básicas de supervivencia. Entre estas señales, el Factor Liberador de Corticotropina (CRF) emerge como un actor principal, especialmente en lo que respecta a nuestra capacidad para percibir y responder al estrés. Pero, ¿qué significa exactamente CRF en el contexto cerebral y por qué es tan importante?
CRF son las siglas en inglés de Corticotropin-releasing factor, que en español se traduce como Factor Liberador de Corticotropina. Este neuropéptido es una molécula fundamental en el sistema nervioso central, responsable de mediar una amplia gama de respuestas a estímulos aversivos o estresantes. Su influencia se extiende a las respuestas conductuales, cognitivas, autonómicas, neuroendocrinas e inmunológicas.
- Más Allá del CRF: La Familia de Péptidos Relacionados
- Los Receptores del CRF: CRF1 y CRF2
- Un Mapa en el Cerebro: Distribución de CRF y sus Receptores
- La Comunicación Celular: Vías de Señalización
- El Director de Orquesta del Estrés y la Conducta
- Cuando el Sistema Falla: CRF y Trastornos
- Regulando la Señal: Desensibilización y Downregulation
- Hacia el Futuro: Antagonistas del CRF
Más Allá del CRF: La Familia de Péptidos Relacionados
El CRF no trabaja solo. Pertenece a una familia de péptidos estrechamente relacionados que también juegan roles cruciales en la fisiología del estrés, tanto a nivel central como periférico. Estos incluyen las urocortinas (urocortina 1, urocortina 2 y urocortina 3), así como péptidos no mamíferos como la sauvagina (aislada de ranas) y la urotensina I (aislada de peces). La urocortina 1 (UCN1) fue descubierta después del CRF y nombrada por su similitud con la urotensina I y el CRF. Posteriormente, se identificaron la urocortina 2 (UCN2) y la urocortina 3 (UCN3), que inicialmente fueron llamadas "stresscopin-related peptide" y "stresscopin", respectivamente, sugiriendo su papel en las respuestas de 'afrontamiento' al estrés. Sin embargo, el nombre urocortina se adoptó debido a su alta homología con la UCN1 y sus acciones biológicas más allá del afrontamiento. La conservación evolutiva de estos péptidos, presentes incluso en especies tan antiguas como la rana de uñas africana, subraya su importancia fundamental para la homeostasis y la supervivencia.
La estructura de estos péptidos es notablemente conservada a través de las especies. El CRF mamífero es un péptido de 41 aminoácidos. Su función biológica está determinada por el extremo C-terminal amidado, que se une al bolsillo de unión extracelular del receptor. El extremo N-terminal, por su parte, contacta otras partes del receptor para iniciar la señalización celular. Las formas mamíferas de UCN1, UCN2 y UCN3 también son péptidos con estructuras y propiedades farmacológicas específicas, aunque existen algunas diferencias entre especies y en su procesamiento. Por ejemplo, el UCN2 humano carece del sitio clásico de amidación C-terminal, y la potencia del UCN3 humano en el receptor CRF2 es menor que la de su homólogo de ratón.
Los Receptores del CRF: CRF1 y CRF2
Las acciones del CRF y los péptidos relacionados están mediadas principalmente por la activación de dos subtipos de receptores acoplados a proteínas G (GPCR) de clase B1 en el sistema nervioso central y la hipófisis anterior: los receptores CRF1 y receptores CRF2. Ambos receptores son polipéptidos que comparten una alta identidad de secuencia (más del 70% entre ellos y más del 80% entre homólogos de la misma especie). Las regiones más conservadas son los lazos intracelulares y las siete hélices transmembrana (TM1-7), con una conservación de más del 90% y 85% respectivamente. Notablemente, el lazo intracelular 3 (IC3), crucial para el acoplamiento a la proteína G estimuladora (GαS), está 100% conservado en todos los receptores CRF conocidos.
Existen múltiples isoformas funcionales del receptor CRF2 (CRF2a, CRF2b, CRF2c), que difieren en sus extremos N-terminales. El CRF2a es la única variante encontrada en especies no mamíferas, mientras que el CRF2a y CRF2b se expresan en mamíferos. El CRF2c solo se ha detectado en regiones límbicas del sistema nervioso central humano. Aunque hay diferencias mínimas en sus perfiles farmacológicos, el splicing probablemente determina la distribución tisular y celular de estos receptores. En contraste, las supuestas variantes del receptor CRF1, principalmente identificadas en tejidos humanos, a menudo carecen de actividad de unión o señalización significativa y no cumplen los criterios de variantes funcionales según los comités de nomenclatura.
Un Mapa en el Cerebro: Distribución de CRF y sus Receptores
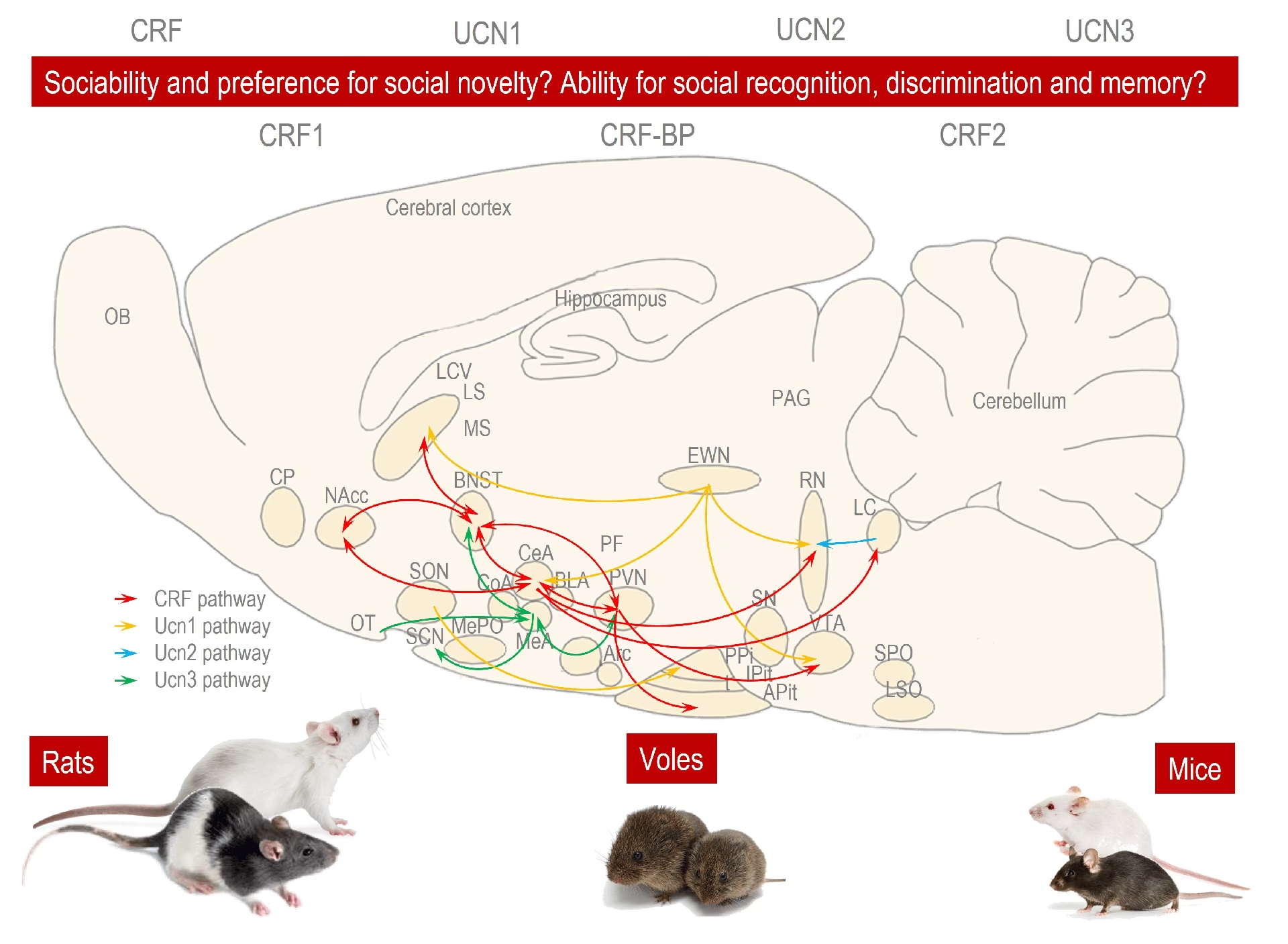
La localización de CRF y sus receptores en el sistema nervioso central proporciona pistas importantes sobre sus funciones. Las neuronas que expresan CRF están ampliamente distribuidas en el cerebro de mamíferos, con niveles particularmente altos en regiones como el núcleo paraventricular (PVN) y el área lateral del hipotálamo, los bulbos olfatorios, el neocórtex, los circuitos límbicos (incluyendo núcleos amigdalinos y el núcleo del lecho de la estría terminal, BNST), el hipocampo y regiones del tronco encefálico como el núcleo del tracto solitario y el locus coeruleus (LC).
Los receptores CRF1 tienen una distribución amplia en el SNC de roedores, encontrándose en el neocórtex, núcleo dorsomedial hipotalámico, núcleo basolateral de la amígdala (BLA), septum medial y neuronas dopaminérgicas de la sustancia negra, área tegmental ventral y tronco encefálico. También se observan en neuronas colinérgicas. En primates, los receptores CRF1 están presentes en muchas regiones neocorticales, especialmente en las cortezas prefrontal y cingulada, y en el LC y CeA. La hipófisis anterior de roedores y primates expresa altos niveles de receptores CRF1, cruciales para la secreción de ACTH.
Los receptores CRF2, en contraste, tienen una distribución más restringida y se concentran en regiones cerebrales discretas. En roedores, son prominentes en el núcleo ventromedial hipotalámico, septum lateral (LS), núcleos amigdalinos corticales y mediales, núcleo dorsal del rafe (DRN) y núcleo del tracto solitario. En el DRN, la expresión de CRF2 es significativamente más abundante que la de CRF1, localizándose en neuronas serotoninérgicas y GABAérgicas. En primates, la expresión de CRF2 también se encuentra en regiones neocorticales, amígdala central (CeA) y la hipófisis anterior. La co-expresión de CRF1 y CRF2 en algunas regiones sugiere una regulación coordinada.
La distribución de los ligandos endógenos también varía. CRF tiene una afinidad mayor por el receptor CRF1 que por el CRF2. UCN2 y UCN3 son ligandos altamente selectivos para el receptor CRF2, con UCN2 mostrando generalmente mayor afinidad que UCN3 por el CRF2a. UCN1, sauvagina y urotensina I se unen a ambos receptores, pero muestran alta afinidad por el CRF2, mientras que h/rCRF y oCRF tienen menor afinidad por este subtipo.
La Comunicación Celular: Vías de Señalización
Aunque los dominios transmembrana e intracelulares de los receptores CRF1 y CRF2 son altamente homólogos, lo que sugiere que se acoplan a proteínas G similares y usan segundos mensajeros parecidos, la señalización puede variar según el contexto celular. El modo dominante de señalización para ambos receptores, especialmente el CRF1, es la activación de la vía de la adenilil ciclasa-proteína quinasa A (PKA). La unión del agonista cambia la conformación del receptor, aumentando su afinidad por la proteína Gs. La subunidad α de Gs se acopla al lazo intracelular 3, estimulando la adenilil ciclasa y aumentando la producción de AMP cíclico. El AMP cíclico activa la PKA, lo que lleva a eventos posteriores como la fosforilación de CREB.
Sin embargo, los receptores CRF también pueden señalizar a través de otras vías. Se ha observado la activación de la vía de la fosfolipasa C-proteína quinasa C (PKC), posiblemente acoplándose a Gqα. Esto resulta en un aumento de los niveles de calcio intracelular y la formación de inositol 1,4,5-trifosfato (IP3). Esta vía parece depender de las características del fondo celular, ya que no ocurre en todas las líneas celulares que expresan receptores CRF.
Además, los receptores CRF pueden activar la vía de la Akt/proteína quinasa B (PKB) y la cascada de la cinasa regulada por señal extracelular (ERK)-MAP cinasa. La activación de CRF1 o CRF2 puede llevar a la fosforilación de Akt y ERK1/2, implicando mecanismos como PI-3 cinasa, Ras-Raf1 cinasa y MEK1/2. Estas vías de señalización adicionales sugieren una complejidad en la respuesta celular a la activación del receptor CRF, y su reclutamiento puede depender del tipo celular y del estímulo.
El Director de Orquesta del Estrés y la Conducta
Uno de los roles mejor establecidos del CRF en el cerebro es su función central en la regulación del Eje Hipotalámico-Pituitario-Adrenal (HPA), la principal vía neuroendocrina de respuesta al estrés. El CRF liberado desde el hipotálamo estimula la hipófisis anterior para liberar hormona adrenocorticotrópica (ACTH), que a su vez actúa sobre las glándulas suprarrenales para liberar glucocorticoides (como el cortisol). Este eje es fundamental para movilizar recursos y preparar al cuerpo para enfrentar amenazas.
Además de su papel neuroendocrino, el CRF tiene efectos directos en la conducta mediada por sus receptores en diversas áreas cerebrales. El receptor CRF1 es el principal mediador de muchas conductas asociadas a la ansiedad y la depresión, así como de las respuestas conductuales al estrés. Estudios preclínicos con antagonistas de CRF1 o deleciones genéticas de este receptor han demostrado una atenuación significativa de conductas defensivas en roedores, como la congelación (freezing), la evitación, las respuestas de sobresalto y la agresión defensiva. Estos efectos son particularmente notables en animales con alta ansiedad basal o expuestos previamente a estrés, sugiriendo que los antagonistas de CRF1 podrían ser especialmente efectivos en pacientes con trastornos afectivos bajo estrés considerable.
El papel de los receptores CRF2 en la ansiedad y el estrés es menos claro y ha arrojado resultados contradictorios. Una hipótesis sugiere que la activación de CRF1 inicia respuestas de miedo y ansiedad, mientras que la activación de CRF2 restablece la homeostasis al contrarrestar los efectos aversivos de la señalización de CRF1. Una hipótesis alternativa propone que CRF1 y CRF2 contribuyen a modos defensivos opuestos: CRF1 mediando respuestas defensivas activas ante estresores escapables, y CRF2 mediando respuestas de ansiedad y depresión inducidas por estresores incontrolables. La investigación en el núcleo dorsal del rafe (DRN), una región rica en receptores CRF2, apoya esta última hipótesis, sugiriendo que la activación de CRF2 en esta área es crucial para el desarrollo de la indefensión aprendida, un modelo de depresión inducida por estrés incontrolable.

La plasticidad del sobresalto acústico, una medida de la capacidad de la información sensorial para modular conductas defensivas, también está influenciada por los receptores CRF. La activación de CRF1 parece ser necesaria y suficiente para los déficits en la inhibición prepulso (PPI) del sobresalto inducidos por CRF y para los aumentos en la magnitud del sobresalto. La activación de CRF2, sin embargo, parece oponerse a la acción de CRF1 sobre la PPI, mientras que puede potenciar los aumentos en la magnitud del sobresalto. Esto sugiere que CRF1 puede reducir la flexibilidad conductual, mientras que CRF2 podría aumentarla, modulando cómo la información sensorial impacta las respuestas defensivas.
Cuando el Sistema Falla: CRF y Trastornos
La disfunción del sistema CRF se ha implicado fuertemente en la etiología de diversos trastornos psiquiátricos. Indicadores de sistemas CRF centrales hiperactivos, como la hipersecreción de CRF y el funcionamiento anormal del eje HPA, se han identificado en subpoblaciones de pacientes con trastornos de ansiedad, estrés y depresión. Aunque los receptores CRF se desensibilizan rápidamente en presencia de altas concentraciones de agonistas (un mecanismo normal para limitar la respuesta), una disregulación concomitante de los mecanismos que controlan la magnitud y duración de la señalización del receptor CRF también puede contribuir a la neurotransmisión mejorada observada en estos pacientes.
Un ejemplo clínico de disfunción del receptor CRF1 es la enfermedad de Cushing, caracterizada por hipercortisolemia dependiente de ACTH. En las células adenomatosas corticotropas de pacientes con Cushing, los receptores CRF1 no se desensibilizan ni se internalizan adecuadamente en respuesta al CRF, lo que resulta en una señalización persistentemente mejorada y una secreción aumentada de ACTH.
Regulando la Señal: Desensibilización y Downregulation
La actividad de los receptores CRF está finamente regulada a nivel molecular para prevenir una estimulación excesiva. La desensibilización homóloga, un proceso por el cual la exposición prolongada a un agonista reduce la respuesta del receptor, es un mecanismo clave. Este proceso a menudo implica la fosforilación del receptor por quinasas de receptores acoplados a proteínas G (GRKs), como GRK2 y GRK3, seguida por el reclutamiento de arrestinas (como βarrestina1), que impiden el acoplamiento del receptor a la proteína G y promueven su internalización en vesículas recubiertas de clatrina. La internalización puede llevar a la degradación del receptor (downregulation) o a su reciclaje y resensibilización.
La exposición prolongada al CRF o al estrés puede inducir desensibilización y downregulation de los receptores CRF1 en la hipófisis anterior, un mecanismo de retroalimentación negativa. Sin embargo, en ciertas condiciones o tipos celulares (como en las células adenomatosas de Cushing o algunas líneas celulares), esta regulación puede ser defectuosa. El estrés agudo o crónico también puede alterar la expresión de mRNA y la unión de los receptores CRF en diferentes regiones cerebrales de manera dependiente del área y del tipo de estrés.
Hacia el Futuro: Antagonistas del CRF
Dada la fuerte evidencia que vincula la señalización hiperactiva del CRF, especialmente a través del receptor CRF1, con los trastornos de ansiedad, estrés y depresión, el sistema CRF se ha convertido en un objetivo terapéutico prometedor. Se están desarrollando intensivamente antagonistas de moléculas pequeñas del receptor CRF1 como potenciales tratamientos farmacoterapéuticos para el trastorno de ansiedad generalizada, el trastorno de pánico, el trastorno de estrés postraumático y la depresión mayor.
Aunque el papel de los receptores CRF2 en la patofisiología de estos trastornos es menos claro y más controvertido, si se confirma que contribuyen significativamente a la ansiedad y la depresión, el desarrollo de antagonistas selectivos de CRF2 también podría ser terapéuticamente útil. El diseño de estos antagonistas se basa en la comprensión de la estructura-actividad de los péptidos y en la identificación de sitios de unión en los receptores.
Comparativa: Receptores CRF1 vs CRF2
| Característica | Receptor CRF1 | Receptor CRF2 |
|---|---|---|
| Distribución Principal (Roedores) | Amplia (Corteza, Hipocampo, Amígdala BLA, Hipotálamo PVN, Hipófisis Ant.) | Restringida (Septum Lateral, Amígdala Cortical/Medial, Hipotálamo VMH, DRN, Hipófisis Ant. (baja)) |
| Afinidad por Ligandos Endógenos | Alta por CRF y UCN1; Baja por UCN2, UCN3 | Alta por UCN1, UCN2, UCN3; Baja por CRF |
| Rol Hipotetizado en Ansiedad/Estrés | Mediador principal de respuestas de ansiedad/miedo y eje HPA | Rol controvertido; posible modulación o oposición a efectos CRF1; implicado en indefensión aprendida |
| Potencial Terapéutico (Antagonistas) | Prometedor para trastornos de ansiedad y depresión | Potencial menos claro, requiere más investigación |
Preguntas Frecuentes sobre el CRF Cerebral
¿Qué es el CRF en el cerebro?
CRF significa Factor Liberador de Corticotropina. Es un neuropéptido clave en el cerebro que media las respuestas conductuales, cognitivas, autonómicas, neuroendocrinas e inmunológicas al estrés.¿Cuáles son los principales receptores del CRF en el cerebro?
Los dos subtipos principales son el receptor CRF1 y el receptor CRF2. Ambos son receptores acoplados a proteínas G y se encuentran en diferentes regiones del sistema nervioso central.¿Cómo funciona el CRF a nivel celular?
Principalmente activa la vía de señalización del AMP cíclico-PKA a través de la proteína Gs. También puede activar otras vías como la PLC-PKC, Akt y MAP cinasa, dependiendo del tipo de célula.¿Qué papel juega el CRF en la respuesta al estrés?
Es fundamental en la activación del eje Hipotalámico-Pituitario-Adrenal (HPA), que resulta en la liberación de hormonas del estrés. También influye directamente en conductas relacionadas con el miedo y la ansiedad.¿Está relacionado el CRF con los trastornos de ansiedad y depresión?
Sí, la evidencia sugiere que un sistema CRF central hiperactivo, particularmente a través del receptor CRF1, contribuye a la patofisiología de estos trastornos.¿Se están desarrollando tratamientos dirigidos al sistema CRF?
Sí, los antagonistas selectivos del receptor CRF1 están siendo investigados intensivamente como posibles nuevos fármacos para tratar trastornos de ansiedad y depresión.
En conclusión, el sistema del Factor Liberador de Corticotropina en el cerebro es un componente vital en nuestra respuesta al estrés y un regulador complejo de la conducta y la fisiología. La investigación continua sobre sus péptidos, receptores y vías de señalización no solo profundiza nuestra comprensión de las bases neuronales del estrés y los trastornos afectivos, sino que también abre nuevas vías para el desarrollo de terapias innovadoras que podrían aliviar el sufrimiento asociado a estas condiciones.
Si quieres conocer otros artículos parecidos a CRF en el Cerebro: El Factor Clave del Estrés puedes visitar la categoría Neurociencia.
