El cerebro humano es una red de complejidad asombrosa, donde innumerables moléculas trabajan en concierto para dar forma a nuestros pensamientos, emociones y comportamientos. Entre estos actores cruciales se encuentra la proteína de unión al elemento de respuesta a cAMP (CREB), un factor de transcripción que reside en el núcleo de las células neuronales y actúa como un interruptor maestro para la expresión de genes.
CREB es mucho más que una simple proteína; es un integrador esencial de diversas señales intracelulares. Su actividad se correlaciona directamente con procesos neuronales fundamentales como la proliferación, diferenciación, supervivencia, neurogénesis y, de manera crucial, la plasticidad sináptica, que es la base del aprendizaje y la memoria. Investigaciones recientes han puesto de relieve su participación en las vías de señalización relacionadas con la patogénesis y la terapia de trastornos mentales severos, incluyendo la esquizofrenia, lo que lo convierte en un foco de investigación de gran relevancia en la neurociencia moderna.
- ¿Qué es CREB? Fundamentos Moleculares
- Estructura y Variantes de CREB
- Cascadas de Señalización que Regulan a CREB
- La Interacción entre Dopamina y CREB
- CREB, Neurotrofinas y Neurodesarrollo
- El Rol de CREB en la Esquizofrenia
- CREB y la Regulación del Estado de Ánimo en el Núcleo Accumbens
- CREB y la Formación de la Memoria
- CREB y la Potenciación a Largo Plazo (LTP)
- Tabla Comparativa: Diferentes Modelos de Ratón CREB y sus Efectos
- Interacciones con Genes de Susceptibilidad a la Esquizofrenia
- CREB como Blanco Terapéutico Potencial para la Esquizofrenia
- Preguntas Frecuentes sobre CREB
- Conclusión
¿Qué es CREB? Fundamentos Moleculares
La proteína de unión al elemento de respuesta a cAMP (CREB) es un factor de transcripción que se localiza principalmente en el núcleo celular. Su función principal es regular la expresión de genes. Para ejercer su acción, CREB debe ser activada, lo que ocurre principalmente mediante la fosforilación de un residuo específico, la Serina 133 (Ser133), por diversas quinasas activadas por receptores, como la proteína quinasa A (PKA), la quinasa dependiente de calmodulina (CaMK), las quinasas activadas por mitógenos (MAPK) y otras. Una vez fosforilada, CREB se une a secuencias de ADN específicas conocidas como elementos de respuesta a cAMP (CRE) en las regiones promotoras de sus genes diana. Esta unión, junto con el reclutamiento de la proteína de unión a CREB (CBP), inicia el proceso de transcripción.
La actividad de CREB en las neuronas es vital para una amplia gama de procesos celulares. Desde asegurar la supervivencia de las células hasta facilitar la formación de nuevas neuronas (neurogénesis) y fortalecer las conexiones entre ellas (potenciación sináptica a largo plazo), CREB juega un papel indispensable en la función cerebral. Su capacidad para responder a diversas señales y modular la expresión génica lo posiciona como un nodo crítico en las redes de señalización neuronales.
Estructura y Variantes de CREB
Los genes que codifican para CREB en humanos y ratones constan de 11 exones. A partir de este gen, se producen tres isoformas principales: α, β y Δ, mediante un proceso conocido como splicing alternativo. Aunque estas isoformas se expresan en la mayoría de los tejidos y comparten funciones similares, presentan pequeñas diferencias estructurales.
La estructura primaria de la proteína CREB se divide en cuatro dominios funcionales, comenzando desde el extremo N-terminal hasta el C-terminal:
- Dominio Q1: Responsable de la actividad transcripcional basal. Se localiza en el N-terminal e interactúa con la proteína de unión a TATA (TBP), promoviendo la transcripción génica.
- Dominio KID (Kinase Inducible Domain): Ubicado en la región media, este dominio es central para la regulación de CREB. Contiene múltiples sitios de fosforilación, siendo el más crucial la Serina 133 (Ser133). La fosforilación en este sitio es esencial para la activación transcripcional de CREB.
- Dominio Q2: Una región rica en glutamina, importante para la activación constitutiva y para la interacción con el complejo de iniciación de la ARN polimerasa II. Este dominio facilita el reconocimiento y la unión a la secuencia CRE canónica (5′-TGACGTCA-3′).
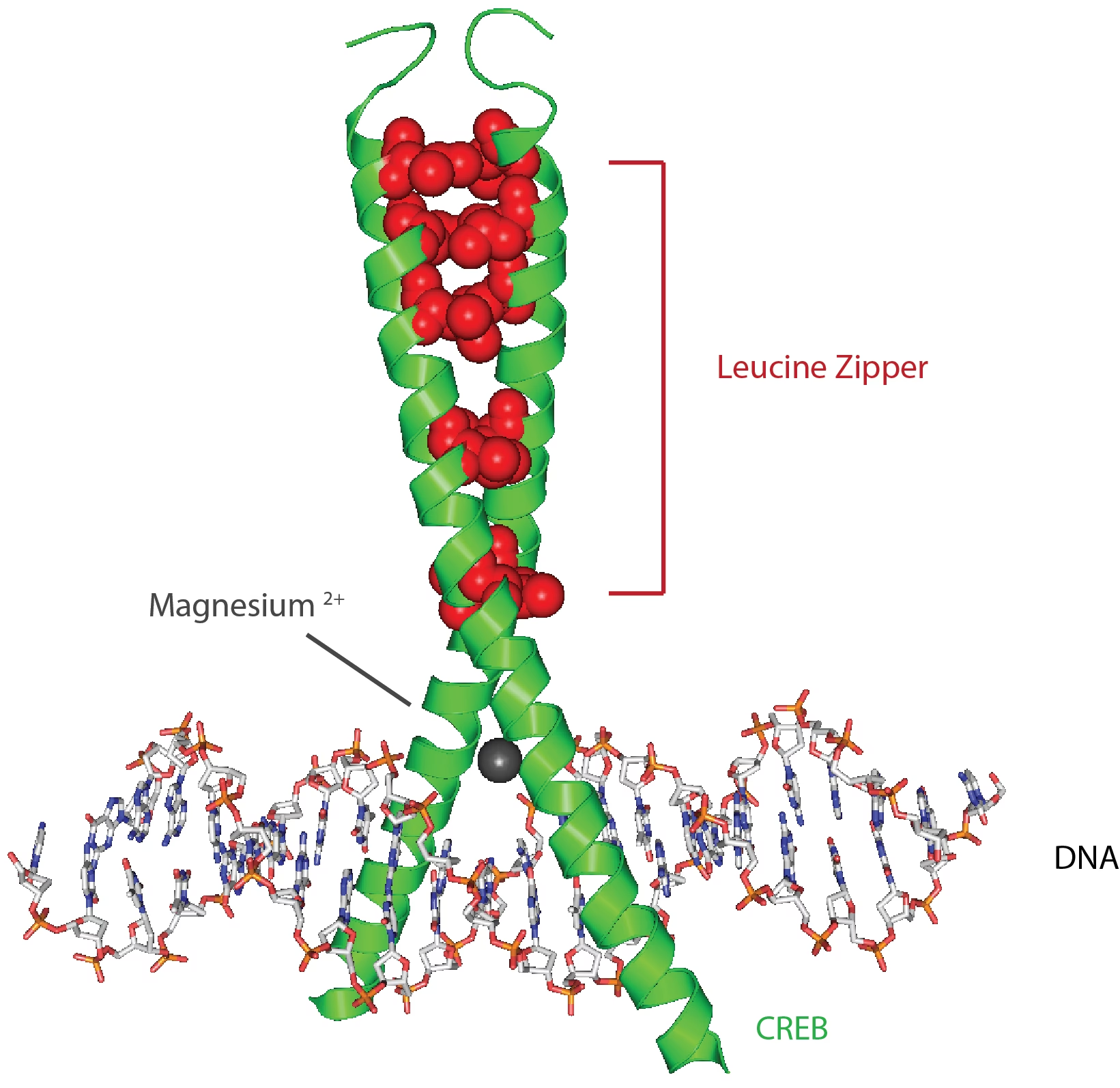
- Dominio bZIP (basic region/leucine zipper): Localizado en el extremo C-terminal, este dominio es responsable de la dimerización de CREB (formando homodímeros o heterodímeros con otros miembros de la familia como ATF-1 o CREM) y de su unión al ADN. Los iones de Mg2+ facilitan significativamente esta unión.
Aunque la fosforilación en Ser133 es la más estudiada y aumenta drásticamente la actividad transcripcional de CREB, no altera su estructura secundaria ni su afinidad por el ADN. Otros sitios de fosforilación en el N-terminal, como Ser129, Ser142 y Ser143, también pueden influir en la actividad de CREB. Por ejemplo, la fosforilación en Ser142 por CaMK II puede inhibir la actividad de CREB, sugiriendo una compleja regulación mediante múltiples modificaciones postraduccionales.
Cascadas de Señalización que Regulan a CREB
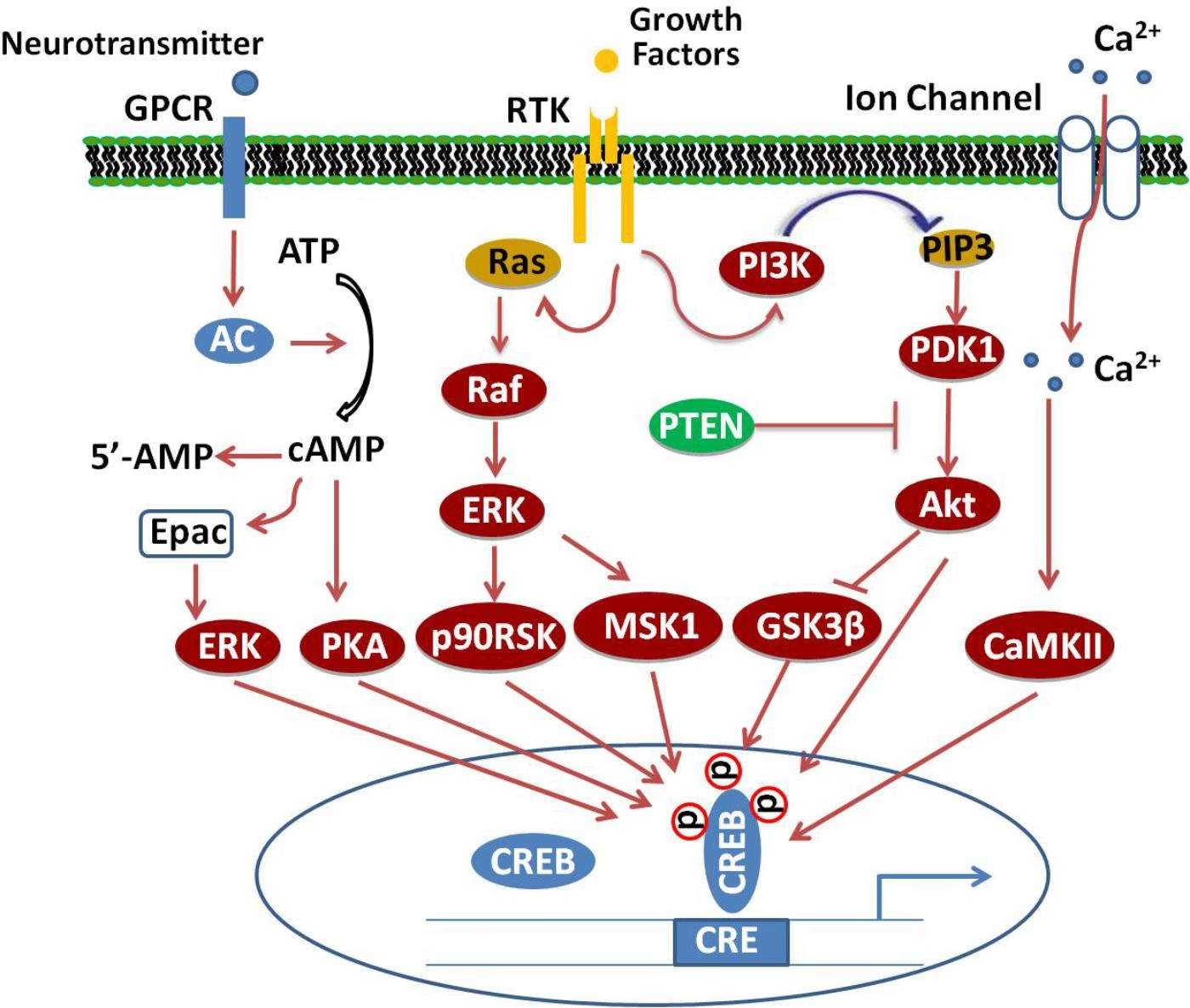
La actividad de CREB es modulada por una compleja red de vías de señalización intracelular que convergen en sus sitios de fosforilación. La fosforilación en Ser133 es el evento clave que desencadena su actividad transcripcional. Este sitio puede ser fosforilado por una variedad de quinasas, incluyendo PKA (activada por cAMP), Akt (parte de la vía PI3K), PKC, CaMKII y CaMKIV (activadas por calcio), p90RSK y MSK1 (parte de las vías MAPK).
La vía canónica del cAMP-PKA-CREB es una de las más conocidas. El aumento de los niveles intracelulares de cAMP, a menudo desencadenado por la activación de receptores acoplados a proteínas G (GPCRs), activa la PKA. La subunidad catalítica de PKA se transloca al núcleo y fosforila a CREB en Ser133, lo que permite el reclutamiento de CBP y la activación de la transcripción de genes con elementos CRE en sus promotores.
Además del cAMP, el cGMP también puede influir en la fosforilación de CREB a través de la proteína quinasa G (PKG), que también fosforila Ser133. Esta doble fosforilación por PKA y PKG puede amplificar la actividad de CREB.
Otras vías importantes incluyen la vía Ras/Raf/MEK/ERK/p90RSK, activada por factores de crecimiento que se unen a receptores tirosina quinasa (RTKs), y la vía PI3K/Akt/GSK3β. Akt puede fosforilar directamente a CREB en Ser133, mientras que GSK3β fosforila a CREB en Ser129, lo que puede tener efectos moduladores.
La desfosforilación de CREB, que apaga su actividad transcripcional, está mediada por varias fosfatasas. Las serina/treonina fosfatasas como PP1, PP2A y PP2B son capaces de remover los grupos fosfato de CREB, especialmente de Ser133. PP2A en el núcleo es particularmente efectiva. PP1 también reprime la actividad de CREB, y PP2B, dependiente de calcio, acelera la desfosforilación. El equilibrio entre la actividad de estas quinasas y fosfatasas determina el nivel de fosforilación de CREB y, por tanto, la magnitud de la transcripción génica dependiente de CRE.
La Interacción entre Dopamina y CREB
La dopamina, un neurotransmisor crucial en el cerebro, ejerce una influencia significativa sobre la actividad de CREB, lo que subraya la importancia de CREB en vías neurales clave. La interacción se produce a través de los receptores de dopamina (D1R y D2R), que están acoplados a proteínas G y activan diferentes cascadas de señalización.
La activación de los receptores D1R, que están acoplados a proteínas Gs, generalmente aumenta los niveles intracelulares de cAMP, lo que a su vez activa la PKA y conduce a la fosforilación de CREB en Ser133. Por otro lado, la activación de los receptores D2R, acoplados a proteínas Gi, típicamente reduce la producción de cAMP y la actividad de la adenilil ciclasa, lo que podría esperarse que disminuya la fosforilación de CREB. Sin embargo, estudios han demostrado que el tratamiento crónico con agonistas de D2R puede, paradójicamente, aumentar la actividad de PKA y la fosforilación de CREB, posiblemente debido a mecanismos compensatorios como la desregulación de los receptores D2R.
Además de la vía del cAMP, los receptores D2R también pueden estar acoplados a la fosfolipasa Cβ (PLCβ), lo que lleva a un aumento del calcio intracelular y la activación de la PKC. Tanto el calcio (a través de CaMK) como la PKC son capaces de fosforilar y activar CREB.
La proteína DARPP-32 (fosfoproteína regulada por dopamina y cAMP de 32 kDa) es otra molécula que parece vincular la señalización mediada por D2R y CREB. En ratones deficientes en DARPP-32, los niveles basales de fosforilación de CREB estaban elevados, y la capacidad de D2R para inducir la fosforilación de CREB se perdió.
Interesantemente, la estimulación de D1R y D2R con agonistas también puede activar la quinasa Akt, que se transloca al núcleo y fosforila directamente a CREB en Ser133 en neuronas estriatales. Estos hallazgos revelan la complejidad de la interacción dopamina-CREB, donde múltiples vías pueden converger para modular la actividad de este factor de transcripción.
CREB, Neurotrofinas y Neurodesarrollo
La hipótesis del neurodesarrollo de la esquizofrenia sugiere que las anormalidades en el desarrollo temprano del cerebro aumentan el riesgo de aparición de síntomas clínicos más tarde en la vida. En este contexto, las neurotrofinas, y en particular el factor neurotrófico derivado del cerebro (BDNF), desempeñan un papel fundamental en el desarrollo neuronal, la plasticidad sináptica y la supervivencia de las células nerviosas.
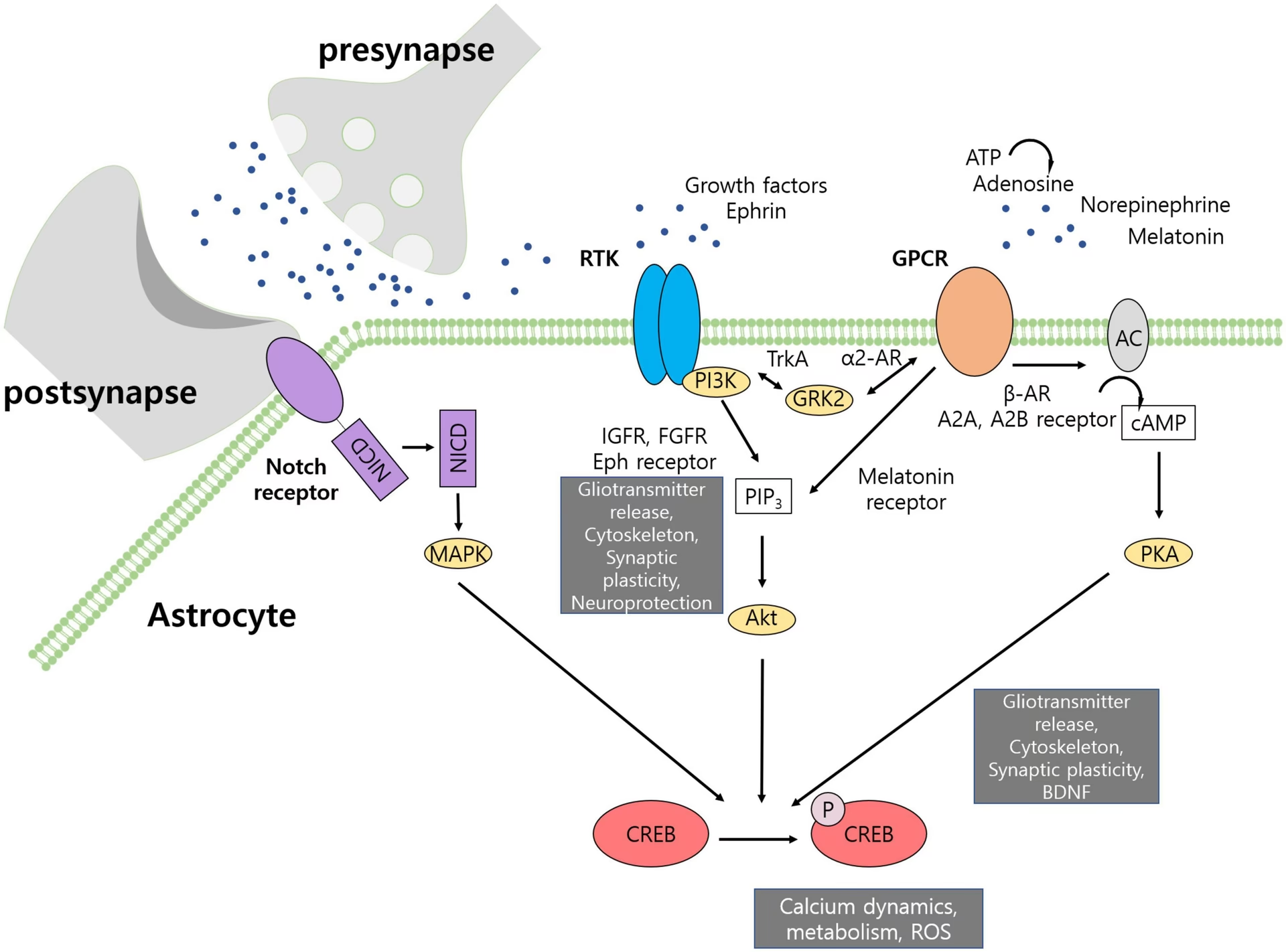
Existe una relación mutuamente reguladora entre CREB y BDNF. BDNF es una de las principales dianas transcripcionales de CREB. Cuando CREB es fosforilado y activado, se une a elementos CRE en la región promotora del gen BDNF, promoviendo su transcripción y aumentando la expresión de BDNF. De manera recíproca, BDNF es un potente activador de CREB. La unión de BDNF a su receptor TrkB desencadena cascadas de señalización intracelular, como la vía del calcio/CaMKIV y la vía Ras/Erk/Rsk/MSK1, que culminan en la fosforilación de CREB en Ser133.
Esta interacción es crucial para varios procesos neuronales. BDNF regula el crecimiento y la complejidad de las dendritas, estructuras neuronales fundamentales para la formación de redes sinápticas funcionales, un proceso en el que interviene la señalización MAPK y CREB. La fosforilación de TrkB induce la activación y translocación de MAPKs al núcleo, activando MSK1, una quinasa importante para la fosforilación de CREB. Ratones deficientes en MSK1 muestran déficits en la plasticidad sináptica y la memoria, así como en la fosforilación de CREB mediada por BDNF.
Además, BDNF es un factor pro-supervivencia que protege las neuronas, y su efecto neuroprotector a menudo está asociado con la activación de la vía de señalización de CREB. En resumen, la vía CREB/BDNF constituye un eje esencial para el neurodesarrollo y la supervivencia neuronal, y las disfunciones en esta vía pueden contribuir a la patología de trastornos como la esquizofrenia.
El Rol de CREB en la Esquizofrenia
La esquizofrenia es una enfermedad mental compleja caracterizada por alteraciones en el pensamiento, la percepción, las emociones y el comportamiento. Aunque sus causas son multifactoriales, incluyendo factores genéticos y ambientales, las disfunciones en la transmisión dopaminérgica y las alteraciones del neurodesarrollo son hipótesis centrales.
CREB emerge como una molécula clave en la comprensión de la patofisiología de la esquizofrenia por varias razones:
- Convergencia de Señalización Dopaminérgica: Como se mencionó, la señalización de los receptores de dopamina (tanto D1R como D2R) influye en la fosforilación y actividad de CREB. Dada la implicación de la dopamina en los síntomas de la esquizofrenia, las alteraciones en la respuesta de CREB a las señales dopaminérgicas podrían contribuir a la enfermedad.
- Interacción con Neurotrofinas: La estrecha relación entre CREB y BDNF es particularmente relevante, ya que la disfunción de BDNF y las vías neurotróficas se han asociado con la esquizofrenia. Una señalización CREB/BDNF deficiente podría alterar el neurodesarrollo y la plasticidad sináptica, procesos afectados en los pacientes.
- Evidencia en Cerebros Postmortem: Estudios patológicos en cerebros postmortem de individuos con esquizofrenia han revelado anormalidades en la expresión y la actividad de CREB. Se ha observado una disminución significativa en los niveles de proteína y gen de CREB, así como en su actividad de unión a elementos CRE, en regiones cerebrales como el giro cingulado, una estructura límbica implicada en la emoción, el aprendizaje y la memoria que muestra alteraciones en la esquizofrenia.
- Variantes Genéticas: Se han identificado variantes genéticas específicas en el gen CREB en pacientes con esquizofrenia (como -933T a C y -413G a A), lo que sugiere una posible contribución genética directa a la disfunción de CREB en la enfermedad.
- Interacción con Genes de Susceptibilidad: Diversos genes de susceptibilidad asociados con la esquizofrenia, como DISC1, NRG-1 y dysbindin-1, están vinculados a vías de señalización (como PI3K/Akt) que convergen en CREB, implicando a CREB como un posible mediador de los efectos de estos genes en la patología.
- Modelos Animales y Terapia: La modulación de la función de CREB en modelos animales de esquizofrenia (por sobreexpresión o deleción/mutación) ha demostrado afectar comportamientos relevantes para la enfermedad. Además, algunos fármacos antipsicóticos parecen ejercer parte de sus efectos terapéuticos influyendo en la fosforilación y actividad de CREB en regiones cerebrales clave.
En conjunto, estas líneas de evidencia sugieren que la disfunción de CREB y las vías de señalización que regula (dopamina, neurotrofinas, genes de susceptibilidad) juegan un papel en la patofisiología de la esquizofrenia. Esto posiciona a CREB como una diana potencial para el desarrollo de nuevas estrategias terapéuticas.
CREB y la Regulación del Estado de Ánimo en el Núcleo Accumbens
El núcleo accumbens (NAc) es una región cerebral clave en el sistema de recompensa y está profundamente implicado en la regulación del estado de ánimo, la motivación y la respuesta a estímulos emocionales y estresantes. CREB se expresa abundantemente en el NAc, y su actividad en esta región es un modulador crucial del comportamiento animal frente a estímulos psiquiátricos.
La actividad de CREB en el NAc está influenciada por entradas dopaminérgicas (vía D1R y D2R) y glutamatérgicas. Estudios experimentales han demostrado que alterar la actividad de CREB específicamente en el NAc es suficiente para modificar el comportamiento. Por ejemplo, el aumento de la actividad de CREB en el NAc mediante transferencia génica reduce la sensibilidad al estrés y a estímulos emocionales. Por el contrario, la activación sostenida de CREB en esta área puede producir síntomas similares a la anhedonia (incapacidad de experimentar placer) y la depresión en modelos animales.
La inhibición de la función de CREB en el NAc, por ejemplo, utilizando una forma dominante negativa de CREB (mCREB), aumenta la preferencia por sustancias adictivas como la cocaína y la morfina, así como por la sacarosa, lo que sugiere que la actividad de CREB en el NAc está relacionada con estados disfóricos y la abstinencia.
En el contexto de la esquizofrenia, se ha observado que la actividad de PKA y la fosforilación de CREB están disminuidas en el NAc en modelos animales. El tratamiento con antipsicóticos puede aumentar la actividad de CREB en esta región, y esta respuesta neuroadaptativa parece facilitar la recuperación del gating sensoriomotor (una medida de la capacidad del cerebro para filtrar información sensorial), que está gravemente afectado en pacientes con esquizofrenia. Estos hallazgos sugieren que la modulación de CREB en el NAc podría ser relevante para el tratamiento de ciertos síntomas en la esquizofrenia.
CREB y la Formación de la Memoria
Uno de los roles más estudiados de CREB es su participación esencial en la formación de la memoria a largo plazo (MLP). La consolidación de la MLP, a diferencia de la memoria a corto plazo (MCP), requiere la síntesis de nuevas proteínas, un proceso que está regulado por la transcripción de genes.
Numerosos estudios en una variedad de organismos, desde invertebrados como Aplysia y Drosophila hasta mamíferos como ratones, han demostrado la importancia de CREB en este proceso. La fosforilación de CREB en Ser133, a menudo desencadenada por la activación de PKA y otras quinasas durante o después del aprendizaje, es un paso crítico para iniciar las cascadas transcripcionales necesarias para la consolidación de la memoria.
La investigación con modelos animales genéticamente modificados ha proporcionado evidencia sólida. Ratones con una deleción convencional de las isoformas α y Δ de CREB (ratones CREBαΔ KO) mostraron déficits en la formación de memoria contextual y espacial. Sin embargo, estos estudios iniciales se vieron complicados por la posibilidad de mecanismos compensatorios (como la sobreexpresión de la isoforma β de CREB o CREM) y diferencias en el fondo genético de los ratones.
Para superar estas limitaciones, se desarrollaron ratones transgénicos que permitían una modulación más controlada de la actividad de CREB:
- Ratones que expresan una forma dominante negativa de CREB (KCREB), que bloquea la unión al ADN de los miembros de la familia CREB, mostraron déficits en la memoria espacial.
- Ratones con un represor inducible de CREB (CREBIR), que se activa con tamoxifeno, mostraron un deterioro severo en la memoria de miedo contextual y señalizada a largo plazo, pero no en el aprendizaje inicial o la memoria a corto plazo.
- Ratones que expresan formas dominantemente activas de CREB (Y134F y DIEDML), que facilitan su activación transcripcional, mostraron una mejora significativa en la consolidación de la memoria a largo plazo en diversas tareas (reconocimiento social, miedo contextual, laberinto de Morris).
Estos estudios confirman el papel positivo de CREB en la consolidación de la MLP. Curiosamente, los ratones con niveles moderados de activación de CREB (Y134F, DIEDML) mostraron mejora en la memoria, mientras que aquellos con una activación extremadamente alta (CREB-VP16) presentaron anomalías, sugiriendo que un equilibrio óptimo en la actividad de CREB es crucial para la función de la memoria.
Además de su papel directo en la MLP a través de la transcripción, CREB también puede influir indirectamente en la MCP. Los ratones con formas activas de CREB (Y134F, DIEDML) mostraron niveles aumentados de BDNF en el hipocampo, y estos ratones también exhibieron una mejora en la MCP. La infusión de BDNF en el hipocampo mejoró la MCP en ratones de tipo salvaje, mientras que los inhibidores de BDNF la perjudicaron. Esto sugiere que CREB, al regular la expresión de BDNF, puede influir en la MCP, aunque este efecto no dependa de la síntesis de proteínas inmediatamente después del entrenamiento.
CREB y la Potenciación a Largo Plazo (LTP)
La Potenciación a Largo Plazo (LTP) es un aumento persistente en la fuerza de las sinapsis que se considera el correlato celular de la memoria y la plasticidad sináptica. La LTP, especialmente su fase tardía (L-LTP), requiere la síntesis de nuevas proteínas y la expresión génica, al igual que la consolidación de la memoria a largo plazo.
La investigación ha demostrado que CREB es un regulador positivo crucial de la L-LTP. La pérdida de función de CREB bloquea la inducción de la L-LTP en el hipocampo. Por el contrario, la activación de CREB facilita la inducción de la L-LTP.
Estudios con ratones transgénicos que expresan formas activas de CREB han proporcionado información clave. Ratones que expresan CREB-VP16, una proteína quimérica con un dominio de activación transcripcional muy potente, mostraron un umbral reducido para la inducción de L-LTP en las neuronas CA1 del hipocampo. Mientras que en ratones de tipo salvaje se requieren múltiples trenes de estimulación tetánica para inducir L-LTP duradera, en los ratones CREB-VP16, un solo tren de estimulación era suficiente para inducir una potenciación de larga duración.
Este efecto se atribuye en parte al aumento de la expresión basal de BDNF en los ratones CREB-VP16. BDNF, un blanco transcripcional de CREB, es crucial para la L-LTP. El aumento de BDNF facilita que las sinapsis capturen este neurotrofina y fortalezcan la potenciación sináptica incluso con un estímulo más débil, un mecanismo que se vincula con el concepto de etiquetado sináptico.
De manera similar, los ratones que expresan las formas dominantemente activas Y134F y DIEDML de CREB también mostraron LTP mejorada en las neuronas CA1 del hipocampo. Estos hallazgos, consistentes con los de los ratones CREB-VP16 (aunque la magnitud de la activación de CREB fuera diferente), refuerzan la idea de que CREB es un regulador positivo de la LTP. La capacidad de CREB para promover la expresión de genes necesarios para el mantenimiento a largo plazo de las modificaciones sinápticas es fundamental para este proceso.
Tabla Comparativa: Diferentes Modelos de Ratón CREB y sus Efectos
| Modelo de Ratón | Modificación de CREB | Efectos en Memoria | Efectos en LTP | Notas |
|---|---|---|---|---|
| CREBαΔ KO | Deleción de isoformas α y Δ | Déficits en memoria contextual y espacial (en algunos fondos genéticos) | Bloqueo de L-LTP | Posible compensación por otras isoformas/familiares. Letalidad perinatal sin deleción condicional. |
| KCREB Transgénico | Expresión dominante negativa de CREB | Déficits en memoria espacial (en CA1 dorsal) | No especificado en el texto proporcionado | Expresión específica en algunas regiones (e.g., CA1, estriado). |
| CREBIR Transgénico | Represor inducible de CREB (requiere tamoxifeno) | Deterioro severo de MLP (contextual y señalizada) | No especificado en el texto proporcionado | Efecto rápido tras inducción. |
| CREB-VP16 Transgénico | Expresión de forma quimérica hiperactiva | Anomalías en memoria espacial | Umbral reducido para L-LTP | Nivel de activación de CREB muy alto. |
| Y134F Transgénico | Expresión de forma dominantemente activa (mayor afinidad por PKA) | Mejora de MLP y MCP | LTP mejorada | Nivel de activación de CREB moderado. |
| DIEDML Transgénico | Expresión de forma dominantemente activa (unión constitutiva a CBP) | Mejora de MLP y MCP (más pronunciada que Y134F) | LTP mejorada | Nivel de activación de CREB moderado-alto. |
Interacciones con Genes de Susceptibilidad a la Esquizofrenia
La esquizofrenia tiene un componente genético significativo, aunque no se atribuye a un único gen sino a la combinación de múltiples factores de riesgo. Los estudios de asociación de genoma completo (GWAS) han identificado varias regiones cromosómicas y genes potencialmente implicados. Curiosamente, algunos de estos estudios apuntan a la participación de vías de señalización como las del calcio y la de CREB, así como genes relacionados con los receptores NMDA y proteínas sinápticas.
Aunque la conexión directa entre genes de susceptibilidad específicos y CREB aún se investiga, existen vínculos indirectos a través de vías de señalización convergentes. Por ejemplo, genes como DISC1 (Disrupted-in-Schizophrenia 1), NRG-1 (Neuregulina-1) y dysbindin-1 se han asociado con la esquizofrenia y desempeñan roles en el desarrollo neuronal y la plasticidad sináptica. Estos genes están vinculados a la vía de señalización PI3K/Akt. Como se mencionó anteriormente, Akt es una quinasa que puede fosforilar directamente a CREB en Ser133.
Así, es plausible que algunos genes de riesgo para la esquizofrenia ejerzan parte de sus efectos patológicos al modular la actividad de la vía PI3K/Akt, que a su vez influye en la función de CREB. Otros candidatos genéticos sugeridos por los GWAS que podrían interactuar con la vía cAMP/PKA/CREB incluyen el propio gen CREB1, CREM, PPP3CB (que codifica una subunidad de la fosfatasa PP2B) y PRKAR1A (que codifica una subunidad reguladora de PKA).
La complejidad de la esquizofrenia radica en la interacción de múltiples genes y factores ambientales. CREB, al ser un integrador clave de diversas señales intracelulares, podría actuar como un punto de convergencia donde las disfunciones desencadenadas por varios genes de susceptibilidad se manifiestan en alteraciones de la función neuronal y el neurodesarrollo, contribuyendo al riesgo de desarrollar la enfermedad. Se necesita más investigación genética humana para aclarar completamente estas complejas interacciones.
CREB como Blanco Terapéutico Potencial para la Esquizofrenia
Dada la implicación de CREB en la patofisiología de la esquizofrenia, particularmente su rol en el neurodesarrollo, la plasticidad sináptica y la respuesta a la dopamina, se plantea la posibilidad de dirigir la investigación y el desarrollo de fármacos hacia esta molécula.
La lógica sugiere que la activación de la señalización de CREB podría tener efectos beneficiosos en la terapia de la esquizofrenia, por ejemplo, promoviendo la plasticidad y el neurodesarrollo afectados. De hecho, algunos fármacos antipsicóticos, tanto típicos como atípicos (como haloperidol, olanzapina, amisulpride), han demostrado influir en la fosforilación y/o los niveles de expresión de CREB en diferentes regiones cerebrales y modelos experimentales, aunque con patrones a veces distintos dependiendo del fármaco y la etapa de maduración neuronal.
Por ejemplo, el haloperidol puede inducir la fosforilación de CREB en el estriado, mientras que la olanzapina y el litio han mostrado aumentar los niveles de CREB y BDNF en el hipocampo y el córtex prefrontal de ratas, lo que sugiere que estos fármacos podrían ejercer efectos neuroadaptativos a través de la vía CREB/BDNF.
Sin embargo, la modulación de CREB como estrategia terapéutica no es sencilla. Como se observó en los estudios de memoria, una activación crónica o excesivamente alta de CREB también puede tener consecuencias deletéreas, como convulsiones epilépticas y pérdida neuronal en ciertas áreas cerebrales. Por lo tanto, la clave podría estar en lograr un equilibrio, manteniendo la actividad de CREB en un nivel óptimo: ni demasiado baja (lo que podría contribuir a déficits de neurodesarrollo y plasticidad) ni demasiado alta (lo que podría causar neurotoxicidad).
Dirigir la terapia hacia sitios de fosforilación específicos distintos de Ser133, o modular las fosfatasas que actúan sobre CREB, o influir en las vías de señalización que actúan de manera antagónica sobre CREB, podrían ser enfoques farmacológicos más refinados. También es importante considerar que CREB regula la transcripción de múltiples genes, y los efectos terapéuticos (o adversos) podrían depender de la combinación específica de genes diana cuya expresión se vea alterada.
Además, la investigación postmortem ha mostrado un aumento de las células positivas para CREB fosforilado en la amígdala de sujetos que murieron por suicidio, mientras que el litio pudo disminuir estos niveles. Esto subraya la necesidad de considerar cuidadosamente el impacto de la modulación de CREB en la regulación del estado de ánimo y el riesgo de suicidio, especialmente en poblaciones con trastornos psiquiátricos.
Preguntas Frecuentes sobre CREB
- ¿Qué activa a CREB?
CREB es activado principalmente por la fosforilación en Serina 133. Esta fosforilación es llevada a cabo por una variedad de quinasas como PKA, CaMKs, Akt, MAPK, MSK1, entre otras. La activación de estas quinasas es desencadenada por diversas señales extracelulares como neurotransmisores (ej. dopamina vía D1R), factores de crecimiento (ej. BDNF) y actividad neuronal. - ¿Es la actividad de CREB siempre beneficiosa?
No necesariamente. Si bien la activación de CREB es crucial para procesos como la formación de memoria a largo plazo, la plasticidad sináptica y la supervivencia neuronal, una activación crónica o excesiva puede tener efectos perjudiciales, incluyendo pérdida neuronal y alteraciones en el comportamiento. Un equilibrio adecuado en la actividad de CREB parece ser fundamental para la función cerebral saludable. - ¿Cómo se relaciona CREB con las enfermedades mentales?
La disfunción de la señalización de CREB se ha asociado con varios trastornos psiquiátricos y neurológicos, incluyendo la esquizofrenia, la depresión, la adicción y el autismo. En la esquizofrenia, se han encontrado niveles alterados de CREB en ciertas regiones cerebrales y se cree que participa en la patología a través de su interacción con la señalización dopaminérgica, las neurotrofinas y genes de susceptibilidad. - ¿Se puede utilizar a CREB como blanco para medicamentos?
Sí, la investigación está explorando el potencial de dirigir la modulación de CREB o las vías que lo regulan para el tratamiento de trastornos como la esquizofrenia. Algunos fármacos antipsicóticos existentes ya parecen influir en la actividad de CREB. Sin embargo, desarrollar terapias dirigidas a CREB requiere superar desafíos, como lograr una modulación equilibrada (evitando la sobreactivación perjudicial) y entender completamente la compleja red de genes y vías que CREB regula.
Conclusión
CREB es una proteína central en la neurociencia, actuando como un factor de transcripción que integra una multitud de señales para regular procesos fundamentales en el sistema nervioso central, incluyendo la memoria, la plasticidad sináptica, el neurodesarrollo y la supervivencia neuronal. Su disfunción se ha implicado significativamente en la patofisiología de la esquizofrenia, donde parece actuar como un punto de convergencia para las alteraciones en la señalización dopaminérgica, las vías neurotróficas (como la de BDNF) y los efectos de ciertos genes de susceptibilidad.
La investigación en modelos animales ha proporcionado una comprensión profunda de cómo la modulación de CREB puede influir en comportamientos relevantes para la esquizofrenia y ha sugerido que algunos de los efectos terapéuticos de los fármacos antipsicóticos podrían estar mediados, al menos en parte, a través de su impacto en la vía de CREB. Sin embargo, la complejidad de la regulación de CREB, incluyendo la interacción de múltiples quinasas y fosfatasas, diferentes sitios de fosforilación y la necesidad de mantener un equilibrio en su actividad (evitando tanto la inhibición como la sobreactivación crónica), presenta desafíos para el desarrollo de terapias dirigidas.
A pesar de estos desafíos, el creciente conocimiento sobre el papel de CREB en la salud y la enfermedad cerebral lo posiciona como una diana prometedora para futuras investigaciones y el desarrollo de tratamientos innovadores para la esquizofrenia y otros trastornos neuropsiquiátricos. Dilucidar por completo la compleja red de genes diana de CREB y sus interacciones en el contexto de la enfermedad será clave para desbloquear su potencial terapéutico.
Si quieres conocer otros artículos parecidos a CREB: Un Factor Clave en Neurociencia puedes visitar la categoría Neurociencia.
