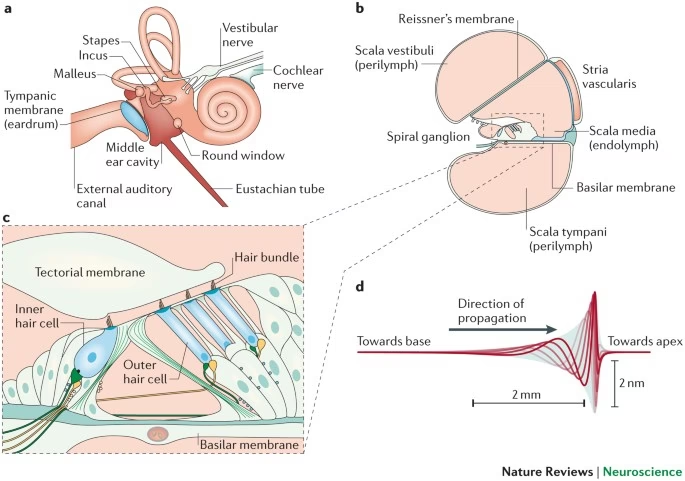
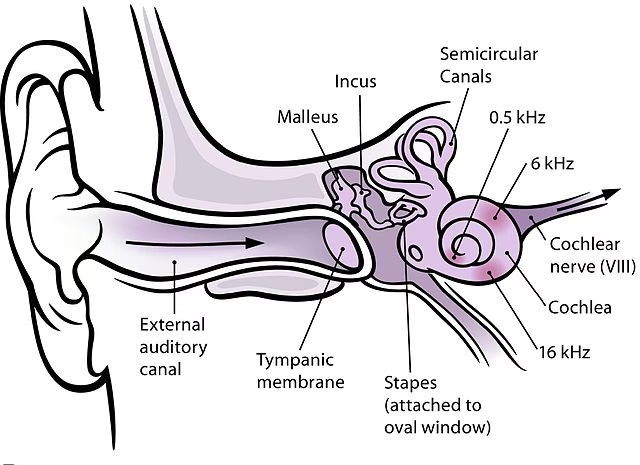
Nuestra capacidad para percibir el mundo sonoro depende de una compleja maquinaria biológica, donde el oído interno juega un papel fundamental. Específicamente, la cóclea, con su intrincada estructura en forma de espiral, alberga las células sensoriales que convierten las vibraciones mecánicas del sonido en señales eléctricas. Estas señales electrobiológicas constituyen el primer paso en la vía auditiva neuronal, siendo recogidas por las fibras nerviosas del VIII par craneal, también conocido como nervio vestibulococlear. Las somas neuronales de la porción auditiva de este nervio residen en un núcleo especializado dentro de la cóclea, llamado ganglio espiral. Este artículo profundiza en la anatomía y fisiología de estas neuronas cruciales para la transmisión del mensaje auditivo desde el órgano de Corti hasta el sistema nervioso central.

El VIII par craneal está formado por neuronas sensoriales que inervan el oído interno, abarcando tanto los receptores vestibulares (equilibrio) como los auditivos (audición). La porción auditiva está compuesta por fibras aferentes cocleares que establecen contacto con las células ciliadas sensoriales del órgano de Corti. Los cuerpos celulares de estas neuronas se localizan, como se mencionó, en el ganglio espiral coclear, situado en el canal espiral de Rosenthal, dentro del modiolo (el eje central de la cóclea). Aquí es donde se origina la vía auditiva neural que transporta la señal generada por la transducción mecanoeléctrica del sonido en las células ciliadas de los mamíferos.
Los Dos Tipos de Neuronas del Ganglio Espiral
En el ganglio espiral coclear se pueden distinguir dos poblaciones neuronales principales, diferenciables mediante tinciones clásicas o por la expresión de neurofilamentos específicos: las neuronas aferentes Tipo I y las neuronas aferentes Tipo II.
Neuronas Tipo I: Las Principales Transmisoras
Las fibras aferentes Tipo I constituyen la gran mayoría de la población neuronal del ganglio espiral, representando entre el 90% y el 95% del total, aunque este porcentaje puede variar ligeramente entre especies. Son neuronas bipolares de gran tamaño, cuyas somas y proyecciones están mielinizadas. Estas fibras conectan directamente las células ciliadas internas (CCI) del órgano de Corti con los núcleos cocleares en el tronco encefálico.
Sus dendritas penetran en el órgano de Corti a través de la habenula perforata y se distribuyen de manera radial, formando el plexo espiral interno antes de inervar las CCI. La conexión es muy específica: cada dendrita contacta únicamente con una célula ciliada interna en su polo basal. Sin embargo, cada célula ciliada interna recibe contactos de entre 10 y 20 dendritas aferentes Tipo I. Esta convergencia permite una representación significativa de cada pequeña porción del órgano de Corti en el ganglio espiral.
Estas sinapsis entre las CCI y las fibras Tipo I son sinapsis excitatorias de tipo Gray I, utilizando el glutamato como neurotransmisor principal. Funcionalmente, las fibras aferentes Tipo I se pueden clasificar en tres subpoblaciones según su tasa de descarga espontánea: alta, media y baja. Estas subpoblaciones presentan diferencias adicionales en la ubicación, complejidad o contenido mitocondrial de las terminaciones que contactan con el polo basal de las CCI.
Neuronas Tipo II: Un Papel Menos Comprendido
En contraste, las neuronas aferentes Tipo II del ganglio espiral representan solo el 5% al 10% de la población total. Son neuronas pseudounipolares y amielínicas. A diferencia de las Tipo I, inervan las células ciliadas externas (CCE) del órgano de Corti. Expresan específicamente un neurofilamento de 200 kD que permite su detección experimental.
Sus dendritas, tras entrar en el órgano de Corti por la habenula perforata, se distribuyen a través del plexo espiral interno, ramificándose y cruzando el túnel de Corti por su base para alcanzar las CCEs. Cada rama contacta con una CCE, formando sinapsis. Lo distintivo de estas sinapsis es el patrón de inervación: cada neurona Tipo II inerva aproximadamente entre 15 y 20 CCEs, mientras que cada CCE recibe un único contacto de una fibra aferente Tipo II. La distribución de los contactos dendríticos de las Tipo II en las CCEs no es aleatoria, prefiriendo inervar CCEs de la misma fila y aumentando el número de CCEs contactadas desde la base al ápice de la cóclea y en las filas más alejadas del túnel.
Aunque durante mucho tiempo sus características neuroquímicas fueron menos claras debido a su baja población y actividad, estudios recientes han confirmado que estas fibras también reciben entradas glutamatérgicas de las CCEs y pueden ser moduladas por ATP. A pesar de que ambos tipos neuronales son glutamatérgicos, existen diferencias notables que explican su fisiología distinta, como la ya mencionada inervación asimétrica.
Neurotransmisores de las Fibras Aferentes Cocleares
Diversas sustancias neuroactivas están implicadas en la transmisión de la información sonora desde las células sensoriales del órgano de Corti hasta la vía auditiva central. Como se ha detallado, las fibras aferentes Tipo I del VIII par craneal son neuronas glutamatérgicas. Se ha aceptado ampliamente que el aminoácido excitatorio glutamato es el neurotransmisor entre las CCI y las fibras Tipo I desde su primera descripción. Hallazgos posteriores morfológicos, bioquímicos y electrofisiológicos han respaldado esta conclusión.
Se ha propuesto un proceso completo de reciclaje del glutamato en estas sinapsis para eliminar el glutamato liberado de la hendidura sináptica, inactivarlo y reponer las reservas de glutamina en las CCI para producir nuevo glutamato. Las células gliales cocleares involucradas en la recaptación de glutamato de la hendidura sináptica entre la CCI y la fibra Tipo I son las células de Schwann mielínicas de la lámina espiral ósea, que muestran la actividad de glutamina sintetasa necesaria para convertir el glutamato en glutamina. El control preciso de la concentración de glutamato en la hendidura sináptica es vital para evitar el daño neurotóxico derivado de un aumento excesivo.
La membrana postsináptica de la dendrita aferente Tipo I bajo la CCI posee los receptores de neurotransmisores necesarios para activar la neurona tras la liberación de glutamato. Se han descrito los dos tipos principales de receptores glutamatérgicos: ionotrópicos y metabotrópicos.
Receptores Ionotrópicos
Los receptores ionotrópicos de glutamato (tipos NMDA, AMPA y KA) están implicados en la transmisión sináptica rápida. Los receptores no-NMDA, como los AMPA y KA, tienen un canal iónico asociado permeable a Na+ y K+ que se abre al ser activado por glutamato o agonistas específicos. La administración de AMPA o KA, incluso a bajas concentraciones, puede alterar el potencial de acción compuesto del VIII par, probablemente debido a un aumento de la actividad de descarga espontánea de la neurona Tipo I seguido de una depresión postexcitatoria. Esto puede llevar a eventos neurotóxicos y la muerte neuronal.
El receptor NMDA tiene un canal iónico permeable a cationes como Na+, K+ y Ca2+, un sitio de unión para glutamato y otro para glicina, que actúa como coagonista. Está bloqueado de forma voltaje-dependiente por Mg2+. Los receptores NMDA y no-NMDA forman un complejo funcional. La activación del NMDA depende de una despolarización previa de la membrana postsináptica, mediada por los receptores no-NMDA, para liberar el bloqueo de Mg2+ y permitir el paso de iones, especialmente Ca2+.
Receptores Metabotrópicos
Los receptores metabotrópicos de glutamato, Grupos I y II, también se han descrito en las terminales dendríticas de las fibras del VIII par. Estos receptores, acoplados a proteínas G, tienen efectos más lentos y se han relacionado con efectos moduladores sinápticos a largo plazo.
En cuanto a las neuronas Tipo II, como se mencionó, también establecen sinapsis excitatorias glutamatérgicas con las CCEs. Sin embargo, su baja actividad comparada con las Tipo I se explica en parte por diferencias en la liberación de neurotransmisor (liberación de vesículas individuales con baja probabilidad por las CCEs vs. liberación multivesicular por las CCI) y la estructura dendrítica (proceso dendrítico largo que contacta múltiples CCEs vs. dendritas radiales cortas que contactan una sola CCI).
Control del Sistema Nervioso Central: El Sistema Olivococlear
La actividad de las fibras Tipo I del ganglio espiral está modulada activamente por el sistema olivococlear eferente lateral (OLES). Este sistema neuromodulador se origina en neuronas amielínicas del complejo olivar superior lateral en el tronco encefálico. Las fibras del OLES llegan a la cóclea a través del tracto de Rasmussen, el nervio vestibular y la anastomosis de Oort.
Establecen dos tipos de contactos axodendríticos con las neuronas aferentes Tipo I: sinapsis axodendríticas "en passant" y terminaciones axodendríticas termino-laterales. Aunque las fibras Tipo I son glutamatérgicas, sus dendritas en las zonas de contacto con el OLES poseen receptores para diversas sustancias neuroactivas presentes en las fibras eferentes. Se han descrito dos tipos principales de sustancias: neurotransmisores típicos como GABA, acetilcolina, dopamina o serotonina, y neuromoduladores como CGRP, encefalinas o dinorfinas.
Toda la evidencia experimental sugiere que el OLES es un sistema modulador que permite al SNC, específicamente al complejo olivar superior, controlar la actividad de las neuronas Tipo I. Esto es posible gracias a un circuito reflejo que involucra a las neuronas Tipo I (que llevan la información de las CCI), los núcleos cocleares y el complejo olivar superior. Desde el olivar superior, dos tractos eferentes alcanzan la cóclea: desde la oliva medial (OM) parten axones que inervan las CCEs (sistema olivococlear eferente medial - OMES), y desde la oliva superior lateral (OSL) parten las neuronas del OLES que contactan con las fibras Tipo I.
Un ejemplo de este control es la respuesta a la estimulación sonora, que aumenta el recambio de dopamina coclear, liberada por las fibras del OLES y actuando sobre receptores D-2. La administración de un agonista D-2 puede bloquear los efectos del ruido sobre las fibras Tipo I. Esto sugiere que la dopamina y otras sustancias del OLES podrían jugar un papel importante en la modulación y la protección contra el ruido de las fibras aferentes Tipo I.
Patofisiología: Excitotoxicidad y Sordera
Las fibras del VIII par craneal pueden estar implicadas en diversas patologías auditivas y/o vestibulares. Aunque la etiología de muchas hipoacusias reside en el órgano de Corti, las fibras nerviosas del ganglio espiral y las disfunciones sinápticas entre las células ciliadas y las fibras aferentes también se relacionan con algunas sorderas.
La patofisiología de las sinapsis glutamatérgicas puede estar en la base de hipoacusias como el trauma acústico, la presbiacusia, ciertos tipos de sordera (incluso relacionados con mareos), la hipoxia, la isquemia o la pérdida auditiva genética.
Daños cocleares, como la hinchazón dendrítica en el polo basal de las CCI, se encuentran típicamente en condiciones patológicas experimentales como hipoxia, anoxia/isquemia o trauma acústico. Estos estados llevan a un aumento de la concentración de glutamato en la hendidura sináptica. En el SNC, este exceso es el inicio de un proceso neurotóxico llamado excitotoxicidad, donde una estimulación prolongada de los receptores de glutamato de la fibra nerviosa puede agotar los mecanismos de eliminación de glutamato y culminar en la muerte neuronal.
El mecanismo de la excitotoxicidad involucra la activación sucesiva de los receptores ionotrópicos de glutamato no-NMDA y NMDA. El aumento de glutamato puede deberse a diversas causas, siendo relevante la condición isquémica por disminución del flujo sanguíneo coclear. La falta de oxígeno reduce los mecanismos de eliminación de glutamato dependientes de ATP, aumentando su concentración sináptica. Esto activa prolongadamente los receptores no-NMDA, abriendo sus canales iónicos y permitiendo la entrada libre de Na+ y agua, causando el edema dendrítico. Una vez que la despolarización resultante libera el bloqueo de Mg2+ de los receptores NMDA, se permite la entrada de Ca2+. Este aumento del calcio intracelular, junto con el liberado de los almacenes intracelulares, activa la cascada de caspasas apoptóticas y lleva a la muerte neuronal.
En la cóclea, el proceso de excitotoxicidad, resultado de condiciones patológicas, se observa en las fibras glutamatérgicas del ganglio espiral que inervan las CCI. La exposición al ruido y las condiciones hipóxicas/isquémicas pueden reducir el flujo sanguíneo coclear y activar prolongadamente las CCI, liberando un exceso de glutamato. Esto sobreactiva los receptores postsinápticos, produciendo las típicas lesiones excitotóxicas: hinchazón dendrítica bajo las CCI y la muerte de neuronas del ganglio espiral, sugiriendo una base patofisiológica común. Estas lesiones son muy similares a las producidas experimentalmente al administrar agonistas de glutamato (NMDA, AMPA, KA).
Las fibras aferentes Tipo II, debido a su bajo número, diámetro y actividad, han sido más difíciles de estudiar. Parecen no verse afectadas por el sonido o condiciones patológicas que dañan las Tipo I, como la estimulación acústica o la ototoxicidad por aminoglucósidos. Sin embargo, se ha sugerido que se activan por ATP liberado de las células de soporte de Deiter cuando las CCEs están dañadas. Por ello, se han definido como potenciales nociceptores, que podrían detectar estímulos auditivos dañinos o mediar la sensación de ruidos dolorosamente fuertes.
Existen otras patologías que afectan las neuronas del ganglio espiral, directa o indirectamente, como la presbiacusia. Modelos experimentales con ratones han mostrado una correlación entre la edad y la disminución del número de neuronas en el ganglio espiral, sugiriendo que la neurotoxicidad y/o apoptosis contribuyen a la sordera relacionada con la edad. Esto posiciona a las neuronas del ganglio espiral como un posible objetivo terapéutico para paliar la sordera por envejecimiento.
Conclusión
Aún queda mucho por comprender sobre la anatomía y fisiología de las neuronas del VIII par craneal a nivel del ganglio espiral y su relación con las neuronas del complejo olivar superior que controlan la actividad del receptor auditivo y las fibras Tipo I. La reciente descripción del neurotransmisor de las sinapsis CCE-fibras Tipo II abre nuevas posibilidades terapéuticas, quizás farmacológicas, para controlar la actividad del órgano de Corti. La investigación continua sobre estas neuronas es fundamental para entender y tratar diversas formas de pérdida auditiva.
Preguntas Frecuentes
¿Qué es el ganglio espiral?
Es el conjunto de somas neuronales sensoriales ubicado en el modiolo de la cóclea. Sus fibras nerviosas, el VIII par craneal, inervan las células ciliadas sensoriales del órgano de Corti y transmiten la señal auditiva al sistema nervioso central.
¿Cuántos tipos de neuronas hay en el ganglio espiral?
Clásicamente se distinguen dos tipos principales: las neuronas Tipo I, que constituyen la gran mayoría (90-95%), y las neuronas Tipo II, que representan el 5-10% restante.
¿Qué células sensoriales inerva cada tipo de neurona?
Las neuronas Tipo I inervan exclusivamente las células ciliadas internas (CCI). Las neuronas Tipo II inervan las células ciliadas externas (CCE).
¿Cuál es el principal neurotransmisor en estas sinapsis?
El neurotransmisor principal liberado por las células ciliadas para activar las fibras aferentes es el glutamato. En las sinapsis con las neuronas Tipo II, también se menciona la modulación por ATP.
¿Cómo modula el cerebro la actividad de estas neuronas?
El sistema nervioso central, a través del sistema olivococlear lateral (OLES) que se origina en el complejo olivar superior, envía fibras eferentes que contactan directamente con las dendritas de las neuronas Tipo I, utilizando diversos neurotransmisores y neuromoduladores para filtrar o modular la señal auditiva.
¿Qué es la excitotoxicidad en el contexto de la cóclea?
Es un proceso patológico causado por una concentración excesiva y prolongada de glutamato en la hendidura sináptica entre las células ciliadas internas y las neuronas Tipo I. Esto sobreestimula los receptores de glutamato, provocando una entrada masiva de iones (sodio, calcio) que puede llevar a la hinchazón de las dendritas y, eventualmente, a la muerte neuronal. Se asocia con trauma acústico e isquemia.
¿Las neuronas Tipo II transmiten el mensaje auditivo principal?
Se cree que las neuronas Tipo I son las principales responsables de codificar el mensaje auditivo que llega al cerebro. Las neuronas Tipo II, con su baja actividad y patrón de inervación, podrían informar más sobre el estado mecánico del órgano de Corti o actuar como nociceptores (detectores de estímulos auditivos dañinos o dolorosos).
Comparativa: Neuronas Tipo I vs. Tipo II
| Característica | Neuronas Tipo I | Neuronas Tipo II |
|---|---|---|
| % Población | 90-95% | 5-10% |
| Morfología | Bipolar | Pseudounipolar |
| Mielina | Mielinizadas | Amielínicas |
| Célula Sensorial Inervada | Células Ciliadas Internas (CCI) | Células Ciliadas Externas (CCE) |
| Patrón de Inervación | Cada fibra → 1 CCI Cada CCI → 10-20 fibras | Cada fibra → ~15-20 CCEs Cada CCE → 1 fibra |
| Neurotransmisor Principal | Glutamato | Glutamato (modulado por ATP) |
| Actividad | Alta | Baja |
| Función Sugerida | Codifica el mensaje auditivo principal | Informa sobre aspectos mecánicos, posible nocicepción |
| Vulnerabilidad (Excitotoxicidad) | Alta | Baja / No afectada |
Si quieres conocer otros artículos parecidos a Neuronas de la Cóclea y la Audición puedes visitar la categoría Neurociencia.
