El camino hacia nuevos tratamientos médicos y terapias es largo y complejo, pavimentado con años de investigación preclínica y, finalmente, la rigurosa evaluación de los ensayos clínicos. Estos estudios en seres humanos son esenciales para determinar si una intervención es segura y efectiva. Sin embargo, no todos los ensayos clínicos alcanzan sus objetivos predefinidos. A menudo, generan lo que se conocen como resultados negativos. Aunque la palabra 'negativo' pueda sonar desalentadora y evocar una sensación de fracaso, en el ámbito de la investigación, estos resultados distan mucho de ser inútiles. De hecho, comprender qué sucede cuando un ensayo clínico 'falla' y, más importante aún, qué hacer con esos resultados, es fundamental para el progreso científico y la protección de futuros pacientes.
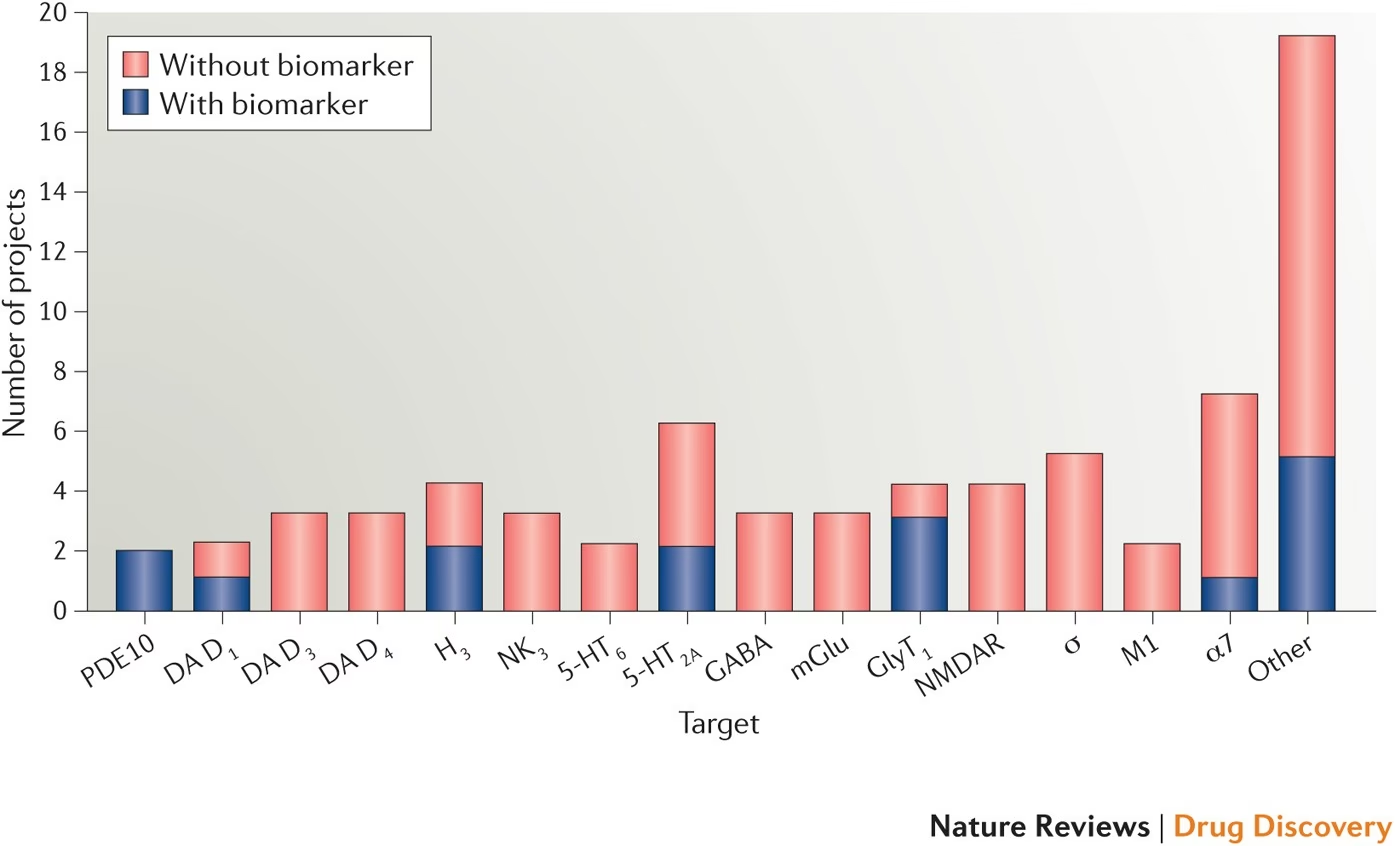
La noción de éxito o fracaso en un ensayo clínico se define en gran medida por sus objetivos predefinidos, conocidos como puntos finales. Estos puntos finales pueden ser clínicos, como la mejora de los síntomas o las tasas de supervivencia, o subrogados, como cambios en biomarcadores que indican una progresión más lenta de una enfermedad. Un ensayo puede tener múltiples objetivos, incluyendo alcanzar un número específico de participantes o demostrar la seguridad de la intervención. Si un ensayo no logra cumplir estos criterios, se considera que ha fallado. Sin embargo, la naturaleza de este 'fracaso' es crucial. Un ensayo que no pudo completarse (quizás por dificultades de reclutamiento) ofrece aprendizajes sobre diseño y operación, pero un ensayo que falla debido a efectos adversos graves o a la ineficacia de la intervención genera datos de un valor incalculable.
- El Problema de Ocultar Resultados Negativos
- El Valor Innegable de los Resultados Negativos
- Compartiendo el Conocimiento: Publicación de Resultados Negativos
- ¿Por Qué Fallan los Ensayos Clínicos (Especialmente en Fase 3)?
- Factores que Influyen en el Éxito o Fracaso
- Impacto del Fracaso en Fase 3
- Reduciendo el Riesgo de Fracaso
- ¿Es Realmente un Fracaso un Ensayo 'Fallido'?
- ¿Qué te Descalifica para Participar en un Ensayo Clínico?
- Preguntas Frecuentes
El Problema de Ocultar Resultados Negativos
Durante mucho tiempo, existió una tendencia a no publicar los resultados negativos de los ensayos clínicos. La lógica aparente era simple: si la intervención no funcionó, ¿qué utilidad tienen los resultados? Sin embargo, esta práctica tiene consecuencias perjudiciales y costosas, pudiendo ascender a miles de millones de euros a nivel global.
La no publicación de resultados negativos crea un sesgo de publicación. Esto significa que el conjunto de conocimientos disponibles sobre una intervención o enfermedad queda incompleto y sesgado hacia resultados positivos. Imagine un escenario: un ensayo de fase II sobre un fármaco para el cáncer de pulmón de células pequeñas no muestra beneficio clínico (un resultado negativo). Si estos resultados no se publican, otros equipos de investigación, al revisar la literatura, no encontrarán información sobre este fracaso y podrían decidir invertir tiempo y recursos en investigar la misma intervención, solo para llegar a la misma conclusión negativa. Este ciclo de duplicación de esfuerzos y desperdicio de recursos se perpetúa si los resultados negativos permanecen ocultos.
A pesar de los esfuerzos crecientes por la transparencia en los ensayos clínicos y la obligación legal de registrar los estudios y sus resultados en bases de datos públicas (como ClinicalTrials.gov en EE. UU.), una proporción significativa de los resultados de los ensayos sigue sin publicarse. Esto subraya la persistencia del problema y la necesidad de promover activamente la difusión de todo tipo de resultados.

El Valor Innegable de los Resultados Negativos
Lejos de ser un simple registro de lo que no funcionó, los resultados negativos poseen un valor considerable para diversas partes interesadas:
- Pacientes: La publicación de resultados negativos, especialmente aquellos relacionados con la seguridad, puede prevenir que futuros pacientes se expongan a riesgos innecesarios participando en ensayos de intervenciones ineficaces o inseguras. Además, los participantes de un ensayo tienen derecho a conocer los resultados de la investigación en la que contribuyeron.
- Investigadores: Compartir resultados negativos permite a otros investigadores evitar repetir estudios con el mismo diseño o intervención, ahorrando tiempo y recursos valiosos. Más allá de evitar errores, los resultados negativos pueden ofrecer información crucial sobre los mecanismos de una enfermedad o la biología de un objetivo terapéutico, inspirando nuevas direcciones de investigación y enfoques innovadores.
- El Mundo Científico y Médico: La publicación de resultados negativos contribuye al cuerpo de conocimiento general sobre una intervención, una enfermedad y los métodos de investigación. Fortalece la transparencia, la reproducibilidad y la rendición de cuentas en la investigación clínica, pilares fundamentales de la ciencia rigurosa.
Compartiendo el Conocimiento: Publicación de Resultados Negativos
Dependiendo de la ubicación geográfica y las regulaciones locales, puede existir la obligación legal de registrar y publicar los resultados de los ensayos clínicos. Sin embargo, existen opciones adicionales para maximizar la difusión de los resultados negativos:
- Repositorios de Datos: Subir los datos brutos o resumidos a repositorios de datos públicos permite que otros investigadores analicen y reutilicen la información.
- Servidores de Preimpresión: Publicar los resultados en servidores de preimpresión (como bioRxiv o medRxiv) permite compartirlos rápidamente con la comunidad científica antes de una revisión formal por pares.
- Revistas Científicas: Muchas revistas científicas, incluyendo algunas de acceso abierto y otras específicas de ensayos clínicos (como Trials o BMC Research Notes), aceptan y publican resultados negativos. Es crucial que la publicación sea transparente y describa claramente el diseño del estudio, los métodos y los resultados, independientemente de su signo.
¿Por Qué Fallan los Ensayos Clínicos (Especialmente en Fase 3)?
El desarrollo de fármacos es un proceso con una alta tasa de abandono. Miles de ideas de nuevos medicamentos se investigan cada año, pero solo una pequeña fracción llega al mercado. La mayoría de los fracasos ocurren en las etapas tempranas, particularmente en Fase 2, donde entre el 60% y el 70% de los ensayos no logran avanzar. Sin embargo, los fracasos en Fase 3 son los más críticos y costosos. Aunque la tasa de fracaso es menor (alrededor del 30-40%), el tiempo y la inversión acumulados hasta esta etapa son significativos.
Las razones principales por las que los ensayos de Fase 3 no tienen éxito suelen ser:
| Razón Principal | Descripción | Frecuencia Estimada (Fase 3) |
|---|---|---|
| Falta de Eficacia | La intervención no demuestra el beneficio clínico esperado o no cumple el punto final primario definido en el protocolo. Es la razón más común de fracaso en Fase 3. | ~57% |
| Problemas de Seguridad | La intervención causa efectos adversos graves o inesperados que superan los beneficios potenciales, o el perfil de seguridad es inaceptable. | ~17% |
| Falta de Viabilidad Comercial | Aunque la intervención pueda ser segura y algo efectiva, no demuestra una ventaja clara sobre los tratamientos existentes o no se considera que tenga suficiente potencial de mercado para justificar la inversión adicional necesaria para su aprobación y comercialización. | Menos frecuente que eficacia/seguridad, pero significativa. |
Otras causas de fracaso pueden incluir dificultades de reclutamiento, problemas operativos o fallos en el diseño del estudio.
Factores que Influyen en el Éxito o Fracaso
Más allá de la eficacia y la seguridad, una compleja red de factores puede influir en el resultado de un ensayo clínico:
- Características del Fármaco: Las nuevas entidades moleculares (NMEs) tienden a tener tasas de fracaso más altas que otros tipos de fármacos. Las moléculas grandes (biológicos) a menudo tienen una tasa de éxito mayor que las moléculas pequeñas.
- Área Terapéutica: Algunas áreas, como las enfermedades crónicas (Alzheimer, diabetes) o áreas complejas como la oncología, las enfermedades infecciosas o los trastornos del sistema nervioso central, históricamente presentan tasas de fracaso más altas.
- Factores Estratégicos: Los fármacos desarrollados internamente (self-originated) pueden tener tasas de fracaso más altas que aquellos licenciados de otras compañías. La inversión en áreas menos saturadas o con mecanismos de acción muy novedosos, aunque potencialmente más rentables, también conlleva un mayor riesgo de fracaso.
- Complejidad Operacional y de Diseño: Diseños de protocolo complejos, largos tiempos de ciclo y una mayor carga de trabajo para los centros de investigación pueden impactar negativamente en el rendimiento del ensayo. La complejidad de los criterios de elegibilidad (inclusión y exclusión) también ha sido identificada, incluso mediante análisis avanzados como el procesamiento del lenguaje natural (NLP), como un factor que puede predecir el resultado de un ensayo.
- Tamaño de la Empresa: Las empresas más pequeñas pueden experimentar tasas de fracaso más altas en comparación con las grandes compañías farmacéuticas.
- Factores Regulatorios: Aunque las agencias reguladoras establecen estándares estrictos, ciertas designaciones especiales (como el estatus de medicamento huérfano) pueden mejorar las tasas de éxito.
El uso de modelos de aprendizaje automático (ML) y el análisis de grandes conjuntos de datos están permitiendo identificar y predecir con mayor precisión qué factores tienen más probabilidad de influir en el éxito o fracaso de un ensayo, ofreciendo información valiosa para optimizar el diseño y la estrategia.
Impacto del Fracaso en Fase 3
El fracaso en la fase final de desarrollo tiene repercusiones significativas:
- Impacto en Pacientes: Los pacientes, que a menudo han invertido tiempo y esfuerzo considerables y pueden tener pocas alternativas de tratamiento (especialmente en enfermedades raras o avanzadas), pueden experimentar una profunda decepción al ver fallar lo que podría haber sido su última esperanza.
- Impacto Financiero: Los ensayos clínicos, particularmente los de Fase 3, implican inversiones financieras masivas. Un fracaso en esta etapa representa una pérdida económica considerable para los patrocinadores (empresas farmacéuticas o instituciones de investigación) y los inversores.
Reduciendo el Riesgo de Fracaso
Si bien el fracaso nunca puede eliminarse por completo, el riesgo puede mitigarse significativamente mediante un diseño de ensayo clínico robusto y estratégico. Un diseño optimizado, una revisión rigurosa del protocolo y una comunicación eficiente entre todas las partes (investigadores, patrocinadores, pacientes, reguladores) son clave. Anticipar posibles complicaciones y, por ejemplo, definir objetivos secundarios con valor potencial (incluso si el primario no se cumple), puede añadir valor incluso si el resultado principal es negativo.
¿Es Realmente un Fracaso un Ensayo 'Fallido'?
El término 'ensayo fallido' puede ser engañoso. Incluso cuando un ensayo no alcanza su objetivo primario, genera una gran cantidad de datos médicos y científicos. Estos datos pueden proporcionar 'pruebas de concepto' o confirmar mecanismos de acción de fármacos que requieren investigación adicional. Un resultado negativo bien documentado es una pieza vital del rompecabezas científico, informando futuras investigaciones y evitando caminos sin salida. En este sentido, un ensayo que genera datos valiosos, incluso si no aprueba la intervención, no es un fracaso total, sino una contribución al conocimiento.
¿Qué te Descalifica para Participar en un Ensayo Clínico?
Como nota relacionada, la participación en ensayos clínicos se rige por criterios estrictos. Cada estudio tiene sus propias reglas de elegibilidad, que incluyen criterios de inclusión (características que debes tener para participar) y criterios de exclusión (características que te impiden participar). Estos criterios se basan típicamente en la edad, género, estado de salud general, tipo y etapa de la enfermedad, historial de tratamientos previos y otras condiciones médicas. No cumplir con uno o varios de estos criterios es la razón principal por la que una persona puede ser descalificada para participar en un ensayo en particular, asegurando que los participantes sean adecuados para la pregunta de investigación específica y se minimicen los riesgos.
Preguntas Frecuentes
¿Qué significa un resultado negativo en un ensayo clínico?
Significa que la intervención probada no demostró el beneficio esperado o no cumplió con los objetivos predefinidos del estudio, a menudo debido a falta de eficacia o problemas de seguridad.
¿Por qué es importante publicar los resultados negativos?
Para evitar que otros investigadores repitan estudios inútiles, ahorrar recursos, informar a pacientes sobre riesgos potenciales y contribuir de manera transparente al conocimiento científico general.

¿En qué fase fallan más ensayos?
La mayor tasa de abandono ocurre en la Fase 2. Sin embargo, los fracasos en Fase 3 son más costosos debido a la inversión acumulada.
¿Un ensayo fallido es una pérdida total?
No. Incluso los ensayos fallidos generan datos valiosos que informan futuras investigaciones, mejoran la comprensión de enfermedades y terapias, y contribuyen al conocimiento científico.
¿Qué puedo hacer si mi ensayo tiene resultados negativos?
Asegurarte de que los resultados se registren en bases de datos públicas y considerar publicarlos en revistas científicas o servidores de preimpresión para compartirlos con la comunidad.
En resumen, el fracaso es una parte inherente del proceso de investigación y desarrollo de nuevas terapias. Si bien los resultados negativos pueden ser desalentadores y costosos, especialmente en las fases avanzadas como la Fase 3, su valor para la ciencia, la investigación futura y, crucialmente, para los pacientes, es innegable. La transparencia, la difusión de todos los resultados y un diseño de estudio cuidadoso son fundamentales para maximizar el aprendizaje de cada ensayo, independientemente de su resultado primario, y así seguir avanzando en la búsqueda de tratamientos más efectivos y seguros.
Si quieres conocer otros artículos parecidos a ¿Qué pasa cuando falla un ensayo clínico? puedes visitar la categoría Investigación.
