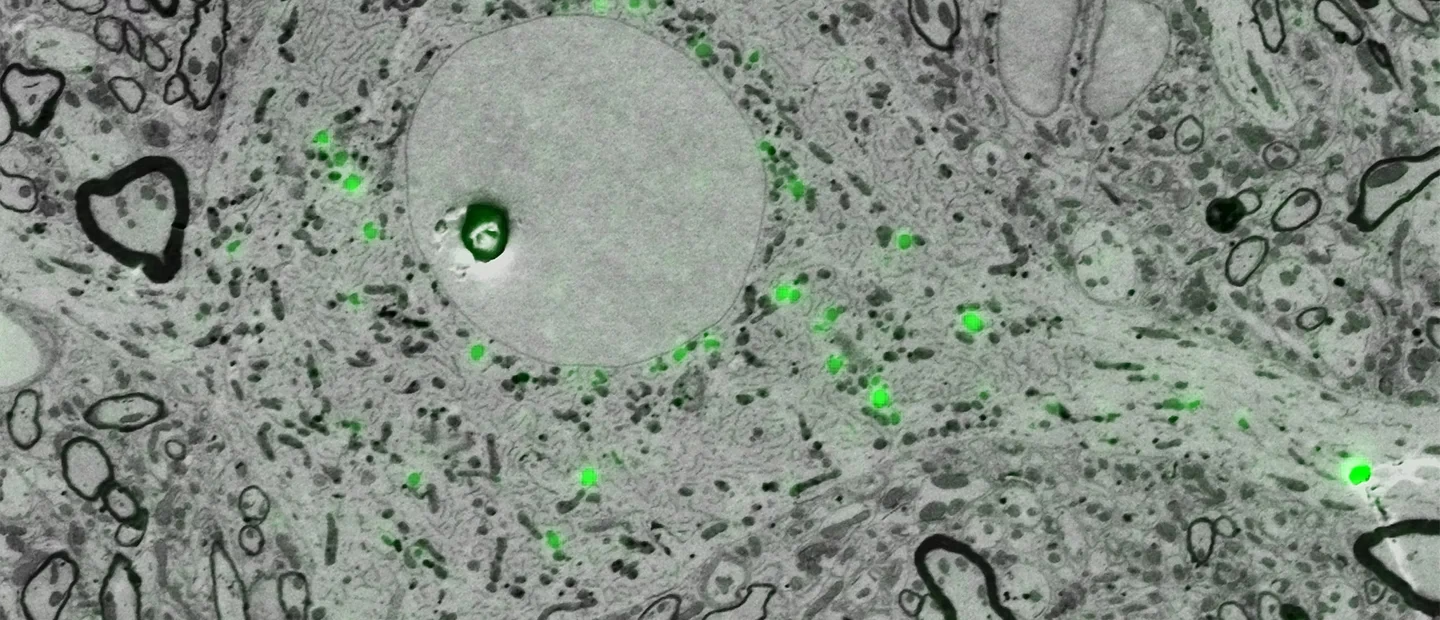
El estudio de los componentes biológicos, desde células completas hasta intrincados complejos moleculares, requiere herramientas que permitan visualizarlos con un detalle sin precedentes. Durante mucho tiempo, la microscopía óptica y la microscopía electrónica han ofrecido visiones complementarias pero limitadas individualmente. La microscopía óptica, utilizando fotones, es excelente para observar células vivas o fijadas y localizar componentes específicos mediante marcadores fluorescentes, pero su resolución está limitada por la difracción de la luz, típicamente alrededor de los 250 nanómetros, aunque las técnicas de super-resolución pueden alcanzar los 50 nm. Por otro lado, la microscopía electrónica, empleando electrones, ofrece una resolución mucho mayor, capaz de distinguir detalles a nivel molecular, pero generalmente requiere que las muestras estén fijadas y procesadas de maneras que impiden la observación de procesos dinámicos en células vivas y pueden introducir artefactos.
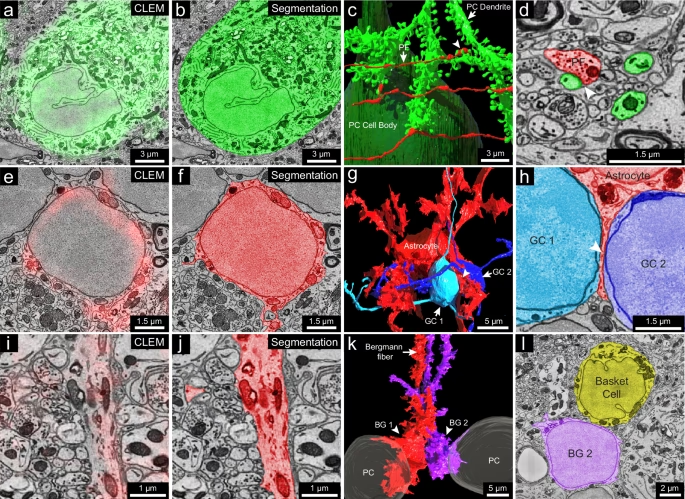
La necesidad de combinar la información contextual y de localización que proporciona la microscopía óptica con el detalle ultraestructural de la microscopía electrónica ha llevado al desarrollo de técnicas avanzadas que cierran esta brecha, como la Microscopía Correlativa de Luz y Electrones (CLEM) y, para obtener estructuras de alta resolución en un estado lo más cercano posible al nativo, la Crio-Microscopía Electrónica (Crio-ME).
- ¿Qué es la Microscopía Correlativa de Luz y Electrones (CLEM)?
- Técnicas Comunes en CLEM
- ¿Qué es la Crio-Microscopía Electrónica (Crio-ME)?
- ¿Por Qué Congelar la Muestra en Crio-ME?
- CLEM vs. Crio-ME: Diferencias y Complementariedad
- Avances Tecnológicos y Automatización
- El Futuro de la Biología Estructural
- Preguntas Frecuentes
- Conclusión
¿Qué es la Microscopía Correlativa de Luz y Electrones (CLEM)?
La CLEM, o Microscopía Correlativa de Luz y Electrones, es una estrategia que integra las capacidades de la microscopía óptica (MO) y la microscopía electrónica (ME) para obtener información complementaria de una misma muestra biológica. La idea central es aprovechar la capacidad de la MO para observar muestras en un estado más cercano al fisiológico (incluso vivas en algunos casos antes de la fijación para ME) y para localizar moléculas específicas mediante fluorescencia, y luego correlacionar esta información con las imágenes de alta resolución obtenidas por ME, que revelan la ultraestructura detallada de la misma región.
Esta combinación es particularmente valiosa en ciencias de la vida porque permite, por ejemplo, seguir un proceso dinámico en una célula viva mediante MO, fijar la célula en un punto de interés y luego examinar la ultraestructura de esa región exacta con ME. Esto proporciona una comprensión mucho más rica de los eventos biológicos, correlacionando la función (vista por MO, a menudo con marcaje fluorescente de proteínas específicas) con la estructura (vista por ME). La CLEM se está utilizando cada vez más en campos como la neurociencia y la virología para examinar muestras que van desde organismos multicelulares hasta el nivel molecular.
Técnicas Comunes en CLEM
La porción de microscopía electrónica en CLEM típicamente se basa en la Microscopía Electrónica de Transmisión (TEM) o la Microscopía Electrónica de Barrido (SEM). Sin embargo, el análisis por microscopía óptica puede implementarse utilizando una variedad de técnicas de MO, incluyendo:
- LSM (Laser Scanning Microscopy)
- EPi (Epi-fluorescent microscopy)
- STORM (Stochastic Optical Reconstruction Microscopy)
- PALM (Photoactivated Localization Microscopy)
- STED (Stimulated Emission Depletion)
- SIM (Structure Illumination Microscopy)
Estas técnicas de super-resolución (como STORM, PALM, STED, SIM) en MO pueden reducir el límite de resolución por debajo de los 250 nm, acercándose a los 50 nm, lo que mejora la correlación con la ME.
Desafíos en la Preparación de Muestras para CLEM
Uno de los principales desafíos en CLEM es la preparación de la muestra. Los métodos de preparación óptimos para MO y ME son a menudo incompatibles. La MO con fluorescencia requiere que las proteínas fluorescentes mantengan su funcionalidad, mientras que la ME (especialmente TEM) a menudo implica deshidratación, inclusión en resina y corte en secciones muy finas (usando un ultramicrótomo). Para SEM, la muestra se recubre con metal. Desarrollar protocolos de preparación que sean compatibles con ambas técnicas y que preserven tanto la fluorescencia como la ultraestructura es crucial y a menudo difícil.
Además de la preparación, alinear las imágenes obtenidas con ambas técnicas es otro reto. La ME enfoca un área XY mucho más pequeña que una imagen típica de MO. Para asegurar que se está observando la misma región de interés, se utilizan marcadores biológicos o artificiales como puntos de referencia. Los sistemas CLEM integrados a menudo vienen en variantes con campo de visión fijo o movible para facilitar esta alineación.
¿Qué es la Crio-Microscopía Electrónica (Crio-ME)?
La Crio-ME, o Crio-Microscopía Electrónica, es una rama de la microscopía electrónica diseñada específicamente para estudiar muestras biológicas sensibles a la radiación en un estado lo más cercano posible a su entorno nativo. El principio fundamental es obtener imágenes de especímenes bajo condiciones criogénicas, típicamente a temperaturas de nitrógeno o helio líquido, utilizando un microscopio electrónico de transmisión.
A diferencia de las técnicas de ME tradicionales que a menudo implican secado o tinción negativa (que puede aplanar las muestras y solo revelar la superficie), la Crio-ME preserva las muestras en una fina capa de hielo vítreo (no cristalino). Este proceso de vitrificación rápida (por ejemplo, mediante congelación por inmersión) inmoviliza las moléculas en un estado hidratado, reduciendo drásticamente el daño causado por el haz de electrones en comparación con la observación a temperatura ambiente. Esta reducción del daño permite usar dosis de electrones más altas sin destruir la estructura, lo que mejora la señal.
Sin embargo, incluso con la protección criogénica, la dosis de electrones debe mantenerse relativamente baja para preservar la estructura a alta resolución. Esto resulta en imágenes con una baja relación señal-ruido. Para superar esto, la Crio-ME a menudo se combina con métodos computacionales de promedio de imágenes. Al promediar un gran número de imágenes de copias idénticas de una estructura (en diferentes orientaciones), se puede mejorar significativamente la relación señal-ruido y reconstruir la estructura tridimensional a alta resolución.
Sub-disciplinas de la Crio-ME
La Crio-ME abarca varias metodologías principales:
- Crio-Tomografía Electrónica (Crio-ET): Permite obtener reconstrucciones 3D de muestras más gruesas o heterogéneas, como células completas o virus. Se toma una serie de imágenes mientras se inclina la muestra respecto al haz de electrones, y estas imágenes se combinan computacionalmente para generar un volumen 3D (un “tomograma”). Es útil para estudiar la organización subcelular y la estructura de complejos únicos o in situ. El promedio de sub-volúmenes de estructuras repetidas dentro de un tomograma puede mejorar la resolución de esas estructuras específicas.
- Crio-ME de Partícula Única: Esta es quizás la variante más utilizada para determinar la estructura de complejos moleculares purificados, como proteínas o complejos proteicos. Se obtienen miles o millones de imágenes 2D de copias idénticas de la partícula en diferentes orientaciones. Estas imágenes se clasifican, alinean y promedian computacionalmente para reconstruir un modelo 3D de alta resolución de la estructura.
- Cristalografía Electrónica: Se aplica a muestras que forman ensamblajes ordenados, como cristales 2D o estructuras helicoidales. El orden inherente de la muestra facilita la alineación y el promedio de las unidades repetidas, permitiendo alcanzar resoluciones muy altas, a veces comparables o superiores a la cristalografía de rayos X para ciertas muestras (como proteínas de membrana en cristales 2D).
¿Por Qué Congelar la Muestra en Crio-ME?
La razón principal para trabajar a temperaturas criogénicas en Crio-ME es minimizar el daño por radiación inducido por el haz de electrones. Los electrones, al interactuar con la materia orgánica, rompen enlaces químicos y generan radicales libres, degradando rápidamente la estructura de la muestra. Congelar la muestra rápidamente en hielo vítreo a temperaturas muy bajas (generalmente -180°C o menos) reduce drásticamente la movilidad molecular y la velocidad de las reacciones químicas inducidas por la radiación. Esto permite que la muestra resista una dosis de electrones significativamente mayor (hasta 6 veces más según algunos estudios) antes de que el daño se vuelva limitante para la resolución. Además, la vitrificación preserva las estructuras biológicas en un estado hidratado y cercano al nativo, evitando los artefactos que pueden surgir de la deshidratación o el secado.
CLEM vs. Crio-ME: Diferencias y Complementariedad
Aunque ambos son avances en microscopía electrónica para biología, CLEM y Crio-ME abordan problemas ligeramente diferentes, aunque pueden combinarse (como en Cryo-CLEM).
La CLEM se centra en correlacionar información. Su objetivo principal es relacionar la localización o dinámica de una molécula o evento específico (visualizado por MO, a menudo con fluorescencia) con la ultraestructura detallada de esa misma región (visualizada por ME). La muestra para la parte de ME en CLEM es típicamente fija (químicamente o por congelación rápida) y puede ser seccionada o preparada de otras maneras. La resolución de la parte de ME en CLEM es alta, pero el desafío clave es la alineación precisa de las imágenes de MO y ME y la compatibilidad de la preparación de la muestra.
La Crio-ME, por otro lado, se enfoca en determinar la estructura 3D de biomoléculas o complejos a alta resolución, a menudo a nivel atómico o casi atómico. Su principal innovación es la preparación de la muestra en hielo vítreo a bajas temperaturas para preservar la estructura en un estado cercano al nativo y mitigar el daño por electrones. Las técnicas de Crio-ME, como partícula única o tomografía, se utilizan para reconstruir directamente la estructura tridimensional de la entidad biológica.

Pueden ser complementarias. Por ejemplo, la Crio-CLEM permite localizar una estructura específica dentro de una célula mediante MO y luego estudiar su ultraestructura o determinar su estructura 3D de alta resolución in situ mediante crio-tomografía electrónica.
| Característica | CLEM | Crio-ME |
|---|---|---|
| Técnicas base | Microscopía Óptica + Microscopía Electrónica (TEM o SEM) | Microscopía Electrónica de Transmisión (bajo condiciones criogénicas) |
| Objetivo principal | Correlacionar localización/función (MO) con ultraestructura (ME) | Determinar estructura 3D de alta resolución (a nivel molecular) |
| Estado de la muestra | MO: Viva o fijada; ME: Fijada (procesada para ME) | Fijada (vitrificada a baja temperatura) |
| Información clave | Localización de componentes, eventos dinámicos, ultraestructura | Estructura 3D de complejos moleculares, arquitectura celular in situ |
| Resolución | Combinación (MO: ~250-50nm; ME: molecular) | Variable (~100 Å hasta ~2 Å o mejor) |
| Muestras típicas | Células, tejidos, organismos donde se busca correlación | Proteínas purificadas, complejos moleculares, virus, células, organelas |
| Desafío principal | Preparación compatible, alineación precisa | Daño por electrones, heterogeneidad conformacional (en partícula única) |
Avances Tecnológicos y Automatización
El rápido progreso en Crio-ME en la última década se debe en gran medida a los avances tecnológicos tanto en hardware como en software. Los nuevos microscopios electrónicos son más estables y permiten una adquisición de datos más controlada. El desarrollo de detectores de electrones directos ha sido revolucionario, ofreciendo mayor sensibilidad y velocidad que las cámaras CCD o la película fotográfica tradicional, y permitiendo la corrección de movimiento de la muestra durante la exposición. La automatización de la adquisición de datos, con software que puede seleccionar automáticamente áreas de interés, enfocar y recoger miles de imágenes durante periodos prolongados sin intervención manual, ha aumentado enormemente el rendimiento.
En el lado computacional, el aumento de la potencia de procesamiento (especialmente con GPUs) y el desarrollo de algoritmos más sofisticados para la alineación, clasificación y reconstrucción de imágenes han sido fundamentales para alcanzar resoluciones cada vez mayores, incluso para complejos con baja simetría o heterogeneidad conformacional. Esto ha transformado la Crio-ME de una técnica nicho a una herramienta de uso generalizado en biología estructural.
El Futuro de la Biología Estructural
La Crio-ME y CLEM están desempeñando un papel crucial en la biología estructural moderna, especialmente al abordar las lagunas dejadas por otras técnicas como la cristalografía de rayos X y la RMN, que son más adecuadas para proteínas individuales o complejos muy homogéneos y pequeños. La Crio-ME es particularmente potente para estudiar grandes complejos macromoleculares, ensamblajes dinámicos y estructuras in situ dentro de las células, que son fundamentales para comprender los procesos biológicos complejos.
Bases de datos como el Electron Microscopy Data Bank (EMDB) reflejan el crecimiento exponencial de estructuras determinadas por Crio-ME. Aunque las estructuras de virus icosaédricos y ribosomas (que tienen alta simetría) dominaron inicialmente, cada vez más estructuras de complejos menos simétricos y más pequeños se están resolviendo a alta resolución. Estas técnicas están permitiendo la visualización de la maquinaria molecular en acción y en su contexto celular, proporcionando información vital para campos que van desde la investigación básica hasta el desarrollo de fármacos.
Preguntas Frecuentes
¿Qué significa CLEM?
CLEM significa Correlative Light and Electron Microscopy, que en español se traduce como Microscopía Correlativa de Luz y Electrones.
¿Qué es la Microscopía Correlativa de Luz y Electrones (CLEM)?
Es una técnica que combina imágenes obtenidas por microscopía óptica (a menudo con marcaje fluorescente para localización) con imágenes de alta resolución de la misma área obtenidas por microscopía electrónica (para detalle ultraestructural). Permite correlacionar la función o localización de componentes con su estructura.
¿Qué es la Crio-Microscopía Electrónica (Crio-ME)?
Es un conjunto de técnicas de microscopía electrónica que obtienen imágenes de muestras biológicas vitrificadas (congeladas rápidamente en hielo no cristalino) a muy bajas temperaturas. Su objetivo es preservar la estructura de la muestra en un estado cercano al nativo y reducir el daño por radiación para permitir la obtención de estructuras 3D de alta resolución.
¿Por qué se congela la muestra en Crio-ME?
La muestra se congela rápidamente para inmovilizar las moléculas en un estado hidratado y formar hielo vítreo, no cristalino. Las bajas temperaturas reducen drásticamente el daño causado por el haz de electrones a la muestra biológica, permitiendo el uso de dosis de electrones suficientes para obtener imágenes de alta resolución sin destruir la estructura.
¿Qué resolución se puede obtener con estas técnicas?
Con CLEM, se combinan resoluciones (óptica: ~250-50nm; electrónica: molecular). Con Crio-ME, la resolución varía según la técnica y la muestra, desde ~100 Å en crio-tomografía de células hasta ~2 Å o mejor en cristalografía electrónica o partícula única para muestras favorables.
¿Qué tipo de muestras se estudian con CLEM o Crio-ME?
CLEM se usa para estudiar células, tejidos o incluso organismos donde se necesita correlacionar la localización de un evento o molécula con la ultraestructura. Crio-ME se aplica a una amplia gama de muestras, incluyendo proteínas purificadas, complejos moleculares, virus, bacterias, organelas y secciones finas de células y tejidos.
Conclusión
La CLEM y la Crio-ME representan avances fundamentales en nuestra capacidad para visualizar la maquinaria molecular de la vida. Al superar las limitaciones de las técnicas de microscopía tradicionales, permiten a los científicos explorar la estructura y función de los componentes biológicos con un detalle y un contexto sin precedentes. Ya sea correlacionando la localización de una proteína específica dentro de una neurona o resolviendo la estructura 3D de un complejo viral a resolución casi atómica, estas técnicas están impulsando descubrimientos en diversas áreas de la biología y abriendo nuevas vías para comprender la salud y la enfermedad.
Si quieres conocer otros artículos parecidos a CLEM y Crio-ME: Ventanas a lo Nano puedes visitar la categoría Neurociencia.