En el vasto y complejo universo de la biología celular y molecular, comprender dónde se encuentran las estructuras y moléculas específicas en relación con la arquitectura general de la célula es un desafío fundamental. Las técnicas de microscopía tradicionales a menudo nos obligan a elegir entre ver la ubicación general de un componente marcado (con microscopía de luz) o ver la estructura fina con un detalle increíble (con microscopía electrónica), pero rara vez ambas cosas simultáneamente y en el mismo contexto. Aquí es donde entra en juego una técnica revolucionaria: la Microscopía Correlativa Luz-Electrones, o CLEM.

CLEM no es simplemente la suma de dos métodos; es una integración poderosa que permite a los investigadores obtener información complementaria de una única muestra. Al combinar la capacidad de la microscopía de luz (generalmente de fluorescencia) para identificar y localizar regiones de interés específicas (marcadas con fluoróforos) con la capacidad de la microscopía electrónica para proporcionar detalles ultraestructurales a escala nanométrica, CLEM ofrece una visión sin precedentes de los sistemas biológicos. Esta correlación permite responder preguntas como: ¿Dónde se encuentra exactamente esa proteína marcada dentro de la sinapsis? ¿Cómo se relaciona la organización del citoesqueleto con la distribución de un orgánulo particular?
¿Qué es la Microscopía Correlativa Luz-Electrones (CLEM)?
La Microscopía Correlativa Luz-Electrones (CLEM) es una técnica que fusiona las capacidades de un microscopio óptico, típicamente un microscopio de fluorescencia, con las de un microscopio electrónico. La esencia de CLEM radica en la capacidad de observar la misma muestra o la misma región de una muestra utilizando estas dos modalidades de imagen fundamentalmente diferentes y luego correlacionar los datos obtenidos.
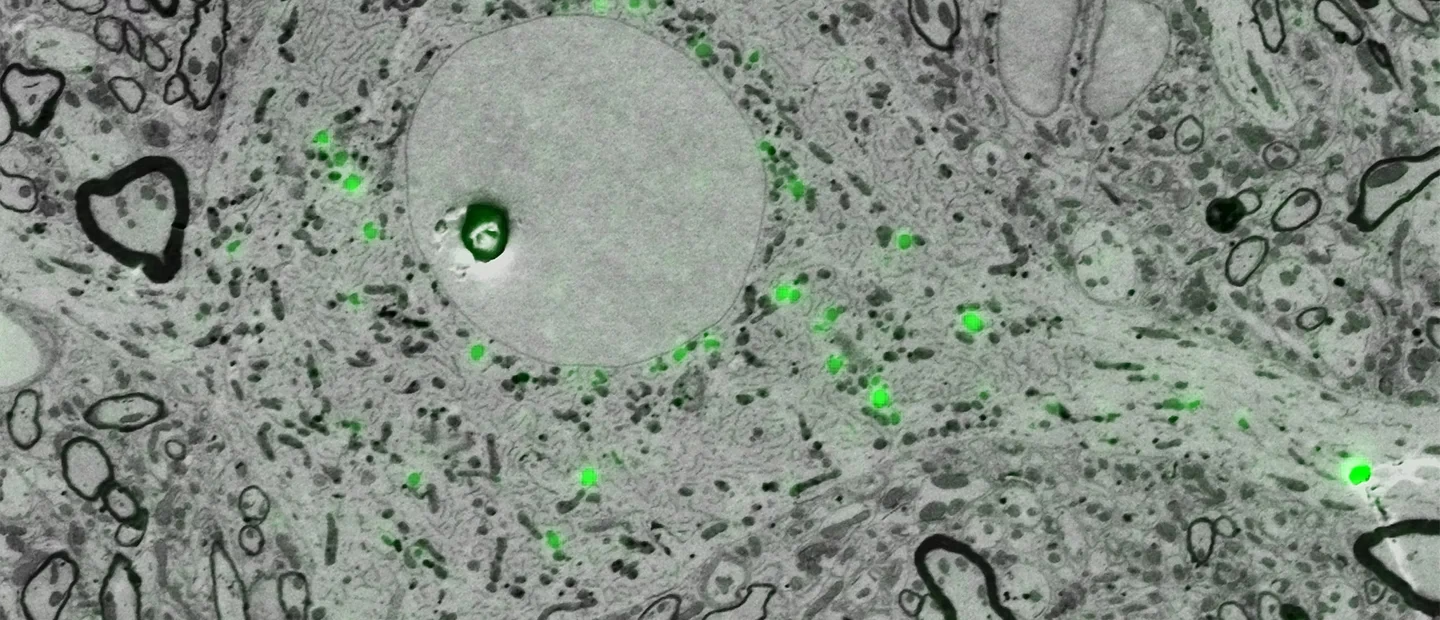
Históricamente, esta correlación se realizaba de forma secuencial y a menudo tediosa. Se preparaba una muestra para microscopía de fluorescencia, se identificaban y se fotografiaban las regiones de interés. Luego, la misma muestra debía ser preparada de manera diferente (y a menudo más drástica) para microscopía electrónica, transportada, localizada nuevamente la misma región y finalmente imageda. La correlación de las imágenes resultantes, tomadas en diferentes momentos, con diferentes preparaciones y en diferentes instrumentos, requería un software complejo y era propensa a errores o cambios en la muestra.
Los sistemas CLEM integrados han revolucionado este proceso. En un sistema integrado, la muestra se puede observar simultáneamente o de forma muy rápida y secuencial con un haz de electrones y una ruta de luz óptica dentro del mismo instrumento. Esto simplifica enormemente el flujo de trabajo, lo hace más rápido y reduce drásticamente la posibilidad de que la muestra sufra alteraciones o desplazamientos entre las adquisiciones de datos. La superposición de las dos imágenes se facilita enormemente, a menudo realizándose de forma automática gracias a la precisión de la integración.
La Sinergia de Dos Modalidades: Luz y Electrones
La potencia de CLEM reside en la complementariedad de la información proporcionada por cada tipo de microscopio:
Microscopía de Fluorescencia
La microscopía de fluorescencia utiliza la luz visible para excitar fluoróforos (moléculas que emiten luz a una longitud de onda diferente tras ser excitadas) que se han introducido en la muestra. Estos fluoróforos pueden ser colorantes específicos, anticuerpos marcados (inmunomarcaje) o proteínas fluorescentes genéticamente codificadas (como GFP). La gran ventaja de la microscopía de fluorescencia es su capacidad para etiquetar selectivamente moléculas o estructuras específicas y hacerlas visibles, incluso si son raras o están distribuidas de forma compleja. Permite visualizar procesos dinámicos en células vivas (aunque en CLEM a menudo se trabaja con muestras fijadas o congeladas) y utilizar múltiples etiquetas fluorescentes simultáneamente para diferenciar varias regiones de interés. Sin embargo, la resolución de la microscopía de luz está limitada por la difracción de la luz, generalmente a unos 200-300 nanómetros, lo que impide ver los detalles finos de la ultraestructura celular.
Recientemente, se han explorado combinaciones aún más sofisticadas, como la correlación de mediciones de tensión molecular basadas en FRET (Transferencia de Energía por Resonancia de Förster, una técnica de fluorescencia que mide la proximidad molecular) con microscopía crioelectrónica. Un estudio de Kumar et al. utilizó esta aproximación para investigar cómo la fuerza sobre la proteína talina, un componente clave de las adhesiones focales que conecta las integrinas al filamento de actina, se relaciona con la organización de la actina. Descubrieron que las regiones con alta tensión en talina presentaban filamentos de actina altamente alineados y lineales, mientras que las regiones de baja tensión mostraban una estructura de actina menos organizada. Este ejemplo ilustra cómo la fluorescencia puede proporcionar información funcional y de estado (como la tensión molecular) que luego se correlaciona con la estructura fina.
Microscopía Electrónica
En contraste, la microscopía electrónica utiliza un haz de electrones acelerados en lugar de luz. Dado que la longitud de onda de los electrones acelerados es mucho más corta que la de la luz visible, los microscopios electrónicos pueden superar el límite de difracción de la luz y alcanzar resoluciones mucho mayores, típicamente en el rango de los nanómetros o incluso sub-nanómetros. Esto permite visualizar la ultraestructura celular con un detalle asombroso: membranas, orgánulos, complejos proteicos y la organización molecular dentro de las células y tejidos. Sin embargo, la microscopía electrónica requiere que las muestras sean muy delgadas (para que los electrones puedan atravesarlas), a menudo fijadas químicamente y deshidratadas, y observadas en vacío, condiciones que no son compatibles con la vida celular y pueden introducir artefactos. Además, la microscopía electrónica por sí sola no permite identificar fácilmente moléculas específicas a menos que se utilicen técnicas de marcaje con partículas de oro, que tienen sus propias limitaciones.
¿Por Qué Combinar Ambas Técnicas?
La principal motivación detrás de CLEM es obtener una comprensión más completa de los sistemas biológicos combinando la información contextual y molecular de la microscopía de luz con los detalles estructurales de alta resolución de la microscopía electrónica. Permite:
- Localizar estructuras o moléculas fluorescentemente marcadas dentro de su contexto ultraestructural.
- Identificar regiones de interés raras o específicas (visible por fluorescencia) para su posterior análisis detallado por microscopía electrónica.
- Correlacionar eventos dinámicos observados en microscopía de luz en células vivas (si se usan protocolos CLEM en células vivas antes de la fijación) con la estructura fina de las células fijadas en un momento dado.
- Estudiar la relación espacial entre diferentes componentes celulares.
Esta capacidad de correlación es invaluable en diversas disciplinas de las ciencias de la vida, incluyendo la neurociencia (para estudiar la ultraestructura de sinapsis marcadas, la localización de receptores, etc.), la investigación de tejidos (para analizar la organización celular y tisular en detalle) y la investigación de proteínas (para ver dónde se localizan y cómo interactúan en su entorno nativo).
CLEM Tradicional vs. CLEM Integrado
La evolución hacia sistemas CLEM integrados ha traído mejoras significativas:
| Característica | CLEM Tradicional (Secuencial) | CLEM Integrado |
|---|---|---|
| Proceso | Imágenes separadas en diferentes microscopios, posible transporte de muestra. | Imágenes en el mismo instrumento o con mínimo manejo de muestra. |
| Tiempo | Más lento, requiere más pasos de preparación y transferencia. | Más rápido, flujo de trabajo optimizado. |
| Preparación de muestra | Puede requerir diferentes preparaciones para cada microscopio, o adaptaciones complejas. | Preparación unificada o compatible para ambas modalidades. |
| Integridad de la muestra | Mayor riesgo de cambios, daños o desplazamiento de la muestra entre adquisiciones. | Menor riesgo de cambios, la muestra permanece estable. |
| Correlación de imágenes | Manual o semi-automática, requiere software complejo, puede ser laboriosa. | Automática o altamente facilitada por la integración del hardware y software. |
| Complejidad | Mayor complejidad logística y técnica. | Menor complejidad operativa una vez establecido el sistema. |
La integración reduce la complejidad y aumenta la eficiencia, haciendo que CLEM sea más accesible y fiable para una gama más amplia de aplicaciones.
Cryo-CLEM: Preservando el Estado Nativo
Una variación particularmente poderosa y cada vez más utilizada es la Microscopía Correlativa Luz-Electrones Criogénica, o Cryo-CLEM. Esta técnica combina las ventajas de la microscopía de fluorescencia con la microscopía electrónica en condiciones criogénicas, es decir, a temperaturas muy bajas.
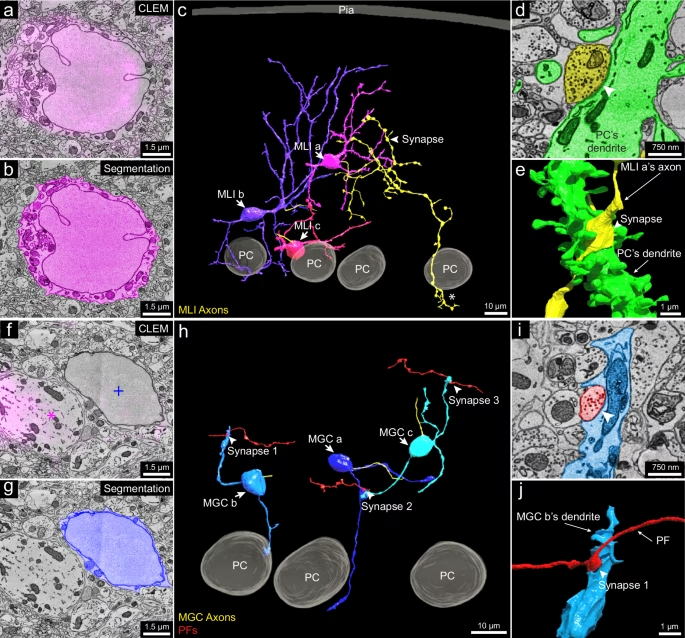
El uso de condiciones criogénicas es crucial porque permite vitrificar (congelar rápidamente sin formación de cristales de hielo) las células o tejidos en un estado lo más cercano posible a su estado nativo in vivo. Esto evita los artefactos que pueden introducirse con la fijación química y la deshidratación utilizadas en la microscopía electrónica convencional. Cryo-CLEM es especialmente valioso para estudiar la ultraestructura de moléculas diana significativas con funciones celulares específicas en su contexto celular casi nativo.
El flujo de trabajo típico de Cryo-CLEM implica:
- Vitrificar la muestra: Usando métodos como la inmersión en etano líquido (por ejemplo, con un Vitrobot) o la congelación por alta presión (por ejemplo, con un EM ICE).
- Microscopía de Fluorescencia Criogénica: Imaging la muestra vitrificada en un microscopio de fluorescencia adaptado para operar a bajas temperaturas (como un confocal criogénico sp8). Esto permite localizar las estructuras o moléculas fluorescentemente marcadas en la muestra congelada.
- Microscopía Electrónica (Tomografía o FIB-SEM): Transferir la muestra al microscopio electrónico para obtener imágenes de alta resolución. Si la muestra es lo suficientemente delgada (menos de ~500 nm), se puede realizar directamente tomografía crioelectrónica (por ejemplo, en un Krios) para obtener una reconstrucción 3D de la ultraestructura. Si la muestra es más gruesa, se puede usar una técnica de fresado con haz de iones focalizado (FIB) acoplado a un microscopio electrónico de barrido (SEM) (por ejemplo, con un Aquilos) para cortar láminas delgadas (lamellas) de la región de interés identificada por fluorescencia, antes de realizar la tomografía.
- Correlación: Usar software especializado (como Maps) para correlacionar las imágenes de fluorescencia y electrónicas, alineando las regiones marcadas con la ultraestructura circundante.
Cryo-CLEM, a menudo seguido por crio-tomografía electrónica 3D, es una técnica de vanguardia que permite revelar la ubicación de moléculas con alta resolución temporal y espacial por fluorescencia, y luego analizar su estructura 3D a resolución molecular dentro del contexto celular por tomografía. Es una herramienta indispensable para la biología estructural in situ.
Preguntas Frecuentes sobre CLEM
¿Qué tipo de información obtengo con CLEM?
Obtienes información dual: la ubicación precisa de moléculas o estructuras específicas marcadas (de la microscopía de luz) y la ultraestructura detallada del entorno circundante a nivel nanomolecular (de la microscopía electrónica). Es la combinación de 'dónde está' con 'cómo es su entorno detallado'.
¿Es CLEM adecuado para células vivas?
Directamente, no. La microscopía electrónica requiere que las muestras estén fijadas y, a menudo, deshidratadas o vitrificadas (en el caso de Cryo-CLEM), lo cual no es compatible con la vida celular. Sin embargo, puedes observar células vivas por microscopía de fluorescencia, fijarlas rápidamente en un estado particular de interés y luego procesarlas para CLEM.
¿Cómo se realiza la correlación entre las imágenes de luz y electrónicas?
En sistemas integrados, el hardware y el software están diseñados para facilitar la alineación automática o semi-automática, a menudo usando puntos de referencia o fiduciales en la muestra. En enfoques secuenciales, se utilizan marcadores en la rejilla o portaobjetos y software especializado para superponer las imágenes basándose en estos puntos de referencia.
¿Cuál es la principal ventaja de Cryo-CLEM sobre CLEM convencional?
La principal ventaja es la preservación de la muestra en un estado casi nativo mediante vitrificación. Esto evita los artefactos que pueden introducir la fijación química y la deshidratación, permitiendo una visualización más fiel de la ultraestructura y la localización molecular in situ.
¿En qué campos de la neurociencia se aplica CLEM?
En neurociencia, CLEM es crucial para estudiar la ultraestructura de las sinapsis y las espinas dendríticas, la localización subcelular de receptores, canales iónicos o proteínas del citoesqueleto, la organización de las mielina, la estructura de los axones, y la patología de enfermedades neurodegenerativas a nivel ultraestructural, correlacionando marcadores moleculares con cambios morfológicos.
En resumen, la microscopía correlativa luz-electrones, especialmente en sus formas integradas y criogénicas, representa un avance significativo en nuestra capacidad para visualizar la biología celular y molecular. Al tender un puente entre la resolución molecular de la microscopía de luz y el detalle ultraestructural de la microscopía electrónica, CLEM nos permite explorar el mundo microscópico con una profundidad y un contexto sin precedentes, abriendo nuevas vías para el descubrimiento científico en campos tan diversos como la neurociencia, la biología celular y la investigación de enfermedades.
Si quieres conocer otros artículos parecidos a CLEM: Uniendo Mundos Microscópicos puedes visitar la categoría Neurociencia.
