Durante mucho tiempo, los trastornos del sueño y las alteraciones del ritmo circadiano se consideraron simplemente síntomas o consecuencias tardías de las enfermedades neurodegenerativas. Sin embargo, la investigación reciente ha revelado una verdad mucho más compleja y preocupante: los problemas de sueño y la desregulación del ritmo circadiano a menudo aparecen *antes* del diagnóstico clínico de la neurodegeneración o en sus etapas iniciales. Esta observación sugiere una relación potencialmente bidireccional, donde no solo la enfermedad afecta el sueño, sino que los trastornos del sueño y las alteraciones circadianas pueden acelerar o contribuir al proceso neurodegenerativo.

Entender esta compleja interconexión es crucial, no solo para mejorar la calidad de vida de los pacientes, sino también para identificar posibles biomarcadores tempranos y, quizás algún día, desarrollar terapias preventivas o modificadoras de la enfermedad dirigidas a regular el sueño y los ritmos biológicos.
- La Interconexión entre Sueño, Ritmo Circadiano y Neurodegeneración
- Trastornos del Sueño como Predictores y Aceleradores de la Neurodegeneración
- La Disrupción Circadiana Agrava el Proceso Neurodegenerativo
- La Progresión de la Neurodegeneración Promueve la Disrupción Circadiana y los Trastornos del Sueño
- Tabla Comparativa: Trastornos del Sueño/Circadianos y Enfermedades Neurodegenerativas
- Preguntas Frecuentes
- Conclusión
La Interconexión entre Sueño, Ritmo Circadiano y Neurodegeneración
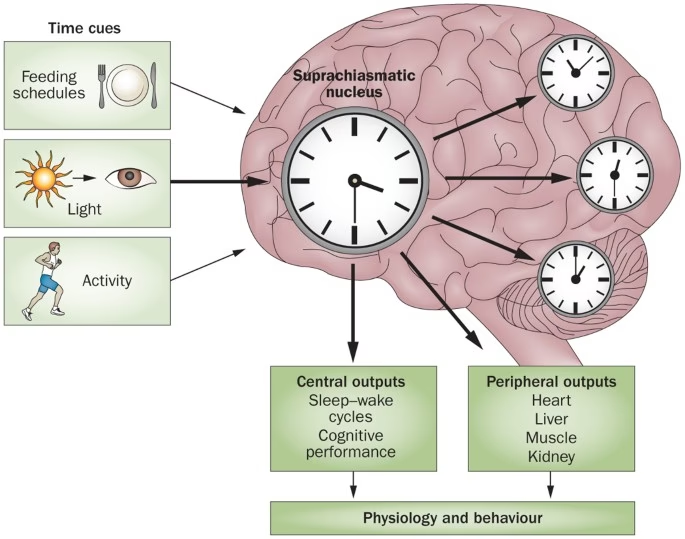
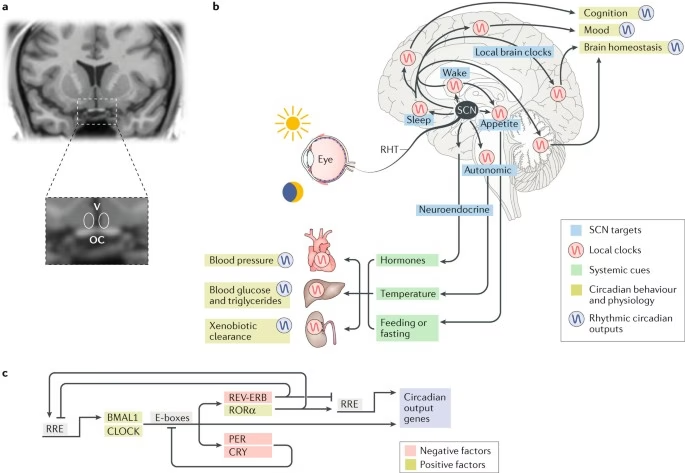
El ritmo circadiano es un ciclo biológico interno de aproximadamente 24 horas que regula una amplia gama de procesos fisiológicos, incluyendo el ciclo sueño-vigilia, la temperatura corporal y la liberación de hormonas. El sueño, por su parte, es un estado fisiológico complejo esencial para funciones críticas como la consolidación de la memoria, la eliminación de desechos metabólicos del cerebro (incluyendo proteínas asociadas a enfermedades neurodegenerativas) y la restauración neuronal.
Cuando este delicado equilibrio se rompe, ya sea por trastornos del sueño primarios o por una desregulación del ritmo circadiano, el cerebro puede volverse más vulnerable. La investigación sugiere que la falta crónica de sueño o un ritmo circadiano alterado pueden contribuir a la acumulación de proteínas tóxicas, aumentar la neuroinflamación y afectar la salud sináptica, procesos todos ellos implicados en la neurodegeneración.
Trastornos del Sueño como Predictores y Aceleradores de la Neurodegeneración
Numerosos trastornos del sueño han sido identificados como posibles marcadores prodrómicos (síntomas tempranos que preceden al diagnóstico) o factores de riesgo para el desarrollo o la progresión de enfermedades neurodegenerativas específicas.
Trastorno de Conducta del Sueño REM (RBD)
El RBD es quizás el ejemplo más destacado de un trastorno del sueño con un fuerte vínculo prodrómico. Se caracteriza por la pérdida de la atonía muscular normal durante la fase REM del sueño, lo que lleva a que las personas "actúen" sus sueños, a menudo con movimientos violentos o vocalizaciones. El RBD está reconocido como un predictor muy potente de las α-sinucleinopatías, un grupo de enfermedades que incluye la Enfermedad de Parkinson (EP), la Demencia con Cuerpos de Lewy (DCL) y la Atrofia Multisistémica (AMS).
Estudios longitudinales han demostrado que un alto porcentaje de individuos con RBD aislado (sin diagnóstico neurológico previo) desarrollarán una α-sinucleinopatía en los años siguientes. Se estima una tasa de conversión significativa, lo que sugiere que el RBD aislado es, en muchos casos, una manifestación temprana de un proceso neurodegenerativo subyacente, a menudo asociado con la acumulación de la proteína α-sinucleína en el cerebro.
Si bien la asociación más fuerte es con las α-sinucleinopatías, algunos estudios han explorado el vínculo entre el RBD y la Enfermedad de Alzheimer (EA). Sin embargo, la evidencia sugiere que, en muchos casos, los pacientes con RBD que desarrollan demencia presentan una "patología mixta", con características tanto de la EA como de la DCL, lo que refuerza la conexión principal del RBD con las α-sinucleinopatías.
Insomnio
El insomnio crónico, caracterizado por dificultad para iniciar o mantener el sueño, también ha sido implicado en el proceso patológico de la EA. La privación del sueño, tanto en estudios animales como humanos, se ha asociado con un aumento en la formación y depósito de la proteína beta-amiloide (Aβ), una de las características distintivas de la EA. Además, la duración objetiva corta del sueño y la interrupción del ritmo circadiano pueden tener un efecto adicional en el riesgo de EA.
Revisiones sistemáticas y estudios longitudinales han encontrado que el insomnio contribuye significativamente a un mayor riesgo de incidencia de EA. La gravedad creciente del insomnio a lo largo del tiempo también se ha relacionado con un mayor riesgo de deterioro de la memoria o demencia. Para la EP, la evidencia es más limitada, aunque algunos estudios sugieren una mayor incidencia de insomnio antes del diagnóstico. Sin embargo, no está claro si el insomnio es una causa o un síntoma prodrómico temprano de la EP.
Apnea Obstructiva del Sueño (OSA)
La OSA, un trastorno caracterizado por episodios repetidos de obstrucción de las vías respiratorias superiores durante el sueño, se ha asociado con hipoxia intermitente (niveles bajos de oxígeno), neuroinflamación y fragmentación del sueño. Estos factores pueden acelerar la neurodegeneración al afectar la eliminación de Aβ y agravar los ovillos neurofibrilares de tau en la EA, o al dañar el sistema dopaminérgico nigroestriatal y promover la agregación de α-sinucleína en la EP.
Numerosos estudios han confirmado el papel emergente de la OSA en la incidencia o progresión temprana de condiciones neurodegenerativas. Se ha observado un mayor riesgo de desarrollar deterioro cognitivo leve (MCI) o demencia, especialmente en casos de OSA severa. La adherencia a la terapia de presión positiva en las vías respiratorias (CPAP), el tratamiento principal para la OSA, podría reducir el riesgo de diagnóstico de EA o MCI y ralentizar el deterioro cognitivo. Para la EP, también se ha revelado un mayor riesgo en individuos con apnea del sueño, con evidencia de niveles elevados de α-sinucleína en plasma en pacientes con OSA.
Excesiva Somnolencia Diurna (EDS)
La EDS es otro predictor emergente de neurodegeneración. Muchos estudios han identificado una asociación temporal entre la EDS y el riesgo de demencia o EA, incluso independientemente de otras enfermedades crónicas. La EDS en adultos mayores cognitivamente normales se ha asociado con un adelgazamiento más prominente de la materia gris en regiones vulnerables a la patología de la EA y con una mayor acumulación de Aβ en ciertas áreas del cerebro.
La EDS también es un marcador prodrómico robusto de la EP, con un riesgo 2-3 veces mayor de incidencia de EP en la población general. Sin embargo, los resultados son inconsistentes sobre si la EDS predice la conversión a neurodegeneración en individuos con RBD aislado. La relación exacta entre la EDS y la patología de los cuerpos de Lewy no está completamente clara, y se necesita más investigación para determinar si la EDS precede a la patología o es una consecuencia temprana.
Síndrome de Piernas Inquietas (RLS) y Otros Trastornos del Movimiento relacionados con el Sueño
Algunos estudios prospectivos sugieren que el RLS, caracterizado por una necesidad irresistible de mover las piernas, a menudo acompañada de sensaciones desagradables, se asocia con un riesgo 1.5-2.5 veces mayor de incidencia de EP. Sin embargo, el vínculo patológico con el sistema dopaminérgico no está completamente establecido.
En general, los trastornos del movimiento relacionados con el sueño (SRMD) se han asociado con un mayor riesgo de demencia por todas las causas, siendo esta asociación más pronunciada en mujeres y personas de mediana edad. La somnambulismo, una parasomnia NREM, también se ha asociado con un mayor riesgo de tener EP.
La Disrupción Circadiana Agrava el Proceso Neurodegenerativo
Además de los trastornos del sueño específicos, la desregulación del propio ritmo circadiano de actividad, inicialmente vista como un síntoma, ahora se considera que puede estar involucrada en la aparición o progresión de la neurodegeneración. En otras palabras, la disrupción circadiana puede preceder a la sintomatología clínica o aumentar el riesgo de enfermedades neurodegenerativas.
En la EP, pocos estudios han examinado la asociación temporal entre la disrupción del ritmo circadiano y la enfermedad. Sin embargo, aquellos que lo han hecho sugieren que una ritmicidad circadiana debilitada se asocia con un mayor riesgo de incidencia de EP, incluso después de excluir diagnósticos tempranos. Esto indica que la disrupción del ritmo circadiano podría ser un marcador prodrómico para la EP.
En la EA, se ha observado un desalineamiento circadiano más evidente en pacientes con MCI antes del diagnóstico de EA. Estudios recientes muestran que individuos con EA preclínica (con evidencia de patología Aβ en PET pero sin síntomas cognitivos) demuestran una mayor fragmentación del ritmo de actividad-reposo, independientemente de la edad. Esto sugiere que la disrupción circadiana está involucrada tempranamente en la patogénesis de la EA.
La investigación en modelos animales ha revelado que la disrupción del ritmo circadiano puede alterar las oscilaciones diarias de Aβ en el cerebro y acelerar la acumulación de placas amiloides. Estos hallazgos refuerzan la evidencia del papel potencial de la regulación circadiana en la EA.
La disrupción circadiana, evaluada a través de indicadores conductuales como la actigrafía (seguimiento de la actividad) o hábitos de sueño irregulares (como trabajar en turnos nocturnos o levantarse tarde), se ha asociado consistentemente con un mayor riesgo de deterioro cognitivo y demencia en estudios epidemiológicos. Una menor amplitud del ritmo de actividad de 24 horas, una mayor variabilidad intradía (fragmentación) y una menor estabilidad interdiaria (regularidad) se asocian con un mayor riesgo de desarrollar demencia por EA o de transicionar de MCI a demencia por EA.
La Progresión de la Neurodegeneración Promueve la Disrupción Circadiana y los Trastornos del Sueño
La relación bidireccional significa que, a medida que las enfermedades neurodegenerativas progresan, también tienden a exacerbar los problemas de sueño y la disrupción circadiana.
En la EP, aunque los trastornos del sueño son comunes, los cambios rítmicos a lo largo del proceso de la enfermedad no siempre se han notado. Sin embargo, algunos estudios sugieren que los pacientes con estadios más avanzados de EP tienden a ser más activos más tarde en el día, indicando una alteración del ritmo circadiano relacionada con la gravedad de la enfermedad. Los trastornos del sueño coexistentes, como el RBD, también pueden aumentar la variabilidad del ritmo circadiano. Es importante considerar el papel de la medicación dopaminérgica en estos cambios, ya que algunos trastornos del sueño, como la EDS y el RLS, pueden ser consecuencias de la terapia a medida que la enfermedad progresa y las dosis o complicaciones aumentan.
En la EA, los estudios que utilizan indicadores funcionales y biológicos de disrupción circadiana muestran cambios más severos o irregulares a medida que la enfermedad avanza. La fragmentación del ciclo de actividad-reposo y la actividad nocturna aumentan con la gravedad de la EA. El desalineamiento de fase (adelanto o retraso) también se vuelve más prominente en estadios avanzados. Indicadores biológicos como los niveles de melatonina también muestran patrones alterados a medida que la enfermedad progresa.
Aunque el envejecimiento normal ya se asocia con ciertas alteraciones circadianas, la patología de la EA parece impulsar la disfunción circadiana de manera independiente. La alta prevalencia de EA preclínica en adultos mayores sugiere que, en muchos estudios que examinan la disrupción circadiana o los trastornos del sueño como predictores, los participantes de edad avanzada podrían ya estar en una etapa temprana de la enfermedad, lo que explicaría por qué una patología subyacente puede conducir a la disfunción circadiana y del sueño.
La prevalencia de trastornos del sueño en individuos con EA es alta, alrededor del 39%. Incluso en la etapa de MCI, los pacientes ya muestran alteraciones del sueño a nivel objetivo y subjetivo. A medida que la demencia empeora, los trastornos del sueño coexistentes, como la EDS, pueden agravarse por factores mediadores como la depresión comórbida y la disminución del compromiso social. La OSA también es común en individuos con EA. Sin embargo, la asociación longitudinal entre la OSA u otros trastornos del sueño específicos y la progresión de la EA aún no se ha explorado a fondo.
Tabla Comparativa: Trastornos del Sueño/Circadianos y Enfermedades Neurodegenerativas
| Trastorno del Sueño / Circadiano | Enfermedades Neurodegenerativas Asociadas | Tipo de Asociación (Prodrómica/Bidireccional/Riesgo) |
|---|---|---|
| RBD | EP, DCL, AMS (α-sinucleinopatías) | Fuerte predictor prodrómico |
| Insomnio | EA (riesgo aumentado), EP (posible prodrómico) | Riesgo aumentado (EA), Posible prodrómico (EP) |
| OSA | EA/Demencia, EP | Riesgo aumentado, Acelerador potencial |
| EDS | EA/Demencia, EP | Predictor prodrómico (ambas) |
| RLS | EP | Riesgo aumentado |
| Disrupción Ritmo Circadiano | EP, EA/Demencia | Prodrómico (EP), Implicado tempranamente (EA), Agravado por progresión (ambas) |
Preguntas Frecuentes
¿El RBD siempre conduce a la Enfermedad de Parkinson?
No siempre, pero la probabilidad es muy alta. La mayoría de las personas con RBD aislado terminarán desarrollando una α-sinucleinopatía, siendo la EP la más común, seguida de la DCL y la AMS. Se considera un predictor muy fuerte.
¿El insomnio puede causar Alzheimer?
La investigación sugiere una fuerte asociación y un mayor riesgo de EA en personas con insomnio crónico. No se puede afirmar definitivamente que sea una causa directa, pero la privación del sueño y el insomnio parecen contribuir a la acumulación de proteínas patológicas asociadas a la EA, actuando potencialmente como un factor que acelera o facilita el proceso.
¿La apnea del sueño está relacionada con la demencia?
Sí, numerosos estudios han encontrado una asociación significativa entre la apnea obstructiva del sueño (OSA) y un mayor riesgo de desarrollar deterioro cognitivo leve y demencia, incluida la Enfermedad de Alzheimer. La hipoxia intermitente y la fragmentación del sueño causadas por la OSA podrían dañar el cerebro y acelerar los procesos neurodegenerativos.
¿Las enfermedades como el Parkinson o el Alzheimer afectan el sueño?
Absolutamente. Las alteraciones del sueño y del ritmo circadiano son síntomas comunes en las enfermedades neurodegenerativas. A medida que estas enfermedades progresan, las dificultades para dormir, la fragmentación del sueño, la somnolencia diurna y la desregulación de los ritmos circadianos tienden a empeorar, lo que impacta significativamente la calidad de vida de los pacientes y sus cuidadores.
¿Es la relación entre sueño y neurodegeneración unidireccional?
La evidencia actual sugiere fuertemente que la relación es bidireccional. Los trastornos del sueño y la disrupción circadiana pueden ser marcadores tempranos o factores que contribuyen al inicio o la progresión de la neurodegeneración. A su vez, el proceso neurodegenerativo daña las áreas del cerebro que regulan el sueño y los ritmos circadianos, lo que lleva a una exacerbación de estos problemas.
Conclusión
La conexión entre el sueño, el ritmo circadiano y las enfermedades neurodegenerativas es profunda y compleja. Los trastornos del sueño no son solo síntomas molestos, sino posibles señales de advertencia y, quizás, incluso contribuyentes activos al daño cerebral. La investigación en esta área está abriendo nuevas vías para la detección temprana y el desarrollo de intervenciones terapéuticas. Optimizar la salud del sueño y mantener ritmos circadianos saludables podría convertirse en una estrategia importante en la prevención y el manejo de estas devastadoras enfermedades. Se necesitan más estudios longitudinales y mecanicistas para desentrañar completamente esta intrincada red de interacciones y aprovechar este conocimiento para mejorar la vida de millones de personas afectadas por la neurodegeneración.
Si quieres conocer otros artículos parecidos a Ritmos Nocturnos Rotos: Sueño y Neurodegeneración puedes visitar la categoría Neurociencia.