La rotación axial de la Tierra cada 24 horas ha obligado a la mayoría de los organismos a evolucionar y adaptarse a un ciclo recurrente y dramático de día y noche. Los sistemas endógenos de cronometraje circadiano son la solución evolutiva a este desafío; estos sistemas permiten a los seres vivos reconocer la hora ambiental local y medir el paso del tiempo. El resultado es la capacidad de anticipar eventos diarios periódicos, orquestar programas temporales internos de actividades conductuales y funciones metabólicas (y otras fisiológicas), y establecer de manera flexible el orden y la programación de dichas actividades y funciones para (presumiblemente) optimizar la aptitud en el mundo natural.

- ¿Qué son los Ritmos Circadianos?
- El Lenguaje de los Relojes Biológicos
- La Red Interna del Tiempo
- El Núcleo Supraquiasmático: El Maestro Orquestador
- La Regulación del Sueño y la Vigilia
- Regulación Circadiana y Homeostática del Momento y Contenido del Sueño
- Cómo Separar las Influencias Circadianas y Homeostáticas
- Marcadores de los Ritmos Circadianos Humanos
- Interacción Circadiana y Homeostática en el Sueño
- Comportamientos que Afectan tu Reloj Interno
- Trastornos del Ritmo Circadiano
- Preguntas Frecuentes sobre los Ritmos Circadianos
- Conclusión
¿Qué son los Ritmos Circadianos?
Los ritmos circadianos son fenómenos biológicos que exhiben una oscilación inherente de aproximadamente 24 horas. Son innatos, persistiendo incluso en condiciones ambientales constantes (como la oscuridad perpetua, donde 'corren libremente') y a lo largo de generaciones. Son notablemente precisos y robustos, manteniendo su regularidad incluso frente a cambios de temperatura. Esta capacidad de medir y anticipar el tiempo es vital para ajustar la duración y el momento de los períodos de descanso y actividad, la alimentación y otras funciones a un nicho ecológico específico. Además, este sistema es fundamental para la adaptación exitosa a las estaciones, permitiendo el seguimiento del cambio en la duración del día para activar estrategias invernales de conservación de energía, modificar la coloración para evadir depredadores, sincronizar eventos reproductivos o emprender migraciones de miles de kilómetros utilizando el sol como brújula compensada en el tiempo. El reloj circadiano es, de hecho, un reloj para todas las estaciones.
El Lenguaje de los Relojes Biológicos
Como todos los fenómenos rítmicos, las propiedades de los ritmos circadianos pueden describirse en términos matemáticos:
- Período (τ): La duración de un ciclo completo del ritmo. En condiciones constantes, el período endógeno suele ser cercano a 24 horas, pero rara vez exactamente 24 horas.
- Fase (φ): Un punto de referencia definido y estable dentro del ciclo del ritmo (por ejemplo, el momento de la temperatura corporal mínima o el inicio de la actividad).
- Amplitud: La magnitud de la variación dentro de un ciclo del ritmo (por ejemplo, la diferencia entre el valor máximo y mínimo).
La ritmicidad circadiana es la manifestación observable de un marcapasos interno que funciona como un 'reloj' mediante el reajuste diario de su oscilación de aproximadamente 24 horas por señales ambientales de 24 horas. Este proceso se conoce como arrastre (o 'entrainment'). El arrastre permite que el organismo adopte una relación de fase estable con el entorno. De la multitud de señales de arrastre posibles, conocidas como 'zeitgebers' (término alemán para 'dadores de tiempo'), la luz es la más potente y la mejor estudiada.
Las curvas de respuesta de fase fótica cuantifican rigurosamente las respuestas de reajuste de los ritmos a pulsos de luz presentados a lo largo del ciclo circadiano. Estas curvas revelan cómo la interacción de una oscilación endógena con un ritmo de respuesta a la luz puede conducir a un arrastre preciso y exacto al ciclo natural de luz:oscuridad (día:noche) y desplazarlo a una nueva fase (por ejemplo, después de viajar a través de zonas horarias). Para el arrastre, el reloj se reajusta para que su período intrínseco coincida con las 24 horas; la luz administrada justo antes del amanecer avanzará su ritmo, mientras que la exposición a un estímulo lumínico idéntico (en duración, longitud de onda e intensidad) después del anochecer retrasará su ritmo.
Es importante destacar que un estímulo también puede afectar la expresión de un ritmo sin arrastrar su reloj subyacente; dicho mecanismo se ha denominado 'enmascaramiento', porque evita o actúa aguas abajo del reloj y, por lo tanto, 'enmascara' el verdadero estado del reloj. Por ejemplo, estudios sobre el ritmo de la temperatura corporal en humanos (que está significativamente influenciado por el reloj circadiano) han revelado que factores enmascaradores como la luz nocturna, los niveles de actividad, los cambios posturales, las horas de las comidas y el sueño pueden alterar significativamente su valor. Por lo tanto, determinar el ritmo circadiano endógeno de la temperatura corporal central requiere condiciones especializadas en las que estos factores enmascaradores se minimicen o se distribuyan uniformemente durante 24 horas.
Aunque históricamente la búsqueda del reloj se centró en su ritmicidad autosostenida, es la fase de arrastre (por ejemplo, el momento del inicio del sueño, o la temperatura mínima, o el pico de actividad locomotora en relación con el ciclo luz:oscuridad) lo que importa para la supervivencia en la naturaleza. El período de libre curso del reloj y la fase de arrastre están sistemáticamente relacionados entre sí, de modo que los relojes más rápidos (período más corto) tienden a conducir a una fase de arrastre más temprana; pero la fase de arrastre también se ve afectada por otros factores, incluida la intensidad de la luz y la exposición previa a diferentes duraciones del día.
La fase de arrastre a veces se denomina 'cronotipo', o el fenotipo temporal de un individuo o una población (como en las 'alondras' matutinas y los 'búhos' nocturnos), y ha proporcionado una ventana para comprender cómo los determinantes genéticos y las limitaciones ecológicas (incluidas las impuestas por nuestra propia vida urbana y las costumbres sociales) dan forma a los comportamientos rítmicos.
La Red Interna del Tiempo
Aunque los ritmos diarios –la apertura y el cierre de las hojas al unísono con la alternancia del día y la noche, por ejemplo– se conocen desde la antigüedad, nuestra comprensión mecanicista del cronometraje diario y anual ha florecido en los últimos 50 años, abarcando ahora detalles a nivel molecular, celular, tisular, orgánico e incluso social. El mecanismo oscilatorio básico es intracelular, centrado en un conjunto de 'genes reloj' que funcionan dentro de bucles de retroalimentación autorregulatoria negativa, reprimiendo rítmicamente la transcripción de sus propios ARNm. Los mecanismos reguladores postranscripcionales y postraduccionales también contribuyen claramente a las propiedades fundamentales del ritmo.
Es notable que los factores de transcripción 'reloj' no operan únicamente dentro de los bucles de retroalimentación del reloj; regulan la transcripción de genes controlados por el reloj aguas abajo en una amplia gama de vías metabólicas y de otro tipo de la célula. Este vínculo comienza a sugerir cómo el movimiento de un reloj molecular puede traducirse en un programa de 24 horas de eventos bioquímicos. La identificación de 'genes reloj' permitió la construcción de ratones transgénicos portadores de reporteros bioluminiscentes, contribuyendo al descubrimiento de que las células, los tejidos y los órganos de todo el cerebro y el cuerpo expresan osciladores circadianos.
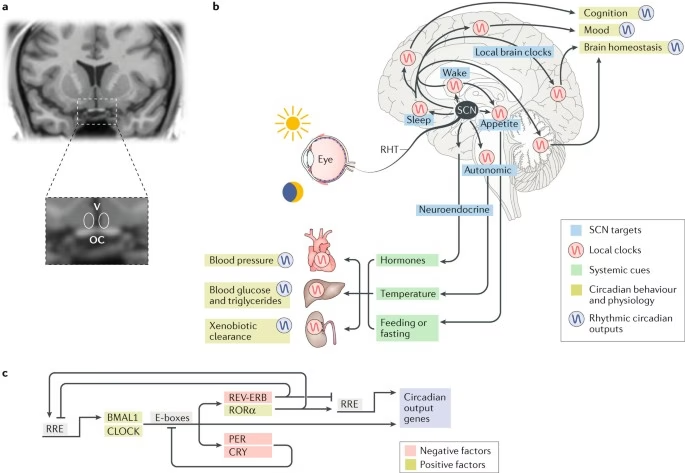
En mamíferos, el núcleo supraquiasmático (NSQ) del hipotálamo anterior (discutido a continuación) orquesta esta red de tiempo interno, en la que la multiplicidad de relojes 'periféricos' exhibe relaciones de fase definidas pero permutables entre sí y el ciclo ambiental luz:oscuridad. Esta coordinación está mediada por la interacción de una serie de factores de acoplamiento que transmiten las señales de salida del NSQ a los relojes subsidiarios –incluidos los ritmos de comportamiento (por ejemplo, descanso y actividad, alimentación y ayuno), temperatura corporal, niveles hormonales (por ejemplo, cortisol, melatonina) y actividad neural– en diversas combinaciones y fuerzas. Este sistema puede garantizar la homeostasis a lo largo del tiempo; como solo un ejemplo, la correcta sincronización del reloj hepático de la glucogenólisis compensatoria y la exportación de glucosa permite el mantenimiento de los niveles de glucosa plasmática durante el ayuno nocturno.
Al ajustar las fuerzas de acoplamiento y las velocidades de los osciladores, la red debería ser capaz de realinear adaptativamente la fase relativa de sus componentes bajo condiciones internas y externas cambiantes. Tales circunstancias a corto plazo podrían incluir la disponibilidad de alimentos en un momento inesperado, así como interacciones sociales. Por otro lado, la desalineación patológica –entre el entorno y el comportamiento, o entre el comportamiento y el NSQ, o entre el NSQ y los relojes periféricos, o entre los relojes periféricos– podría ser tanto una consecuencia como una causa de al menos algunos de los síntomas del envejecimiento y la enfermedad.

El Núcleo Supraquiasmático: El Maestro Orquestador
El NSQ es un núcleo hipotalámico bilateralmente emparejado que se extiende a horcajadas sobre la línea media, bordeando el tercer ventrículo por encima del quiasma óptico. Aunque está presente en diversas especies, se ha estudiado más intensamente en roedores. Sus actividades metabólicas y de disparo neuronal exhiben ritmos circadianos in vivo e in vitro; in vivo, existe una estrecha congruencia entre el ritmo de la actividad eléctrica y el perfil temporal del descanso y la actividad conductual, con efectos de retroalimentación de la locomoción y el sueño que dan forma a la onda de la tasa de disparo del NSQ.
Los ritmos circadianos conductuales, fisiológicos y hormonales dependen de la integridad del NSQ; la ablación del núcleo resulta en arritmicidad circadiana sin interrumpir los mecanismos homeostáticos, mientras que los injertos neuronales de tejido NSQ fetal restablecen la ritmicidad conductual en receptores arrítmicos con lesiones en el NSQ. Los ritmos restaurados por los trasplantes exhiben propiedades características de los marcapasos circadianos de los donantes en lugar de los de los huéspedes.
El arrastre fótico de la ritmicidad del NSQ se basa en una entrada retiniana monosináptica que codifica principalmente la luminancia, involucra la señalización por glutamato y péptido activador de la adenilato ciclasa pituitaria (PACAP), y refleja la actividad de una clase de células ganglionares retinianas intrínsecamente fotorreceptoras (ipRGCs) que expresan melanopsina; otras ipRGCs parecen servir para efectos moduladores de la luz en aspectos del sueño y el estado de ánimo.
Las salidas neuronales del NSQ son en su mayoría intrahipotalámicas, pero con conexiones cercanas a objetivos clave. A través de la zona subparaventricular ventral, estas incluyen vías polisínapticas a grupos celulares activos durante el sueño y la vigilia, lo que sugiere una influencia circadiana en ambos estados conductuales que depende del tiempo. Otra salida importante es a través del sistema simpático y su inervación de la glándula pineal, que impulsa la síntesis y secreción nocturna de melatonina. Tanto las especies diurnas como las nocturnas muestran altos niveles de melatonina durante la noche (fase oscura), con su duración inversamente relacionada con la duración del día (fase clara).
El reloj circadiano en el NSQ es en sí mismo una red compleja acoplada de osciladores neuronales (y gliales) heterogéneos. Se han definido 'módulos' anatómicos por neurotransmisores y otros biomarcadores, con consecuencias funcionales tras su manipulación genética específica: una región receptora de retina (denominada 'núcleo') que incluye neuronas que expresan polipéptido intestinal vasoactivo (VIP) y péptido liberador de gastrina; una 'corteza' neuronal de vasopresina arginina; y otros grupos celulares identificados que se superponen a estas subdivisiones. De alguna manera, estas unidades anatómicas están acopladas dinámicamente para producir propiedades emergentes del reloj del NSQ que son críticas para su función. Los mecanismos a nivel de circuito permiten la precisión del reloj (generación de un período de conjunto estable a partir de oscilaciones celulares 'desordenadas'), la robustez (persistencia frente a perturbaciones genéticas) y la plasticidad (dispersión de fase celular en respuesta a la duración cambiante del día).
La Regulación del Sueño y la Vigilia
El resultado circadiano más obvio es la sincronización del sueño y la vigilia. El sueño es un comportamiento complejo, con múltiples sitios y funciones. Exteriormente, implica cambios en la conciencia, la capacidad de respuesta y la postura. Dentro del organismo, provoca cambios en todos los sistemas fisiológicos. A diferencia del coma y la anestesia, el sueño es único en su capacidad para cambiar rápida y reversiblemente a un estado de vigilia completamente funcional sin manipulación farmacológica externa.
El sueño es necesario para la fisiología normal; la muerte ocurre si hay privación de sueño a largo plazo. Los múltiples cambios que ocurren durante el sueño son importantes para todo el cuerpo, no solo para el cerebro. Sorprendentemente, 'la' función del sueño es desconocida. Como dijo el Dr. Alan Rechtschaffen: 'Si el sueño no cumple una función absolutamente vital, es el mayor error que la evolución haya cometido jamás'. Durante el tiempo que los animales duermen, no se están reproduciendo, alimentando o defendiendo, tres comportamientos importantes para la supervivencia de la especie. Por lo tanto, el hecho de que el sueño o un comportamiento similar al sueño haya persistido en todas las especies animales sugiere que es necesario para el funcionamiento fisiológico normal.
Probablemente hay múltiples funciones 'de' –o, más propiamente, 'que ocurren durante'– el sueño, lo que sugiere que el sueño es la plataforma durante la cual ocurren múltiples procesos fisiológicos. El sueño no solo es necesario para sentirse 'descansado'; durante el sueño se realiza trabajo metabólico, inmunológico, de aprendizaje y otros procesos fisiológicos. Se esperaría que cada uno de estos procesos fisiológicos tuviera su propio curso temporal de acumulación y decaimiento, por lo que 'suficiente' sueño para una función puede ser diferente que para otra. Por lo tanto, 'completar' estas funciones se esperaría que fuera parte de la regulación del momento o la duración del sueño.
Incluso el sueño no es uniforme; se compone de sueño no REM (movimientos oculares rápidos) y sueño REM, que están regulados de manera diferente. Se necesitan más estudios para determinar el curso temporal de acumulación y decaimiento de cada uno de estos procesos, ya que también se esperaría que el momento y la duración del sueño estuvieran regulados para aumentar las posibilidades de supervivencia.
Regulación Circadiana y Homeostática del Momento y Contenido del Sueño
El Modelo de Dos Procesos es el marco dominante para comprender el momento y el contenido del comportamiento del sueño a nivel del organismo completo y áreas cerebrales específicas. Los dos procesos son la ritmicidad circadiana (Proceso C) y la homeostasis del sueño (Proceso S).
- Proceso S (Homeostasis del Sueño): Aumenta durante la vigilia y disminuye durante el sueño. Marcadores aceptados incluyen el Sueño de Onda Lenta (SWS) o la Actividad de Onda Lenta (SWA, ~0.5-4.5 Hz) durante el sueño, y ondas de ~12.25-25.0 Hz durante la vigilia en el EEG. El agente bioquímico putativo es la adenosina.
- Proceso C (Ritmo Circadiano): Regula la propensión al sueño y la vigilia a lo largo del ciclo de 24 horas, independientemente del tiempo que se haya estado despierto o dormido.
Los niveles de los marcadores del Proceso S aumentan con la duración de la vigilia y disminuyen durante el sueño. Consistente con esto, la cafeína, un antagonista del receptor de adenosina, disminuye la 'somnolencia'. La acumulación y el decaimiento del Proceso S se modelan matemáticamente como exponenciales saturadas, consistentes con datos que indican que el sueño perdido no se recupera minuto a minuto y, por lo tanto, debe estar involucrado un factor de intensidad (por ejemplo, aumento de SWA).

Para un curso temporal más largo de homeostasis del sueño, como se ve con la restricción crónica del sueño (múltiples noches con sueño insuficiente), SWS o SWA no son marcadores apropiados y el curso temporal de acumulación y recuperación es diferente que para la privación de sueño (un episodio continuo de vigilia). Un cambio bioquímico hipotético es en las concentraciones de receptores de adenosina.
Cómo Separar las Influencias Circadianas y Homeostáticas
Una dificultad para determinar el efecto relativo de la ritmicidad circadiana y los factores homeostáticos del sueño es que el momento circadiano (fase) y la acumulación y decaimiento homeostático del sueño covarían: en un horario de 24 horas con sueño nocturno y vigilia diurna, tanto la fase circadiana como la duración del tiempo despierto (durante el cual aumenta la homeostasis del sueño) o dormido (durante el cual disminuye la homeostasis del sueño) avanzan a la misma velocidad.
Para abordar esto, se han desarrollado varios protocolos especializados:
- Rutina Constante: Los sujetos permanecen despiertos durante 40 horas o más en condiciones de postura constante y luz tenue, con comidas pequeñas y frecuentes. Permite estudiar la vigilia en todas las fases circadianas y minimizar el enmascaramiento, pero induce privación de sueño.
- Desincronización Forzada: Los sujetos viven en 'días' de duración no estándar (por ejemplo, 28 horas o 42.85 horas). El marcapasos circadiano (~24.2h) no puede arrastrarse a este ciclo, lo que lleva a la desincronización entre los procesos circadianos y homeostáticos. Crea combinaciones de tiempo despierto/dormido y fase circadiana que no ocurren en un horario de 24 horas, permitiendo separar sus efectos.
- Desincronización Espontánea: Ocurre cuando los individuos pueden autoseleccionar sus horarios de sueño/vigilia y luz/oscuridad. A menudo resulta en un período observado más largo que el endógeno (~24.2h), quizás debido a la exposición a la luz que favorece los retrasos. Aunque no permite estudiar todas las combinaciones, ha proporcionado información útil.
Marcadores de los Ritmos Circadianos Humanos
Los ritmos circadianos generados por el NSQ influyen fuertemente en el momento del inicio y final del sueño, y en la sincronización del sueño REM dentro de un episodio de sueño. La estrecha regulación del NSQ sobre la ritmicidad de la melatonina la convierte en un marcador valioso del momento circadiano si se recoge bajo condiciones de luz tenue, ya que la exposición ocular a la luz suprime la melatonina.
Otro marcador del momento y la amplitud circadianos es la temperatura corporal central (TCC). Sin embargo, dados los efectos enmascaradores dependientes de la fase circadiana del sueño/vigilia y la actividad sobre la TCC, no puede utilizarse como marcador de fase y amplitud circadianas excepto en condiciones de hospitalización altamente controladas. Los marcadores de melatonina (generalmente el inicio de la melatonina en luz tenue, DLMO) y TCC (generalmente el mínimo de la curva sinusoidal ajustada) están estrechamente ligados tanto en fase (es decir, el DLMO ocurre ~6 horas antes del mínimo de TCC) como en amplitud.
Paradójicamente, aunque los niveles de melatonina son altos cuando los individuos suelen estar cansados, no es eficaz como hipnótico cuando se toma para el insomnio y/o a la hora habitual de dormir de un individuo. Por otro lado, la melatonina o sus agonistas pueden cambiar la fase del marcapasos circadiano de personas videntes y ciegas y, a través de ese mecanismo, afectar el sueño.
Interacción Circadiana y Homeostática en el Sueño
En humanos, el impulso circadiano para el sueño es más fuerte cerca del final del episodio de sueño habitual, quizás para consolidar el sueño a medida que el impulso homeostático disminuye durante el episodio de sueño. Mientras tanto, el impulso circadiano para la vigilia es más fuerte unas horas antes de la vigilia habitual durante la 'zona de mantenimiento de la vigilia', quizás para consolidar la vigilia a medida que el impulso homeostático del sueño se acumula durante un episodio de vigilia de ~16 horas.
Es más probable que el sueño REM ocurra hacia el final del episodio de sueño habitual, tanto porque ese es el momento en que el impulso circadiano promueve el sueño REM como porque la 'competencia' sueño NREM-REM a lo largo de la noche ha disminuido la presión del sueño NREM a medida que la homeostasis del sueño disminuye. El momento y el contenido del sueño, incluida la latencia del sueño y la vigilia dentro de un episodio de sueño, están regulados por una interacción no lineal entre estos procesos circadianos y homeostáticos del sueño: la magnitud de la influencia circadiana depende de cuánto tiempo un individuo ha estado despierto o dormido.
Cuando una persona acaba de despertar, hay poca variación circadiana en la latencia del sueño; de manera similar, cuando una persona acaba de dormirse, hay poca variación circadiana en la vigilia dentro de un episodio de sueño. Sin embargo, si la persona ha estado despierta durante mucho tiempo, la latencia del sueño depende de la fase circadiana (gran amplitud de influencia circadiana); y si la persona ha estado dormida durante mucho tiempo, la cantidad de vigilia dentro del episodio de sueño depende de la fase circadiana. Por lo tanto, cuando la homeostasis del sueño y la fase circadiana están alineadas, hay una latencia del sueño relativamente corta y un sueño consolidado sin vigilia significativa dentro de los episodios de sueño. Sin embargo, los dos están desalineados en el desfase horario ('jet lag') y el trabajo por turnos; durante estas condiciones, el sistema circadiano promueve el sueño cuando el individuo desea estar despierto y promueve la vigilia cuando el individuo desea estar dormido.
La combinación no lineal de la homeostasis del sueño y la fase circadiana también afecta algunas frecuencias del EEG y la actividad cortical y subcortical en el cerebro medida por fMRI.
Comportamientos que Afectan tu Reloj Interno
Existen efectos directos e indirectos de comportamientos que pueden afectar tanto la ritmicidad circadiana como la homeostasis del sueño. La luz durante los tiempos oscuros normales puede inducir el sueño en roedores, y la oscuridad durante los tiempos claros normales puede inducir la vigilia. Además, como se describió anteriormente, la sincronización autoseleccionada de luz:oscuridad puede afectar el estado de alerta y los ritmos circadianos, lo que a su vez afecta la sincronización del sueño (que ocurre en la oscuridad).
Es notable que la sincronización autoseleccionada de luz:oscuridad afecta de manera diferente a los cronotipos 'alondra' tempranos frente a los 'búho' tardíos y su fase circadiana. Cuando las alondras y los búhos pueden elegir sus propios horarios de iluminación, la fase circadiana es más tardía en los búhos que en las alondras; pero cuando todos están expuestos al mismo horario de luz:oscuridad, la fase circadiana es aproximadamente la misma en todos.
La cafeína puede afectar directamente el sistema circadiano, además de aumentar el estado de alerta, lo que luego incluye un aumento de la exposición a la luz que puede afectar directamente el reloj circadiano. Los horarios autoseleccionados de luz:oscuridad pueden estar involucrados en algunos trastornos del sueño del ritmo circadiano.
Trastornos del Ritmo Circadiano
Las alteraciones en el ritmo circadiano pueden manifestarse como trastornos del sueño, a menudo pasados por alto, con efectos perjudiciales para la salud. Estos trastornos suelen implicar una desalineación entre el horario de sueño de una persona y el ciclo ambiental físico/social de 24 horas. Los más prevalentes incluyen:
| Trastorno | Descripción | Características Clave | Población Común |
|---|---|---|---|
| Síndrome de Fase de Sueño Retrasada (DSPD) | Tendencia a acostarse y levantarse significativamente más tarde que la mayoría. | 'Búhos nocturnos', dificultad para conciliar el sueño a la hora deseada, dificultad para despertar por la mañana. | Adolescentes, adultos jóvenes. |
| Síndrome de Fase de Sueño Avanzada (ASPD) | Tendencia a acostarse y levantarse significativamente más temprano que la mayoría. | 'Alondras' extremas, somnolencia vespertina temprana, despertar matutino muy temprano. | Ancianos, personas con deterioro cognitivo. |
| Trastorno del Sueño por Trabajo por Turnos (SWSD) | Insomnio y/o somnolencia excesiva debido a horarios de trabajo no convencionales (nocturnos, rotatorios). | Fatiga extrema, mayor riesgo de accidentes, deterioro cognitivo. | Trabajadores de turnos. |
| Trastorno del Ritmo Sueño-Vigilia No de 24 Horas | El período endógeno difiere significativamente de 24 horas, sin arrastre al ciclo día/noche. | El horario de sueño se retrasa progresivamente cada día. | Personas ciegas sin percepción de luz, raramente en videntes. |
| Trastorno del Ritmo Sueño-Vigilia Irregular | Ausencia de un patrón de sueño-vigilia claro y consolidado. | Múltiples siestas diurnas/nocturnas, sueño fragmentado. | Personas con daño cerebral, demencia, discapacidad intelectual. |
| Jet Lag | Desalineación temporal del reloj interno con la nueva zona horaria después de un viaje rápido a través de múltiples husos horarios. | Insomnio, fatiga, problemas digestivos, dificultad de concentración. | Viajeros transmeridianos. |
Estos trastornos a menudo se diagnostican erróneamente como insomnio o somnolencia excesiva. Las personas propensas a desarrollarlos incluyen trabajadores por turnos y personas ciegas (debido a la incapacidad de percibir la luz para el arrastre). La luz artificial de dispositivos electrónicos también puede interferir con el mantenimiento de ritmos adecuados.
La desalineación del ritmo circadiano también está vinculada a diversas condiciones crónicas, incluyendo diabetes, obesidad, depresión, trastorno bipolar y trastorno afectivo estacional. El tratamiento de estos trastornos a menudo combina enfoques farmacológicos, terapia de luz y el establecimiento de un horario de sueño-vigilia regular y estable.
Preguntas Frecuentes sobre los Ritmos Circadianos
¿Qué es un ritmo circadiano en neurociencia?
Es un ciclo endógeno de aproximadamente 24 horas que regula procesos biológicos y conductuales. En neurociencia, se centra en cómo el cerebro, particularmente el Núcleo Supraquiasmático (NSQ), genera y controla estos ritmos, y cómo influyen en la función neural y el comportamiento, especialmente el ciclo sueño-vigilia.
¿Cómo funciona el reloj circadiano principal en el cerebro?
El reloj principal se encuentra en el Núcleo Supraquiasmático (NSQ) del hipotálamo. Consiste en una red de neuronas que contienen 'genes reloj' que operan en bucles de retroalimentación molecular de ~24 horas. El NSQ recibe información lumínica directamente de la retina y utiliza esta información para sincronizar su ritmo interno con el ciclo día-noche. Luego, envía señales a otras áreas del cerebro y del cuerpo para coordinar los ritmos periféricos.
¿Qué factores externos pueden afectar mi ritmo circadiano?
El factor más influyente es la luz, especialmente su exposición en momentos inapropiados (por la noche). Otros factores incluyen el horario de las comidas, la actividad física, la temperatura, el estrés, ciertos medicamentos, los horarios de trabajo (turnos) y los viajes a través de zonas horarias (jet lag).
¿Qué sucede si mi ritmo circadiano está desalineado o interrumpido?
La desalineación puede llevar a trastornos del sueño, como dificultad para conciliar o mantener el sueño, o somnolencia excesiva. A largo plazo, las interrupciones crónicas se asocian con un mayor riesgo de problemas de salud, incluyendo trastornos metabólicos (diabetes, obesidad), cardiovasculares, inmunes y de salud mental (depresión, trastornos del estado de ánimo). También puede afectar negativamente la función cognitiva, la memoria y el rendimiento.
¿Cómo puedo mejorar o 'reajustar' mi ritmo circadiano?
Mantener un horario de sueño regular, incluso los fines de semana, es fundamental. Exponerse a la luz natural por la mañana y limitar la luz brillante (especialmente la luz azul de las pantallas) por la noche ayuda a sincronizar el reloj. La actividad física regular, evitar la cafeína y el alcohol antes de acostarse, y crear un ambiente de sueño oscuro, silencioso y fresco también son importantes. En casos de trastornos significativos, la terapia de luz y, en ocasiones, la medicación (como la melatonina bajo supervisión médica) pueden ser útiles.
Conclusión
La neurobiología circadiana y la regulación del sueño-vigilia afectan virtualmente todos los sistemas fisiológicos, incluyéndose mutuamente. Los comportamientos autoseleccionados también pueden afectar estos procesos, lo que lleva a ciclos que pueden causar (por ejemplo, jet lag, trabajo por turnos y/o otros trastornos del sueño del ritmo circadiano) o empeorar (por ejemplo, metabólicos, inmunes, cognitivos) enfermedades o trastornos. Comprender la fisiología subyacente es crucial para desarrollar y probar educación apropiada, intervenciones farmacéuticas y de otro tipo para disminuir estas consecuencias adversas. La compleja interacción entre el reloj circadiano, principalmente orquestado por el NSQ, y la presión homeostática del sueño es fundamental para la salud y el bienestar, y su desincronización es un área clave de investigación y tratamiento en la neurociencia moderna.
Si quieres conocer otros artículos parecidos a El Reloj Interno: Neurociencia Circadiana puedes visitar la categoría Neurociencia.
