El dolor es una señal vital que nos alerta sobre posibles daños o peligros. Sin embargo, para millones de personas en todo el mundo, el dolor se convierte en una experiencia persistente, durando mucho más allá del proceso de curación inicial. Este fenómeno, conocido como dolor crónico, no es simplemente una prolongación del dolor agudo. La investigación reciente en neurociencia sugiere cada vez más que el dolor crónico implica cambios profundos y duraderos en el sistema nervioso central, particularmente en el cerebro, lo que lleva a considerarlo no solo como un síntoma, sino como una compleja enfermedad en sí misma.
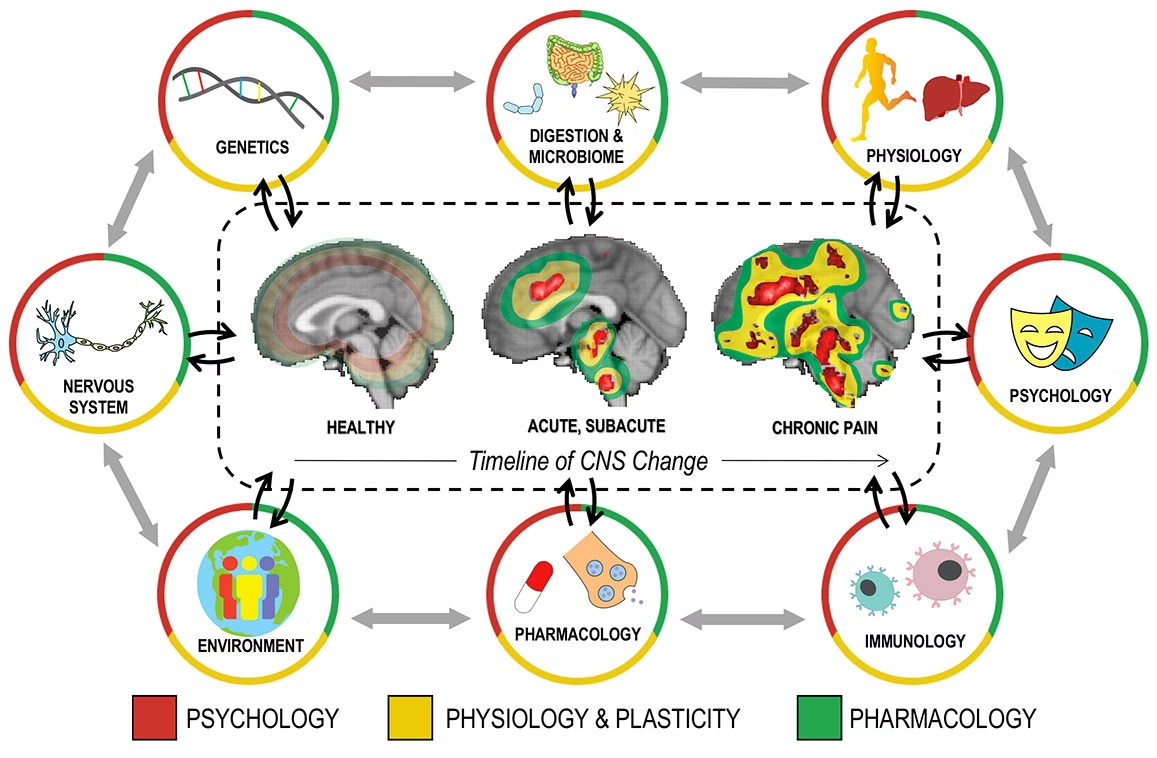
Durante mucho tiempo, el dolor crónico fue visto principalmente como una consecuencia directa de una lesión o enfermedad periférica. Si bien a menudo se origina en el sistema nervioso periférico, la evidencia actual demuestra que, con el tiempo, el dolor crónico se “centraliza”. Esto significa que el propio sistema nervioso central, incluyendo la médula espinal y el cerebro, experimenta adaptaciones maladaptativas que perpetúan la sensación de dolor, incluso si la causa original ha desaparecido o disminuido. Es un proceso de aprendizaje maladaptativo donde el cerebro, en lugar de “olvidar” el dolor una vez resuelta la lesión, se vuelve hipersensible y continúa generando señales de dolor.
- ¿Por qué el Dolor Crónico es Considerado Neurológico?
- Las Vías del Dolor y su Cronificación
- El Cerebro del Dolor Crónico: Estructura y Función Alteradas
- Dolor Crónico, Emoción y Cognición: Un Vínculo Neuronal
- El Rol de los Neurotransmisores y las Células Gliales
- Enfoques Terapéuticos Dirigidos al Cerebro
- Preguntas Frecuentes sobre el Dolor Crónico y el Cerebro
- Conclusión
¿Por qué el Dolor Crónico es Considerado Neurológico?
La naturaleza neurológica del dolor crónico radica en los cambios que induce en el sistema nervioso. A diferencia del dolor agudo, que es una respuesta de alerta útil y transitoria, el dolor crónico implica una reorganización a largo plazo de las vías neuronales. Estas alteraciones pueden afectar múltiples aspectos de la función, estructura y química cerebral.
Las enfermedades neurológicas primarias, como la esclerosis múltiple, el Parkinson, las lesiones de la médula espinal, los accidentes cerebrovasculares, o las neuropatías periféricas, a menudo tienen el dolor crónico como un componente significativo. Esto subraya la estrecha relación entre el dolor persistente y las disfunciones del sistema nervioso. Sin embargo, incluso el dolor crónico que se inicia por una lesión no neurológica puede desarrollar características neurológicas a medida que se centraliza.
La sensibilización central es un mecanismo clave en este proceso. Implica un aumento de la excitabilidad de las neuronas en la médula espinal y el cerebro, lo que hace que respondan de forma exagerada a estímulos normales o incluso en ausencia de estímulos. Las vías del dolor se vuelven hipersensibles, amplificando las señales o generando dolor espontáneamente. Este fenómeno de plasticidad neuronal, aunque a menudo asociado al aprendizaje y la memoria, puede volverse perjudicial en el contexto del dolor crónico, creando una especie de “memoria del dolor” persistente en el sistema nervioso central.
Las Vías del Dolor y su Cronificación
Para entender cómo el dolor se vuelve crónico, es crucial revisar las vías por las que viaja la señal dolorosa. El dolor comienza con la detección de estímulos nocivos (mecánicos, térmicos, químicos) por los nociceptores en los tejidos periféricos. La información viaja a través de las fibras nerviosas primarias (fibras Aδ y C) hasta el ganglio de la raíz dorsal y, desde allí, hacen sinapsis con neuronas en el asta dorsal de la médula espinal.
En el asta dorsal, se liberan diversos neurotransmisores, como el glutamato y la sustancia P, que transmiten la señal a las neuronas de segundo orden. Estas neuronas cruzan al lado opuesto de la médula y ascienden hacia el cerebro a través del tracto espinotalámico lateral, llegando al tálamo. El tálamo actúa como una estación de relevo, enviando la información a varias áreas corticales, incluida la corteza somatosensorial (que procesa la localización e intensidad del dolor) y otras regiones implicadas en los aspectos emocionales y cognitivos del dolor.
Además de la vía espinotalámica, existen otras vías ascendentes (espinorreticular y espinomesencefálica) que proyectan a áreas cerebrales involucradas en los aspectos emocionales y de modulación del dolor, como la amígdala, el hipotálamo, la sustancia gris periacueductal (PAG) y el núcleo accumbens.
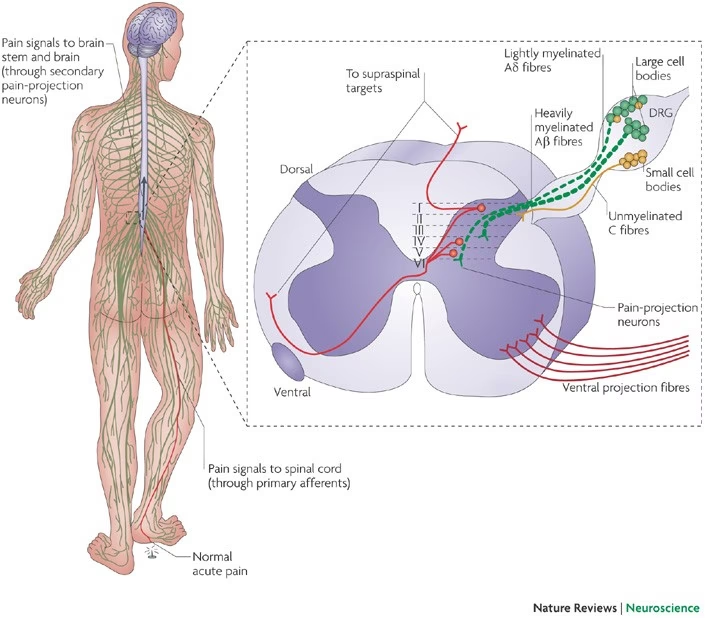
El cerebro también cuenta con sistemas descendentes de modulación del dolor, que se originan en áreas como la PAG y la médula rostral ventral (RVM). Estas vías envían señales hacia abajo a la médula espinal, donde pueden inhibir o facilitar la transmisión de señales dolorosas. En el dolor crónico, se cree que hay un desequilibrio en estos sistemas, con una disminución de la inhibición descendente o un aumento de la facilitación.
La cronificación del dolor implica cambios en múltiples niveles de estas vías, desde la sensibilización de los nociceptores periféricos (en algunos casos) y las neuronas del asta dorsal, hasta complejas reorganizaciones en las redes cerebrales.
El Cerebro del Dolor Crónico: Estructura y Función Alteradas
El dolor crónico no se limita a activar las áreas cerebrales asociadas con la percepción sensorial del dolor. Implica cambios estructurales y funcionales duraderos en una red más amplia de regiones cerebrales, particularmente aquellas que forman parte del sistema corticolímbico, involucrado en la emoción, la motivación y la cognición.
Entre las áreas clave afectadas se encuentran:
- Corteza Prefrontal (CPF): Especialmente la corteza prefrontal medial (CPFm). Esta región es crucial para la toma de decisiones, el control emocional y la regulación de la amígdala. En el dolor crónico, se han observado reducciones en el volumen de CPFm y una función alterada, lo que podría contribuir a la dificultad para extinguir la “memoria” del dolor y a problemas emocionales.
- Corteza Cingulada Anterior (CCA): Juega un papel central en los aspectos afectivos y motivacionales del dolor, así como en la atención y el control cognitivo. La CCA recibe información del tálamo y la integra con señales emocionales de otras áreas. El aumento de actividad en la CCA se asocia a menudo con las emociones negativas en el dolor crónico.
- Amígdala: Conocida por su papel en el procesamiento del miedo y las emociones, la amígdala se activa en estados de dolor y contribuye a los aspectos afectivos. Se ha observado un aumento de la excitabilidad neuronal en el núcleo central de la amígdala en modelos de dolor neuropático, lo que subraya su implicación en las respuestas emocionales maladaptativas.
- Hipocampo: Fundamental para la memoria y la navegación espacial, el hipocampo también está implicado en la regulación del eje hipotálamo-pituitaria-adrenal (HPA), relacionado con el estrés. Se han reportado reducciones en el volumen del hipocampo y alteraciones en la neurogénesis en el dolor crónico, lo que puede contribuir a déficits cognitivos y trastornos del estado de ánimo.
- Núcleo Accumbens (NAc): Parte del circuito de recompensa mesolímbico, el NAc integra información cortical y afectiva y asigna valor y motivación. Cambios en la conectividad del NAc se han asociado con la transición del dolor agudo al crónico, sugiriendo que la alteración de los circuitos de recompensa puede ser un factor en la persistencia del dolor y la anhedonia (incapacidad de sentir placer).
- Sustancia Gris Periacueductal (PAG): Aunque también implicada en la modulación descendente del dolor (supresión), la PAG integra información de centros superiores y puede contribuir a la complejidad del procesamiento del dolor a nivel cerebral.
Estos cambios en el sistema corticolímbico y sus interacciones no son solo una consecuencia pasiva del dolor; se cree que contribuyen activamente a su mantenimiento y amplificación, así como a la alta comorbilidad con trastornos emocionales y cognitivos.
Dolor Crónico, Emoción y Cognición: Un Vínculo Neuronal
La experiencia del dolor crónico rara vez se presenta de forma aislada. Con frecuencia, va acompañada de trastornos del estado de ánimo, como depresión y ansiedad, así como de déficits cognitivos (problemas de memoria, atención, velocidad de procesamiento). La neurociencia ha comenzado a desentrañar por qué esta comorbilidad es tan común.
Una razón fundamental es la superposición de las redes neuronales implicadas en el dolor y las emociones/cognición. Como se mencionó, áreas como la CCA, la amígdala, el CPF y el hipocampo son centrales tanto para el procesamiento del dolor como para la regulación emocional y las funciones cognitivas.
Además, el dolor crónico y la depresión, por ejemplo, comparten mecanismos neurobiológicos subyacentes, incluyendo cambios en la plasticidad sináptica y alteraciones en los sistemas de neurotransmisores monoaminérgicos (serotonina, dopamina, norepinefrina).

La transición del dolor agudo a crónico a menudo se asocia con un cambio en el patrón de actividad cerebral, pasando de un enfoque en las regiones sensoriales (como la corteza somatosensorial) a una mayor implicación de las regiones límbicas y prefrontales asociadas con la emoción y la motivación. Esto sugiere que, con el tiempo, el aspecto afectivo del dolor (lo que “siente” el cerebro sobre el dolor) se vuelve más prominente que el aspecto puramente sensorial (dónde y cuán intenso es).
Esta interconexión explica por qué los enfoques terapéuticos que abordan los aspectos psicológicos y conductuales, como la terapia cognitivo-conductual (TCC), son a menudo efectivos en el manejo del dolor crónico, no porque el dolor sea “imaginario”, sino porque abordan las alteraciones cerebrales que contribuyen a la experiencia persistente del dolor y sus consecuencias emocionales.
El Rol de los Neurotransmisores y las Células Gliales
La compleja neuroquímica del cerebro juega un papel fundamental en la cronificación del dolor. Una amplia gama de neurotransmisores y otras moléculas de señalización están implicadas:
- Glutamato: Es el principal neurotransmisor excitador en el SNC y un actor clave en la sensibilización central y la plasticidad sináptica. La activación de receptores de glutamato, como los NMDA y AMPA, es crucial para los cambios a largo plazo que subyacen al dolor crónico.
- GABA (Ácido Gamma-Aminobutírico): Es el principal neurotransmisor inhibidor. En condiciones de dolor neuropático e inflamatorio crónico, a menudo hay una disminución del control inhibitorio GABAérgico, lo que contribuye al aumento de la excitabilidad neuronal.
- Neuropéptidos: Una familia diversa de moléculas de señalización (como la sustancia P, CGRP, neuropéptido Y) distribuidas en las vías del dolor, que modulan la transmisión y percepción del dolor, a menudo interactuando con las células gliales.
- Factores Neurotróficos: Moléculas como el Factor de Crecimiento Nervioso (NGF) y la Interleucina-6 (IL-6) pueden promover el crecimiento de fibras nociceptivas y contribuir a la sensibilización central y periférica.
- Óxido Nítrico (NO): Un gas soluble que actúa como neuromodulador. La enzima nNOS, que produce NO, a menudo se regula al alza en condiciones de dolor crónico, implicando al NO en la persistencia del dolor.
- Péptidos Opioides Endógenos: Moléculas como las encefalinas y dinorfinas, que actúan sobre los receptores opioides, son parte del sistema analgésico endógeno. Alteraciones en este sistema pueden influir en la respuesta al dolor.
- Endocannabinoides: Moléculas producidas por el cuerpo que actúan sobre los receptores cannabinoides (CB1, CB2), modulando la transmisión del dolor y la neuroinflamación. Son un área de interés para nuevas terapias.
- Leptina y Orexina: Péptidos que, además de sus roles conocidos (metabolismo, ciclo sueño-vigilia), también están implicados en la modulación del dolor.
- Melatonina: Conocida por regular los ritmos circadianos, también tiene efectos analgésicos y puede ser útil en condiciones de dolor crónico asociadas a trastornos del sueño.
Además de las neuronas, las células gliales (microglía, astrocitos) desempeñan un papel crítico. Consideradas tradicionalmente solo como células de soporte, ahora se sabe que interactúan activamente con las neuronas y liberan sustancias (citoquinas inflamatorias, quimioquinas, neurotransmisores) que pueden amplificar o mantener la señal del dolor, contribuyendo a la neuroinflamación y la sensibilización.
Enfoques Terapéuticos Dirigidos al Cerebro
Dado que el dolor crónico implica cambios en el cerebro, los enfoques terapéuticos más prometedores son aquellos que reconocen y abordan esta complejidad neurológica. Si bien los analgésicos tradicionales (como los opioides o los AINEs) pueden ser útiles inicialmente o para ciertos tipos de dolor, a menudo son menos efectivos o problemáticos para el dolor crónico generalizado, en parte porque no abordan adecuadamente los mecanismos de centralización y las alteraciones cerebrales.
Las terapias farmacológicas que modulan los neurotransmisores implicados en la sensibilización central y los aspectos emocionales del dolor, como algunos antidepresivos (inhibidores de la recaptación de serotonina y norepinefrina) o los fármacos que actúan sobre los canales de calcio (gabapentina, pregabalina), son ejemplos de tratamientos dirigidos a nivel del SNC.
Más allá de la farmacología, las terapias que apuntan a la plasticidad cerebral maladaptativa están ganando importancia. Esto incluye:
- Terapias Psicológicas: Como la TCC, que ayuda a los pacientes a cambiar la forma en que piensan y responden al dolor, influyendo indirectamente en las redes cerebrales asociadas.
- Técnicas de Reentrenamiento Cerebral: Como la terapia de imaginería motora graduada o el entrenamiento con espejo, utilizadas en síndromes como el dolor regional complejo, que buscan corregir las representaciones cerebrales distorsionadas del cuerpo.
- Estimulación Cerebral No Invasiva: Como la estimulación magnética transcraneal repetitiva (EMTr), que puede modular directamente la actividad en áreas cerebrales implicadas en el procesamiento y modulación del dolor (como la corteza motora o la PAG).
Además, enfoques integradores como el ejercicio, el yoga y la nutrición adecuada pueden influir en la neuroquímica y la función cerebral, ofreciendo beneficios analgésicos.
A pesar de estos avances, el tratamiento del dolor crónico sigue siendo un desafío. La falta de biomarcadores objetivos y la complejidad individual de cada caso dificultan la identificación de los mecanismos específicos en cada paciente. Esto subraya la necesidad crítica de una mayor investigación y una formación más especializada para los profesionales de la salud, particularmente los neurólogos, en el manejo del dolor crónico.

| Aspecto | Dolor Agudo | Dolor Crónico |
|---|---|---|
| Duración | Corto (horas a semanas) | Largo (meses a años) |
| Función | Señal de alarma protectora | Enfermedad en sí misma, incapacitante |
| Mecanismo Principal | Activación de nociceptores periféricos | Sensibilización central, cambios en redes cerebrales |
| Áreas Cerebrales Clave Iniciales | Corteza somatosensorial, tálamo (aspecto sensorial) | Sistema corticolímbico (aspectos emocionales, cognitivos, motivacionales) |
| Plasticidad Neuronal | Adaptaciones transitorias | Reorganización estructural y funcional duradera (plasticidad maladaptativa) |
| Relación con Lesión Original | Directamente relacionado | Puede persistir independientemente de la lesión inicial |
| Comorbilidades Comunes | Bajas | Altas (depresión, ansiedad, trastornos del sueño, déficits cognitivos) |
Preguntas Frecuentes sobre el Dolor Crónico y el Cerebro
¿El dolor crónico “está todo en mi cabeza”?
No en el sentido de que sea imaginario. Aunque el dolor crónico implica cambios significativos en el cerebro, esto no significa que el paciente lo esté inventando. Significa que las vías y centros de procesamiento del dolor en el cerebro han cambiado de tal manera que generan o mantienen la sensación de dolor de forma persistente, incluso sin una causa periférica continua. Es una enfermedad real con bases neurobiológicas.
¿Pueden los cambios cerebrales causados por el dolor crónico ser reversibles?
La plasticidad cerebral es bidireccional. Así como el cerebro puede adaptarse para mantener el dolor, también tiene la capacidad de cambiar en respuesta a terapias dirigidas. Las terapias que abordan la sensibilización central, modifican la actividad de redes neuronales específicas o reentrenan las respuestas cerebrales (como la TCC o la EMTr) buscan precisamente inducir una plasticidad adaptativa que revierta o atenúe los cambios maladaptativos.
¿Qué áreas del cerebro cambian en el dolor crónico?
Se han observado cambios estructurales y funcionales en múltiples áreas, especialmente las del sistema corticolímbico: corteza prefrontal (medial), corteza cingulada anterior, amígdala, hipocampo y núcleo accumbens. También hay cambios en el asta dorsal de la médula espinal y posiblemente en la PAG.
Esto se debe en parte a que las mismas redes cerebrales y sistemas de neurotransmisores están involucrados tanto en el procesamiento del dolor como en la regulación del estado de ánimo y la emoción. El dolor crónico altera estas redes compartidas, haciendo que los individuos sean más vulnerables a desarrollar trastornos afectivos.
¿Necesito ver a un neurólogo si tengo dolor crónico?
Si bien muchos tipos de dolor crónico son manejados por diferentes especialistas, dado que el dolor crónico implica cada vez más mecanismos a nivel del sistema nervioso central, un neurólogo con experiencia en el manejo del dolor puede ser un recurso valioso, especialmente en casos complejos o cuando el dolor está asociado a una enfermedad neurológica primaria.
Conclusión
El dolor crónico es un desafío de salud global que va mucho más allá de ser un simple síntoma. La creciente evidencia científica lo posiciona como una compleja enfermedad del sistema nervioso, caracterizada por cambios profundos y duraderos en el cerebro y la médula espinal. Comprender el dolor crónico desde una perspectiva neurobiológica, reconociendo la implicación de la sensibilización central, las alteraciones en el sistema corticolímbico y el papel de neurotransmisores y células gliales, es fundamental para desarrollar estrategias de tratamiento más efectivas y dirigidas. La colaboración entre diferentes especialidades médicas y un enfoque terapéutico multimodal que aborde tanto los aspectos sensoriales como los emocionales y cognitivos son esenciales para mejorar la calidad de vida de quienes viven con esta debilitante condición.
Si quieres conocer otros artículos parecidos a Dolor Crónico: ¿Una Enfermedad Cerebral? puedes visitar la categoría Neurociencia.

