La neurociencia celular es una rama fundamental de la neurociencia que se enfoca en el estudio de las células que componen el sistema nervioso: las neuronas y las células gliales. Comprender la estructura, función y comunicación de estas unidades celulares es esencial para desentrañar los misterios del cerebro y su funcionamiento complejo. A diferencia de otros campos de la neurociencia que pueden centrarse en circuitos o sistemas completos, la neurociencia celular profundiza en los mecanismos moleculares y eléctricos que operan dentro y entre las células individuales.

- Neuronas y Células Gliales: Los Actores Principales
- La Función Neuronal: Excitabilidad y Señales Eléctricas
- El Potencial de Acción: Un Evento Eléctrico Dinámico
- Estructura y Formación de Sinapsis: Los Puntos de Conexión
- Neurotransmisores, Transportadores, Receptores y Mecanismos de Señalización
- Plasticidad Sináptica: La Base del Aprendizaje y la Memoria
- Técnicas y Áreas de Estudio en Neurociencia Celular
- Preguntas Frecuentes sobre Neurociencia Celular
Neuronas y Células Gliales: Los Actores Principales
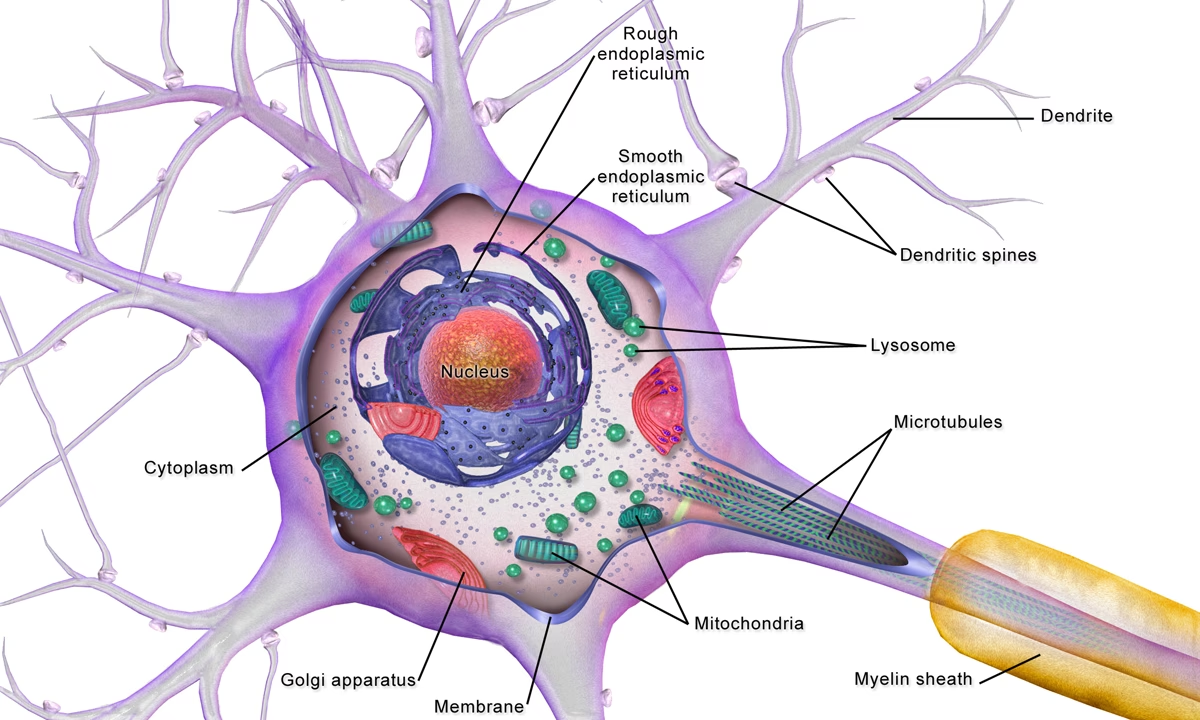
El sistema nervioso está compuesto principalmente por dos tipos de células: las neuronas y las células gliales. Las neuronas son quizás las más conocidas, especializadas en la recepción, propagación y transmisión de impulsos electroquímicos. Se estima que solo el cerebro humano contiene más de ochenta mil millones de neuronas. Es importante destacar que las neuronas presentan una enorme diversidad en cuanto a su morfología y función. No todas se ajustan al estereotipo de la neurona motora con dendritas y axones mielinizados que conducen potenciales de acción. Algunas, como las células fotorreceptoras, carecen de axones mielinizados que conduzcan potenciales de acción. Otras, como las neuronas unipolares encontradas en invertebrados, ni siquiera tienen prolongaciones distintivas como las dendritas.
La distinción funcional entre neuronas y otras células excitables, como las células cardíacas o musculares, tampoco es siempre clara o útil. La diferencia fundamental entre una neurona y una célula no neuronal es, en muchos casos, una cuestión de grado en sus propiedades de excitabilidad y comunicación. Sin embargo, su rol en la transmisión de información en redes complejas es lo que las define en el contexto del sistema nervioso.
La otra clase principal de células en el sistema nervioso son las células gliales, o glía. Durante mucho tiempo, se pensó que su función principal era simplemente el soporte y la nutrición de las neuronas. Sin embargo, la investigación reciente ha revelado que las células gliales desempeñan roles mucho más activos, incluida la modulación de las sinapsis. Por ejemplo, las células de Schwann, un tipo de glía que se encuentra en el sistema nervioso periférico, pueden modular las conexiones sinápticas entre las terminales presinápticas de las placas motoras y las fibras musculares en las uniones neuromusculares. Esta capacidad de influir en la comunicación neuronal subraya su importancia para el funcionamiento normal del sistema nervioso.
La Función Neuronal: Excitabilidad y Señales Eléctricas
Una característica distintiva de muchas neuronas es su excitabilidad. Esta propiedad les permite generar dos tipos de impulsos eléctricos o cambios en el voltaje de su membrana: los potenciales graduados y los potenciales de acción.
- Potenciales Graduados: Ocurren cuando el potencial de membrana se despolariza o hiperpolariza de manera gradual, siendo su magnitud proporcional a la intensidad del estímulo aplicado a la neurona. Estos potenciales suelen ser locales y se atenúan rápidamente con la distancia.
- Potenciales de Acción: A diferencia de los potenciales graduados, el Potencial de Acción es un impulso eléctrico de 'todo o nada'. Una vez que se alcanza un cierto umbral de excitación, se dispara un evento de despolarización rápido y estereotipado que se propaga activamente a lo largo del axón sin perder intensidad. Aunque son más lentos que la propagación pasiva de los potenciales graduados, los potenciales de acción tienen la ventaja crucial de viajar largas distancias en los axones con poca o ninguna disminución en su amplitud. Gran parte de nuestro conocimiento actual sobre los potenciales de acción proviene de los experimentos clásicos realizados por Sir Alan Lloyd Hodgkin y Sir Andrew Huxley utilizando el axón gigante del calamar.
El Potencial de Acción: Un Evento Eléctrico Dinámico
El modelo de Hodgkin-Huxley del potencial de acción en el axón gigante del calamar ha sido la base para gran parte de la comprensión actual de las bases iónicas de este fenómeno. El modelo postula que la generación de un potencial de acción está determinada principalmente por el movimiento de dos iones clave: Na+ (sodio) y K+ (potasio).
Un potencial de acción se puede dividir en varias fases secuenciales:
- Umbral: Después de varias despolarizaciones locales graduadas del potencial de membrana, se alcanza el umbral de excitación.
- Fase Ascendente (Despolarización): Al alcanzar el umbral, los canales de sodio dependientes de voltaje se activan, lo que lleva a una rápida entrada masiva de iones Na+ en la célula. A medida que los iones Na+ entran, el potencial de membrana se despolariza aún más, activando más canales de sodio dependientes de voltaje. Este proceso es un ejemplo de retroalimentación positiva.
- Fase Descendente (Repolarización): A medida que la fase ascendente alcanza su pico (el potencial de membrana se vuelve positivo), los canales de Na+ dependientes de voltaje se inactivan. Simultáneamente, los canales de potasio dependientes de voltaje se activan, lo que resulta en un movimiento neto de iones K+ hacia afuera de la célula. Esta salida de carga positiva repolariza el potencial de membrana, devolviéndolo hacia su valor de reposo.
- Fase de Hiperpolarización (Undershoot o Periodo Refractario Absoluto): La repolarización del potencial de membrana continúa, a menudo resultando en una breve fase en la que el potencial de membrana se vuelve más negativo que el potencial de reposo. Esta hiperpolarización ocurre porque los canales de potasio dependientes de voltaje se inactivan mucho más lentamente que los canales de sodio.
- Recuperación: A medida que más canales de K+ dependientes de voltaje se inactivan y las bombas iónicas restablecen los gradientes, el potencial de membrana se recupera gradualmente hasta su estado de reposo normal y estable.
Estructura y Formación de Sinapsis: Los Puntos de Conexión
Las neuronas se comunican entre sí a través de estructuras especializadas llamadas sinapsis. Las sinapsis son uniones estrechas entre dos células, donde una neurona (la neurona presináptica) transmite una señal a otra célula (la neurona o célula postsináptica). Existen dos tipos principales de sinapsis:
| Característica | Sinapsis Eléctrica | Sinapsis Química |
|---|---|---|
| Conexión | Uniones en hendidura (Gap junctions) | Hendidura sináptica |
| Mecanismo de transmisión | Flujo directo de iones a través de canales | Liberación y difusión de neurotransmisores |
| Velocidad | Muy rápida, casi instantánea | Más lenta |
| Modulación/Complejidad | Generalmente simple, excitación o inhibición directa | Altamente modulable, efectos excitadores o inhibidores complejos |
| Direccionalidad | A menudo bidireccional | Generalmente unidireccional (presináptica a postsináptica) |
Las sinapsis eléctricas se caracterizan por la formación de uniones en hendidura que permiten que los iones y otras moléculas orgánicas pequeñas pasen directamente de una célula a otra. Esto permite una transmisión de señal muy rápida y sincrónica.
Las sinapsis químicas, por otro lado, se caracterizan por la liberación de neurotransmisores desde la neurona presináptica hacia una hendidura sináptica. Estos neurotransmisores se difunden a través de la hendidura y se unen a receptores específicos en la membrana postsináptica. Aunque son más lentas que las sinapsis eléctricas, las sinapsis químicas ofrecen una mayor flexibilidad y capacidad de modulación.
Neurotransmisores, Transportadores, Receptores y Mecanismos de Señalización
Los neurotransmisores son mensajeros químicos que son sintetizados dentro de las propias neuronas. Una vez sintetizados, se empaquetan y almacenan en pequeñas sacos membranosos llamados vesículas sinápticas, que se agrupan en las terminales presinápticas (botones terminales) de la neurona.
Cuando un potencial de acción llega a la terminal presináptica, provoca un cambio en el voltaje que activa los canales de calcio dependientes de voltaje incrustados en la membrana presináptica. Esto permite la entrada de iones Ca2+ en el terminal. La entrada de Ca2+ es un paso crítico, ya que los iones Ca2+ se unen a proteínas asociadas con las vesículas sinápticas, desencadenando su movimiento hacia la membrana presináptica. Una vez allí, las vesículas se acoplan y se fusionan con la membrana presináptica en un proceso conocido como exocitosis, liberando los neurotransmisores a la hendidura sináptica.
Los neurotransmisores liberados se difunden a través de la hendidura sináptica y se unen a receptores incrustados en la membrana postsináptica de la célula receptora. Existen dos familias principales de receptores postsinápticos:
- Receptores Ionotrópicos: Son una combinación de un receptor y un canal iónico. Cuando el neurotransmisor se une al receptor, provoca un cambio conformacional que abre directamente el canal iónico. Esto permite la rápida entrada o salida de iones específicos (como Na+, K+, Cl-) a través de la membrana postsináptica, lo que resulta en un cambio rápido en el potencial de membrana. Si la entrada de iones positivos (como Na+) despolariza la membrana, se produce un Potencial Postsináptico Excitador (EPSP). Si la entrada de iones negativos (como Cl-) o la salida de iones positivos (como K+) hiperpolariza la membrana, se produce un Potencial Postsináptico Inhibidor (IPSP).
- Receptores Metabótropos: Estos receptores no son canales iónicos en sí mismos. Cuando el neurotransmisor se une, activan cascadas de segundos mensajeros dentro de la célula postsináptica. Estas cascadas pueden conducir a una variedad de efectos, incluida la apertura o cierre de canales iónicos ubicados en otras partes de la membrana postsináptica. Aunque la respuesta de los receptores metabótropos es más lenta que la de los ionotrópicos, tienen la ventaja de amplificar la señal y producir efectos más duraderos y complejos, modulando la respuesta de la célula a iones y otros metabolitos.
Existen numerosos neurotransmisores, cada uno con funciones específicas. Algunos ejemplos incluyen el ácido gamma-aminobutírico (GABA, un neurotransmisor principalmente inhibidor), el ácido glutámico (glutamato, un neurotransmisor principalmente excitador), la dopamina, la norepinefrina, la epinefrina, la serotonina, la melatonina, las endorfinas, las dinorfinas, la nociceptina y la sustancia P.
La integración de los EPSP e IPSP que llegan a la neurona postsináptica determina si se alcanza el umbral de excitación. Si la suma de los estímulos excitadores supera la suma de los estímulos inhibidores y se alcanza el umbral, la neurona postsináptica generará su propio potencial de acción, propagando así la señal.
Plasticidad Sináptica: La Base del Aprendizaje y la Memoria
Un concepto crucial en neurociencia celular es la plasticidad sináptica. Este es el proceso mediante el cual la fuerza o eficacia de las conexiones sinápticas se altera en respuesta a la actividad neuronal. Por ejemplo, cambios a largo plazo en una conexión sináptica pueden resultar en una mayor cantidad de receptores postsinápticos incrustados en la membrana postsináptica, lo que fortalece la sinapsis y hace que la célula postsináptica responda más fuertemente a la liberación de neurotransmisor.
La plasticidad sináptica es considerada uno de los mecanismos neuronales fundamentales que subyacen al aprendizaje y la memoria. La capacidad de las sinapsis para fortalecerse o debilitarse permite que los circuitos neuronales se adapten y cambien con la experiencia.
Técnicas y Áreas de Estudio en Neurociencia Celular
El estudio de las propiedades básicas, la actividad y la regulación de las corrientes de membrana, la transmisión sináptica y la Plasticidad Sináptica son campos activos de investigación en neurociencia celular. Otras áreas importantes incluyen el estudio de la neurotransmisión, la neurogénesis (la formación de nuevas neuronas), la sinaptogénesis (la formación de nuevas sinapsis) y los canales iónicos de las células.
Para investigar estos fenómenos a nivel celular, los neurocientíficos celulares emplean diversas técnicas. Una técnica común, particularmente para estudiar los potenciales eléctricos de las neuronas (como los potenciales de acción y los potenciales sinápticos), es la electrofisiología. El 'Current Clamp' (pinzamiento de corriente) es un método electrofisiológico fundamental que permite a los investigadores controlar la corriente que entra o sale de una neurona y medir los cambios de voltaje resultantes. Experimentos pioneros como los de Hodgkin y Huxley en el axón gigante del calamar sentaron las bases para el uso de técnicas electrofisiológicas en la comprensión de la excitabilidad neuronal.
Además de la electrofisiología, el estudio de la anatomía a nivel de tejido, celular y subcelular es crucial. Técnicas histológicas y microscópicas permiten visualizar la estructura de las neuronas, las células gliales y las sinapsis, proporcionando información vital sobre su organización y patologías, como se investiga en centros dedicados a la investigación de la discapacidad intelectual a nivel celular.
Preguntas Frecuentes sobre Neurociencia Celular
¿Cuál es la diferencia principal entre una neurona y una célula glial?
Las neuronas están especializadas en la transmisión rápida de señales eléctricas y químicas. Las células gliales, aunque no generan potenciales de acción de la misma manera, proporcionan soporte estructural y metabólico a las neuronas y también modulan la actividad sináptica.
¿Qué es un potencial de acción y por qué es importante?
Es un impulso eléctrico rápido de 'todo o nada' que se propaga a lo largo del axón. Es fundamental para la comunicación de señales a larga distancia dentro del sistema nervioso.
¿Cómo se comunican las neuronas entre sí?
Principalmente a través de sinapsis, que pueden ser eléctricas (flujo directo de iones) o químicas (liberación de neurotransmisores).
¿Qué son los neurotransmisores?
Mensajeros químicos liberados por las neuronas en las sinapsis químicas que se unen a receptores en la célula postsináptica para transmitir una señal.
¿Qué significa plasticidad sináptica?
Es la capacidad de las sinapsis para cambiar su fuerza o eficacia en respuesta a la actividad. Se cree que es un mecanismo clave para el aprendizaje y la memoria.
¿Qué técnicas se usan para estudiar neurociencia celular?
Basado en la información proporcionada, se mencionan la electrofisiología (incluyendo técnicas como Current Clamp y experimentos con el axón del calamar) para estudiar la actividad eléctrica, y el estudio de la anatomía a nivel de tejido, celular y subcelular.
En resumen, la neurociencia celular nos proporciona la lente para examinar los componentes básicos del sistema nervioso. Al estudiar neuronas, glía, señales eléctricas, sinapsis y los mecanismos de plasticidad, obtenemos una comprensión fundamental de cómo funciona nuestro cerebro y cómo pueden surgir disfunciones. Es un campo en constante evolución, revelando la asombrosa complejidad y dinamismo de las células que nos permiten pensar, sentir y actuar.
Si quieres conocer otros artículos parecidos a Explorando la Neurociencia Celular puedes visitar la categoría Neurociencia.