En el vasto y complejo entramado del sistema nervioso, la comunicación entre neuronas y otras células es fundamental para cada pensamiento, movimiento y sensación. Esta comunicación se logra principalmente a través de la liberación de neurotransmisores en las sinapsis. Un actor principal en este proceso, que a menudo pasa desapercibido para el observador casual, es el ion calcio. Este pequeño mensajero es crucial no solo para iniciar la liberación de estas sustancias químicas, sino también para otras formas de señalización dentro de la neurona, influyendo incluso en la plasticidad sináptica.
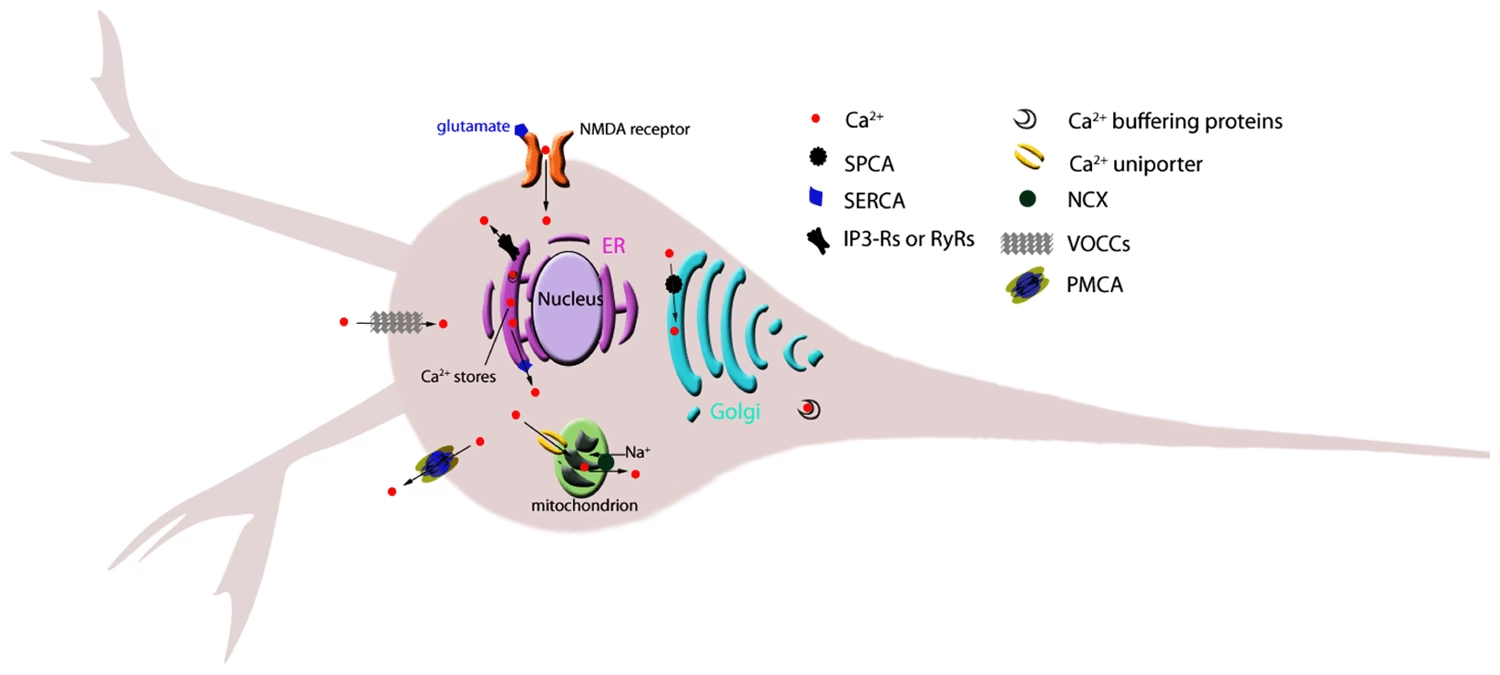
La activación de la mayoría de las sinapsis excitatorias en las neuronas centrales desencadena señales de liberación de calcio desde depósitos intracelulares. Esta liberación de calcio, evocada sinápticamente desde los depósitos, a menudo se activa por la unión del glutamato a receptores metabotrópicos y la subsiguiente activación de receptores de IP3 en espinas dendríticas y dendritas. Existe una creciente evidencia de la presencia de señales de calcio locales causadas por la liberación de calcio inducida por calcio (CICR) a través de la activación de receptores de rianodina o IP3. Trabajos recientes en ratones mutantes indican que la señalización de los depósitos determina la plasticidad sináptica dependiente de la actividad.
- El Calcio: Un Mensajero Crucial en la Neurona
- ¿Cómo Desencadena el Calcio la Liberación de Neurotransmisores en General?
- Acetilcolina: Síntesis, Empaquetamiento y Liberación Dependiente del Calcio
- Receptores de Acetilcolina y la Señalización del Calcio
- Funciones Diversas de la Acetilcolina en el Cuerpo
- Patologías Relacionadas con la Acetilcolina y el Calcio
- Preguntas Frecuentes sobre Calcio y Acetilcolina
- ¿Qué causa la liberación de calcio en las neuronas?
- ¿Puede el calcio desencadenar la liberación de neurotransmisores?
- ¿Cómo libera el calcio la acetilcolina?
- ¿Qué son las proteínas SNARE en la liberación de neurotransmisores?
- ¿Cuáles son los tipos de receptores de acetilcolina?
- ¿Qué sucede con la acetilcolina después de ser liberada?
El Calcio: Un Mensajero Crucial en la Neurona
El Calcio no es solo un componente esencial de los huesos; en el ámbito neuronal, actúa como un mensajero intracelular vital. Su concentración dentro de la neurona es típicamente muy baja en estado de reposo, lo que permite que pequeñas entradas o liberaciones generen grandes cambios relativos en su concentración local, creando señales potentes. En las sinapsis excitatorias, la llegada de una señal puede movilizar calcio tanto desde el exterior como desde reservas internas, como el retículo endoplasmático.
La movilización de calcio desde depósitos intracelulares, a menudo mediados por receptores de IP3, es un mecanismo clave para amplificar o modular las señales sinápticas. La liberación de calcio inducida por calcio (CICR), donde una pequeña entrada de calcio desencadena una liberación mayor de los depósitos, es otro mecanismo que contribuye a la complejidad de la señalización de calcio dentro de la neurona. Estos mecanismos de señalización de calcio son fundamentales para procesos como la plasticidad sináptica, la capacidad de las sinapsis para fortalecerse o debilitarse con el tiempo, lo cual es la base del aprendizaje y la memoria.
¿Cómo Desencadena el Calcio la Liberación de Neurotransmisores en General?
El proceso de liberación de neurotransmisores en el terminal presináptico es exquisitamente sensible a la presencia de calcio. Trabajos recientes han establecido que se encuentran diferentes disposiciones geométricas de canales de calcio en diferentes terminales presinápticos, lo que lleva a un amplio espectro de señales de calcio para desencadenar la liberación de neurotransmisores. Estas señales de calcio son aparentemente transducidas por sinaptotagminas, proteínas de unión a calcio que se encuentran en las vesículas sinápticas.
Nuevos resultados bioquímicos indican que todas las sinaptotagminas experimentan interacciones dependientes de calcio con lípidos de membrana y una serie de otras proteínas presinápticas. Sin embargo, aún no está claro cuál de estas interacciones es directamente responsable de la liberación de neurotransmisores desencadenada por el calcio. Lo que sí es evidente es que la llegada del calcio al terminal presináptico es el evento clave que inicia la cascada molecular que culmina con la fusión de las vesículas sinápticas con la membrana presináptica y la liberación de su contenido en la hendidura sináptica.
Acetilcolina: Síntesis, Empaquetamiento y Liberación Dependiente del Calcio
La Acetilcolina (ACh) es un neuroquímico con una amplia variedad de funciones en el cerebro y otros sistemas orgánicos. Es un neurotransmisor que actúa como un mensaje químico liberado por las neuronas, permitiéndoles comunicarse entre sí y con otras células especializadas como miocitos y células glandulares. Teniendo una estructura química derivada del ácido acético y la colina, los tejidos que utilizan o responden a este mensajero se denominan colinérgicos.
La síntesis de acetilcolina ocurre en los terminales axónicos. Se deriva de dos componentes: colina y un grupo acetilo, este último derivado del coenzima acetil-CoA. La colina está presente en alimentos y es producida por el hígado. Circulando en plasma, cruza la barrera hematoencefálica y es captada por los terminales nerviosos colinérgicos a través de canales de recaptación dependientes de sodio. El paso limitante en la producción de acetilcolina es la disponibilidad de acetato (de acetil-CoA mitocondrial) y colina (directamente del plasma y de la recaptación). La enzima que cataliza la reacción de la colina con el acetil-CoA para crear acetilcolina es la colina acetiltransferasa (CAT), producida en el soma neuronal y transportada al terminal axónico.
Una vez sintetizada, la acetilcolina es empaquetada en vesículas sinápticas. Estas vesículas se acidifican mediante una bomba dependiente de energía (H-ATPasa), creando un gradiente para que la acetilcolina entre a través del transportador vesicular de acetilcolina (VAChT), que intercambia un protón vesicular por una molécula de acetilcolina.
La liberación de acetilcolina se produce cuando un potencial de acción llega al terminal axónico. La despolarización resultante causa la apertura de canales de calcio dependientes de voltaje, permitiendo una entrada masiva de Calcio en el terminal. Esta entrada de calcio es el desencadenante directo para la fusión de las vesículas que contienen acetilcolina con la membrana presináptica y su liberación en la hendidura sináptica. Este proceso depende en gran medida del sistema de proteínas SNARE.
Las proteínas SNARE, como Sinaptobrevina (una v-SNARE en la membrana vesicular), SNAP-25 y Sintaxina-1 (t-SNAREs en la membrana presináptica), trabajan juntas con el calcio para realizar la fusión de la membrana vesicular. Sinaptogmina es otra proteína SNARE unida a la vesícula que actúa como el sensor de calcio para este sistema. Cuando la vesícula se acerca lo suficiente a la membrana presináptica, la proteína citosólica Munc18 actúa como un 'broche' activador, uniendo la Sinaptobrevina a SNAP-25 y Sintaxina-1, acercando las membranas vesicular y presináptica. El complejo proteico citosólico Complexin se inserta entonces en el complejo SNARE formado, impidiendo la fusión espontánea.

Es solo con la introducción de Calcio en la célula, después de la despolarización neuronal, que ocurre la liberación. El calcio se une a la Sinaptotagmina, permitiendo que esta molécula se una a fosfolípidos ácidos en la membrana presináptica y desplace las moléculas de Complexin. La eliminación de Complexin levanta el bloqueo de fusión, permitiendo la fusión vesicular con la membrana presináptica y la liberación de la acetilcolina.
Después de la fusión, la Ca-ATPasa (PMCA) bombea calcio fuera de la neurona y las mitocondrias neuronales captan calcio, ambos procesos dirigidos a disminuir la concentración intracelular de calcio. Con la disminución del calcio, la Sinaptotagmina se disocia del complejo SNARE y se reclutan otras proteínas SNARE para descomponer y reciclar el complejo, preparándose para la próxima ronda de fusión vesicular.
Receptores de Acetilcolina y la Señalización del Calcio
Una vez en la hendidura sináptica, la acetilcolina puede unirse a dos tipos principales de Receptores de Acetilcolina: nicotínicos y muscarínicos.
Los Receptores Nicotínicos de acetilcolina son canales iónicos activados por ligando. Están compuestos por cinco subunidades polipeptídicas que siempre tienen dos o más subunidades alfa y pueden tener subunidades beta, delta y gamma. Al unirse dos moléculas de acetilcolina al receptor nicotínico, la estructura pentamérica cambia su conformación interna, creando un poro transmembrana para el paso de iones sodio, potasio y calcio. El paso de estos iones da lugar a la despolarización de la célula postsináptica.
Los Receptores Muscarínicos de acetilcolina son receptores acoplados a proteínas G (GPCRs), compuestos por un único polipéptido con siete regiones dispuestas en alfa-hélice que atraviesan la membrana. Tienen cinco subtipos: M1, M2, M3, M4 y M5. A diferencia de los nicotínicos, estos son metabotrópicos y funcionan a través de segundos mensajeros. Los subtipos M1, M3 y M5 funcionan a través de la vía de la fosfolipasa C (PLC). Cuando el receptor es activado por acetilcolina, la subunidad alfa activada de la proteína G interactúa con la PLC, activándola. La PLC activada hidroliza el fosfatidilinositol bifosfato en dos segundos mensajeros: inositol trifosfato (IP3) y diacilglicerol (DAG). El IP3 se une a los receptores de IP3 en el retículo endoplasmático liso para liberar Calcio al citosol de la célula, aumentando así la concentración intracelular de calcio. El DAG activa la proteína quinasa C. Los subtipos M2 y M4 funcionan inhibiendo la adenilil ciclasa, reduciendo el cAMP intracelular.
| Tipo de Receptor | Mecanismo | Paso Iónico/Segundo Mensajero | Función Principal (General) | Ubicación (Ejemplos) |
|---|---|---|---|---|
| Nicotínico | Canal Iónico Activado por Ligando | Paso de Na+, K+, Ca++ | Despolarización Rápida | Unión Neuromuscular (N1), Ganglios Periféricos, SNC (N2) |
| Muscarínico (M1, M3, M5) | GPCR (Acoplado a Proteína Gq) | Vía PLC (aumento de IP3 y DAG) → Liberación de Calcio desde RE | Excitatorio (generalmente) | Corteza Cerebral (M1), Glándulas (M1, M3), Músculo Liso (M3), SNC (M5) |
| Muscarínico (M2, M4) | GPCR (Acoplado a Proteína Gi) | Inhibición de Adenilil Ciclasa (reducción de cAMP) | Inhibitorio (generalmente) | Músculo Liso (M2), Tejido Cardíaco (M2), SNC (M4) |
Funciones Diversas de la Acetilcolina en el Cuerpo
La acetilcolina interviene en numerosas funciones fisiológicas, como la regulación de las contracciones cardíacas y la presión arterial, el peristaltismo intestinal, la secreción glandular, etc. Típicamente, la acetilcolina es un mediador excitatorio, aunque puede ser inhibitorio (por ejemplo, en el corazón a través de receptores M2). El sistema de fibras nerviosas colinérgicas que liberan acetilcolina es extenso tanto en el sistema nervioso central como en el periférico. En la periferia, todas las fibras preganglionares (simpáticas y parasimpáticas), las postganglionares parasimpáticas y las fibras motoras que inervan el músculo esquelético voluntario son colinérgicas. En el SNC, el sistema colinérgico tiene extensas ramificaciones en la médula espinal, tálamo, sistema límbico y corteza. La acetilcolina asegura una neurotransmisión rápida pero generalmente fugaz debido a su pronta inactivación por la acetilcolinesterasa.
A través de los receptores muscarínicos, la acetilcolina causa vasodilatación generalizada, disminución de la frecuencia cardíaca y de la fuerza de contracción, disminución de la velocidad de conducción. En el sistema gastrointestinal, aumenta el tono, la amplitud de las contracciones y la actividad secretora. En el sistema respiratorio, causa broncoconstricción. En el sistema urinario, contrae el músculo detrusor de la vejiga. Estimula la secreción de todas las glándulas exocrinas con inervación parasimpática. En el ojo, causa miosis y acomodación. En el sistema reproductor masculino, causa erección.
A través de los receptores nicotínicos, la acetilcolina permite la contracción del músculo esquelético, la liberación de adrenalina y noradrenalina en las glándulas suprarrenales y la activación del sistema simpático en los ganglios periféricos.
Patologías Relacionadas con la Acetilcolina y el Calcio
La alteración o interferencia con la acetilcolina en el sistema nervioso puede resultar en varias patologías. La farmacología a menudo se dirige a los receptores de acetilcolina, la vía o la acetilcolinesterasa para corregir la fisiología humana durante diversas patologías.
La acetilcolina es clínicamente significativa en muchas enfermedades, las más comunes de las cuales incluyen la enfermedad de Alzheimer (EA), el síndrome miasténico de Lambert-Eaton (SMLE) y la miastenia gravis (MG).

Los pacientes con EA tienen un contenido cerebral reducido de colina acetiltransferasa, lo que lleva a una disminución en la síntesis de acetilcolina y una función colinérgica cortical deteriorada. Los inhibidores de la colinesterasa (donepezilo, rivastigmina y galantamina) aumentan la transmisión colinérgica al inhibir la colinesterasa en la hendidura sináptica y proporcionan un beneficio sintomático modesto en algunos pacientes con demencia.
La Miastenia Gravis es un trastorno autoinmune reconocido por el rápido debilitamiento de los músculos esqueléticos después de un uso repetido. La debilidad se debe a un proceso mediado por anticuerpos en el que se producen anticuerpos que tienen tropismo por los Receptores Nicotínicos de acetilcolina o sus proteínas asociadas ubicadas en la membrana postsináptica de la unión neuromuscular.
El Síndrome Miasténico de Lambert-Eaton (SMLE) es un trastorno de reducción de la liberación de ACh desde los terminales nerviosos presinápticos. Esta condición ocurre cuando hay autoinmunidad (producción de autoanticuerpos) contra los canales de calcio dependientes de voltaje que se encuentran en el terminal axónico de las neuronas presinápticas. Esto subraya la importancia crucial del influjo de Calcio presináptico para la liberación adecuada de acetilcolina.
Farmacológicamente, los inhibidores de la colinesterasa pueden ayudar a tratar la enfermedad de Alzheimer y la miastenia gravis, ya que en ambas condiciones hay una reducción severa en la cantidad de estimulación nativa del receptor de acetilcolina. La toxina botulínica funciona impidiendo la liberación de acetilcolina desde los terminales presinápticos, lo que puede ser útil para tratar la espasticidad muscular, arrugas y migrañas. El veneno de la viuda negra tiene el efecto opuesto, causando que las células liberen toda su acetilcolina, provocando una contracción muscular excesiva.
Preguntas Frecuentes sobre Calcio y Acetilcolina
¿Qué causa la liberación de calcio en las neuronas?
La activación de sinapsis excitatorias, la unión de glutamato a receptores metabotrópicos activando receptores de IP3, y la liberación de calcio inducida por calcio (CICR) a través de receptores de rianodina o IP3 desde depósitos intracelulares pueden causar liberación de calcio en las neuronas.
¿Puede el calcio desencadenar la liberación de neurotransmisores?
Sí, el calcio es el principal desencadenante de la liberación de neurotransmisores. El influjo de calcio en el terminal presináptico, mediado por canales de calcio, es transducido por proteínas de unión a calcio como las sinaptotagminas, iniciando la cascada molecular que lleva a la fusión vesicular y la liberación del neurotransmisor.
¿Cómo libera el calcio la acetilcolina?
Cuando un potencial de acción alcanza el terminal axónico, causa la apertura de canales de calcio dependientes de voltaje, permitiendo la entrada de calcio. Este calcio se une a la proteína Sinaptotagmina en las vesículas sinápticas. La unión del calcio a la Sinaptotagmina permite que esta interactúe con proteínas SNARE (Sinaptobrevina, SNAP-25, Sintaxina-1) y fosfolípidos de la membrana presináptica, superando el bloqueo de fusión impuesto por Complexin y permitiendo la fusión de la vesícula con la membrana presináptica para liberar la acetilcolina en la hendidura sináptica.
¿Qué son las proteínas SNARE en la liberación de neurotransmisores?
Las proteínas SNARE son un grupo de proteínas esenciales para la fusión de vesículas membranosas con las membranas diana. En la liberación de neurotransmisores, las v-SNAREs (como Sinaptobrevina) en la membrana vesicular interactúan con las t-SNAREs (como SNAP-25 y Sintaxina-1) en la membrana presináptica. La formación de un complejo SNARE acerca las membranas para la fusión. La Sinaptotagmina, también una v-SNARE, actúa como sensor de calcio dentro de este sistema, regulando la fusión en respuesta a la entrada de calcio.
¿Cuáles son los tipos de receptores de acetilcolina?
Hay dos tipos principales de receptores de acetilcolina: los Receptores Nicotínicos y los Receptores Muscarínicos. Los nicotínicos son canales iónicos activados por ligando que permiten el paso de iones (incluido calcio), causando despolarización. Los muscarínicos son receptores acoplados a proteínas G que actúan a través de segundos mensajeros, como la vía de la fosfolipasa C (que aumenta el calcio intracelular) o la vía de la adenilil ciclasa (que reduce el cAMP).
¿Qué sucede con la acetilcolina después de ser liberada?
Una vez en la hendidura sináptica, la acetilcolina se une brevemente a sus receptores en la célula postsináptica y luego es rápidamente degradada por la enzima acetilcolinesterasa (AChE) en colina y acetato. Esta rápida inactivación asegura que la señal sea transitoria y permite una nueva ronda de comunicación sináptica.
Si quieres conocer otros artículos parecidos a Calcio y Acetilcolina: Señales Clave Neuronales puedes visitar la categoría Neurociencia.

