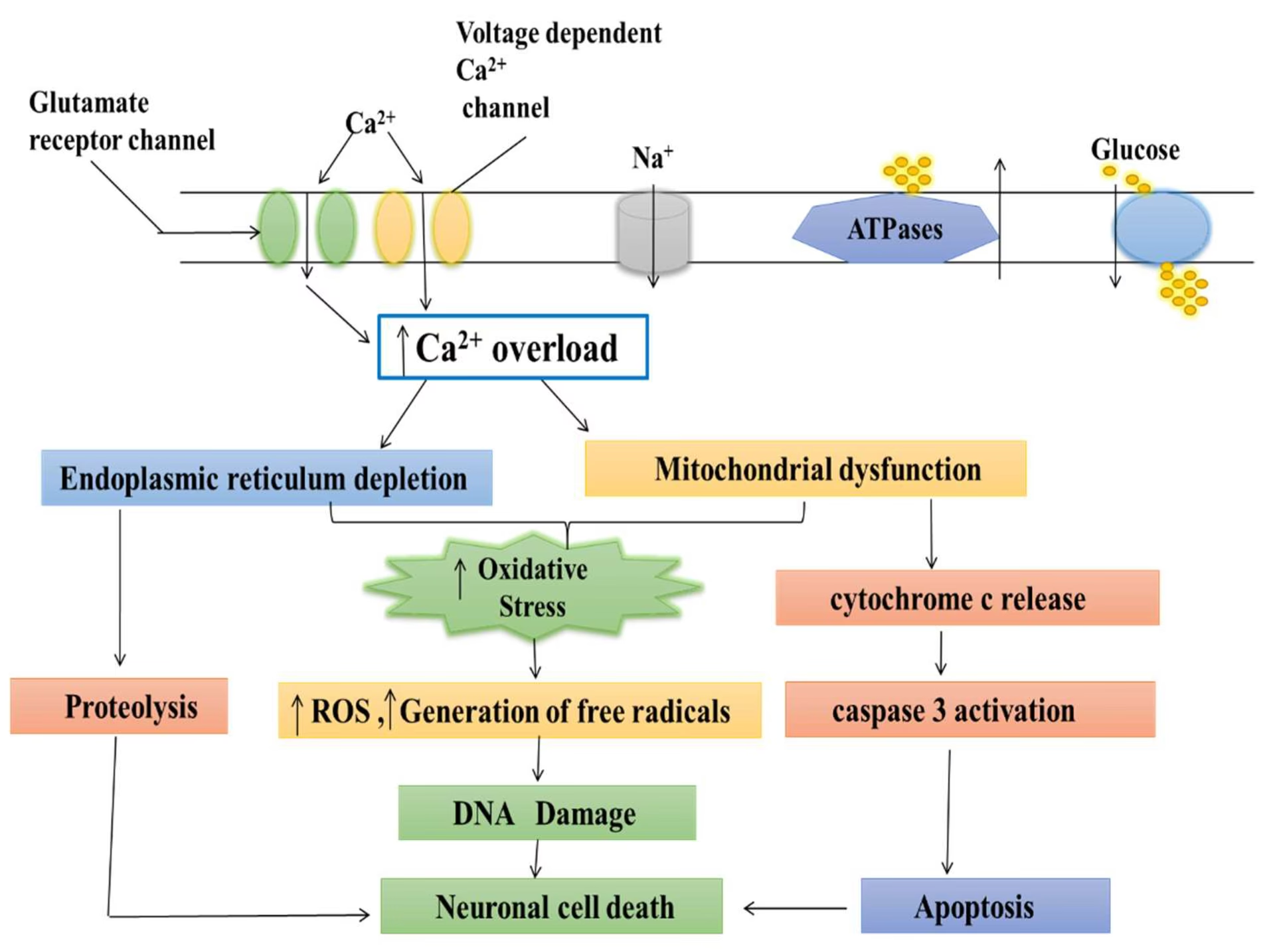
La señalización del calcio es un pilar fundamental para la supervivencia y el correcto funcionamiento de las neuronas. Este ion actúa como un mensajero intracelular clave, participando en procesos tan diversos como la liberación de neurotransmisores, la plasticidad sináptica, la excitabilidad neuronal y, lamentablemente, también en la muerte celular cuando su delicado equilibrio se rompe. Tras una lesión aguda o con el inexorable avance de la edad, la homeostasis del calcio dentro de las neuronas puede verse gravemente alterada, desencadenando una cascada de eventos que culminan en disfunción y pérdida neuronal.
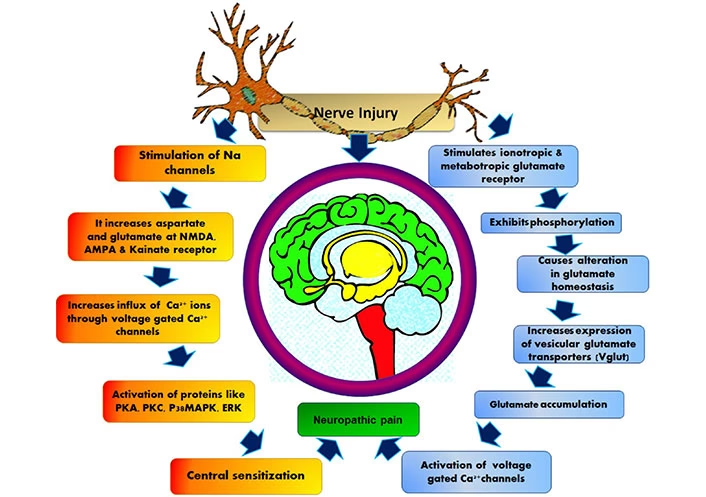
Teóricamente, las intervenciones farmacológicas que modulan los niveles de calcio podrían ofrecer efectos neuroprotectores significativos. Los bloqueadores de canales de calcio (BCC) son una clase de medicamentos ampliamente utilizados, principalmente conocidos por sus efectos cardiovasculares y su capacidad para inducir vasodilatación. Sin embargo, investigaciones recientes han puesto de manifiesto un potencial neuroprotector inesperado, particularmente asociado a los bloqueadores de los canales de calcio de tipo T.
- El Papel Crucial del Calcio en la Salud Neuronal
- Canales de Calcio de Tipo T: Más Allá de la Vasodilatación
- Evidencia de Neuroprotección: Estudios In Vitro e In Vivo
- Mecanismos Moleculares de la Neuroprotección: Un Enfoque en Zonisamida
- Tabla Comparativa de Canales de Calcio Dependientes de Voltaje (VGCC)
- ¿Cómo Afectan los Bloqueadores de Canales de Calcio al Cerebro?
- Bloqueadores de Canales de Calcio: ¿Vasodilatación o Vasoconstricción?
- Preguntas Frecuentes
El Papel Crucial del Calcio en la Salud Neuronal
El calcio entra en la célula a través de transportadores o, más pertinentemente en el contexto neuronal, a través de canales de calcio. Estos canales se dividen en canales activados por ligando y canales de calcio dependientes de voltaje (VGCC). Los VGCC son esenciales para la excitabilidad neuronal, abriéndose en respuesta a cambios en el potencial de membrana y permitiendo la entrada de calcio que impulsa procesos como la liberación de neurotransmisores.
Los VGCC se clasifican en dos grandes grupos: los canales activados por alto voltaje (HVA), que incluyen los tipos L, N, P/Q y R, y los canales activados por bajo voltaje (LVA), conocidos como canales de tipo T. Los canales HVA requieren una despolarización significativa de la membrana para abrirse (alrededor de -20mV), mientras que los canales de tipo T se activan con despolarizaciones mucho menores, cercanas al potencial de reposo neuronal (alrededor de -70mV). Esta diferencia en el umbral de activación es clave para entender sus distintos roles fisiológicos.
Canales de Calcio de Tipo T: Más Allá de la Vasodilatación
Los canales de calcio de tipo T, codificados por las subunidades alfa CaV3.1 (α1G), CaV3.2 (α1H) y CaV3.3 (α1I), se encuentran predominantemente en neuronas, aunque también están presentes en otros tipos celulares como miocitos cardíacos, células marcapasos y células gliales. A diferencia de algunos canales HVA (como los de tipo L), los canales de tipo T suelen carecer de subunidades auxiliares, lo que les confiere propiedades biofísicas y farmacológicas distintivas.
Una característica única de los canales de tipo T es su capacidad para ciclar entre estados abierto y cerrado en un rango de potencial de membrana entre -80mV y -40mV. Esto da lugar a una pequeña corriente de calcio constante, conocida como la "corriente ventana". Esta corriente es fundamental para la ritmicidad neuronal, el establecimiento del potencial de reposo y ciertos aspectos del desarrollo. Sin embargo, un desequilibrio en el manejo del calcio, exacerbado por esta corriente ventana durante situaciones de estrés celular o envejecimiento, puede llevar a una sobrecarga de calcio intracelular, un evento tóxico para la neurona.
El exceso de calcio intracelular puede ser captado por las mitocondrias a través del uniporter de calcio mitocondrial. Aunque una captación moderada es fisiológica y apoya la producción de ATP, una sobrecarga de calcio mitocondrial induce la formación de poros de permeabilidad y la liberación de factores pro-apoptóticos, activando la cascada de muerte celular programada. En modelos de lesión, como la privación de oxígeno y glucosa (OGD) que simula la isquemia, las reservas de ATP se agotan rápidamente. Las neuronas intentan desesperadamente mantener la homeostasis iónica, pero la falla energética agrava la situación. En este contexto, bloquear la entrada excesiva de calcio a través de los canales de tipo T puede retrasar el agotamiento de ATP y prolongar la supervivencia neuronal.
Evidencia de Neuroprotección: Estudios In Vitro e In Vivo
La evidencia del potencial neuroprotección de los BCC de tipo T ha crecido significativamente en las últimas décadas, utilizando diversos modelos de enfermedad neurológica:
Modelo de Isquemia (Privación de Oxígeno y Glucosa - OGD)
Los primeros indicios de neuroprotección de los BCC de tipo T surgieron de estudios in vitro. En cultivos neuronales sometidos a OGD, se observó una protección significativa cuando los niveles de calcio extracelular se reducían artificialmente. Lo notable fue que la adición de BCC a cultivos con niveles normales de calcio produjo una neuroprotección casi idéntica. Esto sugirió que la modulación de la entrada de calcio, y no solo su disponibilidad externa, era clave. La teoría predominante es que al bloquear la "corriente ventana" de los canales de tipo T, se reduce la entrada basal de calcio que, aunque pequeña, contribuye a la sobrecarga en condiciones de compromiso energético, retrasando así la depleción de ATP y la muerte celular. Cabe mencionar que también se ha reportado neuroprotección con bloqueadores de canales L y N en modelos de isquemia.
Modelo de Línea Celular Neuronal
Ciertos anestésicos locales, como la bupivacaína, pueden ser neurotóxicos al causar una sobrecarga de calcio intracelular. En líneas celulares neuronales (como las SH-SY5Y) tratadas con bupivacaína, el calcio intracelular aumenta drásticamente, llevando a la muerte celular. Sin embargo, el pretratamiento con dihidrocloruro, un BCC de tipo T, redujo significativamente el calcio intracelular y proporcionó neuroprotección, demostrando un efecto directo sobre la toxicidad inducida por calcio.

Modelo de Neuropatía Periférica
Los canales de calcio de tipo T están regulados al alza en pacientes y modelos animales con neuropatía periférica, una condición a menudo acompañada de dolor crónico (hiperalgesia). Tras una lesión del nervio ciático en ratas, se observó hiperalgesia que fue notablemente reducida con el uso de BCC de tipo T como mibefradil y etosuximida. En un modelo de lesión del nervio espinal L5-L6 en ratones, se encontró que la densidad de canales de tipo T aumentaba específicamente en las neuronas sensoriales pequeñas del ganglio de la raíz dorsal, que son las responsables de transmitir el dolor. Este aumento disminuye el potencial de reposo de estas fibras, haciéndolas hiperexcitables. Mibefradil y etosuximida aliviaron esta hiperexcitabilidad inducida por la lesión nerviosa, reduciendo así la respuesta al dolor.
Modelo de Pérdida Auditiva
La pérdida auditiva inducida por fármacos, como el cisplatino (un agente quimioterapéutico), es un problema grave. Mientras que los BCC de tipo L (diltiazem, nicardipino, nifedipino) no protegieron las células ciliadas cocleares del daño por cisplatino, los BCC de tipo T (flunarizina, pimozida) sí lo hicieron. Sin embargo, la protección por flunarizina no se debe exclusivamente al bloqueo de canales de tipo T; también actúa a través de mecanismos independientes del calcio, como la activación de vías antioxidantes (induciendo Nrf2) y la inhibición de vías pro-apoptóticas (como NF-κB). La pérdida auditiva inducida por ruido, otra causa común de sordera, también ha mostrado ser susceptible a la modulación por BCC de tipo T. Estudios recientes con trimetadiona y etosuximida demostraron protección de las células ciliadas auditivas y las neuronas del ganglio espiral (SGNs) en modelos animales.
Quizás la evidencia más convincente sobre la implicación directa de un subtipo específico de canal de tipo T proviene de estudios sobre la pérdida auditiva relacionada con la edad (presbiacusia), la enfermedad neurodegenerativa más común asociada al envejecimiento. La subunidad α1H (CaV3.2) de los canales de tipo T se expresa fuertemente en las SGNs y su expresión aumenta con la edad. Ratones genéticamente modificados para carecer de α1H mostraron una audición mejor preservada con el envejecimiento y un número mantenido de SGNs en comparación con los ratones control. Esto sugiere que los canales CaV3.2 juegan un papel en la progresión de la pérdida auditiva relacionada con la edad en esta cepa de ratón. Significativamente, la administración de trimetadiona o etosuximida a estos ratones sin α1H no proporcionó neuroprotección adicional, lo que indica que la protección auditiva de estos BCC de tipo T se ejerce principalmente a través del canal CaV3.2 en este contexto.
Mecanismos Moleculares de la Neuroprotección: Un Enfoque en Zonisamida
Hemos visto numerosos ejemplos que resaltan los efectos neuroprotección de los BCC de tipo T. Sin embargo, salvo en el caso específico de la pérdida auditiva relacionada con la edad y CaV3.2, la mayoría de los estudios no proporcionan evidencia directa de que la protección sea *únicamente* a través del bloqueo de los canales de tipo T. Esto se debe a que los BCC actuales, incluso aquellos considerados "de tipo T", a menudo interactúan con otros objetivos moleculares.
Por lo tanto, la neuroprotección ofrecida por esta clase de fármacos puede deberse tanto al bloqueo de los canales de tipo T como a la modulación de otras cascadas de señalización. Dado que la especificidad de los bloqueadores actuales no es absoluta, cada compuesto puede actuar a través de mecanismos únicos, aunque parcialmente superpuestos.
Para ilustrar esta complejidad, consideremos la zonisamida, un fármaco antiepiléptico aprobado por la FDA que ha mostrado potencial en el tratamiento del dolor neuropático, cefaleas y enfermedades como el Parkinson. La zonisamida no solo bloquea los canales de calcio de tipo T (como CaV3.2), controlando el influjo excesivo de calcio observado en estados patológicos, sino que también posee múltiples mecanismos adicionales que podrían contribuir a su efecto neuroprotección:
- Acción Antioxidante: La zonisamida ha demostrado ser un potente captador de radicales libres de oxígeno, moléculas altamente reactivas que dañan las células.
- Modulación de Enzimas: Inhibe la óxido nítrico sintasa (NOS1), una enzima implicada en la producción de óxido nítrico, que en exceso puede ser neurotóxico. También se ha relacionado con la modulación de la potenciación a largo plazo post-isquémica (iLTP).
- Upregulación de Defensas Celulares: Aumenta la expresión de la superóxido dismutasa (SOD2), una enzima antioxidante clave, y eleva los niveles de glutatión (un importante antioxidante celular) al aumentar la actividad de transportadores de cisteína/glutamato. Promueve la translocación nuclear de Nrf2, un factor de transcripción que activa la expresión de genes antioxidantes de Fase II.
- Inhibición de MAO-B: En modelos de Parkinson (como el inducido por MPTP), la zonisamida protege las neuronas dopaminérgicas al inhibir la monoamino oxidasa B (MAO-B), una enzima que convierte el MPTP en su metabolito tóxico MPP+.
- Factores Neurotróficos: Puede aumentar la expresión de factores neurotróficos como el VEGF (factor de crecimiento endotelial vascular), que apoya la supervivencia y el crecimiento neuronal.
- Modulación de la Liberación de Calcio Intracelular: Inhibe los receptores de rianodina, canales presentes en el retículo endoplasmático que liberan calcio almacenado en respuesta a un aumento del calcio intracelular. Al suprimir este sistema de liberación inducida por calcio, la zonisamida previene la sobrecarga de calcio en estados de hiperexcitabilidad.
Esta diversidad de acciones subraya la complejidad de desentrañar el mecanismo exacto de la neuroprotección para cada BCC de tipo T. Es probable que la protección sea el resultado de una acción combinada sobre múltiples objetivos, siendo el bloqueo de los canales de tipo T uno de ellos, pero no necesariamente el único o el principal en todos los casos.
Tabla Comparativa de Canales de Calcio Dependientes de Voltaje (VGCC)
| Característica | Canales Activados por Alto Voltaje (HVA) | Canales Activados por Bajo Voltaje (LVA) (Tipo T) |
|---|---|---|
| Tipos Principales | L (CaV1.1-1.4), N (CaV2.2), P/Q (CaV2.1), R (CaV2.3) | T (CaV3.1, CaV3.2, CaV3.3) |
| Voltaje de Activación | Más despolarizado (aprox. -20mV) | Menos despolarizado (aprox. -70mV) |
| Cinética de Inactivación | Lenta (corriente de larga duración, "L") | Rápida (corriente transitoria, "T") |
| Conductancia Iónica | Alta | Baja |
| Papel Típico | Liberación de neurotransmisores, acoplamiento excitación-contracción, entrada de calcio sostenida | Ritmicidad neuronal, potencial de reposo, "corriente ventana", activación a bajo umbral |
| Localización Predominante | Terminales sinápticos, músculo, corazón, células endocrinas | Neuronas (especialmente en tálamo, ganglios basales), células marcapasos, glía |
¿Cómo Afectan los Bloqueadores de Canales de Calcio al Cerebro?
Basándonos en la evidencia, los bloqueadores de canales de calcio afectan al cerebro principalmente modulando el influjo de calcio en las neuronas y otras células cerebrales, con un énfasis particular en los canales de tipo T. Al reducir la entrada de calcio a través de estos canales, especialmente en situaciones donde la homeostasis del calcio está comprometida (como isquemia, lesión nerviosa, envejecimiento), ayudan a prevenir la sobrecarga de calcio intracelular.
Esta prevención de la sobrecarga de calcio mitocondrial y la subsiguiente cascada pro-apoptótica es un mecanismo clave de su neuroprotección. Además, como ilustra el caso de la zonisamida, muchos de estos fármacos tienen efectos pleiotrópicos, actuando sobre vías antioxidantes, antiinflamatorias, neurotróficas y modulando otros canales iónicos o enzimas relevantes para la supervivencia y función neuronal.
Por lo tanto, su efecto en el cerebro va más allá de una simple modulación del flujo sanguíneo (que es su principal efecto en vasos periféricos, como veremos) y se centra en la protección directa de la fisiología neuronal frente a insultos o el envejecimiento.

Bloqueadores de Canales de Calcio: ¿Vasodilatación o Vasoconstricción?
Esta es una pregunta importante, ya que los bloqueadores de canales de calcio son ampliamente conocidos por su uso en cardiología e hipertensión. En el contexto de los vasos sanguíneos, los canales de calcio dependientes de voltaje (principalmente los de tipo L en las células del músculo liso vascular) son esenciales para la contracción muscular. Cuando estos canales se bloquean, se reduce la entrada de calcio en las células musculares lisas vasculares, lo que provoca su relajación.
Por lo tanto, la respuesta es clara: los bloqueadores de canales de calcio causan vasodilatación, no vasoconstricción. Este es el mecanismo fundamental por el cual reducen la presión arterial y se utilizan para tratar afecciones como la hipertensión, la angina y ciertos tipos de arritmias. Su efecto vasodilatador, aunque relevante para el flujo sanguíneo cerebral, es distinto de los mecanismos directos de neuroprotección a nivel celular que hemos discutido, aunque ambos pueden ser beneficiosos en ciertas patologías neurológicas (por ejemplo, mejorando el suministro de oxígeno en la isquemia).
Preguntas Frecuentes
¿Qué son los bloqueadores de canales de calcio neuronales?
Son fármacos que modulan la entrada de calcio en las neuronas a través de canales específicos dependientes de voltaje. Si bien todos los canales de calcio neuronales (HVA y LVA) pueden ser objetivos, la investigación reciente se ha centrado en los bloqueadores de los canales de calcio de tipo T (CaV3.1, CaV3.2, CaV3.3) por su potencial neuroprotector.
¿Los bloqueadores de canales de calcio causan vasodilatación o vasoconstricción?
Los bloqueadores de canales de calcio causan principalmente vasodilatación. Actúan relajando el músculo liso de los vasos sanguíneos al bloquear la entrada de calcio necesaria para la contracción.
¿Pueden los bloqueadores de canales de calcio proteger las neuronas?
Sí, existe una creciente evidencia, particularmente para los bloqueadores de canales de calcio de tipo T, que sugiere que pueden proteger las neuronas del daño y la disfunción en diversas condiciones, incluyendo isquemia, neuropatía y pérdida auditiva, al prevenir la sobrecarga de calcio y modular otras vías de supervivencia celular.
¿Actúan todos los bloqueadores de canales de calcio de tipo T solo sobre estos canales?
No. Muchos de los bloqueadores de canales de calcio de tipo T actualmente disponibles, como la zonisamida, tienen múltiples objetivos moleculares además de los canales de tipo T. Sus efectos neuroprotectores pueden ser el resultado de una combinación de acciones.
El desarrollo de fármacos es un proceso lento y costoso. Esto hace que la búsqueda de nuevas aplicaciones para medicamentos que ya han demostrado ser seguros y eficaces en rangos de dosis probados sea una vía muy atractiva. Los bloqueadores de canales de calcio, muchos de los cuales tienen actividad sobre los canales de tipo T, son utilizados por millones de personas de forma segura.
Combinando la vasta cantidad de datos epidemiológicos con la ciencia traslacional, podemos identificar qué fármacos de uso común pueden ser "reutilizados" para la neuroprotección. ¿Qué fármacos son más útiles? ¿Ciertas poblaciones se benefician más? ¿Hay una base genética para esta protección? La importancia de identificar y validar nuevas aplicaciones para fármacos existentes no puede subestimarse. A medida que la prevalencia de muchas enfermedades neurológicas continúa aumentando, la disponibilidad inmediata y el uso protocolizado de agentes que puedan mitigar el daño neuronal se vuelven esenciales. Los datos presentados ilustran el inmenso potencial que los BCC de tipo T tienen en diversas enfermedades neurológicas. Los próximos pasos implican seguir investigando los mecanismos subyacentes y confirmar la eficacia y seguridad de estos agentes para la neuroprotección, abriendo una prometedora "ventana" hacia la salud cerebral.
Si quieres conocer otros artículos parecidos a Bloqueadores de Canales de Calcio y Cerebro puedes visitar la categoría Neurociencia.