Durante mucho tiempo, el estudio del cerebro humano ha presentado desafíos únicos debido a su complejidad y a la dificultad de investigar directamente el tejido vivo. Sin embargo, los avances en neurociencia y biología celular han abierto la puerta a la posibilidad de cultivar células cerebrales en el laboratorio. Esta técnica, conocida como cultivo celular, permite a los investigadores estudiar las neuronas y otras células cerebrales en un entorno controlado, lo que ha revolucionado nuestra comprensión de la función cerebral, las enfermedades neurológicas y el desarrollo de tratamientos.
El cultivo de células cerebrales, tanto de modelos animales como humanos, es una herramienta indispensable para la investigación. Permite aislar tipos celulares específicos, manipular su entorno y observar su comportamiento, crecimiento y respuesta a diferentes estímulos, como fármacos o factores patológicos. Aunque tradicionalmente se han utilizado células de roedores, el cultivo de células cerebrales humanas ofrece la ventaja crucial de estudiar directamente la biología de nuestra propia especie, lo que mejora la relevancia traslacional de los hallazgos.
- ¿Por Qué Cultivar Células Cerebrales?
- Fuentes de Células Cerebrales Humanas para Cultivo
- Tipos Celulares Cultivables y sus Roles
- Técnicas Clave y Consideraciones para el Cultivo
- Desafíos en el Cultivo de Células Cerebrales Humanas
- Ventajas y Limitaciones
- Tabla Comparativa: Fuentes de Células Cerebrales Humanas
- Preguntas Frecuentes (FAQ)
¿Por Qué Cultivar Células Cerebrales?
El cultivo de células cerebrales es fundamental para múltiples áreas de la neurociencia. Proporciona un modelo simplificado pero potente para investigar procesos neuronales básicos como la sinaptogénesis, la plasticidad, la migración celular y la formación de redes neuronales. Permite el estudio detallado de tipos celulares específicos, como las neuronas excitatorias e inhibitorias, los astrocitos, la microglía, los oligodendrocitos, los pericitos y las células endoteliales, entendiendo sus roles individuales y sus interacciones.
Además, los cultivos celulares son esenciales para modelar enfermedades neurológicas y psiquiátricas. Permiten recrear aspectos clave de patologías como el Alzheimer, el Parkinson, la esclerosis múltiple, el glioblastoma o la epilepsia en la placa de cultivo. Esto facilita la identificación de mecanismos moleculares y celulares subyacentes a estas enfermedades y, crucialmente, sirve como plataforma para el cribado de nuevos fármacos y terapias. La capacidad de probar compuestos en células humanas relevantes para la enfermedad es un paso crítico en el desarrollo preclínico de medicamentos, como se destaca en la literatura.
La investigación en el desarrollo de fármacos se beneficia enormemente de los cultivos celulares. Permiten evaluar la toxicidad de compuestos, estudiar su farmacocinética celular y determinar su eficacia en modelos celulares de enfermedad antes de pasar a estudios en animales o ensayos clínicos. Esto acelera el proceso de descubrimiento y reduce los costos asociados.

Fuentes de Células Cerebrales Humanas para Cultivo
Obtener células cerebrales humanas para cultivo puede realizarse a partir de diversas fuentes, cada una con sus propias ventajas y limitaciones:
- Tejido de Biopsia Quirúrgica: Se obtiene de pacientes que se someten a cirugía cerebral por diversas razones (por ejemplo, resección de tumores, tratamiento de la epilepsia). Este tejido está fresco y las células suelen estar en mejores condiciones funcionales iniciales. Permite obtener una variedad de tipos celulares, incluyendo neuronas funcionales.
- Tejido Post-mortem: Se recupera de donantes fallecidos. Aunque la viabilidad celular puede ser un desafío dependiendo del intervalo post-mortem y las condiciones de preservación, se ha demostrado que es posible aislar y cultivar células como microglía, astrocitos, oligodendrocitos e incluso progenitores neuronales y células mesenquimales perivasculares a partir de esta fuente.
- Células Madre Pluripotentes Inducidas (iPSCs): Representan una fuente revolucionaria. Se generan reprogramando células somáticas (como células de la piel o sangre) de cualquier individuo (sano o con enfermedad) para convertirlas en un estado pluripotente similar al embrionario. A partir de estas iPSCs, se pueden diferenciar en prácticamente cualquier tipo de célula cerebral, incluyendo subtipos específicos de neuronas y células gliales. Esta técnica permite generar modelos celulares de enfermedades genéticas o específicas de un paciente.
- Progenitores del Cerebro Adulto: El cerebro adulto, particularmente en regiones como la zona subventricular o el giro dentado, contiene nichos de células progenitoras que pueden ser aisladas y expandidas en cultivo. Estas células tienen la capacidad de diferenciarse en neuronas y células gliales, aunque la neurogénesis en el cerebro adulto humano es limitada en comparación con etapas tempranas del desarrollo.
Tipos Celulares Cultivables y sus Roles
El cerebro es un órgano complejo compuesto por una diversidad de tipos celulares que interactúan estrechamente. Afortunadamente, muchas de estas poblaciones celulares pueden ser aisladas y cultivadas:
- Neuronas: Las células fundamentales para la transmisión de señales. Se pueden cultivar neuronas primarias de tejido (embrionario, postnatal o adulto) o diferenciarlas a partir de iPSCs o progenitores. Es posible obtener subtipos específicos como neuronas piramidales, interneuronas GABAérgicas, etc. Mantener su funcionalidad, incluyendo la formación de sinapsis y la actividad eléctrica, es un objetivo clave en el cultivo.
- Astrocitos: Las células gliales más abundantes, con roles cruciales en el soporte metabólico, la homeostasis iónica, la formación de la barrera hematoencefálica y la modulación sináptica. Se pueden aislar y cultivar a partir de tejido cerebral o diferenciar de iPSCs. Son importantes para estudiar la neuroinflamación y el soporte neuronal.
- Microglía: Los macrófagos residentes del sistema nervioso central, con funciones inmunes, fagocíticas y de vigilancia del entorno cerebral. Se pueden aislar de tejido post-mortem o de biopsia, y también derivar de iPSCs. Son clave en el estudio de la neuroinflamación y las enfermedades neurodegenerativas.
- Oligodendrocitos: Responsables de formar la vaina de mielina que aísla los axones neuronales. Se pueden aislar de tejido o diferenciar de progenitores o iPSCs. Cruciales para estudiar enfermedades desmielinizantes como la esclerosis múltiple.
- Pericitos: Células murales que rodean los vasos sanguíneos cerebrales, componentes clave de la barrera hematoencefálica y la unidad neurovascular. Se pueden aislar y cultivar a partir de tejido. Importantes para estudiar la función vascular cerebral, la neuroinflamación y la integridad de la barrera.
- Células Endoteliales de la Barrera Hematoencefálica: Forman el revestimiento interno de los vasos sanguíneos cerebrales y son la base física de la barrera hematoencefálica. Se pueden cultivar para crear modelos in vitro de la barrera, a menudo en co-cultivo con pericitos y astrocitos para mimetizar la unidad neurovascular.
Técnicas Clave y Consideraciones para el Cultivo
El éxito del cultivo de células cerebrales depende del control meticuloso de múltiples parámetros:
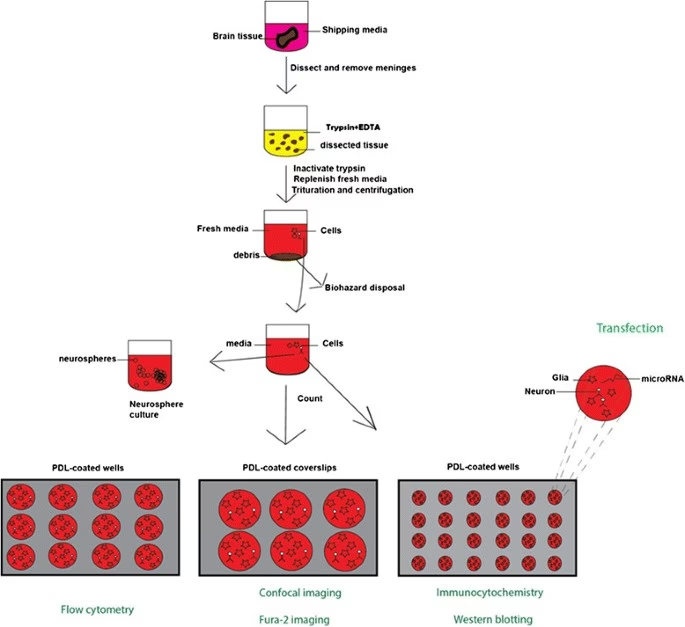
- Aislamiento y Disociación: El tejido cerebral (ya sea fresco o post-mortem) debe ser disociado en células individuales. Esto generalmente implica una combinación de digestión enzimática suave (para romper las conexiones extracelulares) y disociación mecánica. Es crucial optimizar este paso para maximizar la viabilidad celular.
- Medios de Cultivo: Las células cerebrales tienen requisitos nutricionales específicos. Se utilizan medios complejos enriquecidos con factores de crecimiento, suero (aunque a menudo se prefiere medios definidos o suplementados con suero reducido para evitar la proliferación excesiva de ciertas células gliales) y suplementos como glucosa, aminoácidos y vitaminas.
- Condiciones Ambientales: Se mantiene un control estricto de la temperatura (37°C), el pH (generalmente tamponado con CO2 al 5% en una incubadora) y la osmolaridad. La hiperosmolaridad, por ejemplo, causada por la evaporación del medio, puede ser perjudicial.
- Sustrato de Cultivo: Las células cerebrales, especialmente las neuronas, requieren una superficie de cultivo tratada para promover la adhesión. Se utilizan recubrimientos como polilisina (en sus formas L o D), poli-ornitina o proteínas de la matriz extracelular (ECM) como laminina o fibronectina.
- Densidad Celular: La densidad de siembra es crítica. Una densidad demasiado baja puede resultar en falta de soporte trófico y baja viabilidad, ya que las células no secretan suficientes factores de supervivencia. Una densidad demasiado alta puede llevar a la privación de nutrientes, acumulación de desechos y proliferación excesiva de glía. Para cultivos de baja densidad, a menudo se utilizan "capas alimentadoras" (feeder layers) de otras células (por ejemplo, astrocitos) o medios condicionados para proporcionar soporte trófico sin que las células alimentadoras contaminen el cultivo principal.
- Cultivos Mixtos y Co-cultivos: Para mimetizar mejor el entorno cerebral, a menudo se realizan cultivos de múltiples tipos celulares juntos (cultivos mixtos) o se cultivan diferentes tipos celulares en compartimentos separados que comparten el medio (co-cultivos). Los co-cultivos de neuronas y glía son comunes para estudiar la interacción neuro-glial, y los co-cultivos de células endoteliales, pericitos y astrocitos se utilizan para modelar la barrera hematoencefálica.
- Cultivos Organotípicos y Ex-vivo: Además de los cultivos de células disociadas, existen técnicas para mantener porciones de tejido cerebral (rebanadas o explantes) en cultivo. Los cultivos de rebanadas organotípicas, por ejemplo, mantienen parte de la arquitectura tisular y las conexiones sinápticas intactas, permitiendo el estudio de la función de red y la plasticidad en un contexto más cercano al in vivo. Los explantes de meninges o plexo coroideo permiten estudiar la inflamación en estas estructuras.
Desafíos en el Cultivo de Células Cerebrales Humanas
Aunque se han logrado avances significativos, el cultivo de células cerebrales humanas presenta desafíos:
- Obtención de Tejido: La disponibilidad de tejido cerebral humano, especialmente tejido fresco de alta calidad, es limitada y depende de donaciones o procedimientos quirúrgicos.
- Variabilidad: Las células aisladas de diferentes individuos o incluso de diferentes regiones del mismo cerebro pueden mostrar una variabilidad significativa en su comportamiento en cultivo. La edad del donante, la causa de la muerte o la patología subyacente pueden influir en las características celulares.
- Mantenimiento de la Identidad Celular: Algunas células, como las células endoteliales de la barrera hematoencefálica, pueden perder características clave de su fenotipo in vivo cuando se cultivan durante períodos prolongados.
- Proliferación de Glía: En los cultivos primarios de neuronas de tejido, los astrocitos y la microglía tienden a proliferar más rápidamente que las neuronas, pudiendo dominar el cultivo. Se utilizan métodos para enriquecer las poblaciones neuronales o controlar la proliferación glial.
- Recrear la Complejidad del Entorno In Vivo: El cerebro es un órgano tridimensional con complejas interacciones celulares, moleculares y estructurales. Los cultivos 2D simplificados no pueden replicar completamente esta complejidad. Los cultivos 3D (como esferoides u organoides cerebrales, aunque no explícitamente detallados en el texto proporcionado, son una extensión lógica del campo) y los co-cultivos ayudan a abordar esto.
- Viabilidad a Largo Plazo: Mantener la viabilidad y funcionalidad de ciertos tipos celulares, especialmente neuronas maduras, durante semanas o meses en cultivo puede ser difícil.
Ventajas y Limitaciones
A pesar de los desafíos, las ventajas del cultivo de células cerebrales son numerosas. Permiten un control experimental sin precedentes, la capacidad de estudiar mecanismos a nivel celular y molecular, y la posibilidad de realizar estudios de alto rendimiento (high-throughput screening) para el descubrimiento de fármacos. Reducen la necesidad de estudios en animales en las etapas iniciales de la investigación.
Las limitaciones incluyen la simplificación inherente del modelo in vitro en comparación con el cerebro intacto, la posible alteración del fenotipo celular en cultivo y la dificultad de replicar completamente las interacciones complejas que ocurren en el tejido vivo.
Tabla Comparativa: Fuentes de Células Cerebrales Humanas
| Fuente | Ventajas Principales | Limitaciones Principales | Tipos Celulares Comunes |
|---|---|---|---|
| Biopsia Quirúrgica | Tejido fresco, alta viabilidad inicial, representa estado fisiológico/patológico real. | Disponibilidad limitada, variabilidad entre donantes, invasivo. | Neuronas, Astrocitos, Microglía, Oligodendrocitos, Pericitos, Endoteliales. |
| Tejido Post-mortem | Más accesible, permite estudiar cerebros con patologías avanzadas. | Viabilidad reducida, impacto del intervalo post-mortem, posible degradación. | Astrocitos, Microglía, Oligodendrocitos, Progenitores, Pericitos. |
| iPSCs (Células Madre Pluripotentes Inducidas) | Fuente ilimitada, permite modelar enfermedades específicas de paciente, control genético. | Requiere diferenciación compleja, las células pueden no alcanzar madurez completa in vivo, costoso inicialmente. | Neuronas (diversos subtipos), Astrocitos, Microglía, Oligodendrocitos, Pericitos (derivados). |
| Progenitores del Cerebro Adulto | Representan células con potencial neurogénico endógeno, fuente del cerebro adulto. | Aislamiento desafiante, capacidad de diferenciación limitada comparada con iPSCs, nichos específicos. | Neuronas, Astrocitos, Oligodendrocitos. |
Preguntas Frecuentes (FAQ)
¿Es posible cultivar cualquier tipo de célula cerebral humana?
Sí, se han desarrollado métodos para aislar y cultivar la mayoría de los principales tipos celulares del cerebro humano, incluyendo neuronas, astrocitos, microglía, oligodendrocitos, pericitos y células endoteliales. Sin embargo, mantener la funcionalidad y pureza de ciertos tipos puede ser más desafiante que otros.
¿Son las células cultivadas idénticas a las células en el cerebro vivo?
Aunque los cultivos celulares son excelentes modelos, existen diferencias inherentes. Las células en cultivo carecen del complejo entorno tridimensional, las interacciones a largo plazo con otras estructuras cerebrales y las señales sistémicas (como la circulación sanguínea o las hormonas) que reciben en el cerebro vivo. Algunas células pueden alterar su fenotipo en cultivo.
¿Cuánto tiempo pueden sobrevivir las células cerebrales en cultivo?
La duración varía significativamente según el tipo celular, la fuente y las condiciones de cultivo. Algunos tipos celulares, como los astrocitos o la microglía, pueden proliferar y mantenerse en cultivo durante meses o incluso años (ciertas líneas celulares). Las neuronas primarias maduras son más delicadas, pero con técnicas optimizadas, pueden mantenerse funcionales durante semanas o meses. Las células derivadas de iPSCs pueden cultivarse a largo plazo y diferenciarse durante períodos extensos.

¿Se pueden formar redes neuronales funcionales en cultivo?
Sí, las neuronas cultivadas tienen la capacidad de extender axones y dendritas, formar sinapsis y establecer redes neuronales eléctricamente activas. Esto permite estudiar la comunicación neuronal y la plasticidad sináptica in vitro.
¿Para qué se utilizan principalmente los cultivos de células cerebrales humanas en la investigación?
Se utilizan para estudiar mecanismos de enfermedades, identificar dianas terapéuticas, probar la eficacia y toxicidad de fármacos, investigar la función de genes específicos y comprender los procesos básicos de desarrollo y funcionamiento cerebral.
En conclusión, el cultivo de células cerebrales humanas es una herramienta poderosa y en constante evolución que permite desentrañar los misterios del cerebro desde la perspectiva celular. A pesar de los desafíos técnicos, su potencial para acelerar la investigación de enfermedades neurológicas y el desarrollo de tratamientos es inmenso, acercándonos a una comprensión más profunda de la mente humana.
Algunas palabras clave importantes en este campo incluyen cultivo primario, células gliales, neuronas, iPSCs y barrera hematoencefálica.
Si quieres conocer otros artículos parecidos a Cultivo de Células Cerebrales Humanas puedes visitar la categoría Neurociencia.
