La capacidad natural del tejido óseo para regenerarse es notable, permitiendo la reparación de pequeñas áreas dañadas. Sin embargo, los defectos extensos causados por traumas severos, enfermedades degenerativas, anomalías congénitas o la extirpación de tumores a menudo superan esta capacidad intrínseca, requiriendo intervenciones médicas avanzadas para lograr una restauración funcional completa. Actualmente, los injertos óseos autólogos (del propio paciente) o alogénicos (de donantes) se consideran el estándar de oro para reparar estos grandes defectos.
A pesar de su uso extendido, los injertos tradicionales presentan limitaciones significativas. El uso de injertos autólogos implica una cirugía adicional para obtener el tejido, lo que añade morbilidad al paciente. Por otro lado, los injertos alogénicos, aunque evitan la cirugía de extracción, son tratados (por irradiación o liofilización) para reducir el riesgo de rechazo o transmisión de enfermedades. Este procesamiento, sin embargo, disminuye su capacidad de inducir la formación de nuevo hueso, lo que puede llevar al fracaso del injerto. Las matrices óseas celulares, un desarrollo más reciente, buscan mejorar la bioactividad de los injertos, pero conllevan un mayor riesgo de rechazo inmune y no garantizan la viabilidad celular durante la preservación e implantación. Además, la transmisión de enfermedades, la integridad estructural reducida y los costos más elevados son riesgos inherentes a la trasplantación alogénica. Impulsado por estas apremiantes necesidades clínicas, el campo de la ingeniería de tejidos óseos ha surgido y experimentado un rápido desarrollo en las últimas décadas.
La Crucial Interacción Nervio-Hueso
El campo de investigación en ingeniería de tejidos óseos busca desarrollar materiales que superen las capacidades de los autoinjertos y aloinjertos óseos. Actualmente, se dispone de varios tipos de materiales para la ingeniería de tejidos óseos, incluyendo polímeros naturales o sintéticos y materiales inorgánicos. Algunos de estos biomateriales imitan con éxito la estructura y las propiedades mecánicas del hueso. Además, algunas estrategias han logrado cierto éxito en la reparación de defectos óseos utilizando diseños capa a capa para imitar la microestructura jerárquica del hueso. Sin embargo, pocos enfoques han sido capaces de imitar las unidades funcionales dentro del hueso, como los vasos sanguíneos o los nervios, lo que ha llevado a resultados subóptimos.
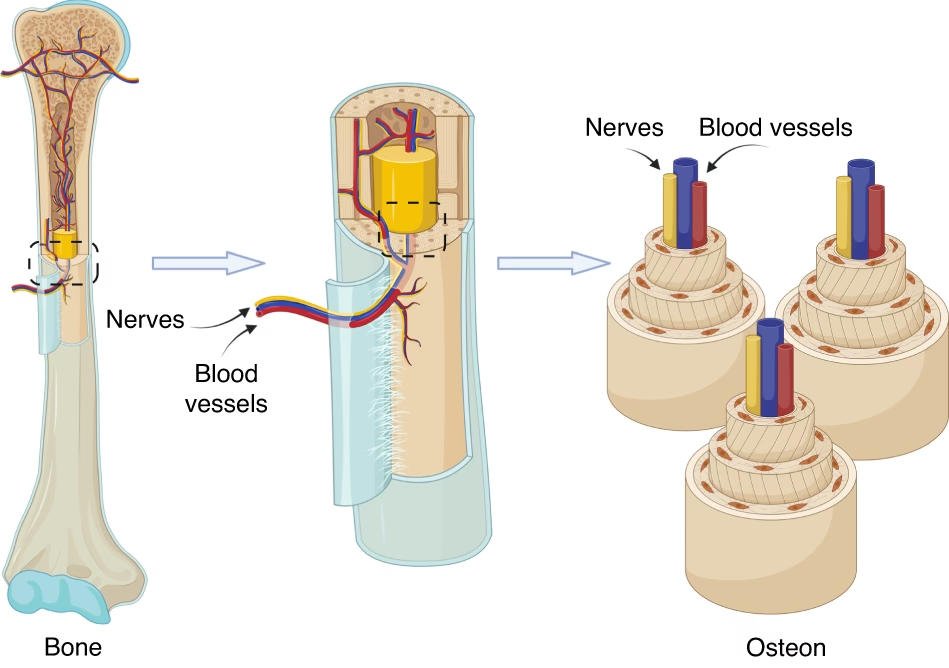
Como se mencionó anteriormente, las fibras nerviosas están ampliamente presentes en el hueso y, hasta cierto punto, influyen en la regeneración del tejido óseo, una función que ha ganado gran atención en los últimos años. Investigaciones previas han enfatizado la estrecha interacción entre el tejido óseo y el tejido neural en diversos estados fisiopatológicos y han propuesto posibles estrategias de andamiaje para la ingeniería de tejidos neuro-óseos. En este campo emergente, los andamios (estructuras tridimensionales que sirven de soporte) han sido ingeniosamente diseñados para transportar células neurales o factores de crecimiento. Este enfoque innovador ha facilitado el desarrollo de intrincadas redes neurales dentro de los andamios, permitiendo una regeneración ósea coordinada por los nervios.
Además, dada la influencia de los neuropéptidos en el proceso de regeneración ósea, la carga directa de estos factores neurogénicos o el aprovechamiento de los efectos favorables del sistema nervioso en la regeneración ósea también se considera una estrategia viable. En este proceso, los nervios brindan apoyo para la angiogénesis (formación de vasos sanguíneos) dentro del andamio. Simultáneamente, la interacción intrincadamente coordinada entre los elementos neuronales y la formación vascular acelera el crecimiento de las células óseas y produce resultados regenerativos sobresalientes. Por lo tanto, a diferencia de los enfoques singulares de la ingeniería de tejidos óseos o la ingeniería de tejidos neurales, la neuro-ingeniería de tejidos óseos enfatiza el papel sinérgico de los nervios durante el proceso de regeneración ósea. La nueva evidencia sugiere que la neuro-ingeniería de tejidos óseos tiene amplias perspectivas de aplicación, pero su estado actual y los conceptos de diseño requieren una mayor elucidación.
Los Pilares de la Neuro-Ingeniería Ósea: Biomateriales
En la reparación de defectos óseos, los biomateriales sirven como marcos tridimensionales para la adhesión, el crecimiento y la diferenciación celular. En la neuro-ingeniería de tejidos óseos, el material del andamio juega un papel crucial en la creación de un entorno propicio para la regeneración de tejidos nerviosos y óseos, y en la facilitación de la comunicación entre ambos. Aunque ya existen diversos materiales disponibles para reparar tejidos neurales y óseos por separado, la investigación se ha centrado de forma limitada en la construcción de materiales específicamente para la neuro-ingeniería de tejidos óseos. Sin embargo, es lógico considerar que los materiales con aplicaciones en la reparación de ambos tipos de tejidos tienen potencial para su uso en este campo. Además, algunos materiales promueven la regeneración ósea al influir en la actividad neural y pueden incorporarse a los materiales de andamiaje de la neuro-ingeniería de tejidos óseos.
Polímeros
Los polímeros son materiales orgánicos compuestos por átomos interconectados mediante enlaces covalentes. Tanto los polímeros derivados de fuentes naturales como los sintéticos son valiosos en la ingeniería de tejidos óseos. Los polímeros naturales, como el colágeno, la gelatina, el ácido hialurónico, el quitosano, el alginato y la seda, son producidos por organismos vivos. Se degradan en dióxido de carbono y agua, lo que resulta en reacciones inflamatorias mínimas in vivo. Los polímeros sintéticos, incluyendo el ácido poliláctico (PLA), el ácido poliglicólico (PGA) y el ácido poli(láctico-co-glicólico) (PLGA), pueden degradarse en condiciones fisiológicas pero pueden liberar ácidos que inducen inflamación. Sin embargo, los polímeros sintéticos ofrecen versatilidad a través de modificaciones químicas y alteraciones moleculares, permitiendo la personalización de propiedades para aplicaciones específicas, como la incorporación de motivos funcionales para mejorar las interacciones célula-andamio.
Materiales Inorgánicos
En la ingeniería de tejidos óseos, los materiales inorgánicos desempeñan un papel significativo, particularmente las cerámicas bioactivas y los metales. Las cerámicas bioactivas como la hidroxiapatita y el trifosfato de calcio poseen una excelente biocompatibilidad y osteoconductividad debido a su composición similar a la del hueso. También proporcionan un suministro continuo de iones de fósforo y calcio, que promueven la biomineralización. Sin embargo, los materiales cerámicos puros por sí solos no pueden reclutar células, regular la inmunidad o promover la regeneración neurovascular. Por lo tanto, a menudo se utilizan en combinación con otros materiales bioactivos para satisfacer mejor las necesidades de la neuro-ingeniería de tejidos óseos.
Los metales, como el titanio y el acero inoxidable, se utilizan comúnmente en implantes metálicos clínicos. Exhiben una biocompatibilidad y propiedades mecánicas favorables. Sin embargo, la naturaleza no biodegradable de estos implantes a menudo requiere una segunda cirugía para su extracción. Por otro lado, el magnesio, que tiene un excelente módulo de Young similar al del hueso cortical natural, es un metal importante en la ingeniería de tejidos óseos. Los implantes a base de Mg no solo evitan el blindaje por estrés (stress shielding) sino que también contribuyen a la regulación inmune, la regeneración nerviosa, la angiogénesis y la reparación ósea. Notablemente, los estudios han demostrado que el magnesio puede estimular la secreción de CGRP por los nervios, movilizando eficazmente señales endógenas para la reparación nervio-hueso. En consecuencia, el magnesio tiene un gran potencial para aplicaciones en neuro-ingeniería de tejidos óseos.
Materiales Compuestos
En la neuro-ingeniería de tejidos óseos, la demanda de materiales compuestos surge de una multitud de factores intrincados, haciendo que el uso de un solo material sea inviable y, por lo tanto, necesite la utilización de compuestos de materiales existentes. Primero, en el contexto de la neuro-ingeniería de tejidos óseos, la consideración se extiende más allá de la mera reparación y regeneración del tejido óseo para abarcar la crucial promoción de la regeneración del tejido neural. La regeneración de estos dos tipos de tejidos distintos tiene requisitos biológicos y mecánicos dispares. Por ejemplo, los materiales deben ofrecer soporte mecánico para la regeneración del tejido óseo y crear un entorno propicio para el crecimiento de las células neurales. Los biomateriales compuestos ofrecen una solución prometedora para satisfacer estas diversas necesidades.
Además, la neuro-ingeniería de tejidos óseos aspira a replicar fielmente la intrincada estructura y funcionalidad que se encuentra en los tejidos biológicos naturales, lo que implica andamios que imiten las estructuras complejas de los tejidos óseos y neurales al mismo tiempo que brindan funcionalidades biológicas esenciales. Además, el éxito de la regeneración ósea depende de la interacción sinérgica entre los tejidos neurales y óseos. La ventaja de los materiales compuestos reside en su capacidad para facilitar interacciones favorables entre los tejidos neurales y óseos a través de la modulación precisa de las combinaciones de materiales, fomentando así la regeneración sinérgica. Por último, la utilización de materiales compuestos sirve como una estrategia eficaz para superar las limitaciones inherentes asociadas con los materiales individuales.
Los polímeros ofrecen una excelente biocompatibilidad, ya que los polímeros naturales como el colágeno son componentes inherentes de los tejidos biológicos, proporcionando una guía bioinformática innata que mejora la adhesión celular y la regeneración de tejidos. Además, los polímeros sintéticos pueden adaptarse intencionalmente, alineándolos con las funciones deseadas del biomaterial sin alterar sus propiedades intrínsecas. Sin embargo, los polímeros pueden tener propiedades mecánicas relativamente débiles que no necesariamente son suficientes para las altas demandas de resistencia de la neuro-ingeniería de tejidos óseos. En contraste, los materiales inorgánicos como las biocerámicas y los metales exhiben propiedades mecánicas sobresalientes adecuadas para la reparación ósea. Generalmente no provocan respuestas inmunes y, por lo tanto, son bien tolerados en el cuerpo. Sin embargo, algunos materiales inorgánicos pueden carecer de la guía bioinformática necesaria para promover la adhesión celular y la regeneración de tejidos, lo que requiere esfuerzos de mejora adicionales. Además, ciertos materiales inorgánicos pueden inducir reacciones adversas en los sistemas biológicos, lo que requiere una cuidadosa selección y diseño.
Considerando estos factores de manera integral, la práctica común es emplear un enfoque de materiales compuestos integrando polímeros y materiales inorgánicos para maximizar la explotación de sus respectivas ventajas al mismo tiempo que se mitigan sus limitaciones individuales. Esta utilización integrada puede conducir a un rendimiento y una biocompatibilidad más completos, ofreciendo la perspectiva de lograr avances significativos en el campo de la neuro-ingeniería de tejidos óseos. Así, los polímeros y los materiales inorgánicos desempeñan papeles complementarios en la ingeniería biomédica, ofreciendo una mayor esperanza y potencial para el tratamiento y la reparación de tejidos.
Células Semilla: Impulsores de la Regeneración
Las células semilla son elementos fundamentales en la ingeniería de tejidos. Las células semilla ideales para la ingeniería de tejidos óseos deben poseer una fuerte capacidad proliferativa, una robusta adaptabilidad al entorno y una buena compatibilidad tisular. Dado que las células semilla son los principales contribuyentes a la actividad biológica de los andamios de ingeniería de tejidos óseos, la investigación previa en este campo ha enfatizado principalmente su potencial de diferenciación osteogénica, a menudo pasando por alto la influencia de las células semilla en otras células endógenas. Si bien todos los tipos de células madre pueden someterse a diferenciación secundaria, inducir la diferenciación de células madre en linajes neuronales y osteogénicos simultáneamente es innegablemente desafiante. Desde otra perspectiva, en el campo de la neuro-ingeniería de tejidos óseos, se deben considerar todas las células semilla que puedan promover la regeneración sinérgica de tejidos neurales y óseos. Hasta la fecha, se han empleado diversas células semilla, incluyendo células madre mesenquimales, células de Schwann y células endoteliales, en la neuro-ingeniería de tejidos óseos.
Células Madre Mesenquimales de Médula Ósea (CMMO)
Las CMMO son una subpoblación de células que se encuentran en el estroma de la médula ósea de mamíferos. Tienen una notable capacidad para diferenciarse en varios tipos celulares, incluyendo células óseas, cartilaginosas, adiposas, neurales y miogénicas, lo que las convierte en células semilla ideales para la neuro-ingeniería de tejidos óseos. En teoría, cualquier célula madre capaz de diferenciarse en células óseas o nerviosas puede ser utilizada, pero es un desafío inducir simultáneamente la diferenciación neural y osteogénica en las mismas células madre. Por lo tanto, las CMMO a menudo se coinjertan con otras células, particularmente células de Schwann (CS).
Se ha descubierto que el cocultivo de CS y osteoblastos mantiene la secreción normal de factores neurotróficos por las CS y promueve la proliferación y diferenciación de los osteoblastos. En un estudio reciente, se construyó una estructura bicapa, imitando la distribución espacial del hueso craneal y los nervios asociados al cráneo. Este diseño biomimético facilitó enormemente la regeneración ósea al distribuir estratégicamente CS y CMMO. Además, la combinación de nervios sensoriales con CMMO en andamios de β-TCP e implantarlos en sitios de defectos críticos en fémures de conejo mejoró la neovascularización y la formación de hueso nuevo. Los estudios también han demostrado que la matriz extracelular derivada de CMMO, que contiene diversas señales microambientales, como factores bioquímicos, espaciales y biomecánicos, proporciona un entorno favorable para la regeneración nerviosa. Cuando se cargó medio condicionado de células madre mesenquimales en un andamio 3D de policaprolactona (PCL), promovió eficazmente la regeneración nerviosa después de la axotomía. En general, los efectos regenerativos de las CMMO se atribuyen a su capacidad para diferenciarse y reemplazar tejidos dañados, así como a su interacción con los tejidos circundantes a través de la señalización paracrina. Esto crea un microambiente adecuado que regula conjuntamente los procesos de proliferación y diferenciación de tejidos y órganos. Sin embargo, lograr la coadministración de múltiples células semilla en un andamio todavía requiere compromisos en la comunicación e interacciones entre los diferentes tipos celulares.
Células de Schwann (CS)
Las células de Schwann son células gliales periféricas que desempeñan un papel crucial en la regeneración nerviosa periférica. Después de una lesión nerviosa, las CS colaboran con los macrófagos para eliminar los restos de mielina y proliferar para formar bandas que apoyan el crecimiento axonal mediante la secreción de factores de crecimiento y matriz extracelular. Se ha demostrado que el trasplante de CS mejora el crecimiento axonal tanto in vitro como in vivo. Además, se ha descubierto que las CS ejercen efectos nutricionales y reguladores sobre el metabolismo óseo a través de mecanismos complejos. En un modelo de osteotomía mandibular en ratones, la ausencia de CS y sus factores paracrinos resultó en defectos funcionales en las células madre esqueléticas mandibulares, lo que llevó a una disminución en la tasa de reparación ósea mandibular. Estos hallazgos resaltan la importancia de las CS y sus efectos paracrinos en la diferenciación regenerativa de las células madre esqueléticas.
Estudios recientes también han demostrado que las vesículas extracelulares derivadas de células de Schwann promueven la migración, proliferación y diferenciación osteogénica de las CMMO. Los investigadores han utilizado con éxito la tecnología de bioimpresión 3D multicelular para crear un constructo neural-óseo que sirve como un organoide óseo inervado. Se ha demostrado que la incorporación de CS en andamios de ingeniería de tejidos de β-fosfato de calcio con CMMO y células endoteliales (CE) promueve eficazmente la regeneración del tejido óseo a través de los efectos duales de la neurogénesis y la angiogénesis. Estos hallazgos indican las prometedoras perspectivas de investigación y aplicación de las CS en la ingeniería de tejidos óseos. Los estudios futuros deben centrarse en comprender los efectos reguladores de las interacciones entre las CS y varios tipos celulares en el hueso, incluyendo la expresión génica y proteica, así como la transducción de señales intercelulares. La explotación de las características de las CS en la proliferación, secreción, adhesión, migración y diferenciación de células tisulares facilitará el desarrollo de nuevas estrategias terapéuticas adecuadas para aplicaciones clínicas ortopédicas.
Células Endoteliales (CE)
El hueso es un tejido conectivo altamente vascularizado, y una vascularización adecuada es crucial para el desarrollo, la regeneración y la remodelación ósea adecuados. En casos de grandes defectos óseos resultantes de enfermedades o traumas, son necesarios enfoques de injerto óseo o ingeniería de tejidos óseos. Sin embargo, el éxito de la regeneración ósea en ambos métodos depende en gran medida del establecimiento de un suministro sanguíneo adecuado. Además, estudios recientes han destacado la importancia de la comunicación cruzada entre las CE y las células neurales en la regeneración nerviosa periférica.
Los vasos sanguíneos dentro de los nervios en regeneración sirven como vías para la migración de células de Schwann, facilitando la formación de bandas de Büngner que promueven la regeneración axonal. En sistemas de cocultivo, las CE pueden promover la proliferación y migración de CS, contribuyendo a la regeneración nerviosa periférica. Se ha demostrado que las estructuras tubulares alineadas compuestas por CE en constructos nerviosos diseñados mejoran la regeneración nerviosa en modelos de nervio ciático en ratas. El VEGF, un factor de crecimiento crucial involucrado en la regulación de la angiogénesis, puede ser secretado por las CE, y los hidrogeles que contienen VEGF tienen un efecto sinérgico con el BDNF en la regeneración nerviosa periférica. Por lo tanto, las CE también son prometedoras en la ingeniería de tejidos óseos, ya que pueden mejorar simultáneamente la regeneración nerviosa y ósea. Qin et al. produjeron con éxito un andamio cargado de células con propiedades proangiogénicas utilizando tecnología de bioimpresión 3D. Esto se logró incorporando células endoteliales vasculares en una biotinta basada en biocerámicas de Li-Mg-Si (LMS). Los iones bioactivos liberados de LMS, en conjunto con la capacidad de las células vasculares para secretar citocinas ventajosas para las células neurales, apoyaron la diferenciación de células neurales y osteogénicas dentro de los andamios.
Factores Bioactivos Acelulares: Señales Moleculares
Una osteogénesis o neurogénesis efectiva requiere la incorporación de componentes biológicos acelulares, incluyendo factores de crecimiento, péptidos, pequeñas moléculas, fragmentos de ADN/ARN o exosomas, en los andamios. Estos elementos sirven para proporcionar estímulos suplementarios que mejoran la neurogénesis o la osteogénesis. Si bien numerosas investigaciones han profundizado en los impactos de diferentes factores en los tejidos óseos o nerviosos, sigue habiendo una escasez de factores acelulares que puedan fomentar concurrentemente la regeneración de nervios y huesos. Dentro de esta sección, delineamos elementos acelulares que facilitan independientemente la regeneración de hueso y nervios. Además, cuando estos factores se emplean en tándem, exhiben un potencial sustancial dentro del campo de la neuro-ingeniería de tejidos óseos.
Factores de Crecimiento
Las reacciones biológicas son iniciadas por factores de crecimiento, que son proteínas de señalización solubles secretadas por las células. Se unen a receptores de superficie celular y regulan cascadas de señalización intracelular, desempeñando papeles cruciales en varios procesos celulares. En la formación ósea, participan varios factores de crecimiento, incluyendo las proteínas morfogenéticas óseas (BMPs), el factor de crecimiento transformante-β (TGF-β), el factor de crecimiento derivado de plaquetas (PDGF), el factor de crecimiento de fibroblastos (FGF) y el factor de crecimiento similar a la insulina (IGF), entre los cuales la BMP es ampliamente estudiada. La BMP puede estimular células pluripotentes como las CMMO para proliferar y diferenciarse en condrocitos y osteoblastos, promoviendo la formación de hueso nuevo. Así, los factores de crecimiento, cuando están encapsulados dentro de los andamios, pueden utilizarse para tratar fracturas de manera efectiva. Además, se ha demostrado que la BMP estimula la angiogénesis, contribuyendo aún más a la regeneración ósea. Actualmente, BMP-2, 3, 4, 5 y 7 son los principales factores osteogénicos conocidos, siendo BMP-2 y BMP-7 los más estudiados y aprobados por la FDA para la regeneración ósea.
Los factores de crecimiento nervioso (NGF), los factores neurotróficos derivados del cerebro (BDNF), los factores neurotróficos derivados de la glía (GDNF) y los factores neurotróficos-3 y -4 (NT-3, NT-4) son cruciales para el crecimiento y la supervivencia neuronal. Durante la regeneración nerviosa, estos factores neurotróficos desempeñan un papel en la mejora de la diferenciación, el reclutamiento y los procesos de remielinización de las células madre. El gradiente de factores neurotróficos producido por las terminaciones nerviosas después del trauma ejerce efectos tanto estimuladores como inhibidores en la reparación nerviosa. La incorporación de factores neurotróficos en conductos neurales para promover la regeneración nerviosa se ha explorado en varios estudios, a través de enfoques que implican inyección o modificación.
En comparación con los andamios convencionales de ingeniería de tejidos óseos, este enfoque, particularmente con la incorporación de factores de crecimiento nervioso, produce andamios con capacidad neuroatractiva. La incorporación de factores de crecimiento dentro del andamio ofrece potencial para lograr la regeneración sinérgica de componentes óseos y neurales. Sin embargo, la utilización de factores de crecimiento en la neuro-ingeniería de tejidos óseos enfrenta desafíos como costos elevados, actividad biológica inestable y posibles efectos adversos. La aplicación de altas dosis de factores de crecimiento en un intento de mejorar la eficacia terapéutica en el sitio de la fractura puede precipitar inflamación, formación de tumores y desarrollo óseo ectópico en regiones imprevistas, especialmente cuando se emplean en conjunto.
Péptidos Bioactivos
La incorporación de péptidos bioactivos con motivos proteicos activos en andamios ofrece una alternativa rentable al uso de factores de crecimiento. Las secuencias cortas de péptidos derivados de materiales naturales o sintéticos estimulan los receptores de superficie celular y regulan las vías de señalización.
Los péptidos derivados de factores de crecimiento como la osteopontina, BMP-2 y BMP-7 pueden incorporarse en andamios para promover la osteogénesis in vivo. Por ejemplo, un andamio de polímero PA66 modificado que contiene un péptido derivado de BMP-2 y QK (un péptido mimético de VEGF) ha reparado con éxito fracturas femorales severas en ratas SD. El tratamiento con péptido formador de hueso-1 (BFP-1), una secuencia peptídica de BMP-7, aumenta la expresión de genes osteogénicos en las CMMO, lo que lleva a una mayor formación de hueso in vivo que la inducida por los factores de crecimiento originales. Los péptidos derivados de la matriz extracelular que promueven la migración y proliferación celular también son herramientas efectivas en la ingeniería de tejidos óseos. Dos Santos et al. desarrollaron un hidrogel libre de factores de crecimiento que consiste en polipéptidos similares a la elastina (ELPs), poli(etilenglicol) (PEG) y un rango de concentraciones del péptido de adhesión IKVAV. Este hidrogel promueve la angiogénesis y la inervación durante la reparación ósea.
Los péptidos bioactivos también son útiles en la ingeniería de tejido nervioso. Se han utilizado conductos nerviosos que contienen péptidos bioactivos que imitan las funciones de BDNF y VEGF para reparar defectos del nervio ciático en ratas. Estos péptidos mejoran la regeneración nerviosa y promueven la penetración vascular, lo que lleva a la regeneración nerviosa y la recuperación funcional. En nervios periféricos, la laminina desempeña un papel crucial en la migración de células de Schwann y la extensión axonal. Un hidrogel de nanofibras de autoensamblaje de péptidos, dualmente funcionalizado con el motivo IKVAV derivado de laminina y el epítopo peptídico mimético de BDNF RGI, proporciona un microambiente tridimensional para las CS y neuritas, que se utilizó con éxito para unir un defecto de nervio ciático de 10 mm. La secuencia Arg-Gly-Asp (RGD), uno de los ligandos más potentes en proteínas extracelulares naturales, mejora la adhesión y proliferación de las CS y promueve el crecimiento axonal de los ganglios de la raíz dorsal cuando se incorpora en andamios de PCL.
En comparación con las proteínas, los péptidos tienen ventajas únicas. Su estructura química puede controlarse con precisión, son más tolerantes a los cambios de temperatura y pH, y son más convenientes de usar. Hasta la fecha, los péptidos bioactivos se han utilizado ampliamente en el campo de la regeneración nerviosa y la regeneración ósea, pero no se ha estudiado cómo utilizar estos péptidos en la neuro-ingeniería de tejidos óseos. Este enfoque proporciona nuevas oportunidades para la investigación y aplicación futuras.
Pequeñas Moléculas
Las pequeñas moléculas, refiriéndose a compuestos naturales o sintéticos con bajos pesos moleculares, ejercen efectos terapéuticos modulando las funciones celulares. Estas moléculas, caracterizadas por sus propiedades no cargadas o hidrofóbicas, pueden penetrar la bicapa fosfolipídica de la membrana celular.
Se ha descubierto que las moléculas osteoinductivas influyen en varias vías de señalización dentro de las células, incluyendo la señalización de BMP, la vía Hedgehog (Hh) y las vías de señalización Wnt/beta-catenina o AMP cíclico/proteína quinasa A (cAMP/PKA). Por ejemplo, se ha demostrado que la pequeña molécula SVAK-12 potencia la diferenciación osteogénica de mioblastos inducida por BMP-2 in vitro. Además, se ha descubierto que la inyección percutánea de SVAK-12 acelera la formación de callo de fractura femoral en ratas. Los efectos de las estatinas, medicamentos para reducir el colesterol, en la formación ósea también se han observado tanto in vitro como in vivo durante varios años. Investigaciones recientes han demostrado el potencial de la aspirina, un medicamento común para aliviar dolores menores, molestias y fiebres, en la promoción de la regeneración ósea.
Aunque el uso de pequeñas moléculas en la regeneración nerviosa periférica es limitado, muestran potencial para mejorar la viabilidad neuronal, apoyar el crecimiento axonal e influir en la diferenciación neuronal de las células madre. Por ejemplo, GSK-J1, LDN193189, SB431542, CHIR99021 y P7C3-A20 tienen potencial documentado para inducir la diferenciación neural de células madre. Además, se ha demostrado que pequeñas moléculas como LM22B-10, FK506, BT13 y los polisacáridos de Lycium barbarum (LBP) mejoran la regeneración nerviosa tanto in vivo como in vitro. Por otro lado, los medicamentos que compiten con los neurotransmisores que afectan negativamente la osteogénesis también pueden ser beneficiosos para la regeneración ósea. El propranolol, un bloqueador del receptor β-adrenérgico, compite con la NE liberada por nervios simpáticos hiperactivos, bloqueando eficazmente sus efectos negativos sobre la diferenciación osteogénica. De manera similar, la nifedipina, un bloqueador de canales de calcio, promueve la formación ósea al inhibir la liberación de NE.
Los medicamentos de molécula pequeña han generado un interés significativo como posibles sustitutos de los factores de crecimiento debido a su facilidad de síntesis, efectos reguladores y amplia aplicabilidad. Pueden facilitar la regeneración de tejidos modulando vías biológicas, aunque su uso en la regeneración nerviosa requiere una mayor investigación y validación clínica. No obstante, esto ofrece una vía prometedora para la reparación colaborativa en la ingeniería de tejidos nervio-hueso.
Fragmentos de ADN/ARN
Aunque tanto los factores de crecimiento como los péptidos bioactivos pueden estimular la regeneración ósea y nerviosa, la introducción exógena de estos factores a menudo resulta en una disminución de la actividad, una vida media corta y la necesidad de administración repetida de dosis altas. Para abordar estos desafíos, la implantación de fragmentos de ADN/ARN en andamios puede utilizarse como un enfoque alternativo para evitar el uso de altas concentraciones de factores de crecimiento.
La entrega de fragmentos de ADN se puede lograr a través de vectores virales o no virales para dirigir las células y modificar su expresión génica. Sin embargo, la integración permanente de secuencias génicas en el genoma huésped utilizando vectores virales como los retrovirales y lentivirales es indeseable debido a posibles efectos adversos. Los enfoques no virales se consideran más seguros, ya que tienen menor inmunogenicidad y ejercen solo efectos transitorios sobre la expresión génica en comparación con la entrega viral. La carga de ADN plasmídico (pADN) en andamios o nanopartículas catiónicas parece ser una solución potencial a la dificultad de transportar pADN cargado negativamente a través de las membranas celulares. La introducción de ADN plasmídico BMP-2 en defectos óseos puede proporcionar una fuente continua de factores de crecimiento para regular positivamente los genes relacionados con la formación ósea. Los plásmidos de VEGF y los plásmidos de NGF cargados en andamios óseos porosos impresos en 3D pueden reemplazar eficazmente las células semilla y los factores de crecimiento, induciendo una respuesta inmune mínima y promoviendo la regeneración ósea vascularizada y nerviosa. Además, la inyección de un plásmido que codifica el factor de crecimiento de fibroblastos 2 (FGF2) alrededor de los nervios periféricos también ha mostrado potencial para facilitar la regeneración del nervio ciático. Además, la entrega de plásmidos que codifican miR-200c utilizando nanopartículas de CaCO3 resultó en la reparación exitosa de defectos óseos craneofaciales.
Además de las secuencias de ADN, la entrega de ARN también puede emplearse para obstaculizar la traducción de secuencias de ARNm que impiden la regeneración ósea o nerviosa. Los microARN (miRNAs) son ARN no codificantes pequeños y naturales que regulan la expresión génica modulando procesos postranscripcionales. Se han identificado numerosos miRNAs como reguladores clave de los procesos neurobiológicos, incluyendo el crecimiento de neuritas, la sinaptogénesis y la plasticidad neural. La inyección de un hidrogel termosensible para la coadministración de microARN-222 y aspirina (hidrogel miR222/MSN/ASP) promovió la diferenciación neuronal de las CMMO y funcionó sinérgicamente con la aspirina para mejorar la osteogénesis. La carga de miR-29b en un andamio impreso en 3D con capacidad de liberación sostenida también demostró la promoción de la regeneración ósea, similar a los efectos de otras moléculas bioactivas en la ingeniería de tejidos óseos. De manera similar, se ha utilizado siRNA para silenciar genes específicos que inhiben la formación de osteocitos o facilitan la formación de osteoclastos con alta especificidad. El uso de siRNA dirigido a fidgetin-like 2 (FL2), un regulador negativo de la regeneración axonal, puede mejorar significativamente la recuperación funcional nerviosa.
La integración de fragmentos de ADN/ARN en andamios para facilitar la regeneración sinérgica de hueso y nervios es muy prometedora y justifica una mayor exploración.
Vesículas Extracelulares
Casi todos los tipos de células secretan vesículas extracelulares (VEs) que contienen múltiples factores de señalización, como proteínas, lípidos, ARNm, miRNAs y otros ARN no codificantes, lo que permite la comunicación entre células vecinas o distantes durante el proceso de curación natural. Estos ingeniosos portadores, específicamente aquellos derivados de CS, MSCs y macrófagos, que están asociados con la regeneración ósea y nerviosa, han sido investigados para uso terapéutico. La bicapa lipídica protege las cargas dentro de las VEs de la degradación en el entorno extracelular.
En el contexto de la regeneración ósea, la incorporación de exosomas derivados de células de Schwann en hidrogeles como plataforma multifuncional de neuromodulación puede orquestar el microambiente óseo a través de la inmunomodulación, la angiogénesis y la osteogénesis. De manera similar, Su et al. desarrollaron constructos de exosomas@aptámero (EA) acoplando aptámeros dirigidos a fosfatidilserina (PS) con exosomas de células de Schwann reparadoras, que se cargaron en la superficie de fibras electrohiladas para crear un periostio biomimético con la capacidad de promover la regeneración nerviosa y ósea. Además, la combinación de exosomas derivados de células de Schwann con andamios porosos de Ti6Al4V o hidrogeles ha demostrado mejorar eficazmente la eficacia de los andamios para la reparación de defectos óseos in vivo. De manera similar, se ha demostrado que la incorporación de VEs derivadas de MSCs en andamios mejora la reparación ósea en defectos óseos craneales de roedores y promueve la osteogénesis incluso en sitios ectópicos. Los andamios porosos de PLA 3D recubiertos con MSC-Exo han mostrado efectos inmunorreguladores y osteogénicos, reduciendo la expresión de marcadores proinflamatorios y promoviendo la diferenciación osteogénica. Además, los exosomas derivados de macrófagos pueden promover la diferenciación de CMMO hacia un destino osteoblástico a través de microARN-21a-5p. El colágeno mineralizado biomimético puede mediar la regeneración ósea endógena reclutando MSCs y aumentando la secreción de vesículas extracelulares por los macrófagos.
También se ha demostrado que las vesículas extracelulares secretadas por varias células promueven la regeneración nerviosa. Por ejemplo, las CS se comunican con los axones vecinos durante los procesos regenerativos a través de exosomas, que aumentan significativamente la regeneración axonal in vitro y mejoran la regeneración después de una lesión del nervio ciático in vivo. Se ha descubierto que los exosomas derivados de CMMO promueven la regeneración de nervios periféricos a través de la regulación mediada por miRNA de genes relacionados con la regeneración de manera dependiente de la dosis. Los exosomas de macrófagos, que contienen complejos activos de NADPH oxidasa 2 (NOX2), pueden ser absorbidos por los DRG a través de la endocitosis durante la regeneración nerviosa, desempeñando un papel necesario en el crecimiento de neuritas al mediar la señalización de ROS.
Dado que las VEs se han empleado tanto en la reparación ósea como nerviosa, los investigadores dirigen actualmente sus esfuerzos hacia la identificación de VEs que promuevan la curación sinérgica en el hueso y los nervios intraboneales.
Estrategias Innovadoras en Neuro-Ingeniería Ósea
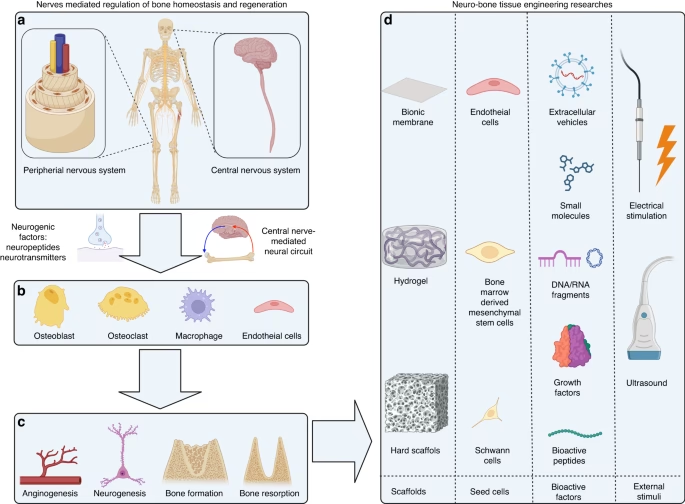
Como una rama potencial de la ingeniería de tejidos óseos, la neuro-ingeniería de tejidos óseos combina la ingeniería de tejidos neurales y la ingeniería de tejidos óseos, enfatizando la importancia de la reparación neural en la regeneración ósea y la comunicación cruzada entre hueso y nervios durante este proceso. Se han explorado varias estrategias, incluyendo:
- Controlar la morfología y las estructuras de la superficie de los andamios.
- Incorporar factores neurotróficos y neuropéptidos en los andamios.
- Utilizar materiales dopados con iones para mejorar la regeneración nerviosa.
- Agregar aditivos conductores para facilitar la señalización neural.
- Construir sistemas de cocultivo celular para promover las interacciones entre células neurales y óseas.
- Aplicar estímulos de campo externos para estimular el crecimiento y la respuesta neural.
Morfología/Micro-Nanoestructuras de Superficie
En el campo de la ingeniería de tejidos, el uso de andamios microestructurados ha atraído una atención significativa para promover la regeneración ósea y nerviosa. Los investigadores se han centrado en imitar morfologías anatómicas complejas e incorporar las propiedades físicas deseadas en los diseños de andamios. Se ha descubierto que la rigidez, rugosidad y porosidad de los materiales óseos influyen en la proliferación y diferenciación neuronal de las células madre.
Notablemente, la diferenciación neural y la diferenciación osteogénica de las células madre difieren, y algunos procesos se favorecen más en matrices más blandas. Incluso sutiles diferencias en la rigidez pueden llevar a la diferenciación de células madre neurales en diferentes tipos de neuronas, como neuronas, oligodendrocitos y astrocitos. Por ejemplo, cuando la rigidez del material del sustrato está por debajo de 500 Pa, las células madre neurales tienden a diferenciarse en neuronas, mientras que los materiales más rígidos promueven la diferenciación de astrocitos u oligodendrocitos. Sin embargo, es importante tener en cuenta que los materiales excesivamente blandos pueden dificultar la diferenciación de células neurales. Por lo tanto, determinar el nivel óptimo de rigidez para los biomateriales óseos es crucial para mejorar el crecimiento y la actividad de las células óseas y neurales en los biomateriales óseos diseñados.
Las células neuronales poseen la capacidad de sentir la topografía de la superficie y exhiben diversas respuestas a diferentes niveles de rugosidad y micropatrones. Cuando se cultivan células de neuroblastoma humano en sustratos de oro, la viabilidad y la capacidad de extensión celular disminuyen significativamente a medida que aumenta la rugosidad de la superficie desde plana hasta una rugosidad promedio de aproximadamente 100 nm. Esta disminución puede atribuirse al aumento de la hidrofilicidad de las superficies rugosas, que reduce la adsorción de proteínas de adhesión celular neuronal hidrofóbicas. Además, las neuronas cultivadas en sustratos rugosos exhiben polaridad interrumpida del citoesqueleto de actina, condensación nuclear y funcionalidad deteriorada. Investigaciones recientes han proporcionado evidencia de que las nanofibras orientadas pueden replicar las señales topográficas de la fibronectina, permitiendo la manipulación precisa de la alineación celular y la manifestación fenotípica. Los andamios compuestos de nanofibras de fibroína de seda y diseñados para imitar la estructura de la matriz extracelular no solo promueven el crecimiento direccional de las neuronas, sino que también apoyan el crecimiento, la migración y la organización de las células endoteliales. Además, se ha descubierto que los microcanales orientados uniformemente longitudinalmente apoyan el crecimiento nervioso, y las matrices de nanopilares en forma de anillo pueden atraer los nervios cercanos para que crezcan a lo largo de las matrices. Li et al. fueron pioneros en el uso de whitlockita dopada con neodimio (Nd@WH) integrada en una membrana de nanofibras de poli(caprolactona) de doble capa con una estructura orientada en la superficie. El micropatrón de la estructura orientada de la capa interna proporciona espacio suficiente para la disposición celular, la formación ósea, la neurogénesis y la angiogénesis. Por lo tanto, el control preciso sobre la rugosidad y disposición a nanoescala de los biomateriales óseos es crítico para regular el crecimiento de las células neuronales en la matriz ósea.
Otro factor crucial que influye en el crecimiento axonal de las células neuronales es la estructura porosa de los biomateriales. Los sustratos porosos proporcionan una mayor área superficial, lo que los hace más propensos a unirse con proteínas neurogénicas. Los estudios han demostrado que las neuronas DRG tienen más probabilidades de desarrollar axones cuando se cultivan en sustratos mesoporosos con poros de aproximadamente 300 nm de tamaño que cuando se cultivan en superficies planas. De manera similar, las células de neuroblastoma exhiben una morfología de extensión y densidad celular mejoradas en sustratos de silicio nanoporosos, con una mejora adicional observada a medida que el tamaño de los poros disminuye de 20 nm a 5 nm. Sin embargo, no hay una diferencia significativa en el crecimiento axonal de las neuronas DRG en comparación con una superficie plana cuando el tamaño de los poros aumenta al rango de micrómetros.
Debido a la distribución heterogénea de vasos sanguíneos y nervios dentro del tejido óseo, el hueso natural exhibe una heterogeneidad inherente que es difícil de replicar. La simulación de estructuras naturales a macroescala proporciona un enfoque factible para satisfacer las necesidades regenerativas de múltiples tejidos. Por ejemplo, la curación del aloinjerto puede acelerarse incorporando constructos modificados con hidrogel degradable por metaloproteinasa de matriz (MMP), que imitan el proceso de curación mediado por el periostio natural al apoyar la migración de células endógenas y la formación de redes neurovasculares. De manera similar, la impresión de un andamio biocerámico en forma de árbol puede crear, a través de la programación precisa de los intervalos de las palas y los ángulos de divergencia, un microambiente espacial que facilita la comunicación cruzada multicelular y la regeneración ósea inervada. Se ha demostrado que los andamios 3D que imitan el sistema de Havers inducen diferenciación osteogénica, angiogénica y neurogénica in vitro al mismo tiempo que aceleran el crecimiento interno de vasos sanguíneos y la formación de hueso nuevo in vivo. Notablemente, los andamios de nanofibras de fibroína de seda que simulan la estructura de la matriz extracelular pueden inducir el crecimiento direccional de las neuronas y facilitar el crecimiento, la migración y la disposición de las células endoteliales.
Modificación con Factores Neurotróficos/Neuropéptidos
Numerosos estudios han investigado exhaustivamente el papel crucial de la reinervación en la regeneración ósea mediante la administración de factores de crecimiento neuronal, con un enfoque particular en NGF y BDNF. Además, se ha descubierto que la aplicación de un andamio nanofibroso coaxial que contiene NGF crea un microambiente neurotrófico que acelera la diferenciación neural de las células madre, mejorando así el proceso de osteogénesis. Durante este proceso, los nervios regenerados inducidos por NGF sostenido pueden actuar como mediadores en la formación de centros de osificación a través de la vía de señalización NGF-TrkA. Estos nervios sensoriales también exhiben un efecto regulador sobre la formación ósea excesiva inducida por BMP-2. Investigaciones previas han demostrado que la administración de BDNF mediante esponjas de colágeno o hidrogeles de ácido hialurónico resultó en una mayor formación ósea en comparación con los grupos de control. Por lo tanto, la carga de varios factores neurotróficos y factores de crecimiento en andamios para la ingeniería de tejidos óseos representa un método eficaz para tratar la osteonecrosis y los defectos óseos segmentarios grandes. Sin embargo, es importante reconocer que estos factores bioactivos exhiben propiedades farmacocinéticas deficientes y son susceptibles a la degradación de proteínas, lo que limita su potencial como agentes terapéuticos.
Es ampliamente reconocido que los factores neurogénicos, incluyendo neurotransmisores y neuropéptidos, desempeñan papeles cruciales en la mediación de la interacción entre nervios y hueso durante el proceso de regeneración ósea. En consecuencia, la incorporación de factores neurogénicos en materiales modificados puede imitar los efectos positivos de los nervios en la regeneración ósea. Los péptidos relacionados con la osteogénesis, en comparación con varios factores de crecimiento macromoleculares, ofrecen varias ventajas, como alta eficiencia, facilidad de síntesis, bajo costo e implantación conveniente en la matriz extracelular. Estos péptidos promueven la adhesión celular y aceleran la mineralización. Además, los neuropéptidos poseen baja toxicidad, alta actividad biológica y alta especificidad, lo que los hace altamente adecuados para la traslación clínica. Entre los neuropéptidos, el CGRP es ampliamente reconocido por sus propiedades anabólicas, lo que lo convierte en un candidato favorable para su introducción en sistemas de regeneración ósea para reemplazar temporalmente la función de los nervios durante las primeras etapas de la curación ósea. Sin embargo, la regeneración ósea es un proceso a largo plazo que necesita la participación continua de factores de crecimiento en cada etapa. Por lo tanto, el diseño de andamios bioactivos gira en torno a mantener la liberación controlada de péptidos altamente activos. Alternativamente, se pueden hacer esfuerzos para integrar células transgénicas en el andamio para establecer una fuente estable de neuropéptidos. Si bien la liberación estable de neuropéptidos es crucial para promover la osteogénesis, la estrategia sin células parece ser más práctica y factible para la aplicación y el desarrollo que el uso de andamios que contienen células transgénicas, ya que el enfoque sin células evita eficazmente el rechazo inmune y las preocupaciones éticas. Además del CGRP, otros neuropéptidos, como el VIP, el SP y la Sema 3 A, han mostrado potencial para su aplicación en la ingeniería de tejidos óseos. Si bien se ha demostrado que la introducción de factores neurogénicos exógenos mejora la reparación de defectos óseos, es importante tener en cuenta que sus efectos biológicos son difíciles de controlar debido al complejo entorno humoral y la expresión generalizada de receptores. La administración inexacta y continua puede provocar efectos secundarios inesperados. Por lo tanto, se espera que los futuros materiales bioactivos imiten dinámicamente los efectos biológicos de los nervios en el hueso durante el proceso de curación ósea.

Materiales Dopados con Iones
La incorporación de iones bioactivos en materiales ha mostrado resultados prometedores para mejorar los marcadores neurogénicos y osteogénicos y activar la neuromodulación en el hueso. El papel de iones metálicos como el ion magnesio (Mg2+), el ion zinc (Zn2+) y el ion cobre (Cu2+) en el crecimiento y la remodelación ósea se ha reconocido desde finales de la década de 1990. Durante las últimas décadas, la investigación ha revelado los efectos reguladores de los cationes en la osteogénesis, la osteoclastogénesis, la angiogénesis y las respuestas inmunes. Sin embargo, la participación del sistema nervioso en la formación de hueso nuevo inducida por iones metálicos solo ha ganado atención recientemente. Diferentes iones desempeñan papeles cruciales en diversas funciones bioquímicas que son esenciales para las diferentes etapas de la regeneración ósea. Su presencia e influencia ayudan a mantener un delicado equilibrio entre las células óseas y neurales. Entre los iones metálicos, el magnesio ha mostrado buenas capacidades de regeneración ósea y nerviosa en estudios recientes. Como elemento comúnmente presente en la naturaleza, el magnesio es abundante en el cuerpo humano. Los implantes de magnesio biodegradables exhiben una excelente biocompatibilidad y bioactividad en comparación con otros polímeros sintéticos.
Estudios recientes han revelado que el Mg2+ liberado de los implantes puede promover la secreción de CGRP de las terminaciones nerviosas sensoriales dentro del hueso. Además, se descubrió que el Mg2+, el Zn2+ y el Cu2+ activan la interocepción esquelética modulando la actividad de los macrófagos. También se descubrió que los iones Zn2+ y Cu2+ desempeñan papeles cruciales en la modulación de la actividad biológica de los factores neurotróficos, que son importantes para la supervivencia y regeneración nerviosa. El tratamiento con Zn2+ en cultivos de células neuronales se ha asociado con un aumento de la unión a BDNF y con una mayor proliferación, mientras que la presencia de Cu2+ afecta sinérgicamente la actividad de las células nerviosas con NGF. Además de los iones metálicos, otros iones inorgánicos también desempeñan un papel en la regeneración ósea inducida por nervios. Por ejemplo, el silicio, un elemento esencial para el cuerpo humano, es necesario para la homeostasis ósea. El vidrio de silicato se ha utilizado como material bioactivo debido a sus efectos positivos en osteoblastos, osteoclastos y células endoteliales. Sin embargo, un estudio reciente proporcionó una nueva perspectiva sobre la regeneración ósea inducida por materiales a base de silicato al desencadenar la liberación de Sema3A de los DRG, lo que promovió la regeneración de defectos femorales en ratas. Los materiales sustitutos óseos actuales ofrecen principalmente propiedades de curación osteoconductora, y muchas estrategias avanzadas de ingeniería de tejidos aún no son prácticas para el uso clínico diario. El examen exhaustivo de los mecanismos fisiológicos de varios iones y su impacto en la regeneración del tejido óseo indica que la incorporación de ciertos iones en los sustitutos óseos existentes puede modificar potencialmente la inflamación, la respuesta inmune, la regeneración ósea y la regeneración nerviosa. La utilización y combinación de iones con biomateriales existentes está influenciada por varios factores. Se ha demostrado que la concentración de iones metálicos liberados es crítica para el proceso de formación ósea. Por lo tanto, es ventajoso tener estos iones cerca del biomaterial implantado, facilitando la regeneración ósea directamente en el sitio del implante.
Nanopartículas Electroactivas
Numerosas funciones fisiológicas están vinculadas a campos eléctricos (CE) endógenos. Estas funciones abarcan el desarrollo y la organización de tejidos, así como su regeneración después de lesiones. Dada la sensibilidad de las células del linaje óseo y las células neurales a la estimulación eléctrica, el empleo de materiales electroactivos podría resultar beneficioso para facilitar la reparación tanto del tejido óseo como del nervioso.
Ha pasado más de un siglo desde la primera síntesis de fósforo negro (BP), que es reconocido como el alótropo más estable del fósforo. Los nanomateriales de BP poseen propiedades ópticas y mecánicas excepcionales, junto con conductividad eléctrica, biocompatibilidad y biodegradabilidad, lo que los hace muy adecuados para diversas aplicaciones biomédicas. Al incorporar BP en un periostio biomimético o hidrogel, se podría estimular la regeneración de nervios y huesos, creando un microambiente favorable para la reparación de tejidos. Mediante la aplicación de estímulos eléctricos a CMMO cultivadas en hidrogeles de BP@PDA, se han observado mejoras significativas en la migración celular y la diferenciación neural dentro de andamios 3D. Además, la liberación continua de iones de fósforo del fósforo negro durante la degradación promueve activamente la mineralización ósea y la diferenciación osteogénica de las células madre mesenquimales.
El polipirrol (PPy), un polímero orgánico, se forma a través de la polimerización oxidativa del pirrol. Debido a su excelente conductividad y propiedades antioxidantes, el PPy muestra un potencial significativo para aplicaciones en ingeniería de tejidos. Se ha descubierto que la modificación de andamios con PPy mejora sus propiedades mecánicas, conductividad eléctrica, osteoconductividad y capacidades de administración de fármacos, y ejerce un efecto positivo en el crecimiento y la diferenciación osteogénica de las células madre de médula ósea. Además, se ha informado que los hidrogeles que incorporan PPy exhiben bioactividad, conductividad eléctrica y propiedades antioxidantes beneficiosas, que ayudan a crear un entorno 3D neuroprotector y neuroinducible para las CMMO encapsuladas, acelerando así la recuperación de una lesión de la médula espinal.
La polianilina (PAni), un polímero semiflexible en forma de varilla, demuestra una conductividad excepcional y sirve como semiconductor orgánico. En consecuencia, los andamios de PLA que incorporan PAni bien distribuida pueden ofrecer un entorno óptimo para el crecimiento y la diferenciación de las CMMO debido a sus propiedades conductoras. Además, el recubrimiento de láminas de titanio médico con PAni puede mejorar sinérgicamente la proliferación celular y la osteogénesis a través de la estimulación eléctrica. Mediante la complejación de nanopartículas de oro con PAni, se pueden administrar nanocompuestos reforzados intracelularmente e inducir la diferenciación de células madre en linajes de células neurales bajo estimulación eléctrica utilizando un electroporador. Además, los hidrogeles compuestos que contienen carboximetil quitosano modificado con PAni, cuando se incorporan dentro de un conducto nervioso, promovieron significativamente la regeneración del nervio ciático y la proliferación de células de Schwann en comparación con los conductos de quitosano huecos.
Los materiales a base de carbono, como el grafeno y los nanotubos de carbono, se utilizan comúnmente como aditivos conductores en la ingeniería de tejidos óseos y nerviosos debido a sus propiedades mecánicas favorables, la falta de citotoxicidad hacia los osteoblastos y la actividad antibacteriana intrínseca. La incorporación de óxido de grafeno reducido (rGO) en hidrogeles aumentó la conductividad eléctrica de los andamios, mejoró la diferenciación osteogénica y neurogénica de las células cargadas y aceleró la regeneración ósea modulando el microambiente inflamatorio diabético. De manera similar, los andamios o conductos nerviosos fabricados combinando PLC y nanotubos de carbono se han aplicado para soportar el crecimiento interno de hueso subcondral y, en consecuencia, la reparación de defectos del nervio ciático de 10 mm en ratas.
En general, los andamios basados en materiales conductores ofrecen el potencial de aprovechar los beneficios de los campos eléctricos biológicos en el tejido óseo y nervioso al mismo tiempo que proporcionan un sustrato que promueve una proliferación celular más rápida que la lograda con materiales sintéticos convencionales. Sin embargo, se necesita más investigación para explorar las capacidades a largo plazo de los andamios óseos conductores y electroactivos implantados.
Sistemas de Cocultivo Celular
Los tejidos fisiológicos consisten en sistemas multicelulares que comprenden diferentes tipos de células que interactúan entre sí para facilitar la viabilidad, la proliferación y el desarrollo. En los últimos años, la ingeniería de tejidos se ha orientado hacia los cocultivos, ya que ofrecen una representación más relevante fisiológicamente de los tejidos naturales, tanto física como biológicamente. En comparación con el cultivo celular tradicional en monocapa, los sistemas de cocultivo imitan estrechamente el entorno in vivo, permitiendo una mejor observación de las interacciones célula-célula, donde las células sirven como fuentes de estímulo para proporcionar las señales deseadas a otros tipos celulares.
El cocultivo de células neurales con células madre pluripotentes ha mostrado efectos positivos en la neurogénesis, ofreciendo una estrategia alternativa para la reinervación. La introducción de CS y células madre derivadas de tejido adiposo (ADSCs) cocultivadas como células semilla en un andamio de fibroína de seda (SF)/colágeno para construir un conducto nervioso diseñado ha demostrado mejorar los microambientes regenerativos y acelerar la regeneración nerviosa. La combinación de células madre con CE en cocultivo no solo promueve el crecimiento de axones DRG, sino que también mejora la orientación neuronal, reduciendo potencialmente el riesgo de enredos axónicos e inhibiendo la formación de neurofibromas. El cocultivo de CS y células madre neurales (NSCs) en conductos nerviosos de laminina-quitosano-poli-láctico-co-glicólico (laminina-quitosano-PLGA) ha mostrado potencial para promover la regeneración nerviosa lesionada en ratas.
En el contexto de la regeneración ósea, a menudo se emplea el cocultivo de CE con osteoblastos para inducir la formación de capilares, mientras que las CE afectan de manera similar la expresión fenotípica y la proliferación de los osteoblastos. Se ha informado que los cocultivos de CMMO y CE mejoran la expresión de marcadores osteogénicos y mejoran la proliferación de células madre. Además, las matrices extracelulares derivadas de sistemas de cocultivo de células madre mesenquimales (MSCs) y células endoteliales de vena umbilical humana (HUVECs) han mostrado mejoras significativas en la proliferación celular en comparación con la lograda en andamios de PCL solo, manteniendo propiedades físicas y mecánicas similares. Cuando se cocultivan preosteoblastos con células progenitoras neurales en un hidrogel nanocompuesto 3D que incorpora whitlockita, se mejoran tanto las actividades neurales como osteogénicas del sistema de cocultivo.
Las células madre ofrecen una versatilidad notable en la ingeniería de tejidos, permitiendo la creación de tejidos y órganos complejos con un potencial regenerativo mejorado. Sin embargo, las preocupaciones éticas, las restricciones regulatorias, los riesgos de rechazo inmune y la posible tumorigenicidad plantean desafíos significativos. En contraste, la integración de múltiples tipos celulares en la ingeniería de tejidos promete replicar las interacciones tisulares naturales y mejorar la funcionalidad, pero implica complejidades en el manejo de diversas poblaciones celulares y en la obtención de aprobación regulatoria. Sin embargo, la creciente popularidad de los sistemas de cocultivo en la ingeniería de tejidos resalta la importancia de abordar desafíos como la selección celular adecuada, la optimización de las proporciones y números celulares, y el refinamiento de los medios de cultivo para impactar significativamente los resultados experimentales. Además, garantizar la supervivencia de estas células semilla en condiciones hipóxicas in vivo antes de que se establezca una vascularización completa sigue siendo crucial para el éxito de las empresas de ingeniería de tejidos.
Estímulos de Campo Externos
El sistema nervioso puede responder a la estimulación externa, lo que lleva a cambios en el comportamiento celular que pueden aprovecharse con fines terapéuticos. La investigación actual se centra en iniciar señales de reparación neurogénicas endógenas. Un neuropéptido anabólico ampliamente reconocido, el CGRP, ha mostrado potencial para mejorar la reparación ósea cuando se mejora su expresión en el microambiente. Típicamente, la liberación de CGRP aumenta en respuesta al calor, el pH bajo y los agonistas de TRPV1. Sin embargo, estas condiciones microambientales pueden afectar la curación ósea normal, lo que hace que no sea práctico trasladar estas estrategias directamente. Como alternativas, se han desarrollado estrategias como la estimulación eléctrica y el ultrasonido pulsado de baja intensidad (LIPUS). Estos enfoques tienen como objetivo estimular el sistema nervioso y obtener efectos beneficiosos en la reparación ósea sin la necesidad de condiciones microambientales extremas.
La estimulación eléctrica (EE) es una modalidad de fisioterapia ampliamente investigada que facilita la reparación y regeneración de tejidos dañados, incluyendo hueso, músculo, piel y nervio. Sin embargo, los parámetros y estrategias de estimulación eléctrica en la neuro-ingeniería de tejidos óseos pueden ser diferentes de los utilizados solo para la regeneración ósea o nerviosa. En estudios previos, se aplicaron campos eléctricos o electromagnéticos directamente en el sitio de la fractura para modular funciones biológicas locales involucradas en el proceso de curación. Para la regeneración ósea, los investigadores suelen utilizar parámetros de estimulación eléctrica específicos, como una frecuencia de 15 hercios, una intensidad de campo eléctrico de 200 mV·mm−1 y un tiempo de tratamiento en el rango de 2–8 h. Para optimizar la regeneración del tejido neural, los ajustes de parámetros para la estimulación eléctrica tienen como objetivo regular el crecimiento y la transducción de señales de las células nerviosas. Por ejemplo, las neuronas hipocampales primarias de ratón y las células PC-12 cultivadas en un andamio con estimulación eléctrica óptima (100-150 mV·cm−1 durante 1 h diaria) exhibieron un crecimiento aumentado tanto de neuritas como de microfibras. Sin embargo, las estrategias de estimulación eléctrica en la neuro-ingeniería de tejidos óseos se centran principalmente en estimular las células nerviosas para regular la síntesis de neuropéptidos específicos, como el CGRP. Se informó que la aplicación de un voltaje de estimulación máximo que no causaba una contracción significativa del músculo inervado (250 mV, 90 μs, 150 Hz, 61.3 μA) mejoró la expresión de CGRP en las neuronas DRG. La implantación de electrodos (10 V, 500 μs y 10 Hz) en el DRG lumbar mejoró la inervación del área de fractura femoral en ratas, estimuló la biosíntesis y liberación de CGRP y, en última instancia, aceleró la curación de la fractura. Estos estudios demostraron que se puede utilizar una amplia gama de parámetros de estimulación eléctrica para estimular las neuronas CGRP+. El uso de los parámetros y estrategias de estimulación eléctrica mencionados anteriormente es prometedor para el futuro desarrollo de implantes con campos eléctricos incorporados que puedan promover la regeneración ósea y nerviosa a través de campos eléctricos y administrar estimulación eléctrica al DRG para promover la regeneración ósea mediada por CGRP a través de la neuromodulación. Así, estos hallazgos proporcionan información valiosa sobre el potencial terapéutico de la neuro-ingeniería de tejidos óseos.
El ultrasonido pulsado de baja intensidad (LIPUS) es un método de fisioterapia comúnmente utilizado que ha demostrado potencial para promover la curación de fracturas. A diferencia de la energía de ultrasonido de alta intensidad, el LIPUS no es térmico ni destructivo, lo que lo convierte en un enfoque prometedor para la reparación y regeneración de tejidos óseos. Estudios recientes han demostrado que el LIPUS puede mejorar eficazmente la proliferación de células de Schwann y la remielinización axonal, promoviendo así la regeneración nerviosa. Además, se ha demostrado que el LIPUS mejora la inervación sensorial positiva para CGRP, lo que contribuye a la osteogénesis, como se observó en un modelo animal de fusión espinal. Sin embargo, en un modelo de rata de fractura tibial después de la resección del nervio ciático, el LIPUS no promovió la curación de la fractura. Estos hallazgos sugieren que los efectos positivos del LIPUS en la regeneración ósea pueden estar mediados por la promoción de la secreción de CGRP de las fibras nerviosas sensoriales. Además, se ha descubierto que el LIPUS aumenta la expresión de ciclooxigenasa 2 (COX-2), una enzima clave involucrada en la síntesis de PGE2, en los osteoblastos. Los niveles elevados de PGE2 en el microambiente local pueden activar la interocepción esquelética, acelerando así la regeneración ósea a través de vías neuronales.
La neuro-ingeniería de tejidos óseos representa un campo de vanguardia que busca superar las limitaciones de las técnicas de reparación ósea convencionales. Al integrar la comprensión de la compleja interacción entre el tejido nervioso y el óseo con avances en materiales, células y factores bioactivos, esta disciplina abre nuevas vías para la restauración funcional de defectos óseos extensos. Aunque persisten desafíos en la traslación clínica y la optimización de estrategias, el potencial para revolucionar el tratamiento de lesiones y enfermedades óseas es inmenso, ofreciendo esperanza para una regeneración ósea más efectiva y completa.
Preguntas Frecuentes
¿Qué es exactamente la neuro-ingeniería de tejidos óseos?
Es un campo de la ingeniería de tejidos que se enfoca en la regeneración de defectos óseos considerando y promoviendo activamente la regeneración y función de los nervios dentro del tejido óseo, aprovechando la interacción sinérgica entre nervios y hueso para mejorar los resultados regenerativos.
¿Por qué son importantes los nervios en la regeneración ósea?
Los nervios están ampliamente presentes en el hueso e influyen en su regeneración. Proporcionan soporte para la formación de vasos sanguíneos y, a través de la liberación de factores neurotróficos y neuropéptidos, coordinan el crecimiento de células óseas y promueven la reparación.
¿Qué tipos de materiales se utilizan en los andamios para esta ingeniería?
Se utilizan diversos materiales, incluyendo polímeros naturales (como colágeno) y sintéticos (como PLA), materiales inorgánicos (como cerámicas bioactivas e iones metálicos como magnesio) y, a menudo, materiales compuestos que combinan las propiedades beneficiosas de polímeros e inorgánicos.
¿Qué son las células semilla en este contexto?
Las células semilla son células que se incorporan a los andamios para promover la regeneración. En la neuro-ingeniería ósea, esto incluye células que pueden diferenciarse en tejido óseo (como células madre mesenquimales de médula ósea) y células que apoyan la regeneración nerviosa (como células de Schwann y células endoteliales).
¿Cómo se utilizan los factores bioactivos acelulares?
Factores como factores de crecimiento (ej. BMPs, NGF), péptidos bioactivos, pequeñas moléculas, fragmentos de ADN/ARN y vesículas extracelulares se incorporan en los andamios para proporcionar señales moleculares que estimulan la diferenciación, proliferación y comunicación celular, mejorando la regeneración de tejidos óseos y nerviosos.
¿Qué estrategias innovadoras se están explorando?
Las estrategias incluyen el diseño de la superficie y microestructura del andamio, la modificación con factores neurotróficos, el uso de materiales dopados con iones, la incorporación de materiales electroactivos, la creación de sistemas de cocultivo celular y la aplicación de estímulos de campo externos como la estimulación eléctrica o el ultrasonido pulsado de baja intensidad.
Si quieres conocer otros artículos parecidos a Neuro-Ingeniería Ósea: Reparando Huesos con Nervios puedes visitar la categoría Neurociencia.
