El traumatismo craneoencefálico (TCE) es una de las principales causas de mortalidad e incapacidad a largo plazo en todo el mundo. Esta lesión cerebral no es un evento estático, sino que desencadena una patología dinámica y compleja que evoluciona en dos fases: una primaria, inmediatamente posterior al impacto mecánico, y una secundaria, que puede durar minutos o días e implica una cascada de eventos moleculares y celulares devastadores. Estos incluyen estrés oxidativo, disfunción mitocondrial, neuroinflamación, edema y muerte neuronal. Además, una característica crucial de esta lesión es la disrupción de la barrera hematoencefálica (BHE), que normalmente protege el cerebro pero cuya alteración complica la entrega de terapias.
Actualmente, no existen fármacos aprobados específicamente por la FDA para el TCE. Los tratamientos disponibles se enfrentan a limitaciones significativas, principalmente debido a la compleja patología de la lesión y la presencia de la BHE, que restringe severamente el acceso de micro y macromoléculas al sitio dañado. Esto genera una necesidad urgente de enfoques terapéuticos innovadores con estrategias de entrega efectivas. La ingeniería de tejidos, que involucra el uso de biomateriales, emerge como una alternativa prometedora.
¿Qué son los Biomateriales y Por Qué son Cruciales para el Cerebro?
Los biomateriales son sustancias diseñadas para interactuar con sistemas biológicos con un propósito médico. En el contexto del TCE y otras lesiones neurológicas, buscan reparar el tejido dañado, servir como andamiaje para el crecimiento celular, o actuar como vehículos para la entrega controlada de fármacos y células terapéuticas. El cerebro es un tejido único: extremadamente delicado, blando y elástico, con una composición celular heterogénea. Esto impone requisitos de diseño muy específicos para los biomateriales destinados a su uso cerebral.
Los principios clave para los biomateriales cerebrales incluyen la biocompatibilidad con el sensible tejido neural, la coincidencia de propiedades mecánicas (rigidez similar al tejido cerebral para evitar gliosis o inestabilidad), la mínima hinchazón para no aumentar la presión intracraneal, y la biodegradabilidad y reabsorbibilidad para evitar inflamación crónica y daño neuronal a largo plazo. Además, deben ser capaces de modular la respuesta inmune y, dependiendo de su uso, promover la adhesión y supervivencia celular o controlar la liberación de fármacos.
Los biomateriales pueden derivarse de fuentes naturales o sintéticas. Los naturales, como el ácido hialurónico (AH), el colágeno o el quitosano, a menudo imitan la matriz extracelular (MEC) nativa, ofreciendo alta bioactividad y buena biocompatibilidad. Sin embargo, pueden variar entre lotes y plantear riesgos inmunogénicos o de patógenos. Los sintéticos, como el PEG o el PLGA, ofrecen mayor estabilidad, control en la fabricación y menor riesgo de respuesta inmune, pero pueden carecer de bioactividad intrínseca, lo que a menudo requiere su funcionalización con moléculas biológicas.
| Propiedad | Biomaterial Sintético | Biomaterial Natural |
|---|---|---|
| Fuente | Sintetizado artificialmente | Fuentes biológicas |
| Biodegradabilidad | Variable, controlable | Naturalmente degradable |
| Inmunogenicidad | Generalmente baja | Potencial respuesta inmune |
| Propiedades Mecánicas | Personalizable para necesidades específicas | Variable |
| Biocompatibilidad | Reducida, puede ser optimizada | Buena biocompatibilidad |
| Factores de Crecimiento | Liberación controlada | Potencial liberación endógena |
| Ejemplos | Poli-anhídridos, poli-ortoésteres, PEG | Colágeno, quitosano, ácido hialurónico |
Tipos Prometedores de Biomateriales para el TCE
Entre la variedad de biomateriales investigados, los hidrogeles, los péptidos autoensamblables y las nanofibras electrohiladas han mostrado un potencial particular para el tratamiento del TCE.
Hidrogeles: Estos materiales están compuestos principalmente por agua (10-20% del peso total) y forman redes poliméricas tridimensionales. Su alta hidrofilia les permite transportar moléculas solubles, nutrientes, oxígeno y fármacos, vital para mantener células endógenas o implantadas. Mimetizan las propiedades físicas de los tejidos nativos, como el alto contenido de agua y la elasticidad, y su porosidad y capacidad de ajuste de forma les permiten rellenar cavidades irregulares dejadas por la lesión. Pueden ser covalentemente entrecruzados (más estables pero a menudo rígidos) o autoensamblados (más deformables). La mayoría de los hidrogeles naturales utilizados en ingeniería de tejido cerebral derivan de polisacáridos y glicosaminoglicanos como el AH y el colágeno. Los hidrogeles sintéticos, como los basados en PEG, son químicamente estables pero requieren funcionalización para mejorar la adhesión celular.
Péptidos Autoensamblables (SAPs): Son un tipo de hidrogel autoensamblado compuesto por unidades repetitivas de aminoácidos que forman estructuras de doble hoja beta en agua. Su naturaleza blanda y deformable les permite adaptarse a la forma de la lesión al ser inyectados. Una ventaja clave es la capacidad de modificar los SAPs añadiendo motivos funcionales (angiogénicos, promotores de crecimiento, neurotróficos, adhesivos a la MEC) para dirigir respuestas biológicas específicas. Los andamios de nanofibras de péptidos autoensamblables (SAPNs) se forman bajo condiciones fisiológicas y presentan alto contenido de agua, alta porosidad y señalización celular mejorada. RADA16-I es un SAPN muy estudiado que ha demostrado promover la regeneración en modelos de lesión cerebral.
Nanofibras Electrohiladas: Se crean estirando una solución polimérica viscoelástica en un campo eléctrico para formar una malla de nanofibras. Su principal ventaja es que imitan la disposición jerárquica de las fibrillas de la MEC nativa (colágeno, laminina), lo que las hace interesantes para la ingeniería de tejidos. Presentan una alta relación superficie-volumen, alta porosidad y propiedades mecánicas similares a la MEC, lo que mejora la adhesión celular, la carga de fármacos y la respuesta a estos. Pueden guiar el crecimiento axonal y, aunque limitan la migración celular por sí solas, esta puede mejorarse incorporándolas en hidrogeles. Materiales naturales (colágeno, quitosano) y sintéticos (PLGA, PCL) se utilizan para su fabricación.
Mecanismos de Reparación y Ejemplos de Investigación
Los biomateriales funcionalizados actúan a través de diversos mecanismos para abordar la naturaleza multifacética del TCE. Estos incluyen:
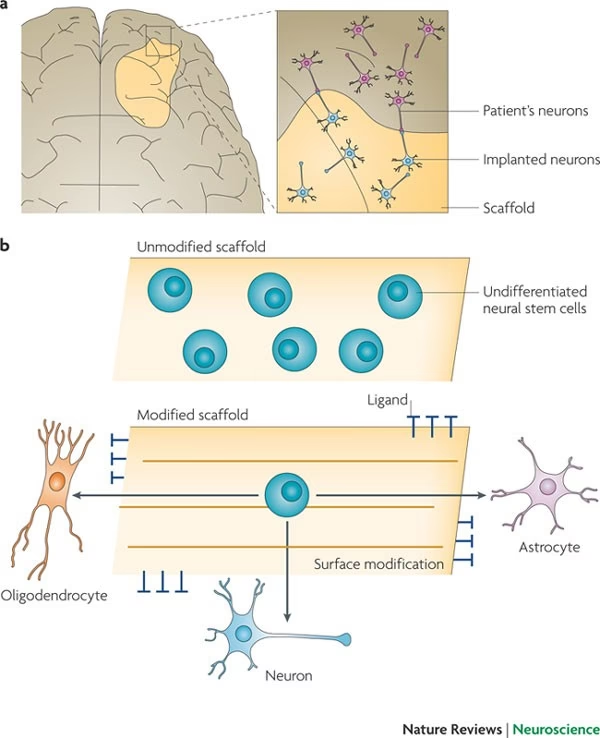
- Promoción de la neurogénesis y mejora de la diferenciación de células madre neurales (endógenas o trasplantadas) hacia neuronas en lugar de astrocitos.
- Inhibición de la apoptosis (muerte celular programada).
- Reducción de la neuroinflamación, que tiene efectos tanto beneficiosos (limpieza de desechos) como perjudiciales (muerte neuronal).
- Combate del estrés oxidativo mediante propiedades antioxidantes.
- Facilitación de la angiogénesis (formación de nuevos vasos sanguíneos), crucial para el suministro de oxígeno y nutrientes al tejido dañado.
- Actuar como vehículos de entrega controlada de células madre, factores de crecimiento, antioxidantes, etc., superando las limitaciones de la administración sistémica.
Numerosos estudios en modelos animales de TCE han demostrado el potencial de estos biomateriales. Por ejemplo, andamios de colágeno/quitosano han mejorado la función neuromotora y cognitiva, facilitando la remodelación de redes neurales y la regeneración de fibras nerviosas. Hidrogeles de gelatina han reducido el área dañada, mitigado la inflamación y mejorado la supervivencia celular. Nanofibras de PLGA cargadas con N-acetilcisteína (un antioxidante) han mostrado neuroprotección. Andamios de péptidos autoensamblables, como RADA16 funcionalizado con motivos de laminina, han incrementado la supervivencia de células madre, disminuido la formación de cicatriz glial y mejorado la regeneración del tejido cerebral. La combinación de biomateriales con células madre y factores de crecimiento a menudo resulta más efectiva que el uso de componentes individuales, ya que los biomateriales proporcionan un microambiente de soporte, mejoran la retención celular en el sitio de la lesión y facilitan la integración de las células trasplantadas.
Desafíos y Limitaciones en el Uso de Biomateriales Cerebrales
A pesar de los resultados prometedores en modelos preclínicos, el desarrollo y la traslación clínica de biomateriales para la regeneración del SNC presentan desafíos significativos. La creación de materiales que sean simultáneamente biodegradables, biocompatibles y mecánicamente flexibles, que imiten el delicado equilibrio de propiedades del tejido cerebral, sigue siendo un reto importante. Es crucial controlar con precisión la tasa de degradación del biomaterial para que coincida con la velocidad de regeneración del tejido; una degradación demasiado lenta puede inhibir la reparación, mientras que una demasiado rápida puede comprometer el soporte estructural y la liberación terapéutica.

Otros obstáculos incluyen la posible respuesta inmune del huésped al material extraño o a sus productos de degradación, la dificultad en lograr la homogeneidad entre lotes (especialmente con materiales naturales), y la necesidad de procedimientos quirúrgicos invasivos para la implantación de algunos tipos de andamios, lo que podría exacerbar la lesión existente. La supervivencia limitada de las células madre trasplantadas en el hostil microambiente del TCE y la ineficiencia en su entrega e implantación efectiva son también barreras significativas para las terapias combinadas.
Aunque se han logrado grandes avances en la formulación de biopolímeros, el biomaterial “perfecto” para su uso en pacientes humanos con TCE aún no se ha diseñado. La mayoría de los ensayos clínicos actuales para TCE se centran en terapias basadas en células madre sin biomateriales, y la experiencia con el ictus sugiere que las células implantadas directamente a menudo no sobreviven bien debido a la inflamación y la falta de soporte microambiental. Se necesita más investigación para abordar problemas como la hemo-compatibilidad, la pirógenicidad y la posible carcinogenicidad a largo plazo.
Para superar estas limitaciones, las futuras investigaciones se centran en el desarrollo de técnicas quirúrgicas mínimamente invasivas, controles rigurosos de contaminación, el diseño de materiales intrínsecamente más biocompatibles, el control preciso de las tasas de biodegradación y la creación de andamios multifuncionales supramoleculares que puedan sintonizarse para el ambiente hostil del TCE.
Preguntas Frecuentes sobre Biomateriales en el Cerebro
¿Los biomateriales utilizados en el cerebro son permanentes? Generalmente, para aplicaciones terapéuticas en el cerebro como el TCE, se buscan biomateriales que sean biodegradables y reabsorbibles. Esto evita la necesidad de una segunda cirugía para retirarlos y minimiza la respuesta inflamatoria crónica. Su tasa de degradación se diseña idealmente para coincidir con la regeneración del tejido.
¿Pueden los biomateriales ayudar a las células madre a sobrevivir en el cerebro lesionado? Sí, uno de los principales usos de los biomateriales es proporcionar un andamiaje y un microambiente de soporte que mejore la supervivencia, la proliferación y la diferenciación de las células madre (tanto las trasplantadas como las endógenas) en el sitio de la lesión. Esto es crucial en el ambiente inflamatorio y carente de soporte tras un TCE.
¿Los biomateriales pueden dañar el tejido cerebral sano? El diseño de biomateriales para el cerebro prioriza la biocompatibilidad para minimizar las reacciones adversas. Sin embargo, la rigidez inadecuada, los productos de degradación tóxicos o una respuesta inmune no deseada son riesgos potenciales que la investigación busca mitigar activamente. Los materiales se seleccionan y modifican cuidadosamente para interactuar de manera segura con el tejido neural.
¿Ya se utilizan biomateriales para tratar el TCE en humanos? A pesar de los resultados prometedores en la investigación preclínica (principalmente en modelos animales), actualmente no existen biomateriales aprobados por la FDA específicamente para el tratamiento del TCE en un entorno clínico rutinario. La investigación se encuentra en fases avanzadas, pero aún no ha llegado a ensayos clínicos a gran escala en humanos para esta aplicación específica.
Conclusión
El TCE representa un desafío terapéutico global significativo, con opciones de tratamiento actuales limitadas por la complejidad de la lesión y la barrera hematoencefálica. Los biomateriales, incluyendo hidrogeles, péptidos autoensamblables y nanofibras electrohiladas, emergen como una vía terapéutica innovadora y prometedora. Estos materiales no solo pueden proporcionar soporte estructural y rellenar cavidades, sino que también pueden ser diseñados para modular el microambiente de la lesión, combatir la neuroinflamación y el estrés oxidativo, y servir como vehículos para la entrega localizada de agentes terapéuticos y células madre.
Aunque la investigación en modelos animales ha demostrado consistentemente su potencial para mejorar la neurogénesis, la angiogénesis, reducir el tamaño de la lesión y promover la recuperación funcional, existen desafíos importantes que deben abordarse antes de su aplicación clínica generalizada en humanos. Estos incluyen perfeccionar la biocompatibilidad, controlar la biodegradación y mejorar la supervivencia celular. A pesar de estas limitaciones, el campo de los biomateriales ofrece una oportunidad invaluable para explorar nuevas estrategias de reparación y regeneración cerebral, abriendo caminos más allá de los enfoques farmacológicos tradicionales para el tratamiento del traumatismo craneoencefálico.
Si quieres conocer otros artículos parecidos a Biomateriales: Esperanza para el Cerebro Lesionado puedes visitar la categoría Neurociencia.

