El miedo es una respuesta fundamental para la supervivencia, un mecanismo de defensa evolutivo que nos protege del peligro. Si bien ciertas reacciones de miedo son innatas, como el sobresalto ante un ruido fuerte, nuestra capacidad para adquirir miedo a estímulos previamente neutros es crucial para adaptarnos a entornos cambiantes. En el laboratorio, el condicionamiento de miedo pavloviano, también conocido como condicionamiento clásico del miedo, se ha convertido en una herramienta esencial para desentrañar las bases anatómicas, celulares y moleculares de la formación de la memoria del miedo en el cerebro de los mamíferos.
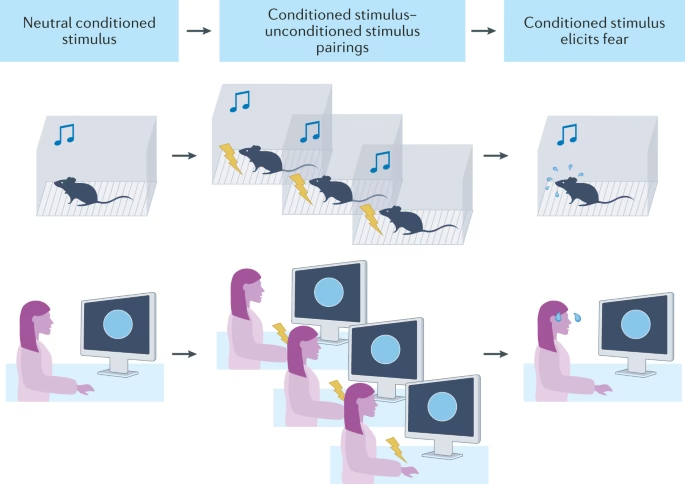
Este modelo, derivado del trabajo pionero de Pavlov sobre el condicionamiento defensivo y utilizado posteriormente por Watson en su célebre estudio del Pequeño Albert, implica el emparejamiento repetido de un estímulo condicionado (EC) emocionalmente neutro con un estímulo incondicionado (EI) aversivo. El EI provoca respuestas incondicionadas (RI) fisiológicas y conductuales automáticas. Tras uno o varios ensayos de emparejamiento EC-EI, el EC por sí solo comienza a elicitar un conjunto de respuestas, conocidas como respuestas condicionadas (RC), características de un estado de miedo. Estas RC pueden cuantificarse e incluyen la congelación (parálisis conductual), respuestas autonómicas (cambios en la frecuencia cardíaca, presión arterial, conductancia de la piel, dilatación pupilar) y respuestas endocrinas (liberación de hormonas del estrés). Estas RC son índices medibles que permiten evaluar el aprendizaje y la memoria emocionales a medida que el organismo adquiere la asociación entre el EC y el EI.
Es importante destacar que, a diferencia del condicionamiento instrumental (que enfatiza las respuestas voluntarias para obtener recompensas o evitar castigos y fue el foco principal del conductismo durante un tiempo), el condicionamiento pavloviano se centra en las respuestas automáticas elicitadas por el EC. Este enfoque ha demostrado ser más fructífero para investigar los mecanismos neuronales subyacentes a la formación de la memoria, especialmente la memoria emocional implícita.
- El Condicionamiento de Miedo como Modelo de Memoria Emocional
- Circuitos Neuronales Implicados
- Mecanismos Celulares: Plasticidad Sináptica
- Mecanismos Moleculares: La Química del Miedo Aprendido
- Mecanismos Epigenéticos
- Plasticidad Presináptica
- Extinción del Miedo y Corteza Prefrontal
- Relevancia Clínica y Consideraciones
- Comparativa: Condicionamiento Pavloviano vs. Instrumental
- Memoria Implícita vs. Explícita en el Miedo
- Preguntas Frecuentes
El Condicionamiento de Miedo como Modelo de Memoria Emocional
La investigación sobre el condicionamiento de miedo ha avanzado significativamente nuestra comprensión de los sustratos neuronales del procesamiento de la memoria emocional. Se considera que el condicionamiento de miedo cae dentro de la categoría de memoria implícita o no declarativa, ya que ocurre normalmente en personas con daño cerebral que afecta la memoria explícita (consciente). Del mismo modo, el daño cerebral que interrumpe el condicionamiento de miedo no suele interferir con la memoria explícita de la experiencia de condicionamiento. Esto sugiere que, en situaciones emocionales, un sistema cerebral forma memorias emocionales implícitas (expresadas como RC) y otro sistema forma memorias explícitas (conscientes) sobre la experiencia. Si bien estos dos tipos de memoria pueden interactuar, el condicionamiento de miedo pavloviano se centra principalmente en la formación implícita de memorias emocionales.
Circuitos Neuronales Implicados
El núcleo de la maquinaria cerebral para el condicionamiento de miedo reside en la amígdala. A lo largo de diversas investigaciones y especies, la amígdala ha emergido consistentemente como una estructura cerebral esencial para la adquisición y expresión del miedo condicionado. Las lesiones en la amígdala antes del entrenamiento impiden el desarrollo de las RC, mientras que las lesiones posteriores al entrenamiento interrumpen la expresión de las RC ya aprendidas.
Las vías subyacentes al condicionamiento de miedo implican la transmisión de información del EC a la amígdala, y la transmisión desde la amígdala a diversas redes de control de la RC en el tronco encefálico.
Vías de Entrada Sensorial a la Amígdala
La información sensorial del EC y del EI llega a la amígdala. Para un EC auditivo, existen dos rutas principales hacia el núcleo lateral de la amígdala:
- Vía Talamo-Amigdalina Directa: Una ruta rápida desde el tálamo auditivo (porción medial del núcleo geniculado medial y núcleo intralaminar posterior) directamente al núcleo lateral de la amígdala. Proporciona una representación más cruda del estímulo.
- Vía Talamo-Cortico-Amigdalina Indirecta: Una ruta más lenta que conecta el tálamo auditivo con el núcleo lateral de la amígdala a través de la corteza auditiva. Proporciona un procesamiento más detallado del estímulo.
Se cree que la vía directa permite una respuesta defensiva rápida a características simples del estímulo, mientras que también puede preparar la amígdala para estímulos más complejos procesados por la vía indirecta. La investigación sugiere que cualquiera de estas vías por sí sola puede ser suficiente para el condicionamiento simple, pero la participación cortical es probable en situaciones más complejas.
Las vías del EI (como un choque eléctrico) también parecen implicar circuitos talamo-amigdalinos y talamo-cortico-amigdalinos que convergen en el núcleo lateral de la amígdala. Por lo tanto, el núcleo lateral de la amígdala actúa como una estación clave donde converge la información del EC y del EI, sugiriendo que este es un sitio crucial para la integración sensorial y la plasticidad sináptica.
Procesamiento Dentro de la Amígdala y Vías de Salida
La información sensorial que llega al núcleo lateral se proyecta a otras áreas dentro de la amígdala, incluyendo los núcleos basal, basolateral accesorio, medial, intercalados y central. El núcleo central ha sido tradicionalmente considerado el principal núcleo de salida del sistema de aprendizaje del miedo.
Las proyecciones del núcleo lateral llegan al núcleo central directamente y a través del núcleo basal y las masas celulares intercaladas. La transmisión a través de estas vías resulta en la desinhibición de las neuronas de proyección del núcleo central. Para la expresión del condicionamiento de miedo simple, la transmisión desde el núcleo lateral al núcleo central es necesaria, aunque el núcleo basal también está implicado.
El núcleo central, a su vez, media las respuestas emocionales a través de conexiones eferentes con centros motores y autonómicos en el tronco encefálico. Por ejemplo, las lesiones en la sustancia gris periacueductal pueden interrumpir la congelación, mientras que otras respuestas como el aumento de la presión arterial permanecen intactas, lo que sugiere que diferentes proyecciones del núcleo central controlan distintas modalidades de RC.
En resumen, la amígdala parece funcionar como la estación central donde se evalúa la significancia emocional del estímulo, independientemente de cómo la información llegue al cerebro o cómo se expresen las respuestas.
Mecanismos Celulares: Plasticidad Sináptica
La convergencia de las vías del EC y el EI en el núcleo lateral de la amígdala sugiere que esta interfaz sensorial puede ser el sitio principal de plasticidad en el circuito del miedo. Estudios de registro de unidad única han mostrado que las células en el núcleo lateral responden a estímulos acústicos con latencia corta y que su tasa de disparo aumenta drásticamente durante el entrenamiento. Estos cambios predicen la adquisición del miedo condicionado y pueden persistir hasta la extinción.
El cambio en la respuesta de las células del núcleo lateral durante y después del condicionamiento de miedo sugiere que las alteraciones en la transmisión sináptica excitatoria son críticas. Gran parte de la investigación se ha centrado en la relación entre la potenciación a largo plazo (LTP) en el núcleo lateral de la amígdala y la formación de la memoria del miedo. La LTP, un aumento duradero en la fuerza de la conexión sináptica, se ha observado en las principales vías de entrada auditiva al núcleo lateral (talamo-amigdalina y cortico-amigdalina). La inducción de LTP en estas vías altera el procesamiento de estímulos auditivos de manera similar a como lo hace el condicionamiento de miedo.
Aunque el núcleo lateral parece desempeñar un papel principal o impulsor en la plasticidad de la amígdala, también se han observado respuestas neuronales condicionadas en los núcleos basal y central, aunque con latencias más largas.

Mecanismos Moleculares: La Química del Miedo Aprendido
Siguiendo la investigación sobre la LTP en el hipocampo, se exploró la posibilidad de que el condicionamiento de miedo involucre una forma de plasticidad sináptica dependiente de los receptores NMDA en la amígdala. Varios estudios han demostrado que el bloqueo de los receptores NMDA en el núcleo lateral (y basal) de la amígdala antes del condicionamiento interrumpe el aprendizaje del miedo. Específicamente, la subunidad NR2B del receptor NMDA ha sido implicada, afectando tanto la memoria a corto como a largo plazo del condicionamiento, lo que sugiere un papel esencial de los receptores NMDA en la plasticidad sináptica inicial.
La LTP en el núcleo lateral de la amígdala también es dependiente de los receptores NMDA. Sin embargo, bajo ciertas condiciones, la LTP asociativa y específica de sinapsis en el núcleo lateral requiere la entrada de calcio a través de canales de calcio dependientes de voltaje tipo L (VGCCs tipo L) en la célula postsináptica, además de los receptores NMDA. Esto sugiere que el condicionamiento de miedo podría requerir una combinación de estos mecanismos celulares.
Una consecuencia inmediata de los aumentos de Ca2+ dependientes de la actividad mediada por NMDAR (y VGCCs tipo L) durante la inducción de LTP es la activación de la Ca2+/calmodulina (CaM)-dependiente proteína quinasa II (CaMKII). La activación de CaMKII en la amígdala es crucial para la adquisición y la formación de la memoria a corto plazo del condicionamiento de miedo, probablemente modulando los receptores glutamatérgicos en las sinapsis del núcleo lateral.
La inserción de nuevos receptores AMPA en las sinapsis es otro mecanismo clave. El condicionamiento de miedo aumenta la expresión superficial de la subunidad GluR1, y bloquear su inserción sináptica perjudica la adquisición del miedo. La inserción de GluR1 dependiente de αCaMKII parece ser un paso importante en la formación y mantenimiento de la memoria a corto plazo.
Consolidación de la Memoria del Miedo
La conversión de la memoria a corto plazo (STM) a memoria a largo plazo (LTM), o consolidación, requiere la síntesis de ARNm y nuevas proteínas en el núcleo lateral de la amígdala, así como la actividad de varias quinasas, incluyendo MAPK y PKA. Estas quinasas, implicadas en la LTP en el núcleo lateral, fosforilan el factor de transcripción CREB. Ratones deficientes en CREB muestran una consolidación de la memoria del miedo deteriorada, mientras que la sobreexpresión de CREB en la amígdala la mejora.
Además de la señalización mediada por Ca2+, las neurotrofinas como el BDNF (Factor Neurotrófico Derivado del Cerebro) también son cruciales para la plasticidad sináptica a largo plazo y la formación de memoria. La señalización mediada por BDNF en la amígdala es crítica para el aprendizaje del miedo, posiblemente promoviendo la activación de quinasas como MAPK.
La consolidación también implica cambios en la expresión génica. El condicionamiento de miedo induce la expresión de genes de respuesta temprana inmediata (como Arc/Arg3.1, Egr-1, Npas4) y tardía en el núcleo lateral. La interferencia con estos genes perjudica la consolidación. Se cree que estos cambios en la expresión génica contribuyen a alteraciones en la estructura sináptica, estabilizando la memoria. Genes implicados en la remodelación del citoesqueleto, como NF-1, y proteínas reguladoras como la cinasa de cadena ligera de miosina y β-catenina, también están implicados.
Mecanismos Epigenéticos
Más allá de los mecanismos moleculares tradicionales, los mecanismos epigenéticos (modificaciones en la estructura de la cromatina y la metilación del ADN) desempeñan un papel crítico adicional en la regulación transcripcional, la plasticidad sináptica y la formación de memoria. La acetilación de histonas, catalizada por HATs y revertida por HDACs, relaja la cromatina y mejora la transcripción. La metilación del ADN, catalizada por DNMTs, generalmente se asocia con la represión transcripcional.
El condicionamiento de miedo pavloviano auditivo aumenta la acetilación de histonas en el núcleo lateral de la amígdala. La infusión de inhibidores de HAT, HDAC o DNMT en el núcleo lateral puede regular la consolidación de la memoria del miedo. Estos hallazgos sugieren que las modificaciones epigenéticas son importantes para la consolidación de la memoria del miedo.
Plasticidad Presináptica
Aunque gran parte de la investigación se ha centrado en los eventos postsinápticos, también hay evidencia de modificaciones presinápticas durante el condicionamiento de miedo. El condicionamiento de miedo puede ocluir la facilitación por pulsos pareados en las entradas corticales al núcleo lateral de la amígdala, un tipo de plasticidad a corto plazo que se cree que es presináptica.
Se ha propuesto que una señal retrógrada actúa para promover la plasticidad presináptica. El óxido nítrico (NO) es un candidato bien caracterizado para este mensajero. El NO, generado postsinápticamente, puede actuar presinápticamente para mejorar la liberación de neurotransmisores, posiblemente a través de la vía de la guanilil ciclasa soluble y la PKG. La inhibición de NOS, guanilil ciclasa o PKG perjudica el condicionamiento de miedo. La señalización de NO dentro de la amígdala parece coordinar cambios moleculares tanto en el lado postsináptico como en el presináptico (en el tálamo auditivo) de la sinapsis talamo-amigdalina durante la consolidación, actuando de manera retrógrada para promover aspectos presinápticos de la plasticidad.
Extinción del Miedo y Corteza Prefrontal
La extinción del miedo, la disminución gradual de la RC cuando el EC se presenta repetidamente sin el EI, es un proceso de aprendizaje activo. Estudios recientes sugieren que la interacción entre la corteza prefrontal y la amígdala puede desempeñar un papel crucial en la extinción del miedo condicionado. Sin embargo, los resultados en esta área son inconsistentes, lo que requiere una evaluación cuidadosa.
Relevancia Clínica y Consideraciones
Muchos de los síntomas conductuales y fisiológicos observados en los paradigmas de condicionamiento de miedo se asemejan a los de los trastornos de ansiedad humanos. Por ello, se acepta generalmente que comprender los mecanismos biológicos de la adquisición y extinción del miedo tiene una relevancia clínica vital. Sin embargo, es crucial ser cauteloso: la similitud sintomática no implica necesariamente que los sustratos neuronales subyacentes al miedo condicionado y a los trastornos de ansiedad sean idénticos (esto sería un error lógico tipo post hoc, ergo propter hoc).
Aunque la hipótesis de la LTP en la amígdala ha recibido un vasto apoyo empírico, existen datos incompatibles y hipótesis alternativas que deben considerarse. Las cuestiones sin resolver sobre la suficiencia de la hipótesis actual y los resultados inconsistentes sobre el papel de la corteza prefrontal en la extinción son puntos críticos para futuras investigaciones sobre los sustratos celulares y moleculares del condicionamiento y la extinción del miedo.
Comparativa: Condicionamiento Pavloviano vs. Instrumental
| Característica | Condicionamiento Pavloviano del Miedo | Condicionamiento Instrumental de Evitación |
|---|---|---|
| Tipo de Aprendizaje | Asociación entre Estímulos (EC-EI) | Asociación entre Conducta y Consecuencia |
| Respuestas Aprendidas | Respuestas automáticas (RC) | Respuestas voluntarias (Evitación) |
| Énfasis Histórico | Pavlov, Watson, resurgimiento en los 70-80s | Conductismo (Hull, Skinner), foco principal 40-70s |
| Modelo de Estudio Neuronal | Considerado superior para mecanismos neuronales básicos (simple) | Resultados complejos, difícil integración neuronal coherente |
| Aplicación en Miedo | Modelo principal para bases neuronales del miedo aprendido | Estudio de conductas de evitación frente al miedo |
Memoria Implícita vs. Explícita en el Miedo
| Característica | Memoria Implícita (No Declarativa) | Memoria Explícita (Declarativa) |
|---|---|---|
| Naturaleza | Inconsciente, automática | Consciente, recordada |
| Ejemplo en Contexto de Miedo | Respuesta de congelación (RC) al EC | Recordar la situación de condicionamiento (dónde, cuándo) |
| Sistemas Cerebrales Clave | Amígdala | Hipocampo, córtex |
| Impacto de Daño Cerebral | Puede estar intacta si la explícita falla (y viceversa) | Puede fallar mientras la implícita está intacta |
| Interacción | Puede modular la formación de memoria explícita | Puede interactuar con sistemas emocionales implícitos |
Preguntas Frecuentes
- ¿Qué es el condicionamiento de miedo pavloviano?
- Es un tipo de aprendizaje asociativo donde un estímulo neutro (estímulo condicionado, EC) se empareja repetidamente con un estímulo aversivo (estímulo incondicionado, EI), haciendo que el EC por sí solo elicite respuestas de miedo (respuestas condicionadas, RC).
- ¿Qué partes del cerebro están involucradas en el condicionamiento de miedo?
- La amígdala es fundamental, particularmente el núcleo lateral, que recibe información sensorial del EC y EI. El núcleo central de la amígdala es clave para la expresión de las respuestas de miedo, proyectando a áreas del tronco encefálico. El tálamo y la corteza también transmiten información a la amígdala.
- ¿Cómo cambia el cerebro durante el aprendizaje del miedo?
- Ocurre plasticidad sináptica, principalmente en el núcleo lateral de la amígdala. Las conexiones sinápticas se fortalecen a través de mecanismos como la potenciación a largo plazo (LTP), que involucran receptores NMDA, canales de calcio, quinasas (CaMKII, MAPK, PKA), factores de transcripción (CREB) y cambios en la expresión génica y la estructura sináptica.
- ¿El condicionamiento de miedo es lo mismo que la ansiedad?
- No necesariamente. Aunque las respuestas conductuales y fisiológicas en el condicionamiento de miedo se parecen a los síntomas de los trastornos de ansiedad humanos, esto no significa que los mecanismos neuronales subyacentes sean idénticos. El condicionamiento de miedo sirve como un modelo para estudiar aspectos del miedo aprendido que pueden ser relevantes para la ansiedad.
- ¿La amígdala es la única estructura importante?
- Si bien la amígdala es esencial, otras estructuras como el tálamo, la corteza y el tronco encefálico son parte del circuito. La corteza prefrontal también parece estar implicada en la extinción del miedo, aunque esta área de investigación presenta resultados menos concluyentes.
Si quieres conocer otros artículos parecidos a Condicionamiento de Miedo Pavloviano puedes visitar la categoría Neurociencia.