El cerebro humano, una maravilla de la biología, posee una asombrosa capacidad para adaptarse y protegerse frente a los desafíos. Entre estas capacidades se encuentran los mecanismos compensatorios o adaptativos. Estos complejos procesos cerebrales se activan en respuesta al mal funcionamiento de diversos sistemas neuronales, como los antioxidantes, neurotróficos, de neurotransmisores e inmunes, entre otros. Su estudio detallado representa un punto de partida crucial para el descubrimiento y desarrollo de enfoques prometedores en el diagnóstico temprano y tratamiento de enfermedades neurodegenerativas, como el Alzheimer y la Enfermedad de Huntington.
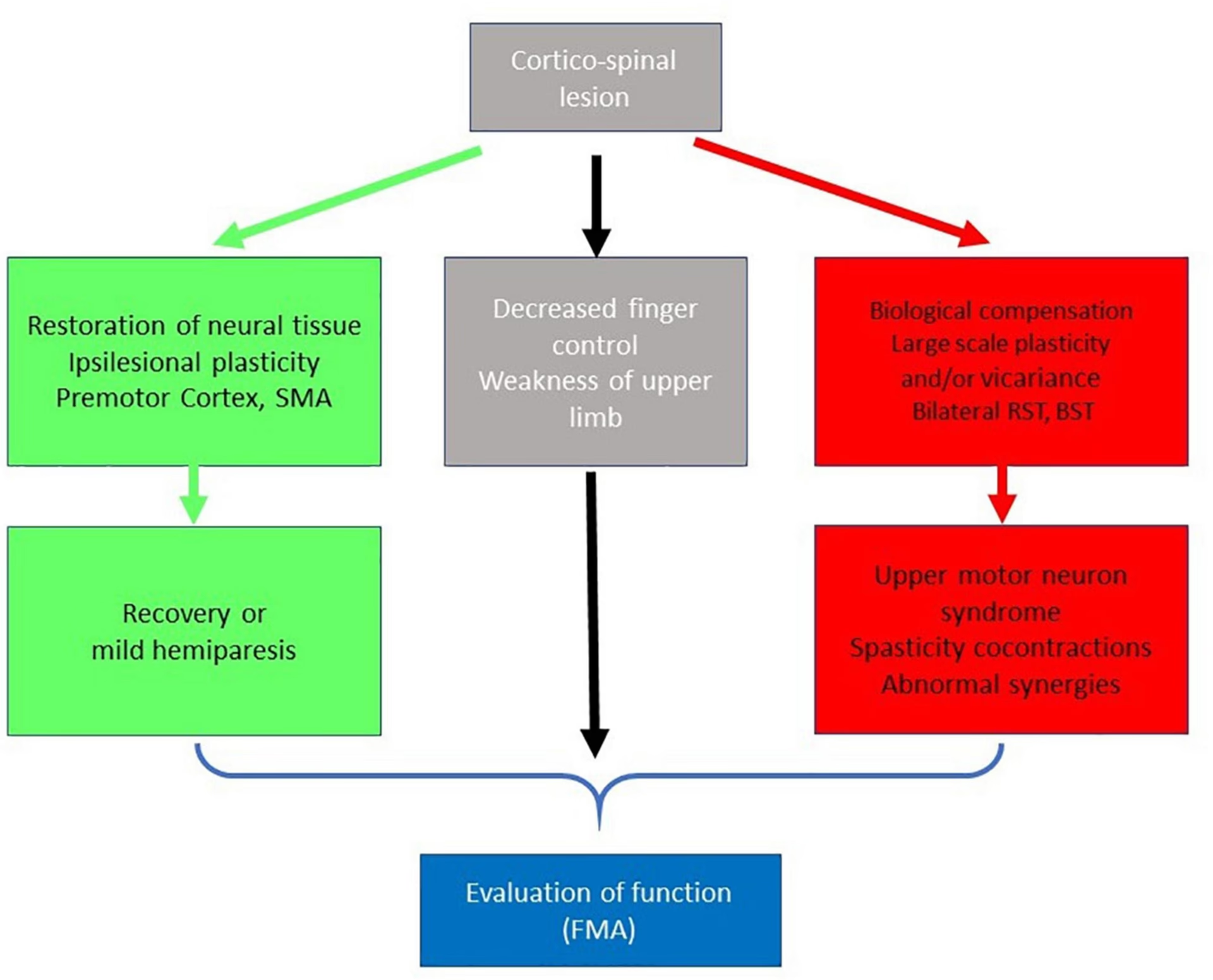
La compensación cerebral, en términos generales, se refiere a la habilidad del cerebro para aumentar la actividad en redes neuronales específicas de una tarea o reclutar regiones corticales adicionales con el fin de mantener el rendimiento conductual. Esta capacidad es vital, especialmente en el contexto de patologías progresivas donde el daño neuronal es constante.
¿Qué son los Mecanismos Compensatorios Cerebrales?
Los mecanismos compensatorios cerebrales son estrategias biológicas intrínsecas que el cerebro emplea para contrarrestar o mitigar los efectos del daño o la disfunción. No son meras reacciones pasivas, sino procesos activos que buscan preservar la homeostasis y la función cognitiva o motora el mayor tiempo posible. Se hipotetiza que estos mecanismos juegan un papel protector frente a la progresión de enfermedades como el Alzheimer (EA) y la Enfermedad de Huntington (EH).
La activación de estos mecanismos puede ocurrir mucho antes de que aparezcan los síntomas clínicos evidentes de una enfermedad neurodegenerativa. Este "periodo latente" o "pre-manifestación" es particularmente interesante para los investigadores, ya que comprender cómo el cerebro se defiende en estas etapas tempranas podría ofrecer nuevas vías para la intervención. Sin embargo, el estudio de la compensación presenta desafíos, especialmente en etapas tardías de la enfermedad, donde los mecanismos pueden estar agotados o hiperactivados, dificultando su análisis detallado.
Mecanismos Compensatorios en la Enfermedad de Alzheimer
La Enfermedad de Alzheimer se caracteriza por el deterioro de la memoria, la demencia, la pérdida de neuronas colinérgicas y la acumulación de péptidos beta-amiloide (Aβ) en placas seniles, así como ovillos neurofibrilares intracelulares de proteína tau hiperfosforilada. Aunque estos elementos son marcadores patológicos de la enfermedad, sorprendentemente, la investigación sugiere que en las etapas tempranas, algunos de ellos podrían estar involucrados en procesos compensatorios.
Compensación a Nivel Molecular y Celular
- Péptidos Aβ y Proteína Tau: Aunque son los principales componentes de la patología, se ha observado que los ovillos neurofibrilares y el Aβ pueden exhibir actividad antioxidante. Además, el Aβ, al ser un quelante de metales (cobre, hierro, zinc), podría participar en funciones neurotróficas normales en el cerebro. La generación de Aβ y la fosforilación de la proteína tau a menudo se asocian con la recuperación de la homeostasis oxidativa celular en las etapas iniciales.
- Glia (Microglia y Astroglia): En la etapa temprana de la EA, tanto la microglía como los astrocitos, que acompañan a la enfermedad, muestran actividad. Se ha demostrado que están involucrados en la eliminación de Aβ y los restos de neuronas dañadas, además de prevenir la maduración de los ovillos neurofibrilares. Sin embargo, en etapas tardías, hay un desequilibrio evidente entre la acumulación y la utilización de Aβ.
- Proteínas Protectoras: En la etapa temprana, pero no tardía, de la progresión de la EA, se ha observado un aumento en el nivel de transtiretina, una proteína que inhibe la agregación de Aβ. La neprilisina, una endopeptidasa degradadora de Aβ, también muestra un perfil similar en el líquido cefalorraquídeo (LCR) de pacientes con EA. El aumento de clusterina, una proteína asociada con la eliminación de restos celulares, y una mayor utilización de Aβ también parecen ser reacciones compensatorias.
- Proteínas de Choque Térmico (HSP70): En modelos animales de EA, se ha encontrado una asociación entre la mejora de la memoria y el aumento de los niveles de HSP70. Esta proteína actúa como chaperona, protegiendo a las neuronas de la agregación y toxicidad del Aβ, y formando complejos estables con la proteína tau, protegiéndola de la hiperfosforilación.
Compensación Sináptica y de Redes
La pérdida de sinapsis es una característica temprana y significativa de la EA. Se ha observado una disminución en los niveles de sinaptofisina (un marcador presináptico) y de la densidad de receptores sinápticos. Sin embargo, parece haber un intento de compensación a través del aumento de la proteína postsináptica PSD-95, conocida por apoyar la función de los receptores AMPA y NMDA, cruciales para la formación de la memoria.
Además, en modelos animales, se ha revelado un aumento en la densidad de receptores serotoninérgicos (5-HT) en la corteza y el hipocampo. Esto se interpreta como una reacción compensatoria a la disminución de la densidad neuronal y el contenido de serotonina en áreas cerebrales clave.
Respuesta Inmune como Compensación
Los niveles de anticuerpos anti-Aβ en suero y LCR pueden correlacionarse con la progresión de la EA, sugiriendo su potencial como marcadores diagnósticos o incluso como un enfoque terapéutico. Esta respuesta inmune parece estar asociada con la eliminación de Aβ del cerebro. Sin embargo, los enfoques inmunológicos tradicionales en etapas tardías han sido ineficaces, posiblemente porque los mecanismos compensatorios ya están comprometidos. Se sugiere que un bloqueo inmunológico selectivo de los objetivos de Aβ que median su neurotoxicidad, preservando sus funciones beneficiosas, podría ser un enfoque más equilibrado en la etapa temprana de la enfermedad.
Mecanismos de Compensación en la Enfermedad de Huntington
La Enfermedad de Huntington es un trastorno genético fatal caracterizado por déficits motores, cognitivos y psiquiátricos progresivos. Aunque la enfermedad se manifiesta clínicamente en la edad adulta, los cambios cerebrales estructurales y funcionales comienzan a ocurrir hasta 20 años antes del diagnóstico.
Durante la etapa pre-manifestación de la EH, hay atrofia significativa en la corteza cerebral, la materia gris y blanca, y especialmente en los ganglios basales (núcleo caudado, globo pálido, putamen). También hay compromiso de la integridad de las fibras de materia blanca y alteraciones en el metabolismo cortical y estriatal. A pesar de estas anomalías generalizadas, los individuos pre-EH a menudo mantienen un nivel normal de funcionamiento cognitivo y motor en las actividades diarias.
Compensación a Nivel de Redes Funcionales
La explicación de esta aparente discrepancia entre el daño cerebral y el rendimiento funcional se atribuye en parte a la compensación cerebral. Los estudios de neuroimagen funcional (fMRI) han demostrado que, en comparación con controles sanos, los individuos pre-EH exhiben una actividad de fMRI aumentada o adicional en diversas redes motoras y cognitivas para mantener un rendimiento comparable en las tareas.
- Aumento de actividad en regiones premotoras durante tareas motoras.
- Hiperactivación en regiones fronto-parietales durante memoria de trabajo verbal.
- Mayor actividad en regiones fronto-estriatales durante procesamiento de recompensa y memoria de trabajo espacial.
- Incremento de actividad en la corteza prefrontal durante el reconocimiento de expresiones faciales.
- Activación adicional en regiones fronto-temporales y ganglios basales durante tareas de función ejecutiva.
Este patrón de sobreactivación de fMRI en múltiples redes, junto con el rendimiento preservado, se ha interpretado como compensación cerebral en la EH.
Desafíos en la Definición y Modelos de Compensación
Sin embargo, esta definición "informal" de compensación basada únicamente en la sobreactivación de fMRI presenta problemas. La sobreactivación podría deberse a otros factores, como efectos de medicación, dediferenciación (una menor especialización de las regiones cerebrales), incapacidad para inhibir la actividad no relacionada con la tarea o diferencias individuales en la respuesta fisiológica del BOLD (señal de fMRI).

Dada la naturaleza progresiva y generalizada de la patología en la EH, es difícil determinar si la sobreactivación de fMRI representa una verdadera compensación beneficiosa o es un producto de los procesos patológicos. Por ello, la comunidad científica ha abogado por la necesidad de caracterizar mejor la compensación utilizando modelos explícitos.
Se han propuesto varios modelos para aclarar si el aumento de actividad de fMRI refleja una respuesta compensatoria beneficiosa o anomalías relacionadas con la edad o la enfermedad. Algunos de estos modelos incluyen HAROLD, PASA, STAC, STAC-r y CRUNCH.
El modelo CRUNCH (Compensation Related Utilization of Neural Circuits Hypothesis) parece ser particularmente relevante y cuantificable para la EH. CRUNCH postula que la actividad de fMRI aumenta a medida que la dificultad de la tarea incrementa (en demandas bajas o intermedias) para compensar esa dificultad. Sin embargo, cuando los individuos alcanzan un "punto CRUNCH", donde la dificultad excede su capacidad, la actividad de fMRI y el rendimiento conductual disminuyen. En el contexto de la EH, se hipotetiza que los individuos pre-EH muestran mayor actividad en cargas de memoria bajas (efecto de sobreactivación compensatoria) y menor actividad en cargas altas, donde alcanzan su límite antes que los controles sanos.
Tipos de Mecanismos Compensatorios Cerebrales
Los mecanismos de compensación actúan en múltiples niveles de organización cerebral. Aquí presentamos una tabla resumen:
| Tipo de Mecanismo | Ejemplo | Función Principal en la Compensación |
|---|---|---|
| Molecular | HSP70, Transtiretina, Neprilisina, Clusterina | Protección contra agregación/toxicidad, eliminación de agregados, mantenimiento de homeostasis. |
| Celular | Actividad de Microglía y Astroglia, Anticuerpos anti-Aβ | Eliminación de restos celulares y agregados, respuesta inmune dirigida a la patología. |
| Sináptico | Aumento de PSD-95, Aumento de Receptores de Neurotransmisores (ej: 5-HT) | Mantenimiento de la función sináptica, ajuste de la excitabilidad neuronal en respuesta a la pérdida. |
| Redes Funcionales | Reclutamiento de áreas adicionales, Sobreactivación en fMRI (modelo CRUNCH) | Redistribución de la carga de procesamiento, mantenimiento del rendimiento conductual a pesar del daño estructural. |
Desafíos y Futuras Direcciones
Aunque se ha avanzado en la comprensión de los mecanismos compensatorios, todavía existen muchos aspectos por explorar. La dificultad para estudiar estos procesos en su fase más activa (la etapa latente o pre-sintomática) es un obstáculo importante. Los modelos animales, como los animales OBX mencionados en la investigación sobre EA, son herramientas valiosas para imitar y estudiar estas etapas tempranas.
Comprender íntimamente cómo funcionan estos mecanismos, cómo interactúan entre sí y cómo manipularlos representa una vía prometedora para el desarrollo de nuevas estrategias. Esto incluye:
- Diagnóstico Temprano: Identificar biomarcadores de compensación que puedan indicar la presencia de patología mucho antes de los síntomas clínicos.
- Prevención y Terapia: Desarrollar enfoques terapéuticos que potencien los mecanismos de compensación endógenos del cerebro o que intervengan selectivamente en procesos patológicos que deprimen la compensación (como el bloqueo inmunológico selectivo de objetivos tóxicos del Aβ).
La idea central es liberar las reservas endógenas del cerebro para protegerlo y mantener su función el mayor tiempo posible.
Preguntas Frecuentes (FAQs)
¿Qué diferencia hay entre compensación cerebral y plasticidad cerebral?
La plasticidad cerebral es un término amplio que se refiere a la capacidad del cerebro para cambiar y adaptarse a lo largo de la vida en respuesta a la experiencia, el aprendizaje o el daño. La compensación cerebral es un tipo específico de plasticidad que ocurre en respuesta a una disfunción o daño, con el objetivo de mantener la función a pesar de la patología subyacente. La compensación es, en esencia, una forma de plasticidad adaptativa frente al deterioro.
¿La compensación cerebral puede prevenir o curar las enfermedades neurodegenerativas?
La compensación no parece prevenir la aparición de la patología subyacente (como la acumulación de Aβ o la expansión del gen HTT), ni tampoco la cura. Sin embargo, puede retrasar significativamente la aparición de los síntomas clínicos y mitigar su gravedad durante un tiempo, permitiendo que los individuos mantengan una calidad de vida funcional a pesar del daño cerebral en progreso. Es un mecanismo de resiliencia.
¿Cómo se mide la compensación cerebral en humanos?
Se utilizan diversas técnicas. La neuroimagen funcional (fMRI) es común, buscando patrones de actividad cerebral aumentados o redistribuidos durante tareas cognitivas o motoras. También se estudian biomarcadores moleculares en fluidos corporales (LCR, sangre) o tejido cerebral (post-mortem) que reflejen la activación de vías compensatorias (ej: niveles de HSP70, transtiretina). Los estudios conductuales que evalúan el rendimiento en relación con el daño cerebral también proporcionan evidencia indirecta.
¿Ocurre la compensación solo en las etapas tempranas?
Los mecanismos compensatorios son particularmente efectivos y detectables en las etapas tempranas o pre-sintomáticas, cuando el daño aún no es abrumador. A medida que la enfermedad progresa y el daño se acumula, estos mecanismos pueden volverse insuficientes, agotarse o incluso volverse disfuncionales, lo que lleva a la aparición y empeoramiento de los síntomas clínicos.
¿Se pueden potenciar los mecanismos de compensación para tratar enfermedades?
Esta es una de las áreas de investigación más activas. La idea es desarrollar terapias que no solo aborden la patología principal (como eliminar Aβ), sino que también fortalezcan la capacidad innata del cerebro para defenderse y compensar el daño. Esto podría implicar potenciar la actividad de proteínas protectoras, mejorar la función glial o modular la respuesta inmune de manera beneficiosa. Entender cómo funcionan estos mecanismos es el primer paso para diseñar tales intervenciones.
Conclusión
Los mecanismos compensatorios cerebrales representan una línea de defensa fascinante y crucial del cerebro frente a la neurodegeneración. Activos mucho antes de la manifestación clínica, estos procesos a nivel molecular, celular, sináptico y de redes funcionales permiten al cerebro mantener la función a pesar del daño subyacente. Aunque su estudio presenta desafíos, especialmente en las etapas avanzadas de la enfermedad, la comprensión profunda de cómo funcionan estos mecanismos de resiliencia cerebral abre vías prometedoras para el desarrollo de estrategias de diagnóstico temprano y enfoques terapéuticos innovadores que busquen potenciar las propias reservas endógenas del cerebro para combatir enfermedades devastadoras como el Alzheimer y la Enfermedad de Huntington.
Si quieres conocer otros artículos parecidos a Compensación Cerebral: Defensa ante Neurodegeneración puedes visitar la categoría Neurociencia.
