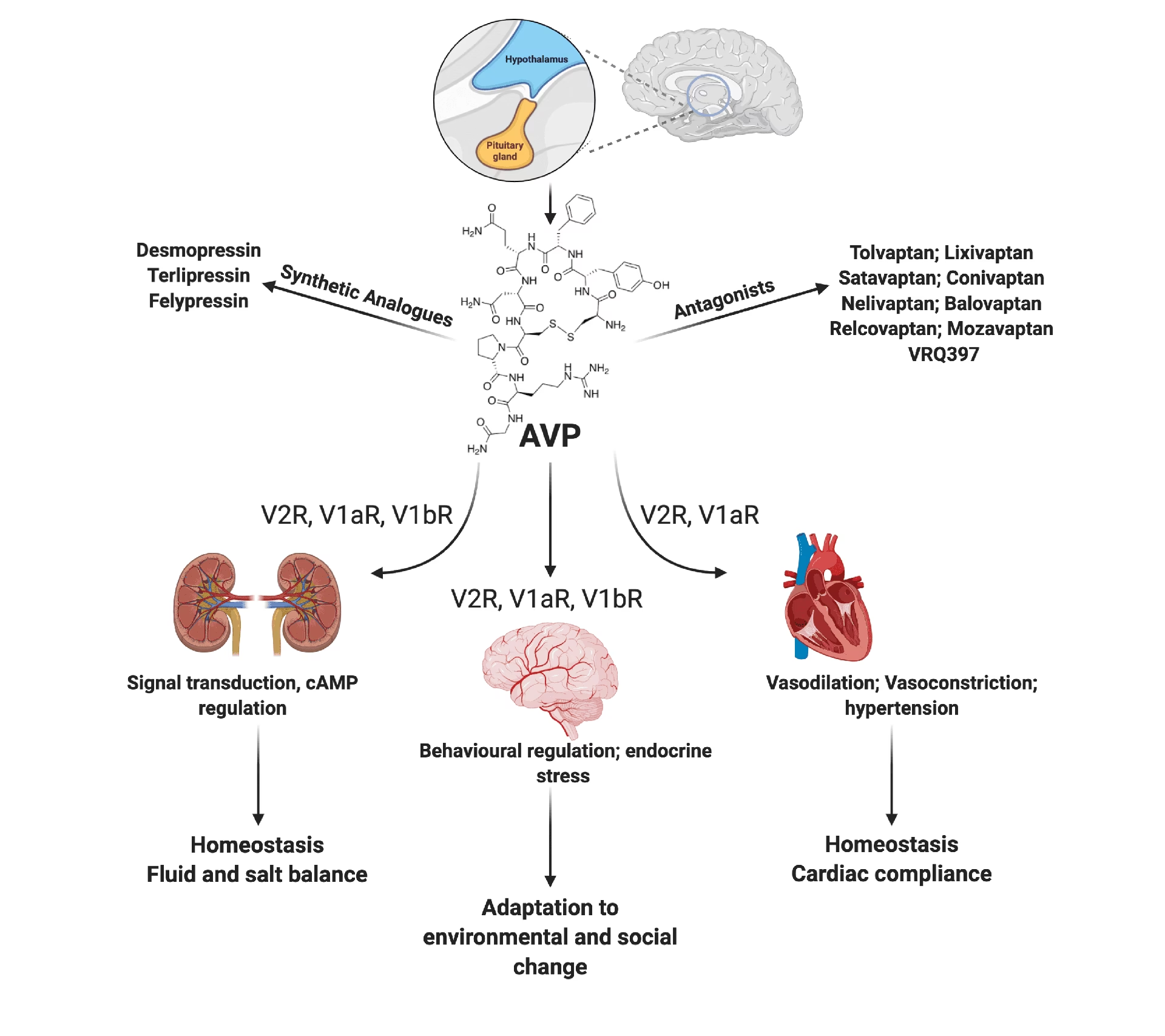
La arginina vasopresina (AVP), un nonapéptido, desempeña un papel crucial en el organismo humano, actuando tanto como hormona como neurotransmisor o neuromodulador. Su estudio en el ámbito de la neurociencia ha revelado una complejidad fascinante, impactando desde funciones autonómicas básicas hasta comportamientos sociales y cognitivos altamente complejos. La AVP es sintetizada en sitios específicos del sistema nervioso central y transportada axionalmente a diversas áreas cerebrales, donde ejerce su función.
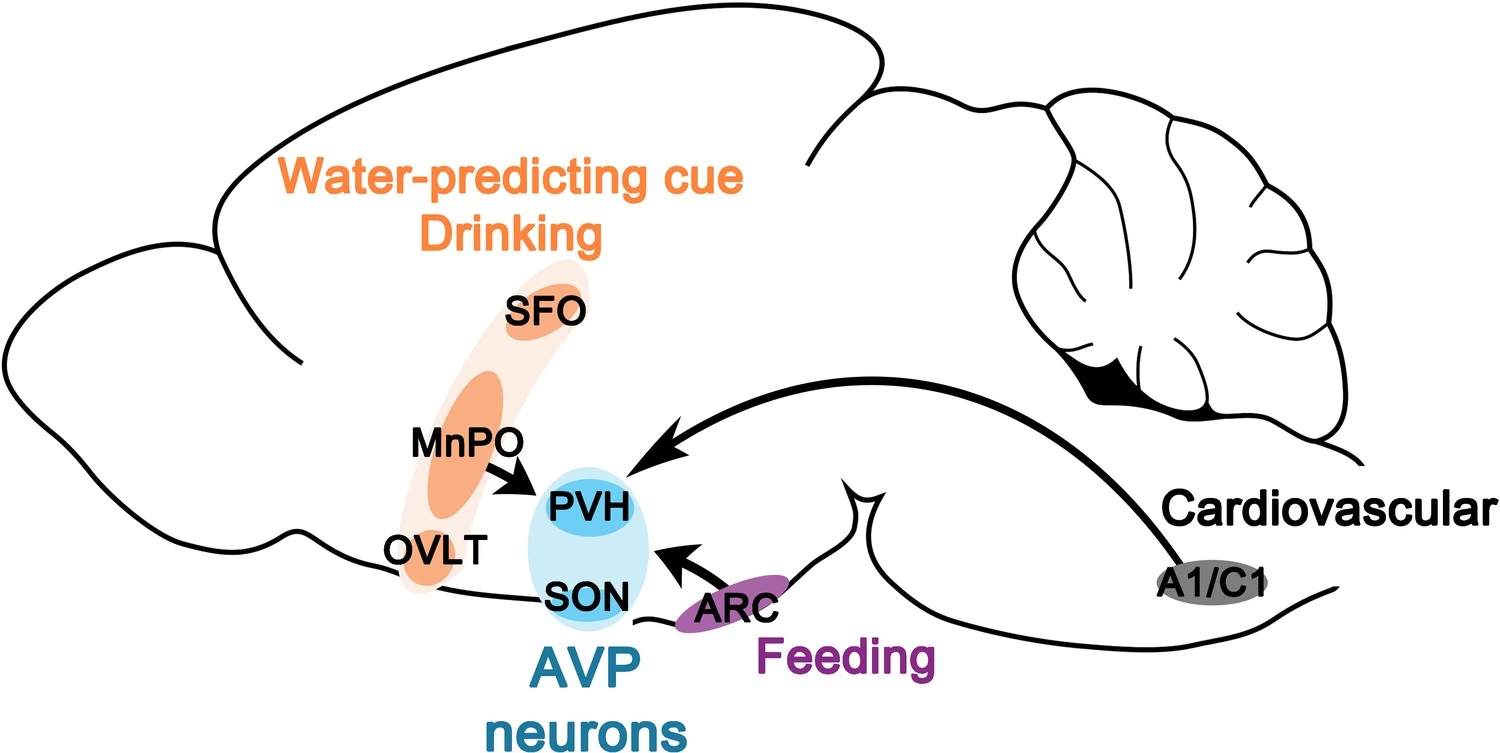
Como hormona, la AVP se dirige a órganos periféricos como los riñones, vasos sanguíneos, hígado, plaquetas y la hipófisis anterior. Sin embargo, es su función como neurotransmisor y neuromodulador en el cerebro la que ha capturado un interés significativo en la neurociencia. Aquí, la AVP está implicada en el control cardiovascular y de la temperatura, así como en estados conductuales y cognitivos complejos, incluyendo la actividad sexual, la formación de vínculos de pareja y el bienestar social. El creciente interés clínico en la copeptina (proAVP) como biomarcador y en los antagonistas de AVP para diversas terapias neurológicas y cardiovasculares subraya su importancia.
- Producción, Liberación y Receptores de AVP
- AVP y Plasticidad Sináptica
- AVP y Actividad Eléctrica Neuronal
- AVP y Actividad Metabólica Neuronal (BOLD)
- AVP y el Ciclo Sueño-Vigilia
- Perspectiva Translacional y Clínica
- Resumen de los Efectos de la AVP
- Preguntas Frecuentes sobre AVP en Neurociencia
- Conclusión y Direcciones Futuras
Producción, Liberación y Receptores de AVP
La producción principal de AVP ocurre en las neuronas magnocelulares del hipotálamo, específicamente en los núcleos supraóptico y accesorias magnocelulares neurosecretoras, así como en las neuronas parvocelulares de los núcleos paraventricular y supraquiasmático. Además, se han identificado cuerpos celulares y fibras con tinción positiva para AVP fuera del hipotálamo, en áreas como el núcleo del lecho de la estría terminal, la amígdala medial, el septum lateral ventral y el locus coeruleus. Existe incluso un sistema AVP intrínseco en el bulbo olfatorio, donde se sugiere su participación en el reconocimiento social.
La AVP sintetizada en las neuronas magnocelulares es liberada a la circulación a través de proyecciones axonales hacia la hipófisis posterior, actuando como hormona. La AVP de las neuronas parvocelulares se secreta a través de la eminencia media y regula principalmente la hormona adrenocorticotrópica de la hipófisis. Curiosamente, la AVP también puede ser liberada desde compartimentos somatodendríticos mediante exocitosis, actuando como neurotransmisor autocrino/paracrino e incluso como neurohormona en blancos distantes. Esta liberación somatodendrítica puede mediar la comunicación entre diferentes poblaciones neuronales, como se ha observado entre neuronas magnocelulares y parvocelulares presimpáticas del núcleo paraventricular.
Como neurotransmisor/neuromodulador, la AVP es transportada vía axonal desde las neuronas parvocelulares a numerosas áreas cerebrales. Estas incluyen estructuras límbicas como el núcleo supraquiasmático, la amígdala y el hipocampo, así como centros autonómicos en el tronco encefálico (núcleo del tracto solitario, núcleo ambiguo, médula ventrolateral rostral, núcleos frénicos, y el complejo pre-Bötzinger) y la médula espinal, donde regula funciones cardiovasculares y respiratorias.
En el sistema nervioso central, la AVP actúa exclusivamente a través de los receptores V1A y V1B. Estos receptores están acoplados a proteínas Gq/11, lo que activa la fosfolipasa Cβ (PLCβ). Esta enzima hidroliza el fosfatidilinositol 4,5-bisfosfato (PIP2) en inositol trisfosfato (IP3) y diacilglicerol (DAG). El IP3, a su vez, moviliza Ca2+ de los depósitos intracelulares, mientras que el DAG activa la proteína quinasa C (PKC). La expresión de estos receptores varía en el cerebro. Estudios en roedores muestran alta expresión de V1A en el bulbo olfatorio, hipocampo, amígdala, núcleo supraquiasmático, septum lateral, hipotálamo, núcleo accumbens, sustancia negra, habénula lateral, rafe dorsal y oliva inferior, con expresión moderada en la médula espinal. El receptor V1B se expresa altamente en la hipófisis anterior en roedores y humanos, con menor expresión en el núcleo accumbens, hipocampo, septum, corteza piriforme, núcleo supraquiasmático, hipotálamo y cerebelo en roedores. En humanos, se confirma alta expresión de receptores AVP en el tálamo, núcleo del lecho de la estría terminal y septum lateral, con menor expresión en la amígdala y el giro dentado.
AVP y Plasticidad Sináptica
Desde hace tiempo se ha reconocido que la AVP puede modular la liberación de glutamato y, consecuentemente, la actividad eléctrica de las neuronas. También se observó que podía afectar los potenciales postsinápticos excitatorios lentos. Sin embargo, la comprensión de los mecanismos celulares subyacentes a la acción de la AVP en neuronas específicas, como las del hipocampo, ha requerido décadas de investigación.
Estudios recientes han demostrado que la AVP puede aumentar la transmisión GABAérgica en neuronas CA1 del hipocampo. No obstante, en condiciones fisiológicas, esta transmisión GABAérgica es superada por una fuerte excitación glutamatérgica directa de las mismas neuronas. Este hallazgo sugiere que la AVP podría estar "ajustando finamente" la excitabilidad de las neuronas CA1 del hipocampo en lugar de ejercer una acción unidireccional (estimulación o depresión). La liberación de GABA mediada por AVP a través de receptores V1A parece depender de proteínas Gq/11 y resultar de la despolarización de interneuronas GABAérgicas por inhibición de canales de K+. La facilitación de la transmisión glutamatérgica en neuronas CA1 por AVP parece estar relacionada con la depresión de canales de K+ rectificadores internos acoplados a proteína G.
En la región CA2 del hipocampo, distinta de CA1, se ha demostrado que los agonistas de V1B potencian selectivamente las respuestas sinápticas excitatorias. Esta potenciación en CA2 depende de la activación del receptor NMDA, calcio y calcio/calmodulina, sin implicar mecanismos presinápticos o PKC. La región CA2 es una red local altamente plástica de neuronas inhibitorias que actúa como un nexo entre la entrada cortical al hipocampo y la salida neuronal de CA1. Se cree que el área CA2 es crucial para la formación de memoria social y está alterada en varios trastornos neuropsiquiátricos.
Dentro de la amígdala, la activación de V1A por AVP es neuroexcitatoria. Esta actividad neuronal inducida por AVP en el núcleo medial de la amígdala central es provocada por la activación de PLCβ, que lleva a la depleción de PIP2 y la subsiguiente apertura de canales TRPC5 y bloqueo de canales Kir. Curiosamente, el Ca2+ intracelular y la PKC no son necesarios para la actividad relacionada con V1A en la amígdala. La microinyección de AVP en la amígdala central evoca una respuesta ansiogénica. En resumen, la AVP actuando directamente sobre las neuronas diana puede resultar en excitación glutamatérgica, pero al mismo tiempo, su acción sobre interneuronas GABAérgicas puede modular finamente estas respuestas excitatorias.
AVP y Actividad Eléctrica Neuronal
La actividad eléctrica es una característica fundamental del tejido neuronal, manifestándose en forma de oscilaciones en múltiples frecuencias. Estas oscilaciones, que van desde ondas lentas hasta altas frecuencias gamma, pueden ser registradas de forma no invasiva en humanos mediante electroencefalografía (EEG) o magnetoencefalografía (MEG). Los neurotransmisores modulan esta actividad oscilatoria a todas las escalas y rangos de frecuencia.
Aunque hay pocos estudios que vinculen directamente la plasticidad sináptica inducida por AVP con la actividad oscilatoria neuronal y la mejora de funciones cognitivas, algunos trabajos en modelos animales sugieren una conexión. Por ejemplo, en un modelo de hipoperfusión cerebral crónica en ratas, el aumento de AVP mejoró el déficit en el aprendizaje y rendimiento espacial, lo cual estuvo acompañado por un aumento en la expresión del receptor NMDA subunidad 2B y la proteína de densidad postsináptica 95, así como cambios en la actividad oscilatoria (potencia de colaterales de Schaffer, sincronía theta entre CA3-CA1, y acoplamiento fase-fase theta-gamma media en CA3-SC). Esto sugiere que la AVP aumenta la plasticidad sináptica en neuronas CA3-CA1, aliviando déficits cognitivos.
En humanos, estudios con potenciales relacionados con eventos (PREs) han investigado los efectos de la AVP en la actividad eléctrica cerebral. La inhalación de AVP en adultos jóvenes y mayores mostró un aumento en la amplitud N2 (70-140 ms post-estímulo) en electrodos frontales y centrales, sugiriendo que la AVP puede aumentar la actividad neuronal asociada con la excitación y el estado de alerta. Sin embargo, solo en voluntarios jóvenes la AVP aumentó significativamente la diferencia de amplitud N2-P3, un componente asociado con el procesamiento de estímulos.

La AVP parece afectar la reactividad emocional y el rendimiento cognitivo de manera sexo-específica. La administración intranasal de AVP en hombres y mujeres ha mostrado patrones diferenciales en la expresión facial y las respuestas electromiográficas (EMG) hacia rostros de modelos del mismo sexo. En hombres, promovió una respuesta agonística, mientras que en mujeres se observó un comportamiento afiliativo. En hombres, altas concentraciones de AVP se asociaron con menor probabilidad de interacciones prosociales con otros hombres. En mujeres, la AVP estimuló un acercamiento amistoso hacia imágenes de mujeres sonriendo. Estos efectos parecen depender del receptor V1A, ya que el antagonismo de V1A disminuye la activación de circuitos amigdalinos por AVP en hombres ante rostros enojados.
Otros estudios con PREs han evaluado los efectos de la AVP en el compromiso con la comunicación social. En hombres, la AVP intranasal aumentó la respuesta P1 a rostros masculinos neutros y positivos (electrodos occipitotemporales), sugiriendo un aumento temprano del estado de alerta y excitación, quizás relacionado con una hostilidad inducida por AVP. Disminuyó las respuestas N170 a rostros masculinos, lo que podría indicar una disminución en las calificaciones de acercamiento a rostros masculinos después de una evaluación inicial de riesgo. En mujeres, la AVP indujo mayores calificaciones de acercamiento a rostros femeninos, en línea con evidencia previa.
Para evaluar la dependencia contextual de los efectos de la AVP, se investigó su impacto en el acercamiento de los hombres a rostros de bebés. La AVP aumentó la respuesta N1 a señales neutras, representando una mayor asignación inicial de recursos atencionales asociados con el estado de alerta y la detección rápida de posibles amenazas. Aunque la respuesta N170 a rostros emocionales se abolió, la respuesta LPP a señales de bebés fue más pronunciada, apoyando un cambio de la evaluación inmediata de riesgos a una atención sostenida de cuidado debido al tratamiento con AVP. En resumen, la AVP parece aumentar la actividad neuronal en circuitos responsables de la asignación de atención a estímulos ambiguos inmediatos, permitiendo luego un cambio hacia la atención sostenida hacia el otro género o rostros de bebés en hombres. En mujeres, aumenta el acercamiento, particularmente hacia el mismo género. Tanto en modelos animales como en adultos jóvenes, la AVP parece aumentar los procesos cognitivos.
AVP y Actividad Metabólica Neuronal (BOLD)
La actividad metabólica neuronal, medida a través de la señal dependiente del nivel de oxígeno en sangre (BOLD) en resonancia magnética funcional (fMRI), también se ve modulada por la AVP. La AVP intranasal aumenta la actividad ante estímulos socialmente relevantes en redes responsables del control emocional.
En hombres, se ha asociado una respuesta BOLD más pronunciada en la amígdala derecha en reacción a imágenes con valencia negativa con un aumento de la conectividad entre la corteza prefrontal medial y la amígdala. Esta fuerte correlación en la actividad BOLD entre ambas regiones, que normalmente tienen una relación inhibitoria, sugiere que la AVP disminuye la capacidad de control de la corteza prefrontal medial sobre la actividad elevada de la amígdala. Esto, junto con el hallazgo de que la AVP aumenta la sincronización amígdala-prefrontal durante la exposición a señales emocionales en hombres, apoya aún más el concepto de que la AVP mejora la reactividad emocional en hombres.
La AVP aumenta la actividad oscilatoria BOLD en respuesta a la cooperación recíproca en el juego del Dilema del Prisionero en el núcleo del lecho de la estría terminal, el septum lateral y la estría terminal en hombres. También disminuye la sincronización de la señal BOLD de la amígdala con el tronco encefálico, mientras aumenta la sincronía con la ínsula anterior ventral (estructuras asociadas con la señalización aferente visceral) y la corteza cingulada anterior subgenual (crítica para la excitación). La AVP también incrementa la similitud de las señales BOLD entre la amígdala y la corteza temporal lateral ventral. En conjunto, la AVP parece enfocar la actividad cerebral en el procesamiento interno dentro de estas estructuras en hombres, a expensas de la información aferente del cuerpo, lo que podría resultar en un mejor juicio en dilemas tácticos complejos.
Estudios adicionales han mostrado resultados variados. Algunos observaron una ligera disminución de la sincronización entre las respuestas BOLD a la cooperación no recíproca (rechazo social simulado) en la amígdala y la ínsula anterior en hombres, sin efecto en mujeres. Otros reportaron un aumento de la sincronización de la señal BOLD durante la elección de acciones cooperativas de alto riesgo entre la corteza prefrontal dorsolateral izquierda y el pálido ventral, el giro cingulado, y los giros frontal medial y superior tras la inhalación de AVP. El pálido ventral es rico en receptores AVP y está asociado con el procesamiento de recompensa dependiente del contexto social. El acoplamiento aumentado entre la corteza prefrontal dorsolateral y el pálido ventral se asoció con una mayor disposición a cooperar en un entorno arriesgado.
La inhalación de AVP parece establecer la cooperación como estrategia por defecto en hombres, requiriendo menos tiempo de procesamiento y control cognitivo. Elegir acciones no cooperativas, en cambio, requiere control cognitivo adicional de la corteza prefrontal dorsolateral, acoplado a actividad en regiones involucradas en la inhibición (corteza prefrontal ventrolateral), el conflicto (corteza cingulada anterior) y la vigilancia emocional (amígdala y giro parahipocampal).
Además, la AVP aumenta la familiaridad social modulando la actividad de la unión temporoparietal izquierda y el surco temporal superior derecho (medida con señales BOLD en hombres y asociada con la teoría de la mente). Un estudio de estado de reposo BOLD mostró que concentraciones más altas de AVP se asociaron con una conectividad y eficiencia reducidas en el cerebro de los hombres, particularmente en áreas donde generalmente tienen mayor conectividad, como la corteza orbital izquierda, el giro frontal inferior izquierdo y el giro temporal superior izquierdo, estructuras importantes para las habilidades verbales. En mujeres, concentraciones más altas de AVP se correlacionaron con menor eficiencia en la corteza parietal izquierda, responsable de las habilidades visoespaciales. Esto sugiere que la concentración de AVP en plasma puede explicar parcialmente las diferencias sexuales típicas en habilidades verbales y visoespaciales.
Finalmente, análisis de la amplitud de fluctuaciones de baja frecuencia en estado de reposo y algoritmos de aprendizaje automático han mapeado el efecto de la AVP intranasal en redes cerebrales a gran escala, incluyendo la red por defecto, sensoriomotora y de saliencia. Esto propone que la AVP ejerce su acción modulando grandes circuitos cerebrales.
AVP y el Ciclo Sueño-Vigilia
El ciclo sueño-vigilia está regulado por redes neuronales complejas en todo el cerebro. Las neuronas de arginina vasopresina en el núcleo paraventricular del hipotálamo (PVHAVP) regulan diversos eventos fisiológicos y comportamientos, y los cambios en el nivel de excitación a menudo acompañan estas respuestas adaptativas mediadas por PVHAVP. Se ha investigado la contribución de estas neuronas a la regulación del sueño-vigilia.
Estudios recientes sugieren que las neuronas PVHAVP promueven el estado de vigilia. La estimulación optogenética de estas neuronas indujo transiciones rápidas a la vigilia tanto desde el sueño NREM como REM. Este efecto de excitación dependió de la expresión de AVP en estas neuronas. De manera similar, la activación quimiogenética de las neuronas PVHAVP aumentó la vigilia y redujo el sueño NREM y REM, mientras que su inhibición quimiogenética redujo significativamente la vigilia y aumentó el sueño NREM.
Se observaron proyecciones densas de neuronas PVHAVP en el hipotálamo lateral, con conexiones potenciales a neuronas de orexina/hipocretina (LHOrx). La estimulación optogenética de las fibras neuronales PVHAVP en el hipotálamo lateral indujo inmediatamente el estado de vigilia, y el bloqueo de los receptores de orexina atenuó drásticamente el efecto de excitación de la activación neuronal PVHAVP. El rastreo monosináptico con virus de la rabia reveló que las neuronas PVHAVP reciben entradas de múltiples regiones cerebrales involucradas en la regulación del sueño-vigilia, así como de aquellas relacionadas con la respuesta al estrés y el metabolismo energético. Además, las neuronas PVHAVP mediaron la excitación inducida por el estrés de novedad y un agonista del receptor de melanocortina. Por lo tanto, los datos sugieren que las neuronas PVHAVP promueven el estado de vigilia a través de las neuronas LHOrx en el sueño-vigilia basal y bajo algunas condiciones de estrés.

Perspectiva Translacional y Clínica
La relevancia clínica de la AVP se manifiesta en el desarrollo de antagonistas de sus receptores para diversas condiciones, como la depresión y la hiponatremia asociada a insuficiencia cardíaca. Antagonistas V1B han mostrado tendencias a reducir puntuaciones de depresión en pacientes con trastorno depresivo mayor. Antagonistas V1A/V2 y V2 han sido probados en ensayos clínicos para pacientes con insuficiencia cardíaca. La ocupación de receptores V1B puede ser monitorizada con trazadores PET novedosos. Además, bloqueadores V1A han mostrado potencial terapéutico en investigaciones preclínicas para reducir el edema cerebral citotóxico y la presión intracraneal.
Aunque una evaluación exhaustiva de los efectos terapéuticos de los antagonistas de AVP está fuera del alcance de este texto, es crucial considerar los efectos de la AVP en las redes cerebrales y los procesos cognitivos, particularmente en las interacciones sociales y el rendimiento cognitivo, al evaluar la seguridad de estos nuevos compuestos. El creciente interés en el uso clínico de bloqueadores V1A/V2 probablemente impulse investigaciones enfocadas en los efectos de la AVP en todo el sistema nervioso central humano.
Resumen de los Efectos de la AVP
La AVP es una molécula con roles duales y complejos en el cerebro. A nivel sináptico, puede modular la liberación de neurotransmisores como el glutamato y el GABA, ajustando finamente la excitabilidad neuronal. A nivel de red, influye en la actividad eléctrica y metabólica, afectando procesos como la excitación, el estado de alerta, la atención, la toma de decisiones sociales y la memoria. Los efectos de la AVP a menudo presentan diferencias significativas entre sexos, particularmente en el procesamiento de señales sociales y la conectividad cerebral.
| Rol de la AVP | Características | Mecanismo/Blancos | Funciones Principales |
|---|---|---|---|
| Hormona | Sintetizada en neuronas magnocelulares (hipotálamo), liberada a circulación (hipófisis posterior). | Actúa en riñones, vasos sanguíneos, hígado, plaquetas, hipófisis anterior. | Regulación del balance hídrico, presión arterial, función hipofisaria (ACTH). |
| Neurotransmisor/Neuromodulador | Sintetizada en neuronas parvocelulares (hipotálamo) y otros núcleos; liberada en SNC. | Actúa a través de receptores V1A y V1B en diversas áreas cerebrales (amígdala, hipocampo, septum, etc.). | Control autonómico, comportamientos sociales, cognición, plasticidad sináptica, ciclo sueño-vigilia. |
Preguntas Frecuentes sobre AVP en Neurociencia
¿Qué significa AVP en neurociencia?
AVP significa Arginina Vasopresina. Es una molécula que funciona como hormona y como neurotransmisor/neuromodulador en el cerebro.
¿Dónde se produce la AVP en el cerebro?
Principalmente en el hipotálamo (núcleos supraóptico, paraventricular y supraquiasmático), pero también en otras áreas como la amígdala, el septum y el locus coeruleus.
¿Cómo actúa la AVP en el cerebro?
Actúa uniéndose a sus receptores, principalmente V1A y V1B, que desencadenan cascadas de señalización intracelular. Modula la liberación de neurotransmisores, afecta la excitabilidad neuronal y la plasticidad sináptica.
¿Qué efectos tiene la AVP en el comportamiento humano?
Influye en comportamientos sociales complejos, la formación de vínculos, la reactividad emocional, el estado de alerta, la atención y procesos cognitivos como la toma de decisiones y la memoria. Muchos de estos efectos son sexo-dependientes.
¿La AVP afecta el sueño?
Sí, estudios recientes sugieren que las neuronas productoras de AVP en el hipotálamo (neuronas PVHAVP) pueden promover el estado de vigilia.
¿Hay diferencias en cómo la AVP afecta a hombres y mujeres?
Sí, la investigación indica diferencias significativas en el procesamiento de señales sociales, la reactividad emocional y los patrones de conectividad cerebral inducidos por la AVP entre hombres y mujeres.
¿Por qué es importante estudiar la AVP en neurociencia?
Comprender cómo la AVP afecta el cerebro es fundamental para desentrañar los mecanismos neuronales de comportamientos complejos y funciones cognitivas, y tiene implicaciones para el desarrollo de terapias para trastornos neurológicos y psiquiátricos.
Conclusión y Direcciones Futuras
Este artículo ha descrito los efectos de la AVP en el cerebro, desde el nivel sináptico hasta el de red. La imagen global es compleja, con la AVP ajustando finamente las respuestas neuronales detrás de la reactividad emocional, la aceptación de riesgos o el funcionamiento cognitivo, particularmente en hombres. La AVP aumenta el estado de excitación y alerta tempranos, con un posible cambio posterior a la atención sostenida en hombres (particularmente hacia rostros femeninos o de bebés). Un aumento en el estado de excitación y alerta se asocia con un control debilitado de la corteza prefrontal medial sobre la amígdala y una mayor conectividad entre la amígdala, la ínsula anterior ventral y la corteza cingulada anterior subgenual en hombres. La AVP parece facilitar la cooperación en un entorno arriesgado en hombres, incluyendo un procesamiento más rápido de señales visuales sociales. Las capacidades cognitivas mejoradas por la exposición a AVP facilitan aún más la toma de decisiones adecuada.
En mujeres, la AVP aumenta el acercamiento y la cooperación con otras mujeres. Sin embargo, muchos estudios se han realizado solo en hombres. Se debe fomentar firmemente la realización de investigaciones sobre AVP en ambos sexos debido a la fuerte influencia de las hormonas sexuales en los efectos ejercidos por la AVP en el cerebro. Estudios futuros con un uso extenso de técnicas de investigación combinadas deberían aclarar aún más las asociaciones entre la actividad eléctrica neuronal local y los efectos de red. Las herramientas de investigación disponibles en neurociencia hacen que tales estudios sean cada vez más factibles. En particular, el uso simultáneo de EEG y fMRI (BOLD) o espectroscopia de infrarrojo cercano podría aclarar la relación entre las respuestas eléctricas y metabólicas neuronales. Además, particularmente en estudios con animales, las grabaciones de potenciales de campo local (posiblemente con estimulación local) deben combinarse con mediciones a nivel de red. Finalmente, los estudios clínicos que investigan el potencial efecto terapéutico de los antagonistas de AVP en el accidente cerebrovascular y la insuficiencia cardíaca también deben monitorear el perfil de seguridad de estos fármacos con respecto a la cognición y el comportamiento, particularmente en hombres. Queda claro que la AVP ejerce una influencia poderosa, aunque muy compleja, en el sistema nervioso central.
Si quieres conocer otros artículos parecidos a AVP en Neurociencia: Rol Doble y Cerebral puedes visitar la categoría Neurociencia.