El cerebro es una red increíblemente compleja de miles de millones de neuronas que se comunican constantemente. Comprender cómo funcionan estas redes y cómo sus patrones de actividad dan lugar a pensamientos, emociones y comportamientos es uno de los mayores desafíos de la ciencia. Durante décadas, los neurocientíficos han buscado herramientas precisas que les permitan manipular la actividad de neuronas específicas para estudiar su papel en circuitos y funciones cerebrales. Recientemente, herramientas innovadoras como la quimiogenética y la optogenética han revolucionado este campo. La quimiogenética, en particular, ofrece un enfoque poderoso mediante el uso de receptores modificados genéticamente que pueden ser activados por fármacos inertes. Dentro de este arsenal, los DREADDs (Designer Receptors Exclusively Activated by Designer Drugs) se han convertido en un pilar fundamental para la manipulación controlada de la actividad neuronal.

Estas herramientas han permitido a los investigadores ir más allá de la simple observación, permitiéndoles intervenir activamente en la función cerebral. La capacidad de encender o apagar poblaciones neuronales definidas con precisión y control temporal ha abierto nuevas vías para investigar la causalidad en los circuitos neurales, en lugar de limitarse a correlaciones. El campo está en constante evolución, con el desarrollo de nuevos DREADDs y herramientas complementarias, como se sugiere en recientes investigaciones que exploran modificaciones novedosas de receptores, incluyendo el uso de receptores opioides.
- ¿Qué son Exactamente los DREADDs?
- hM4Di: La Herramienta Para Silenciar Neuronas
- hM3Dq: La Herramienta Para Activar Neuronas
- Las Diferencias Clave: Inhibición vs. Excitación
- Más Allá de hM4Di y hM3Dq: El Campo en Expansión
- Aplicaciones e Impacto en la Investigación
- Consideraciones y Retos
- Preguntas Frecuentes
- Conclusión
¿Qué son Exactamente los DREADDs?
Los DREADDs son receptores de proteína G (GPCRs) que han sido modificados en el laboratorio para ser insensibles a sus ligandos endógenos naturales, pero que responden potentemente a un ligando sintético que, en condiciones normales, tiene poca o ninguna actividad en el organismo. El ligando más comúnmente utilizado para los DREADDs derivados de receptores muscarínicos (como hM4Di y hM3Dq) es el óxido de clozapina (CNO), aunque metabolitos activos como la descloroclozapina pueden jugar un papel importante en la activación in vivo, dependiendo de la especie y la vía de administración.
La belleza de los DREADDs radica en su especificidad. Al expresar genéticamente estos receptores modificados solo en los tipos de neuronas o regiones cerebrales de interés, los investigadores pueden usar el ligando activador para modular selectivamente la actividad de esa población neuronal específica, dejando el resto del cerebro relativamente inalterado. Esto contrasta con los métodos farmacológicos tradicionales que a menudo afectan a múltiples tipos de receptores y neuronas en todo el cerebro.
hM4Di: La Herramienta Para Silenciar Neuronas
Uno de los DREADDs más ampliamente utilizados es el hM4Di. Este receptor se deriva del receptor muscarínico humano M4. La modificación genética lo hace sensible al CNO (y/o sus metabolitos) pero no a la acetilcolina, el ligando natural del receptor M4.
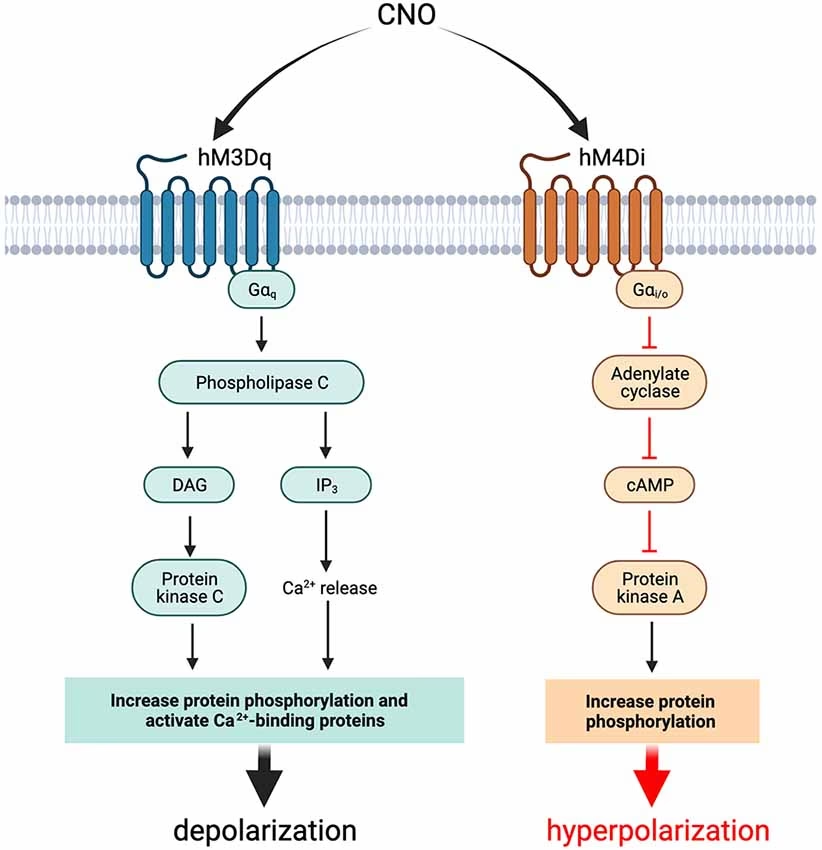
La característica clave del hM4Di es su efecto inhibitorio. Cuando el CNO se une al hM4Di, el receptor acopla predominantemente las vías de señalización de la proteína Gi/o. La activación de Gi/o tiene varios efectos intracelulares que conducen a la supresión de la actividad neuronal:
- Inhibición de la adenilato ciclasa, lo que reduce los niveles de cAMP.
- Activación de canales de potasio rectificadores de entrada (Kir), lo que provoca una salida de iones potasio y una hiperpolarización de la membrana neuronal.
- Inhibición de canales de calcio dependientes de voltaje, lo que reduce la liberación de neurotransmisores.
El resultado neto de la activación del hM4Di es una disminución de la excitabilidad neuronal, lo que puede llevar a una reducción en la tasa de disparo o incluso a la completa inhibición (silenciamiento) de las neuronas que lo expresan. Esto lo convierte en una herramienta invaluable para investigar qué sucede cuando una población neuronal específica deja de funcionar temporalmente. Por ejemplo, si se silencia un grupo de neuronas en el hipocampo con hM4Di y se observa un déficit en la formación de la memoria, se puede inferir que esas neuronas son cruciales para ese proceso.
hM3Dq: La Herramienta Para Activar Neuronas
Por otro lado, tenemos el hM3Dq, otro DREADD muy popular. Este se deriva del receptor muscarínico humano M3. Al igual que el hM4Di, ha sido modificado para responder al CNO (y/o sus metabolitos) pero no a la acetilcolina.
A diferencia del hM4Di, el hM3Dq tiene un efecto excitatorio. Cuando el CNO se une al hM3Dq, el receptor acopla predominantemente las vías de señalización de la proteína Gq. La activación de Gq desencadena una cascada de eventos intracelulares que aumentan la excitabilidad neuronal:
- Activación de la fosfolipasa C (PLC), que hidroliza el PIP2 en IP3 y DAG.
- El IP3 provoca la liberación de calcio de los almacenes intracelulares (como el retículo endoplasmático).
- El DAG (junto con el calcio) activa la proteína quinasa C (PKC).
- La activación de Gq también puede conducir a la apertura de canales catiónicos no selectivos, como los del subtipo TRPC.
El resultado combinado de estos eventos es una despolarización de la membrana neuronal y un aumento en la excitabilidad, lo que a menudo resulta en un incremento en la tasa de disparo de las neuronas que expresan hM3Dq. Esta herramienta es esencial para estudiar qué sucede cuando una población neuronal específica se vuelve más activa de lo normal. Por ejemplo, activar neuronas en la amígdala con hM3Dq puede inducir comportamientos relacionados con la ansiedad o el miedo, permitiendo investigar el papel causal de esas neuronas en tales estados.
Las Diferencias Clave: Inhibición vs. Excitación
La distinción fundamental entre hM4Di y hM3Dq reside en su efecto funcional sobre la neurona y la vía de señalización que activan. Ambos son herramientas quimiogenéticas que responden al mismo ligando (CNO/metabolitos), pero provienen de diferentes receptores muscarínicos y, crucialmente, están acoplados a diferentes proteínas G. Esta diferencia en el acoplamiento a la proteína G determina si el resultado final es la inhibición o la excitación neuronal.
Aquí se presenta una tabla comparativa para visualizar las diferencias principales:
| Característica | hM4Di | hM3Dq |
|---|---|---|
| Origen del Receptor | Receptor Muscarínico M4 Humano | Receptor Muscarínico M3 Humano |
| Ligando Activador | CNO / Metabolitos | CNO / Metabolitos |
| Vía de Proteína G | Principalmente Gi/o | Principalmente Gq |
| Efecto sobre la Neurona | Inhibición (Disminuye la excitabilidad, reduce el disparo) | Excitación (Aumenta la excitabilidad, incrementa el disparo) |
| Aplicación Principal | Silenciar o inactivar neuronas | Activar o aumentar la actividad neuronal |
Más Allá de hM4Di y hM3Dq: El Campo en Expansión
Si bien hM4Di y hM3Dq son los DREADDs más conocidos y utilizados, el campo de la quimiogenética continúa evolucionando. Se han desarrollado otros DREADDs con diferentes características o basados en otros tipos de receptores. Por ejemplo, se han creado DREADDs que acoplan a Gs (generalmente excitatorios) o que son activados por otros ligandos para evitar posibles problemas con el metabolismo del CNO.
La investigación también avanza en la creación de herramientas quimiogenéticas basadas en otros sistemas de receptores, como los receptores opioides, tal como lo sugiere el desarrollo de un nuevo DREADD basado en el receptor κ opioide (KORD) que ofrece una opción de inhibición ortogonal a hM4Di, utilizable con un ligando diferente (Salvinorina B). Del mismo modo, la optogenética, que utiliza la luz para controlar la actividad neuronal mediante canales iónicos sensibles a la luz, es otra técnica poderosa y complementaria. El desarrollo de herramientas como el "opto-MOR", un receptor μ opioide activable por luz, ilustra cómo se están fusionando conceptos de diferentes campos (receptores de GPCRs y control por luz) para crear herramientas aún más sofisticadas para manipular la señalización neuronal.
Estas nuevas herramientas amplían el repertorio disponible para los neurocientíficos, permitiendo estudios más complejos que involucran la manipulación simultánea de múltiples poblaciones neuronales o la activación de vías de señalización específicas con mayor precisión temporal o bioquímica.
Aplicaciones e Impacto en la Investigación
La capacidad de silenciar (con hM4Di) o activar (con hM3Dq) poblaciones neuronales específicas ha tenido un impacto transformador en la neurociencia. Estas herramientas se utilizan para:
- Mapear Circuitos Neurales: Identificar las neuronas que son necesarias (usando hM4Di) o suficientes (usando hM3Dq) para una función o comportamiento particular.
- Estudiar el Comportamiento: Investigar el papel de circuitos específicos en procesos como la memoria, el aprendizaje, la motivación, la ansiedad, la depresión, la adicción y el comportamiento social.
- Modelos de Enfermedades: Manipular la actividad neuronal en modelos animales de trastornos neurológicos y psiquiátricos para comprender los mecanismos subyacentes y probar posibles terapias.
- Investigación de Vías de Señalización: Diseccionar cómo las vías de señalización intracelular (Gi/o vs Gq) en neuronas específicas influyen en su función y en el comportamiento.
Por ejemplo, los investigadores podrían usar hM4Di para silenciar neuronas dopaminérgicas en el área tegmental ventral y ver cómo afecta la motivación o la recompensa, o usar hM3Dq para activar neuronas en la corteza prefrontal para estudiar su papel en la toma de decisiones.
Consideraciones y Retos
Aunque los DREADDs son herramientas potentes, su uso requiere una cuidadosa consideración. La eficiencia de la expresión del receptor, la dosis y farmacocinética del ligando (CNO/metabolitos), y la especificidad de la expresión del DREADD son factores críticos. La preocupación sobre el metabolismo del CNO a clozapina (un fármaco psicoactivo) en algunas especies ha llevado al desarrollo y uso creciente de ligandos alternativos, como la descloroclozapina, que parece ser un activador más potente y tiene perfiles metabólicos diferentes. Además, es importante realizar controles adecuados en los experimentos para descartar efectos inespecíficos del ligando o del vector viral utilizado para entregar el DREADD.
Preguntas Frecuentes
¿Qué significa DREADD?
Significa Designer Receptor Exclusively Activated by Designer Drug (Receptor Diseñado Exclusivamente Activado por Fármaco Diseñado).
¿Cuál es el ligando más común para hM4Di y hM3Dq?
El óxido de clozapina (CNO), aunque sus metabolitos, especialmente la descloroclozapina, pueden ser los principales activadores in vivo.
¿Puedo usar hM4Di y hM3Dq al mismo tiempo?
Sí, en principio. Si se expresan en poblaciones neuronales diferentes (usando, por ejemplo, diferentes promotores o estrategias de focalización), se podría usar CNO para silenciar un grupo (con hM4Di) y activar otro (con hM3Dq) simultáneamente en el mismo animal.
¿Son los DREADDs lo mismo que la optogenética?
No. Los DREADDs son quimiogenéticos (activados por un fármaco), mientras que la optogenética utiliza la luz para activar o inhibir canales o bombas iónicas sensibles a la luz.
¿Son seguros los DREADDs para uso clínico?
Actualmente, los DREADDs son principalmente una herramienta de investigación básica y preclínica. No están aprobados para uso en humanos con fines terapéuticos directos, aunque el principio de manipular la actividad neuronal con precisión podría inspirar futuras terapias.
Conclusión
Los DREADDs hM4Di y hM3Dq representan un avance significativo en la capacidad de los neurocientíficos para investigar la función cerebral. Al permitir la manipulación controlada de la actividad neuronal, ya sea silenciándola (hM4Di mediante Gi/o) o activándola (hM3Dq mediante Gq), estas herramientas han sido fundamentales para desentrañar los roles causales de poblaciones neuronales específicas en circuitos complejos y comportamientos diversos. Junto con otras herramientas innovadoras como los nuevos DREADDs basados en receptores opioides o la optogenética, hM4Di y hM3Dq continúan impulsando la investigación en neurociencia, acercándonos a una comprensión más profunda de cómo funciona el cerebro y qué sale mal en las enfermedades neurológicas y psiquiátricas.
Si quieres conocer otros artículos parecidos a hM4Di vs hM3Dq: Controlando Neuronas puedes visitar la categoría Neurociencia.

