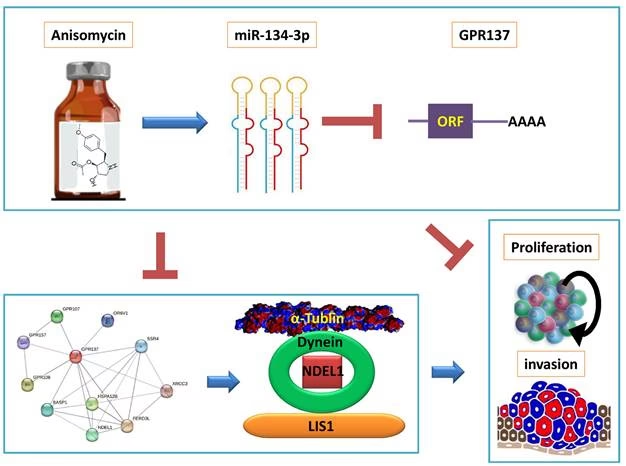
La anisomicina es una sustancia que ha capturado el interés de los neurocientíficos durante décadas, principalmente por su capacidad para inhibir la síntesis de proteínas. Esta propiedad la convierte en una herramienta invaluable para investigar procesos biológicos que dependen de la creación de nuevas proteínas, como la formación de la memoria a largo plazo. Sin embargo, su uso en la investigación ha revelado efectos sorprendentes y complejos, especialmente en el contexto del aprendizaje y la memoria.
A nivel celular, la anisomicina ejerce su efecto principal al interferir con el proceso de traducción, es decir, la síntesis de proteínas a partir del ARN mensajero. Se ha observado que este compuesto inhibe la síntesis de proteínas en diversas fuentes, incluyendo células HeLa, reticulocitos de conejo y Saccharomyces fragilis, así como en extractos libres de células derivados de estos organismos. Curiosamente, no muestra actividad contra extractos de Escherichia coli, lo que sugiere una especificidad en su mecanismo que podría estar relacionada con las diferencias entre la maquinaria de síntesis de proteínas de procariotas y eucariotas. La inhibición de la síntesis de proteínas por la anisomicina es rápida en su inicio y, lo que es crucial para su uso experimental, reversible. A concentraciones que logran una inhibición del 95% de la síntesis proteica, también se observa una inhibición parcial de la síntesis de ADN en células HeLa, aunque su efecto primario y más potente es sobre las proteínas. El mecanismo exacto por el cual la anisomicina detiene la traducción implica su acción en la reacción de transferencia que ocurre después de que se ha formado el aminoacil ARN de transferencia. Esto significa que interfiere en un paso posterior a la unión del aminoácido a su ARN de transferencia correspondiente. En presencia de anisomicina, el péptido naciente (la cadena de aminoácidos en crecimiento) permanece unido a los polirribosomas. Esto sugiere que el fármaco bloquea la elongación o la translocación del ribosoma a lo largo del ARN mensajero, impidiendo la liberación de la cadena proteica completa y la continuación del proceso. Es importante notar que los derivados probados de la anisomicina han mostrado menos del 1% de la actividad inhibitoria del compuesto original, lo que subraya la importancia de la estructura molecular específica de la anisomicina para su potente efecto. La formación de la memoria es un proceso dinámico que tradicionalmente se describe en dos etapas principales: una memoria a corto plazo (MCP) que dura pocas horas y es independiente de la síntesis de nuevas proteínas, y una memoria a largo plazo (MLP) que requiere la síntesis de nuevas proteínas (consolidación). A nivel sináptico, la Potenciación a Largo Plazo (PLP) es considerada un mecanismo clave para la memoria. La PLP también presenta fases: una fase temprana (PLP temprana) independiente de proteínas y una fase tardía (PLP tardía) dependiente de proteínas. La visión convencional postula que la MCP se basa en la PLP temprana y la MLP en la PLP tardía, basándose en estudios de las sinapsis de colaterales de Schaffer en el área CA1 del hipocampo. Sin embargo, las propiedades de la PLP pueden variar según el tipo de sinapsis. Las sinapsis de fibras musgosas, que conectan las células granulares del giro dentado con las neuronas piramidales de CA3, muestran propiedades diferentes. Algunos estudios sugieren que la PLP en las fibras musgosas podría requerir síntesis de proteínas desde sus etapas iniciales.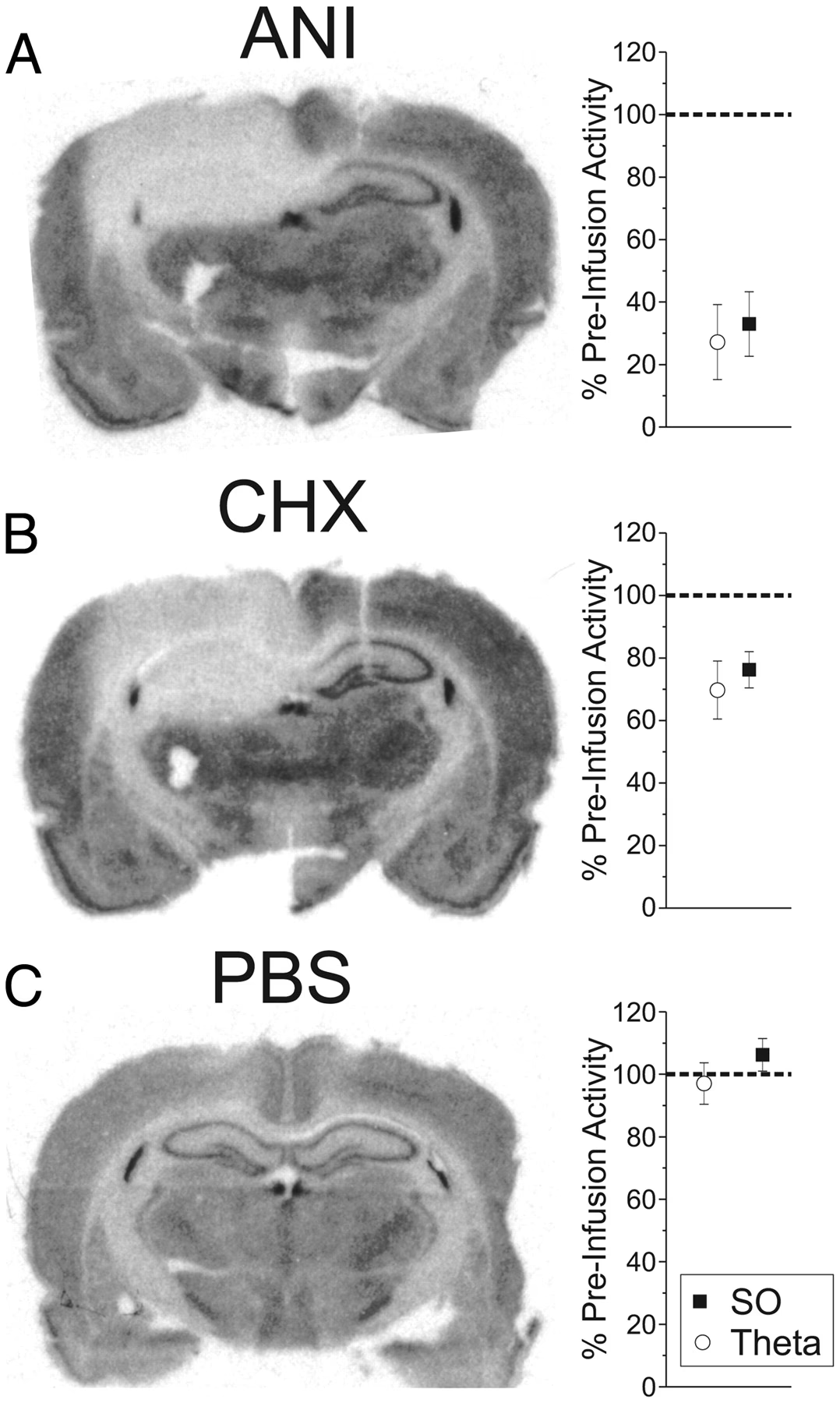
El Mecanismo de Acción de la Anisomicina
Anisomicina y la Formación de la Memoria: Un Vínculo Complejo
 Anisomycin injection impaired long-term but not short-term memory. (D) Freezing response to the exposure to a different context.
Anisomycin injection impaired long-term but not short-term memory. (D) Freezing response to the exposure to a different context.
Esto plantea una hipótesis intrigante: si la síntesis de proteínas es necesaria para la PLP temprana en CA3, entonces la inhibición de la síntesis de proteínas en esta región debería afectar no solo la MLP, sino también la MCP.
Efectos en el Hipocampo: CA1 vs CA3
Para probar esta hipótesis, se realizaron experimentos utilizando condicionamiento de miedo contextual en ratones. Este paradigma de aprendizaje asociativo depende del hipocampo para la representación del contexto y de la amígdala para la asociación aversiva. Se inyectó anisomicina localmente en el área CA1 o CA3 del hipocampo inmediatamente después del entrenamiento y se evaluó la memoria a corto plazo (1 hora) y a largo plazo (24 horas).
Los resultados fueron reveladores:
- Inyecciones en CA1: Como se esperaba por el modelo convencional, la anisomicina en CA1 afectó la memoria a largo plazo (24 horas) pero no tuvo efecto sobre la memoria a corto plazo (1 hora). Esto es consistente con la idea de que la síntesis de proteínas en CA1 es crucial para la consolidación (paso de MCP a MLP) pero no para la formación inicial de la MCP.
- Inyecciones en CA3: Sorprendentemente, la inyección de anisomicina en CA3 afectó significativamente tanto la memoria a corto plazo (evaluada a los 30 minutos y 1 hora) como la memoria a largo plazo (24 horas). Esto sugiere que la síntesis de proteínas en CA3 es necesaria para las etapas tempranas de la memoria contextual.
Estos hallazgos apoyan la idea de que la plasticidad temprana inducida por la experiencia en CA3, que se cree subyace a la MCP contextual, requiere síntesis de proteínas. Se propone que esto se deba a la necesidad de síntesis proteica en las sinapsis de fibras musgosas sobre CA3, que juegan un papel crucial en la rápida elaboración de una representación unificada del contexto.
La rápida afectación de la MCP podría explicarse por la síntesis local de proteínas en las dendritas, un proceso que puede ocurrir en minutos u horas y que es independiente de la transcripción en el soma celular. Las espinas sinápticas de las fibras musgosas en CA3 son particularmente ricas en polirribosomas, lo que respalda esta posibilidad de síntesis local rápida.
Para confirmar que el déficit observado en CA3 afectaba la formación y no la recuperación, se inyectó anisomicina en CA3 30 minutos antes de la prueba de recuperación a las 24 horas. En este caso, no se observó alteración alguna en la memoria, confirmando que el efecto de la anisomicina post-entrenamiento fue sobre los procesos de formación o consolidación inicial, no sobre la recuperación de la memoria ya establecida.
Anisomicina, Reconsolidación y Extinción de la Memoria
Más allá de la formación inicial, la memoria también puede ser modificada después de su recuperación (reconsolidación) o debilitada a través de la extinción. Se realizaron experimentos de evitación inhibitoria en ratas para investigar el papel de la síntesis de proteínas en estos procesos, utilizando inyecciones intrahipocampales de anisomicina después de una re-exposición al contexto de entrenamiento.
Los resultados de estos experimentos revelaron diferentes efectos dependiendo de la duración de la re-exposición:
Re-exposición breve (paradigma de reconsolidación):
Cuando se inyectó anisomicina en el hipocampo después de una re-exposición breve al contexto de entrenamiento (que se espera active la reconsolidación de la memoria), se observó un deterioro en el rendimiento de evitación en una prueba posterior (2 días después). Esto parecía inicialmente consistente con la hipótesis de que la anisomicina interrumpe la reconsolidación de la memoria. Sin embargo, un hallazgo clave fue que este deterioro no fue permanente. En una prueba posterior (6 días después del entrenamiento), las ratas mostraron una recuperación espontánea del rendimiento de evitación, indicando que la traza de memoria original no había sido borrada permanentemente. Un pequeño recordatorio de shock también reinstauró la fuerte evitación.
Re-exposición extendida (paradigma de extinción):
Cuando se inyectó anisomicina después de una re-exposición extendida al contexto (que se espera induzca aprendizaje de extinción), los resultados fueron diferentes. Las ratas control (tratadas con vehículo) mostraron extinción, es decir, una menor evitación en pruebas posteriores. Sin embargo, las ratas tratadas con anisomicina después de la re-exposición extendida *no* mostraron extinción entre la primera re-exposición y la siguiente prueba. Sí mostraron extinción en pruebas posteriores cuando la droga ya no estaba presente. Esto sugiere que la anisomicina bloqueó el *aprendizaje de extinción* que ocurrió durante la re-exposición extendida.
Estos hallazgos en ratas indican que la anisomicina, al inhibir la síntesis de proteínas, puede: (1) deteriorar temporalmente el recuerdo de una memoria reactivada (posiblemente interfiriendo con la reconsolidación, aunque la recuperación espontánea complica esta interpretación), y (2) bloquear la formación de una nueva memoria de extinción. Es crucial que el tratamiento con anisomicina por sí solo, sin la re-exposición al contexto, no afectó la retención de la memoria original, lo que subraya la dependencia del efecto en el proceso activado por la re-exposición.
Consideraciones y Futuras Direcciones
Si bien la anisomicina ha sido una herramienta poderosa para estudiar el papel de la síntesis de proteínas en la memoria, se han planteado preocupaciones sobre sus posibles efectos secundarios no específicos, como la alteración de la liberación de monoaminas o la inhibición de la actividad neuronal per se. Sin embargo, varios estudios sugieren que, cuando se utiliza en dosis bajas y apropiadas (como 25 µg/lado en los experimentos mencionados), la anisomicina puede bloquear selectivamente la plasticidad sináptica sin afectar significativamente la actividad neuronal básica.
El efecto diferencial observado en CA1 versus CA3 y los distintos resultados en los paradigmas de reconsolidación y extinción, todos dependientes de la inhibición de la síntesis de proteínas post-experiencia, refuerzan la especificidad del efecto de la anisomicina en los procesos de aprendizaje y memoria.
A pesar de estos avances, es necesario trabajo adicional para identificar las proteínas específicas cuya síntesis es crucial en las sinapsis de fibras musgosas de CA3 durante el aprendizaje y la plasticidad, así como para confirmar estos hallazgos utilizando enfoques moleculares y genéticos alternativos que eviten por completo los posibles efectos no deseados de los inhibidores farmacológicos.
Tabla Comparativa de Efectos de Anisomicina en el Hipocampo
| Área del Hipocampo | Efecto sobre la Memoria a Corto Plazo (MCP) | Efecto sobre la Memoria a Largo Plazo (MLP) | Plasticidad Sináptica Relevante |
|---|---|---|---|
| CA1 | No afectada | Afectada (deteriorada) | Principalmente Colaterales de Schaffer (PLP tardía) |
| CA3 | Afectada (deteriorada) | Afectada (deteriorada) | Principalmente Fibras Musgosas (posiblemente PLP temprana y tardía) |
Preguntas Frecuentes (FAQ) sobre la Anisomicina y la Memoria
- ¿Cómo inhibe exactamente la anisomicina la síntesis de proteínas?
- La anisomicina interfiere con la reacción de transferencia durante la elongación de la cadena proteica en los ribosomas. Bloquea el movimiento del ribosoma, haciendo que el péptido en crecimiento permanezca unido a él.
- ¿La anisomicina borra la memoria de forma permanente?
- Según los estudios en ratas, el deterioro de la memoria inducido por anisomicina después de una re-exposición breve parece ser temporal, ya que se observó una recuperación espontánea posterior. No parece borrar la traza de memoria original, sino más bien interferir con procesos que ocurren después de la reactivación o durante la formación de nuevas memorias (como la extinción).
- ¿Por qué la anisomicina afecta la memoria de manera diferente en CA1 y CA3?
- Esto parece estar relacionado con las diferencias en los mecanismos de plasticidad sináptica en estas áreas. En CA1, la PLP temprana (base de la MCP) es independiente de proteínas, mientras que la tardía (base de la MLP) sí lo es. En CA3, particularmente en las sinapsis de fibras musgosas, la PLP temprana podría requerir síntesis de proteínas, lo que explicaría por qué la inhibición en CA3 afecta la MCP.
- ¿La anisomicina afecta la capacidad de recordar algo que ya se aprendió?
- Los estudios sugieren que la inyección de anisomicina justo antes de una prueba de recuperación no deteriora el recuerdo de una memoria ya consolidada. Su efecto se observa cuando se administra durante o inmediatamente después de experiencias de aprendizaje o reactivación de la memoria.
- ¿Puede la anisomicina afectar otros tipos de aprendizaje?
- Sí, los estudios en ratas mostraron que la anisomicina puede bloquear el aprendizaje de extinción, que es una forma de nuevo aprendizaje asociativo donde un estímulo previamente temido ya no predice un evento aversivo.
En conclusión, la anisomicina es una herramienta farmacológica que, al inhibir la síntesis de proteínas, ha permitido desentrañar aspectos complejos de la neurobiología de la memoria. Los estudios con anisomicina han desafiado la dicotomía simple de MCP independiente de proteínas y MLP dependiente de proteínas, al demostrar que la síntesis proteica es crucial para las etapas tempranas de la plasticidad en circuitos específicos como el CA3 del hipocampo, y también para la formación de memorias de extinción. Estos hallazgos subrayan la naturaleza dinámica y molecularmente compleja de cómo el cerebro forma, mantiene y modifica nuestros recuerdos.
Si quieres conocer otros artículos parecidos a Anisomicina: Inhibidor de Memoria y Extinción puedes visitar la categoría Neurociencia.

