Los modelos animales han sido una herramienta indispensable en la investigación neurocientífica durante décadas, proporcionando información valiosa sobre los mecanismos biomédicos y evolutivos del sistema nervioso, las enfermedades y el comportamiento. Sin embargo, su uso ha suscitado importantes debates éticos, clínicos y científicos que impulsan la búsqueda de métodos alternativos.
Modelos Animales: Un Legado Histórico
El uso de modelos animales en Neurociencia se remonta a civilizaciones antiguas como los egipcios, griegos y romanos. Los primeros registros incluyen animales como gallinas, perros, peces, palomas, cerdos y ratones, y posteriormente, las ranas se volvieron muy utilizadas. A finales del siglo XIX, se incorporaron organismos invertebrados como nematodos, insectos, planarias, moluscos y crustáceos. En el siglo XXI, los modelos animales más comunes incluyen roedores, nematodos, moscas de la fruta, pez cebra, conejillos de indias, hurones, hámsteres, gallinas, primates no humanos y grandes animales domesticados.
Estos modelos han proporcionado una comprensión profunda del sistema nervioso, los procesos cognitivos, las enfermedades neurodegenerativas, la evolución y el desarrollo de fármacos. Aunque ningún modelo animal puede replicar completamente el cerebro humano debido a la historia evolutiva única de cada especie, ofrecen una herramienta crucial para nuevos descubrimientos y terapias. Cada modelo tiene sus ventajas y desventajas, y el método comparativo y la perspectiva 'One Health' (Una Salud), que conecta a humanos y otros animales, ganan importancia para comprender las bases neurológicas y abordar enfermedades comunes desde una perspectiva evolutiva y biomédica.
La Importancia de los Modelos Animales: Perspectivas Evolutivas y Biomédicas
Los modelos animales han sido fundamentales en estudios evolutivos. Los vertebrados han desarrollado tejidos más especializados y estructuras neurológicas complejas, con sistemas nerviosos y vasculares ramificados, lo que los convierte en modelos adecuados para estudiar condiciones neurológicas humanas. Desde una perspectiva biomédica, han contribuido enormemente a explicar mecanismos y desarrollar nuevas terapias.
Mamíferos: Nuestros Parientes Cercanos y Modelos Clave
Estudiar directamente el origen del cerebro complejo y el sistema nervioso central (SNC) es un desafío. Sin embargo, los métodos comparativos y de desarrollo permiten determinar las alteraciones en el neocórtex durante la evolución mamífera. El enfoque comparativo examina características compartidas y especializaciones adaptativas, comparando cerebros de diversas ramas filogenéticas. El enfoque de desarrollo estudia los mecanismos genéticos y dependientes de la actividad que dan lugar a diferentes fenotipos adultos.
Primates no Humanos
Debido a su estrecha relación filogenética con los humanos, los estudios con primates no humanos (chimpancés, bonobos, macacos) ofrecen resultados con alta translatabilidad. Sus similitudes en organización cerebral, complejidad social y habilidades cognitivas los hacen invaluables. El modelo de macaco parkinsoniano llevó al descubrimiento de la estimulación cerebral profunda como terapia efectiva para la enfermedad de Parkinson. Los macacos Rhesus se usan en estudios evolutivos del cerebro humano, comportamiento y cognición, y en ellos se descubrieron las neuronas espejo. Chimpancés y bonobos son cruciales para entender cambios neurológicos/genéticos específicos de humanos (expansión cortical, comportamiento, cognición, lenguaje) y enfermedades neurodegenerativas (EA, EP, EH, demencia). Avances recientes incluyen terapias para el ictus, comprensión de funciones cognitivas y trastornos psiquiátricos, e interfaces cerebro-máquina. La introducción transgénica de secuencias genéticas humanas en macacos Rhesus ha mostrado desarrollo cerebral neoténico y mejora de la memoria a corto plazo, o el desarrollo de EH, abriendo vías para comprender y tratar estas enfermedades.
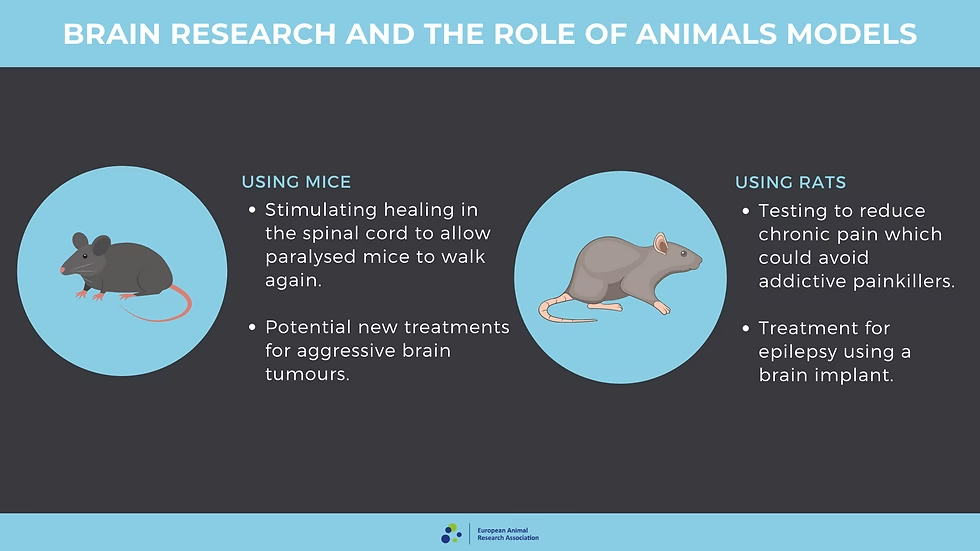
Roedores: La Base de la Investigación
Ratas y ratones son los modelos mamíferos más populares, utilizados en el 18-20% de la investigación del sistema nervioso mamífero. Se emplean para entender la arquitectura neuronal y la evolución cerebral. Existen cientos de miles de cepas mutantes y alteradas, lo que los convierte en modelos genéticos notables. Sus ventajas incluyen ciclo de vida corto, tamaño y facilidad de mantenimiento. La creación de quimeras ratón-humano permite estudiar el crecimiento neural humano y la patogénesis de enfermedades. Modelos quiméricos de ratón se han usado para estudiar EH, tratamiento de hipomielinización congénita, EA y síndrome de Down. Aspectos de la EP (trastornos del sueño, comportamiento, discapacidad motora), depresión, trastornos de ansiedad y fármacos antidepresivos se han modelado en roedores. Son un modelo importante para la EA, aunque la investigación preclínica en roedores requiere mayor rigor, replicación, tamaños de grupo adecuados y evaluación de efectos por sexo.
Otros Mamíferos
Los conejos se usan en estudios preclínicos de enfermedades fetales post-exposición materna a virus, infecciones virales fetales, pruebas de sustancias para el tratamiento de la Esclerosis Múltiple (EM), vacunas y antivirales en conejas preñadas, y efectos de anestesia/cirugía materna. Son ideales para vacunas maternas debido a similitudes embriológicas en el desarrollo del SNC. Presentan un modelo no transgénico para el estudio de la EA. Las similitudes en la curvatura axial y la tasa de cierre del tubo neural con embriones humanos los hacen relevantes para estudiar anencefalia y espina bífida. También se investigó en conejos la evolución de los patrones de cierre del tubo neural. Los cerdos son otro modelo mamífero con perspectivas evolutivas (cierre del tubo neural) y biomédicas (EH, Neurofibromatosis tipo 1), con similitudes anatómicas, fisiológicas y de desarrollo con humanos. Gatos y perros son modelos de compañía notables, sirviendo de puente entre roedores y humanos. Comparten enfermedades neurológicas humanas como tumores cerebrales, epilepsia, lesión medular, ictus y EA. También se estudian cambios relacionados con la edad y atrofia cerebral en ellos.
Vertebrados no Mamíferos: El Pez Cebra
El pez cebra (Danio rerio) ha ganado popularidad por sus embriones/larvas transparentes (visualización en tiempo real), facilidad de cría y bajo costo. Se usa en estudios de función cerebral, trastornos, comportamiento, condiciones inducidas por fármacos y respuestas a fármacos. Es un modelo para trastornos neuroconductuales (depresión, ansiedad) y del neurodesarrollo (epilepsia, esquizofrenia, discapacidad intelectual, TEA). Comparte con mamíferos las tres divisiones básicas del cerebro vertebral: prosencéfalo, mesencéfalo y rombencéfalo. Su relevancia traslacional para humanos es alta.
Invertebrados: Simplicidad y Conservación
Las comparaciones entre el SNC de vertebrados e invertebrados cordados (tunicados, cefalocordados como el anfioxo) ayudan a comprender la evolución del SNC vertebral, aunque hay debate sobre su origen. El anfioxo (Branchiostoma lanceolatum) es clave por su posición filogenética para dilucidar transiciones evolutivas clave. Patrones de expresión génica muestran que su región cerebral frontal se subdivide de forma similar al cerebro vertebral. Se usa en estudios de regeneración del tubo neural y notocorda. La investigación sobre evolución neuronal ha usado modelos como Hydra, medusas, esponjas y celentéreos. Moluscos gasterópodos fueron muy usados. Drosophila es clave para mecanismos moleculares y genéticos. C. elegans, Aplysia y Drosophila se usan para aspectos moleculares y celulares del aprendizaje y la memoria, cuyas bases fundamentales parecen organizarse de forma análoga en invertebrados y vertebrados.
La mosca de la fruta (Drosophila melanogaster) modela trastornos humanos (EA, EP, tumores neurales, daño del SNC, epilepsia). Aunque anatómicamente diferente, conserva vías neurales moleculares esenciales. No modela hemorragias o infartos cerebrales por falta de vasos. Permite expresar proteínas humanas. El nematodo (C. elegans) estudia procesos neurales (función de circuitos, transmisión sináptica), autismo y enfermedades (EP, EA). Sus ventajas son ciclo de vida corto, genoma secuenciado y un sistema nervioso mínimo (~300 neuronas) con red de conexiones sinápticas bien definida, ideal para estudiar envejecimiento, reparación de ADN y neurodegeneración. La babosa marina de California (Aplysia californica) es famosa por estudios de aprendizaje y memoria (corto/largo plazo). Es un buen sistema para estudiar aspectos moleculares, fisiológicos y conductuales de la EA, con muchos ortólogos proteicos humanos. Proporciona un modelo neural para investigación del comportamiento y aprendizaje a nivel de circuito, molecular, celular y de organismo. También permite estudiar efectos del envejecimiento en el transcriptoma de neuronas sensoriales.
| Modelo Animal | Perspectiva Evolutiva | Perspectiva Biomédica |
|---|---|---|
| Chimpancé (Pan troglodytes) | Cambios neurológicos específicos de humanos | Enfermedades neurodegenerativas (EA, EP, EH) |
| Macaco Rhesus (Macaca mulatta) | Neuronas espejo, evolución del comportamiento y cognición | Desarrollo cerebral neoténico, EP, EH |
| Ratón (Mus musculus) | Arquitectura neuronal, evolución cerebral, cierre del tubo neural | SNC quimérico humanizado, EH, EP, Síndrome de Down, hipomielinización |
| Rata (Rattus norvegicus) | Arquitectura neuronal, evolución cerebral, cierre del tubo neural | Depresión, trastornos de ansiedad, fármacos antidepresivos |
| Conejo Europeo (Oryctolagus cuniculus) | Evolución del cierre del tubo neural | Tratamiento de EM, EA, efectos neurológicos de vacunas/antivirales, anencefalia, espina bífida |
| Pez Cebra (Danio rerio) | Evolución del cerebro vertebral, función motora, cognición | Epilepsia, esquizofrenia, discapacidad intelectual, TEA, depresión, ansiedad |
| Mosca de la Fruta (Drosophila melanogaster) | Vías neurales moleculares conservadas | EA, EP, tumores neurales, daño del SNC, epilepsia |
| Nematodo (Caenorhabditis elegans) | Evolución de procesos neurales (circuitos, sinapsis) | Neurodegeneración, autismo, EP, EA |
| Babosa Marina (Aplysia californica) | Aprendizaje, memoria (corto/largo plazo) | EA |
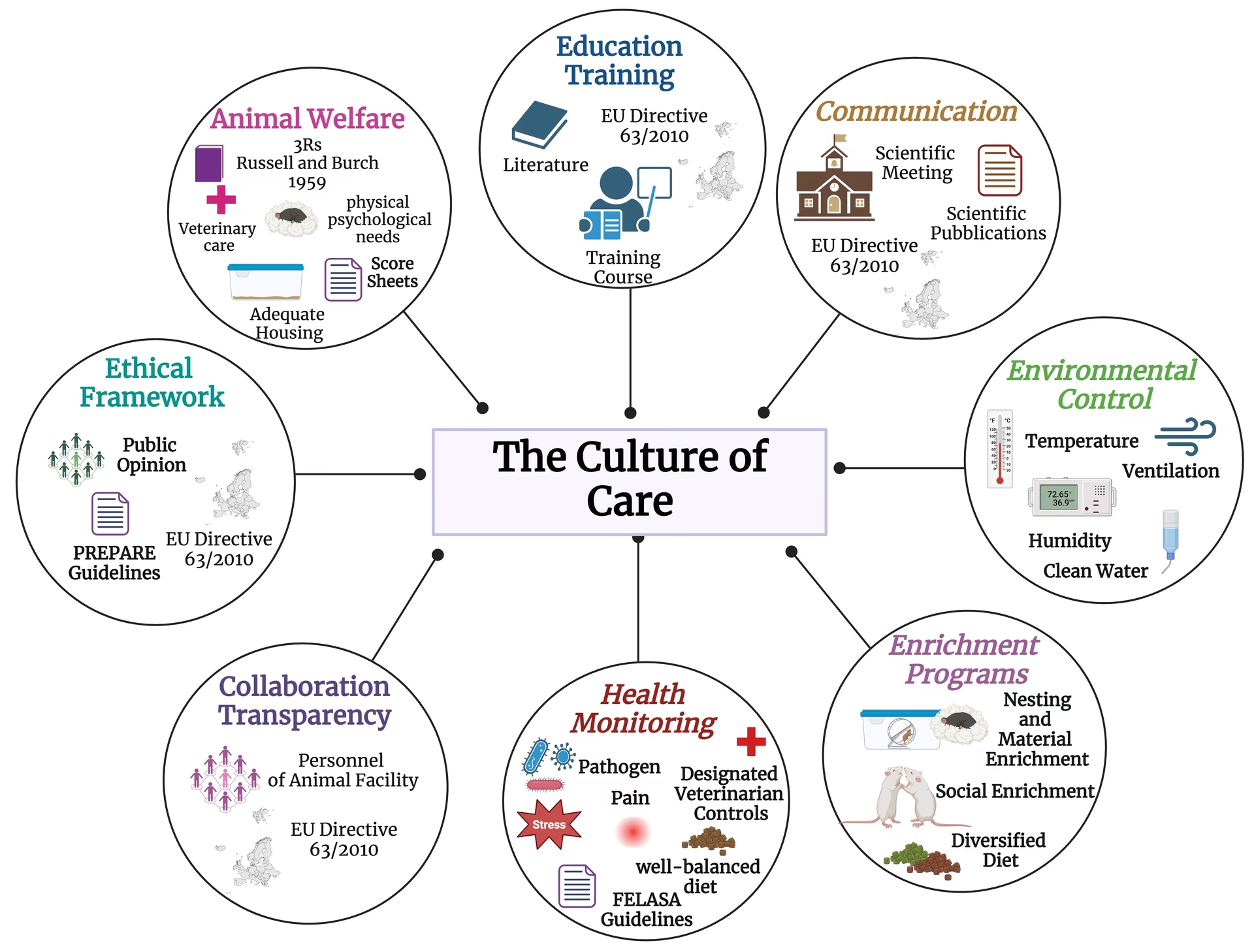
Consideraciones Éticas y el Principio de las 3Rs
El uso de animales en investigación, aunque vital para la salud humana y animal, plantea serias preocupaciones éticas sobre su bienestar. Los animales de laboratorio pueden experimentar dolor, estrés y sufrimiento. La discusión ética sobre el uso de animales se intensificó con la publicación de principios como el de las 3Rs en 1959. Estas buscan Reemplazar, Reducir y Refinar el uso de animales.

Existen leyes y directrices gubernamentales en todo el mundo para regular la experimentación animal, como la Laboratory Animal Welfare Act en EE. UU., el Animals (Scientific Procedures) Act 1986 (ASPA) en el Reino Unido o la Directive 2010/63/EU en la Unión Europea. Instituciones como la IACUC en EE. UU. o la NC3Rs en el Reino Unido promueven prácticas éticas y alternativas. Se ha confirmado que los animales experimentan dolor y angustia, incluso con manejo suave, mostrando marcadores de estrés. A pesar de su contribución, la translatabilidad de los resultados animales a humanos es a menudo limitada. La FDA reconoce que los modelos animales no predicen completamente la seguridad de los fármacos en humanos; casi el 90% del desarrollo de fármacos falla, en parte por esta razón. En neurociencia conductual, la predicción de resultados en humanos falla en más del 90% de los casos. En enfermedades neurodegenerativas, a pesar de los avances, los ensayos preclínicos en animales han sido decepcionantes. Además, el costo de la investigación animal es alto y retrasa el proceso de desarrollo de fármacos.
Alternativas Innovadoras a los Modelos Animales
Estos desafíos han impulsado el interés en enfoques alternativos. Un número creciente de estudios se centra en métodos in vitro (cultivo celular, microscopía) e in silico (modelado computacional). Avances tecnológicos han llevado a estrategias como organoides, sistemas microfisiológicos (órganos en chips, OoCs), células madre pluripotentes inducidas (iPSCs), métodos de imagen avanzados, y modelado computacional (docking molecular, modelos PBPK, modelos QSAR).
Enfoques Alternativos en Detalle
Las técnicas in vitro incluyen cultivos celulares 2D y 3D. Los cultivos 2D son simples y de bajo costo, pero no reflejan la fisiología real del tejido. Los modelos 3D, como los organoides, imitan mejor el entorno celular in vivo, proporcionando datos más precisos para enfermedades, descubrimiento de fármacos e interacciones célula-célula. Los organoides cerebrales, por ejemplo, recapitulan la construcción del tejido, la variedad celular y la maduración, cerrando la brecha con las características in vivo. Los OoCs, como los modelos cerebro en chip, reproducen funciones orgánicas esenciales en entornos normales y patológicos. Otros OoCs relevantes en Neurociencia incluyen la unidad neurovascular, la barrera hematoencefálica y los chips de transducción de señal nerviosa. Estos métodos ofrecen beneficios como menor costo, menor tiempo y procedimientos experimentales menos complejos. Permiten pruebas directas en tejidos humanos, superando problemas de translatabilidad animal. Se han usado técnicas de cultivo celular (3D, organoides, organotípicos, microfluídicos) y microscopía para modelar enfermedades neurodegenerativas (EA, FTD, EP, EH, EM, ELA), trastornos psiquiátricos (esquizofrenia), daño del SNC (lesión axonal, mielinización, respuesta a químicos) y neurodesarrollo. Los organoides neurales derivados de células madre pluripotentes humanas, combinados con aprendizaje automático, predicen neurotoxicidad y modelan trastornos del neurodesarrollo. Las iPSC y ESC humanas se han usado para construir la barrera hematoencefálica y estudiar enfermedades genéticas como EA y síndrome de Rett.
Los métodos in silico (computacionales) incluyen docking molecular, modelos QSAR y modelos PBPK. Se han usado en estudios evolutivos y en Neurociencia para estudiar la evolución de redes neurales ligadas al lenguaje. En algunos estudios, solo se usó modelado computacional para neuronas del cerebro y médula espinal en control motor e ictus. Técnicas estadísticas avanzadas y diseño experimental integrado también han reducido el uso de animales.
Sin embargo, las alternativas enfrentan desafíos. La tecnología de organoides necesita mejorar la heterogeneidad celular, simular el microambiente, y superar la inmadurez y la falta de vascularización. Otros problemas incluyen la biocompatibilidad y costo de hidrogeles, y crear el microambiente inmune humano. Su uso plantea preocupaciones éticas (fuente de células madre, consentimiento, estado moral/legal, potencial de adquirir características humanas, edición genética, quimeras, trasplante, patentabilidad). Los métodos in silico enfrentan desafíos como la abundancia de datos, la necesidad de modelos computacionales de sistemas biológicos, métricas de evaluación estandarizadas, extracción de características, selección de características, interpretabilidad y combinación de métodos. Aunque ofrecen beneficios (menor costo, tiempo, complejidad), algunos investigadores creen que aún están en fase inicial y no pueden reemplazar completamente los modelos animales en investigación preclínica. Pocos métodos alternativos han sido aprobados por autoridades federales y se requiere financiación adicional para su desarrollo y validación.
Preguntas Frecuentes (FAQ)
¿Por qué se siguen utilizando animales en la investigación neurocientífica?
Los animales se utilizan porque son biológicamente similares a los humanos en muchos aspectos y son sensibles a numerosas enfermedades neurológicas. Las regulaciones a menudo exigen pruebas en animales antes de los ensayos en humanos para evaluar la seguridad y eficacia iniciales de tratamientos y fármacos. Aunque las alternativas crecen, la complejidad de un organismo completo aún es difícil de replicar totalmente in vitro o in silico.
¿Cuáles son los principales tipos de modelos animales?
Según la clasificación del texto, los tipos principales incluyen: Invertebrados (como moscas de la fruta o nematodos), Vertebrados (que incluye mamíferos, aves y anfibios), Mamíferos (como roedores, primates, cerdos y perros) y Modelos Animales Alternativos (como pez cebra y Daphnia magna), que se promueven para reducir el uso de animales tradicionales.
¿Qué son los modelos alternativos y cuáles son sus beneficios?
Los modelos alternativos son métodos de investigación que buscan reemplazar, reducir o refinar el uso de animales. Incluyen técnicas in vitro (cultivos celulares 3D, organoides, órganos en chips) y métodos in silico (modelado computacional). Sus beneficios potenciales incluyen menor costo, menor tiempo de desarrollo, mayor relevancia para los resultados humanos (al usar células humanas), y cumplimiento de principios éticos como las 3Rs.
¿Qué son las 3Rs en la ética de la investigación animal?
Las 3Rs son principios éticos fundamentales para el uso de animales en investigación: Reemplazo (evitar el uso de animales siempre que sea posible, usando métodos alternativos), Reducción (minimizar el número de animales utilizados sin comprometer la validez científica) y Refinamiento (mejorar las prácticas de manejo y experimentación para reducir el dolor, el estrés y el sufrimiento de los animales).
Conclusión
Los modelos animales han sido esenciales para el avance de la Neurociencia, proporcionando conocimientos cruciales desde perspectivas evolutivas y biomédicas. Sin embargo, es imperativo considerar el bienestar animal y abordar las limitaciones de translatabilidad a humanos. El auge de enfoques alternativos, como las técnicas in vitro e in silico, ofrece un camino prometedor para complementar y, eventualmente, reemplazar algunos modelos animales. Al adoptar estas alternativas y promover consideraciones éticas rigurosas, podemos avanzar en la investigación neurocientífica cumpliendo con nuestra responsabilidad hacia humanos y otros animales.
Direcciones Futuras
El futuro de la Neurociencia verá una aplicación creciente de métodos alternativos, mejorando el bienestar animal. Avances en cultivos 3D, organoides y sistemas órgano-en-chip, junto con ingeniería genética y células derivadas de pacientes, aumentarán su relevancia para el estudio de enfermedades y la detección de fármacos. La modelización computacional mejorada, incluyendo aprendizaje automático, permitirá predicciones más precisas. La colaboración interdisciplinaria será clave para traducir descubrimientos computacionales en aplicaciones terapéuticas.
Si quieres conocer otros artículos parecidos a Modelos Animales en Neurociencia puedes visitar la categoría Neurociencia.