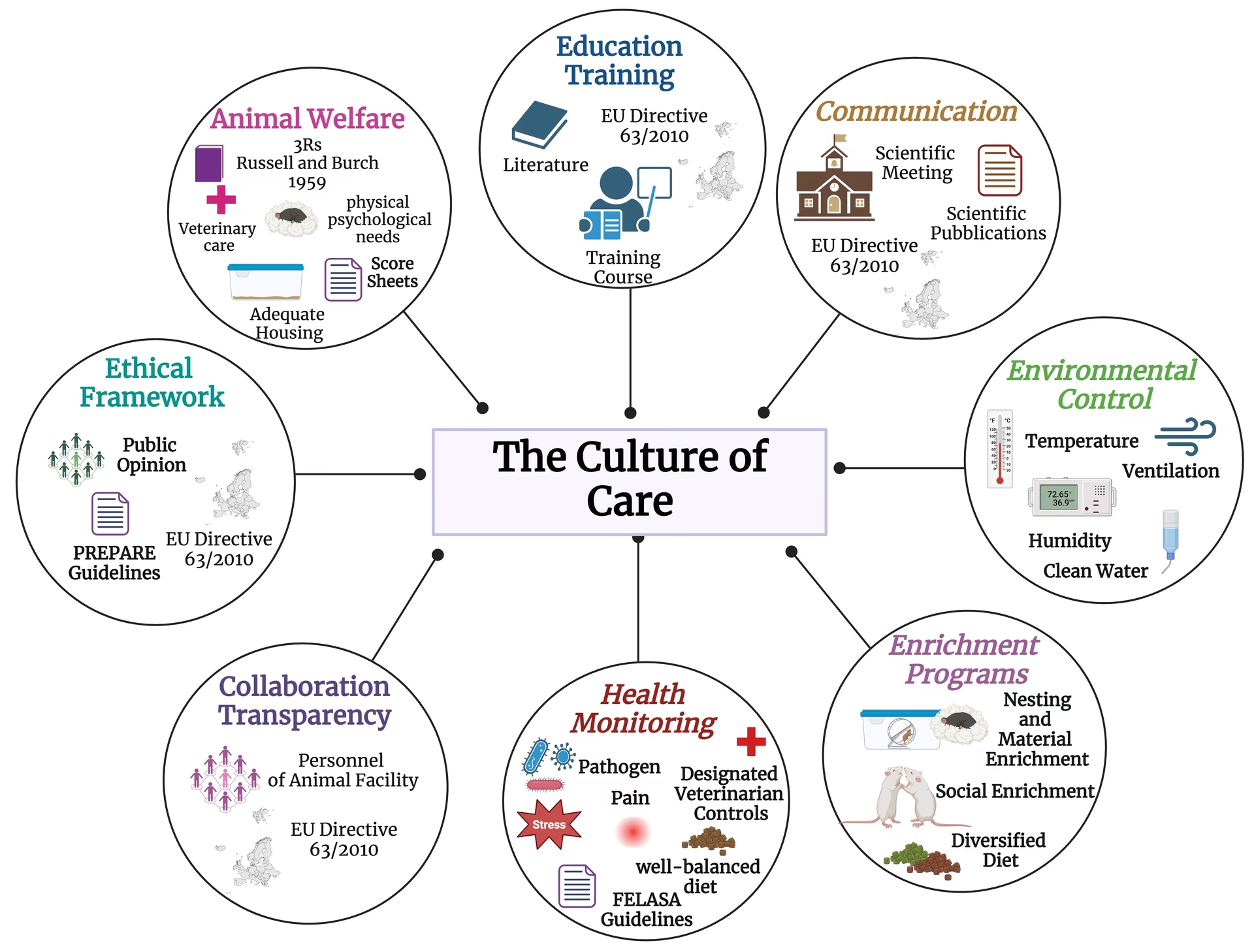
La investigación en neurociencia y farmacología es una tarea compleja que busca desentrañar los misterios del cerebro y desarrollar tratamientos efectivos para una vasta gama de enfermedades, desde trastornos neurodegenerativos hasta adicciones. Para lograrlo, los científicos recurren a diversas herramientas, y entre las más fundamentales se encuentran los modelos animales. Estos nos permiten estudiar procesos biológicos, probar la seguridad y eficacia de nuevos fármacos y comprender las bases neuronales de comportamientos complejos. Su uso es indispensable para el avance del conocimiento y la mejora de la salud humana, actuando como un puente esencial entre los estudios in vitro y las pruebas en humanos.
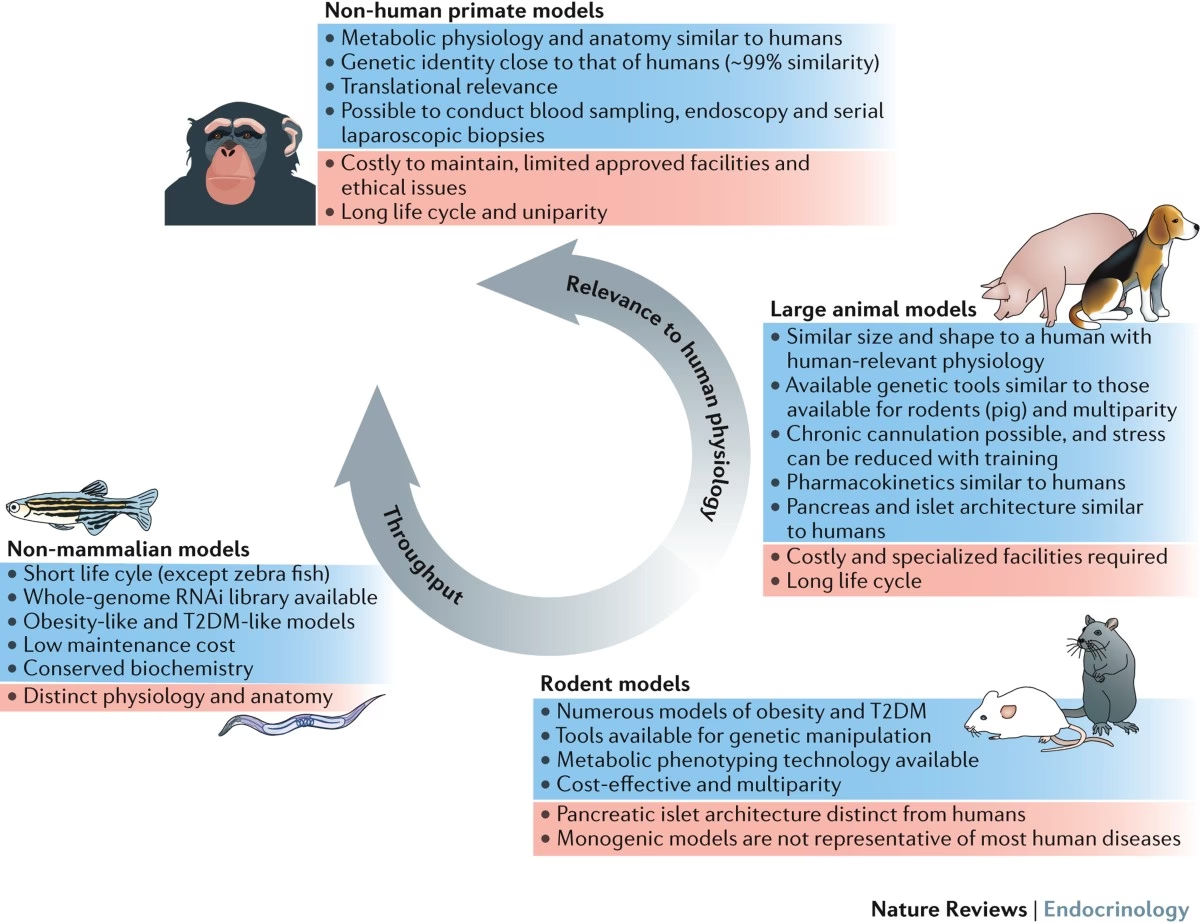
El proceso de descubrimiento de fármacos se ha refinado significativamente en las últimas décadas. Generalmente, sigue etapas bien definidas que incluyen la Identificación de la Diana Terapéutica, la Validación de la Diana, la Identificación del Compuesto Líder, la Optimización del Compuesto Líder y, finalmente, las pruebas preclínicas para evaluar la seguridad y la eficacia. Los modelos animales, especialmente los roedores, desempeñan un papel vital en varias de estas fases, proporcionando sistemas vivos para evaluar la compleja interacción entre un fármaco, un organismo y una enfermedad.
- Modelos Genéticamente Modificados: Herramientas Poderosas en el Descubrimiento de Fármacos
- Modelos Animales en el Estudio del Abuso y la Adicción a Drogas
- Principales Modelos para Investigar la Adicción
- Consideraciones Veterinarias, de Manejo y Éticas (IACUC)
- Preguntas Frecuentes sobre Modelos Animales
Modelos Genéticamente Modificados: Herramientas Poderosas en el Descubrimiento de Fármacos
Los avances recientes en la secuenciación del genoma han potenciado enormemente el uso de modelos animales, en particular los ratones. Técnicas como la recombinación homóloga, CRISPR/Cas9 y la transgénesis aleatoria permiten a los científicos diseñar animales específicamente para probar hipótesis sobre la función génica o para generar modelos que imiten enfermedades humanas. Estos modelos genéticamente modificados ofrecen un nivel de control sin precedentes sobre los factores biológicos que se estudian.
Identificación y Validación de Dianas Terapéuticas
Tradicionalmente, los genes candidatos a dianas terapéuticas se identificaban mediante cribados genéticos en sistemas in vitro o en modelos animales menos costosos, como el pez cebra o la mosca Drosophila melanogaster. Más recientemente, se han utilizado ratones en experimentos de cribado genético para identificar genes vinculados a vías fisiológicas y patológicas específicas. La principal ventaja de usar ratones para estos cribados es la posibilidad de validar directamente los resultados en modelos genéticos de enfermedades ya establecidos.
El objetivo principal de la validación de dianas es explorar si la eliminación o la sobreexpresión de un gen diana podría ser perjudicial para el organismo y confirmar que su modulación alivia los fenotipos asociados con una patología específica. Los modelos más comunes en la validación de dianas son los ratones knockout (KO), en los que se ha eliminado un gen específico. Los modelos KO ofrecen un alto grado de especificidad y, con un diseño correcto, son informativos sobre los efectos tóxicos de inactivar genes definidos.
Sin embargo, un problema con los ratones knockout constitutivos (donde el gen está ausente desde el desarrollo embrionario) es que la ausencia del gen en etapas tempranas puede tener efectos muy diferentes a los que tendría en un animal adulto. El uso de alelos KO condicionales acoplados a recombinasas Cre inducibles puede abordar este problema. Al regular la actividad de la recombinasa Cre, es posible inducir la eliminación genética de un gen diana en la edad adulta, modelando el tratamiento farmacológico de una manera más predictiva.
Además de probar posibles efectos negativos en la fisiología del organismo, un objetivo importante de los experimentos de validación de dianas es verificar que la modulación de los genes diana candidatos mejora la patología en modelos de enfermedades humanas. Un ejemplo notable de validación de diana en ratones fue descrito por Paul Greengard y colaboradores, donde utilizaron un enfoque de ARN de interferencia in vivo para modular la actividad de la proteína activadora de gamma-secretasa (GSAP), una diana potencial para el tratamiento del Alzheimer. El uso de un modelo shRNA proporcionó dos ventajas principales: su simplicidad genética y la reducción, no eliminación completa, de la actividad de GSAP, lo que imitaba más de cerca la dinámica de un tratamiento farmacológico que una eliminación genética total.
Identificación y Optimización de Compuestos Líder
Una vez que un gen es validado como diana para el desarrollo de fármacos, el siguiente paso es seleccionar moléculas capaces de interferir con su función. El uso de química combinatoria, junto con ensayos funcionales de alto rendimiento (HTS), permite la síntesis eficiente de potenciales moléculas terapéuticas.
Debido a los altos costos de desarrollo y mantenimiento de líneas transgénicas, los animales genéticamente modificados no se utilizan típicamente en la identificación inicial de moléculas activas. Sin embargo, después de la selección de un compuesto, los experimentos in vivo son cruciales antes de invertir más recursos para avanzar a la siguiente fase del proceso de desarrollo de fármacos.
Pruebas Preclínicas: Seguridad y Eficacia
Las pruebas in vivo para evaluar la seguridad y la eficacia son un paso crucial en la fase preclínica del desarrollo de fármacos. El uso apropiado de modelos genéticamente modificados puede ayudar a los investigadores preclínicos a abordar muchas de las preocupaciones planteadas por la introducción de un nuevo reactivo químico en el mercado farmacéutico.
Pruebas de Carcinogenicidad Preclínica
Un problema importante es la potencial actividad carcinogénica de los fármacos candidatos. Las agencias reguladoras son muy estrictas en la evaluación de este aspecto de la seguridad de los medicamentos. El modelo de ratón rasH2™ transgénico, desarrollado en Japón, es una herramienta indispensable para los laboratorios involucrados en la evaluación de la genotoxicidad de compuestos. Este modelo es más susceptible a los carcinógenos genotóxicos que los ratones de tipo salvaje. Esto permite una mayor sensibilidad en las pruebas de seguridad y una reducción tanto en el tamaño de la cohorte de animales de prueba como en los plazos del proyecto.
Modelos Animales en el Estudio del Abuso y la Adicción a Drogas
El abuso y la adicción a sustancias son problemas de salud pública ampliamente reconocidos, con un costo social y económico enorme. Institutos nacionales de salud dedican recursos significativos a esta área de investigación, y los experimentos con animales juegan un papel crítico en ella. Estos modelos son fundamentales para comprender la biología, la fisiopatología, los tratamientos clínicos y el cribado de fármacos con potencial de abuso. A diferencia de los estudios clínicos en humanos, en los modelos animales se pueden controlar más fácilmente las variables, permitiendo aislar los efectos directos de las drogas en el comportamiento del animal. Los estudios animales han demostrado que el efecto gratificante no depende de condiciones preexistentes; la exposición a la droga es suficiente para motivar el comportamiento de consumo. La auto-administración por animales de laboratorio de drogas abusadas por humanos apoya el concepto de que las drogas actúan como reforzadores universales, involucrando procesos biológicos comunes a los mamíferos.
A pesar de su valor, la investigación sobre la adicción a drogas es a menudo controvertida y puede ser objeto de críticas. Es vital comprender la base biológica de la dependencia y la adicción para que la sociedad perciba el valor equivalente de esta investigación en comparación con problemas médicos mejor comprendidos como enfermedades cardíacas o cáncer.
Principales Modelos para Investigar la Adicción
Los modelos animales tradicionales de abuso de drogas se enmarcan en la visión conductista que enfatiza la acción de las drogas como reforzadores positivos, al igual que los reforzadores 'naturales' como la comida o el agua. El principio fundamental es que aspectos del comportamiento están controlados por sus consecuencias. Se dice que una droga funciona como reforzador si el comportamiento para obtenerla se mantiene por encima del comportamiento para obtener solución salina u otras condiciones de control. Este paradigma ha sido fundamental para caracterizar las regiones cerebrales y las vías de señalización responsables de los comportamientos gratificantes, conocida como la 'vía de recompensa' (área tegmental ventral, núcleo accumbens, corteza prefrontal). Todas las drogas de abuso aumentan la señalización dopaminérgica en esta vía. Sin embargo, la adicción implica más que solo la recompensa; también incluye el deseo intenso (craving) y la pérdida de control sobre el consumo. La investigación más reciente se centra en modelar estas otras dimensiones, como la vulnerabilidad, la transición del uso controlado al compulsivo y la recaída.
Auto-administración de Fármacos
Este es quizás el modelo más directo para estudiar la correspondencia entre el comportamiento de consumo de drogas en humanos y animales. Implica entrenar a un animal para que se auto-administre una droga, generalmente presionando una palanca o picoteando una tecla en una cámara operante. Se utilizan diversas especies, incluyendo roedores, primates no humanos, perros y gatos.
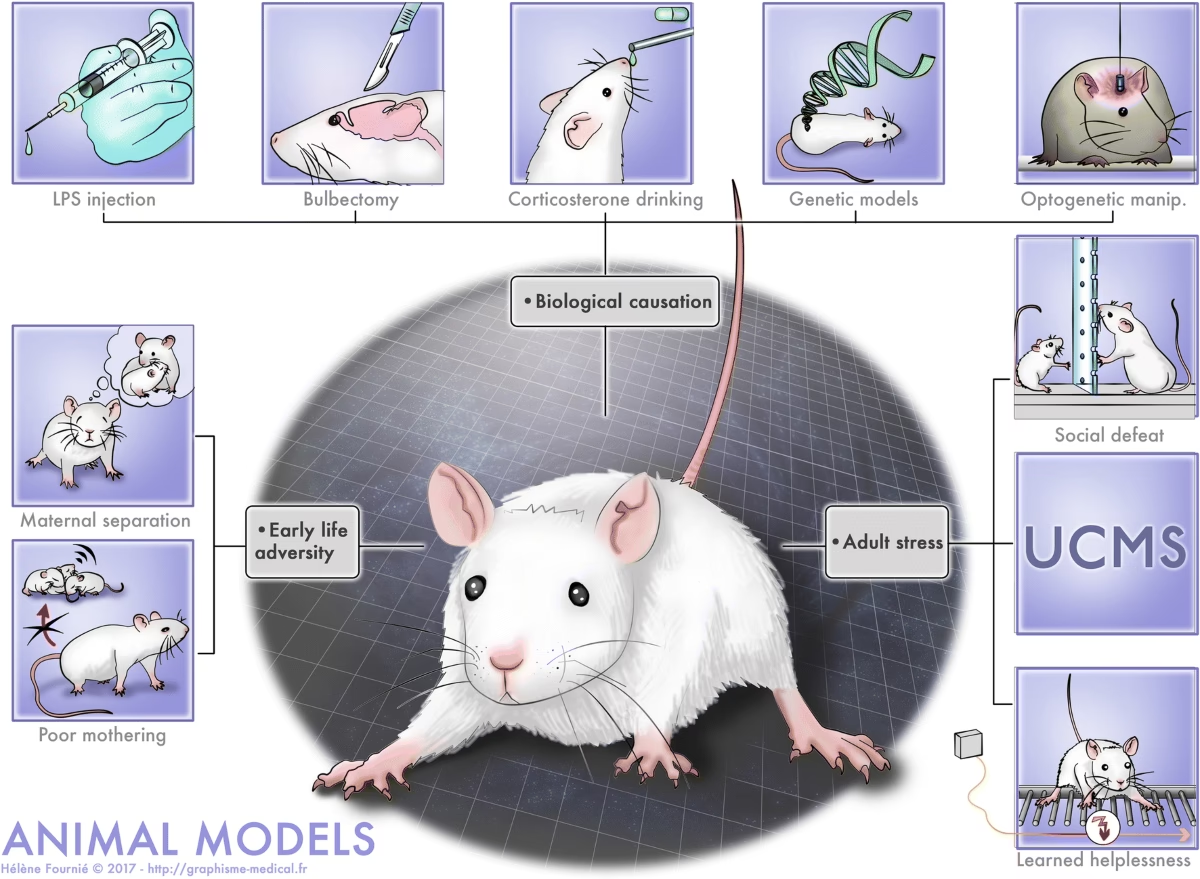
Las rutas de administración más comunes son intravenosa y oral, aunque también se usan otras como intracerebroventricular, intracraneal, inhalación, intragástrica e intramuscular. Generalmente, se elige la ruta más similar a la utilizada por humanos para esa droga particular (oral para alcohol, intravenosa/inhalación simulada para cocaína, heroína, nicotina). Los estudios han revelado que las drogas que son abusadas por humanos generalmente mantienen el comportamiento de auto-administración en animales, y viceversa. Además, se han observado patrones de consumo similares en humanos y animales para varias drogas, lo que valida el modelo.
El modelo de auto-administración se utiliza para estudiar la fase de inicio o adquisición, midiendo la rapidez con la que un animal aprende a auto-administrarse la droga. Esto ayuda a identificar factores biológicos y conductuales que predicen la vulnerabilidad. Se ha observado que factores como los niveles de corticosterona, la liberación de dopamina, la cepa genética, la preferencia por lo dulce, la impulsividad, la edad y el sexo pueden influir en la adquisición. Por ejemplo, las ratas hembra a menudo adquieren la auto-administración de cocaína y heroína más rápido que los machos.
También se utiliza para modelar la transición del uso controlado al compulsivo y el consumo excesivo, características fundamentales de la adicción humana. Esto se logra a menudo mediante procedimientos de auto-administración con acceso extendido (por ejemplo, 6 a 24 horas al día) en lugar de sesiones cortas y limitadas. Bajo condiciones de acceso extendido, los animales pueden mostrar patrones de consumo desregulados y un aumento progresivo en la ingesta, similar a la escalada observada en humanos. Estos modelos de acceso extendido han demostrado ser útiles para identificar factores que predicen la vulnerabilidad durante la transición al uso descontrolado, como las diferencias de sexo.
Preferencia de Lugar Condicionado (CPP)
Este modelo evalúa los efectos gratificantes (o aversivos) de una droga asociando sus efectos con un entorno particular. Los animales se entrenan en una cámara con dos compartimentos distintos (con diferentes señales visuales y táctiles). La administración de la droga se empareja consistentemente con uno de los compartimentos, y la administración de vehículo (placebo) con el otro. En un día de prueba, sin droga, se permite al animal acceder libremente a ambos compartimentos. Si la droga induce un estado positivo o 'gratificante', el animal pasará más tiempo en el compartimento asociado a la droga (preferencia de lugar). Si induce efectos negativos (como la abstinencia precipitada por un antagonista), el animal evitará ese compartimento (aversión de lugar).
La CPP puede proporcionar información sobre el potencial gratificante de nuevas drogas, evaluar el desarrollo de dependencia física (midiendo la aversión por abstinencia) y cribar compuestos terapéuticos que puedan bloquear los efectos gratificantes. Este modelo también ha sido útil para investigar diferencias individuales en la sensibilidad a los efectos gratificantes, como las diferencias de sexo en la respuesta a la cocaína.
Paradigma de Reinstauración
Este modelo se utiliza para investigar los mecanismos subyacentes a la recaída en el consumo de drogas. Los animales se entrenan para auto-administrarse una droga y luego se extingue el comportamiento (ya no reciben la droga al responder). Una vez que la respuesta se reduce, se evalúa la capacidad de varios estímulos para reinstaurar el comportamiento de búsqueda de drogas (respuestas no reforzadas). Se dice que un estímulo reinstaura la respuesta si causa un aumento en el comportamiento que solía ser reforzado por la droga.
Los estudios preclínicos han revelado que los estímulos que reinstauran la búsqueda de drogas en animales de laboratorio son similares a los que desencadenan la recaída en humanos, incluyendo la exposición a factores estresantes, pequeñas dosis de la droga misma (dosis 'priming') y señales ambientales asociadas con el consumo de drogas. Esto demuestra la validez predictiva de este modelo para estudiar los factores que influyen en la recaída y los mecanismos neurobiológicos subyacentes.
Modelos para la Dependencia Física y la Abstinencia
La dependencia física, donde el cuerpo se adapta a la presencia crónica de una droga, puede desempeñar un papel importante en el uso compulsivo, ya que los individuos pueden continuar consumiendo para evitar los síntomas desagradables de la abstinencia. Se utilizan procedimientos de sustitución y procedimientos de dependencia primaria para evaluar el potencial de una nueva droga o formulación para producir dependencia física.
Los procedimientos de sustitución implican establecer dependencia a una droga conocida de abuso y luego sustituirla por la droga novedosa o precipitar la abstinencia con un antagonista y luego administrar la droga novedosa. Si la droga novedosa suprime los síntomas de abstinencia o revierte la abstinencia precipitada, se predice que tiene un potencial de producción de dependencia similar a la droga conocida, basado en el fenómeno de la dependencia cruzada entre compuestos farmacológicamente similares (por ejemplo, diferentes opioides o depresores del SNC).
Los procedimientos de dependencia primaria buscan determinar si la administración repetida o continua de la droga novedosa por sí sola producirá cambios neuroadaptativos que resulten en dependencia física, manifestada por un síndrome de abstinencia al suspender la droga o administrar un antagonista. La presencia de un síndrome de abstinencia indica que la droga probablemente producirá dependencia física en humanos si se auto-administra crónicamente.
Los síndromes de abstinencia varían según la clase farmacológica de la droga. La abstinencia de opioides en roedores puede incluir diarrea, rinorrea, castañeo de dientes, temblores ('wet dog shakes') y disminución del consumo de alimentos. La abstinencia de nicotina puede manifestarse como retorcimientos, jadeos, temblores, castañeo de dientes y un aumento de la respuesta de sobresalto. La abstinencia de depresores del SNC como el etanol o las benzodiazepinas puede causar ansiedad, aumento de la presión arterial y convulsiones potencialmente mortales, lo que puede clasificar estos estudios en categorías de dolor o distrés más altas, requiriendo monitorización cuidadosa y planes de contingencia.
Discriminación de Fármacos
El paradigma de discriminación de fármacos se considera un modelo preclínico de los efectos subjetivos de las drogas en humanos. Se basa en el aprendizaje estado-dependiente, donde los animales aprenden a discriminar entre los efectos internos de una droga y los de un vehículo, asociando cada estado (drogado vs. no drogado) con una respuesta operante diferente que es reforzada (por ejemplo, presionar una palanca izquierda bajo los efectos de la droga y una palanca derecha bajo los efectos del vehículo).
Una vez que el animal ha aprendido a discriminar, se evalúan compuestos novedosos para ver si sustituyen a la droga de entrenamiento (es decir, si el animal responde en la palanca asociada a la droga de entrenamiento bajo los efectos del nuevo compuesto). Si hay sustitución, se considera que el nuevo compuesto tiene efectos de estímulo discriminativo similares a los de la droga de entrenamiento y se predice que producirá efectos subjetivos similares en humanos. La correlación entre la sustitución en este modelo y los informes subjetivos en humanos es muy buena.
Aunque la discriminación de fármacos modela los efectos subjetivos, no mide directamente la 'preferencia' o 'recompensa' de la droga; para eso se usan la auto-administración y la CPP. Sin embargo, la discriminación de fármacos es una herramienta valiosa en la evaluación del potencial de abuso, a menudo utilizada junto con procedimientos de auto-administración para predecir si un nuevo compuesto podría ser abusado por humanos.

Consideraciones Veterinarias, de Manejo y Éticas (IACUC)
Los modelos animales de abuso y adicción a sustancias presentan desafíos únicos para el personal de laboratorio y los comités de ética en investigación con animales (IACUC). Los estudios suelen ser crónicos y complejos, involucrando instrumentación crónica (como catéteres intravenosos), necesidades especiales de alojamiento (a menudo alojamiento individual para proteger dispositivos o debido a efectos conductuales de las drogas), restricciones de comida o agua (para motivar las respuestas operantes a reforzadores), y el manejo del dolor y el distrés, especialmente durante los síndromes de abstinencia.
Los IACUC deben comprender los paradigmas experimentales complejos (horarios de refuerzo de razón fija o progresiva, CPP, reinstauración, extinción) y los términos asociados. El acceso a la droga de estudio está cuidadosamente controlado, minimizando el riesgo de sobredosis. Los animales entrenados son recursos valiosos, por lo que se prioriza su salud y longevidad.
La selección de especies, aunque a menudo se usan roedores, puede requerir primates no humanos por razones de validez del modelo (algunas clases de fármacos, como los antagonistas de NMDA, son difíciles de demostrar como reforzadores en roedores pero no en primates), similitudes anatómicas y fisiológicas (distribución o subtipos de receptores, como los opioides, son más similares entre humanos y primates), o perfiles farmacocinéticos (la biodisposición y la vida media pueden ser predictores más precisos de los parámetros humanos en primates). Las diferencias en la vida media son cruciales para extrapolar estudios de dependencia física.
Los protocolos deben describir los efectos negativos anticipados de las drogas, incluyendo dolor, distrés, efectos sobre el consumo de comida/agua, reacciones adversas a compuestos novedosos y síntomas de abstinencia. El manejo del dolor, especialmente después de procedimientos quirúrgicos para implantar dispositivos, requiere elegir analgésicos que no interfieran con los efectos conductuales de las drogas en estudio (por ejemplo, usar AINE en lugar de opioides).
La cronicidad de los estudios implica que los animales pueden envejecer en el laboratorio, haciendo relevantes enfermedades geriátricas o crónicas (cáncer, amiloidosis, insuficiencia orgánica) que rara vez se ven en estudios más cortos. También deben considerarse enfermedades infecciosas comunes en roedores o primates.
Las restricciones alimentarias, necesarias para motivar el comportamiento operante, requieren un monitoreo regular del peso para asegurar que no se excedan los límites éticos definidos en el protocolo. El alojamiento individual, a menudo necesario, presenta desafíos para el enriquecimiento ambiental, que debe equilibrarse con la necesidad de minimizar variables experimentales.
El manejo de dispositivos crónicos indwelling, como los catéteres, requiere atención a problemas como la colocación incorrecta, la protección contra daños, la pérdida de permeabilidad (trombosis, oclusión) y la infección. Estos problemas se abordan con entrenamiento, materiales adecuados, técnica aséptica y, a veces, el uso de anticoagulantes o enzimas para mantener la permeabilidad.
Las propiedades farmacológicas de las drogas, como el pH de las soluciones de inyección, deben considerarse cuidadosamente para evitar dolor o daño tisular en el sitio de inyección. La administración de drogas inhaladas, especialmente en cámaras de humo, presenta desafíos para asegurar un flujo de oxígeno adecuado.
El equipo especializado (cámaras operantes, brazos giratorios, cámaras de inhalación) requiere protocolos de saneamiento rigurosos, teniendo en cuenta las partes electrónicas sensibles y la prevención de la transmisión de enfermedades entre animales. También son esenciales los planes de contingencia para fallos eléctricos que podrían afectar los sistemas de infusión continua.
Finalmente, el personal de cuidado animal y veterinario debe ser consciente de la importancia de minimizar los cambios ambientales. Variables como cambios de personal, olores, ruidos de construcción, cambios de lecho, el ciclo de luz/oscuridad, el enriquecimiento y el uso de medicamentos para tratar enfermedades pueden afectar significativamente el comportamiento de los animales en estudios de drogas y, por lo tanto, los resultados de la investigación. La comunicación oportuna entre el personal y los investigadores es crucial para planificar y minimizar cualquier impacto adverso.
Preguntas Frecuentes sobre Modelos Animales
¿Por qué se utilizan animales en la investigación farmacológica?
Los modelos animales son necesarios porque permiten estudiar sistemas biológicos complejos (como el cerebro y el comportamiento) en un organismo vivo e intacto. Son cruciales para probar la seguridad y eficacia de nuevos fármacos antes de que puedan ser probados en humanos, proporcionando información vital que no puede obtenerse de estudios in vitro o simulaciones por computadora.
¿Son éticos los modelos animales?
El uso de animales en la investigación es un tema de debate ético. Sin embargo, se considera indispensable para avanzar en nuestra comprensión de las enfermedades y desarrollar tratamientos que salvan vidas y mejoran la salud humana y animal. La investigación está estrictamente regulada por comités de ética (como los IACUC en EE. UU.) que revisan y aprueban los protocolos, asegurando que se apliquen los principios de las 3 R (Reemplazo, Reducción y Refinamiento) para minimizar el número de animales utilizados y cualquier posible dolor o distrés.
¿Qué especies son las más comunes?
Los roedores, especialmente ratones y ratas, son las especies más utilizadas debido a su tamaño, costo, facilidad de manejo, reproducción rápida y la disponibilidad de herramientas genéticas avanzadas. Otras especies importantes incluyen primates no humanos (especialmente para estudios de abuso de drogas o neurociencia traslacional), pez cebra y Drosophila melanogaster (para cribados genéticos iniciales), y a veces perros o gatos para estudios específicos.
¿Cómo ayudan a entender la adicción?
Los modelos animales permiten estudiar aspectos clave de la adicción, como la auto-administración (que modela el consumo), la preferencia de lugar (que modela los efectos gratificantes), la reinstauración (que modela la recaída) y los síndromes de abstinencia (que modelan la dependencia física). Ayudan a identificar las vías cerebrales y los mecanismos moleculares implicados en la adicción y a probar la efectividad de posibles tratamientos farmacológicos o conductuales.
| Modelo | Lo que mide principalmente | Aplicación típica |
|---|---|---|
| Auto-administración de Fármacos | Comportamiento de búsqueda y consumo de drogas, efectos reforzadores, patrones de ingesta. | Evaluar potencial de abuso, estudiar mecanismos de refuerzo, modelar adquisición, escalada y uso compulsivo. |
| Preferencia de Lugar Condicionado | Efectos gratificantes o aversivos de una droga asociados a un entorno. | Cribado rápido de efectos gratificantes/aversivos, evaluar dependencia física (por aversión a la abstinencia), estudiar mecanismos de recompensa. |
| Paradigma de Reinstauración | Vulnerabilidad a la recaída en la búsqueda de drogas después de la abstinencia. | Identificar disparadores de recaída (estrés, señales, priming), probar fármacos para prevenir recaídas, estudiar mecanismos neurobiológicos de la recaída. |
| Discriminación de Fármacos | Efectos subjetivos o estado interno inducido por una droga. | Predecir efectos subjetivos en humanos, evaluar si nuevos compuestos actúan a través de mecanismos similares a drogas conocidas de abuso. |
Si quieres conocer otros artículos parecidos a Modelos Animales en Neurociencia y Farmacología puedes visitar la categoría Neurociencia.