El cerebro humano es una máquina de asombrosa complejidad, donde miles de millones de neuronas se comunican en una intrincada red. Sin embargo, esta delicada maquinaria puede verse alterada por la acumulación de ciertas sustancias, entre ellas, una proteína llamada amiloide. La acumulación anormal de amiloide en el cerebro es un sello distintivo de varias enfermedades neurodegenerativas, con consecuencias devastadoras para la función cognitiva y la salud en general. Entender qué causa estos depósitos y cómo afectan a las células cerebrales es crucial para el desarrollo de terapias efectivas.
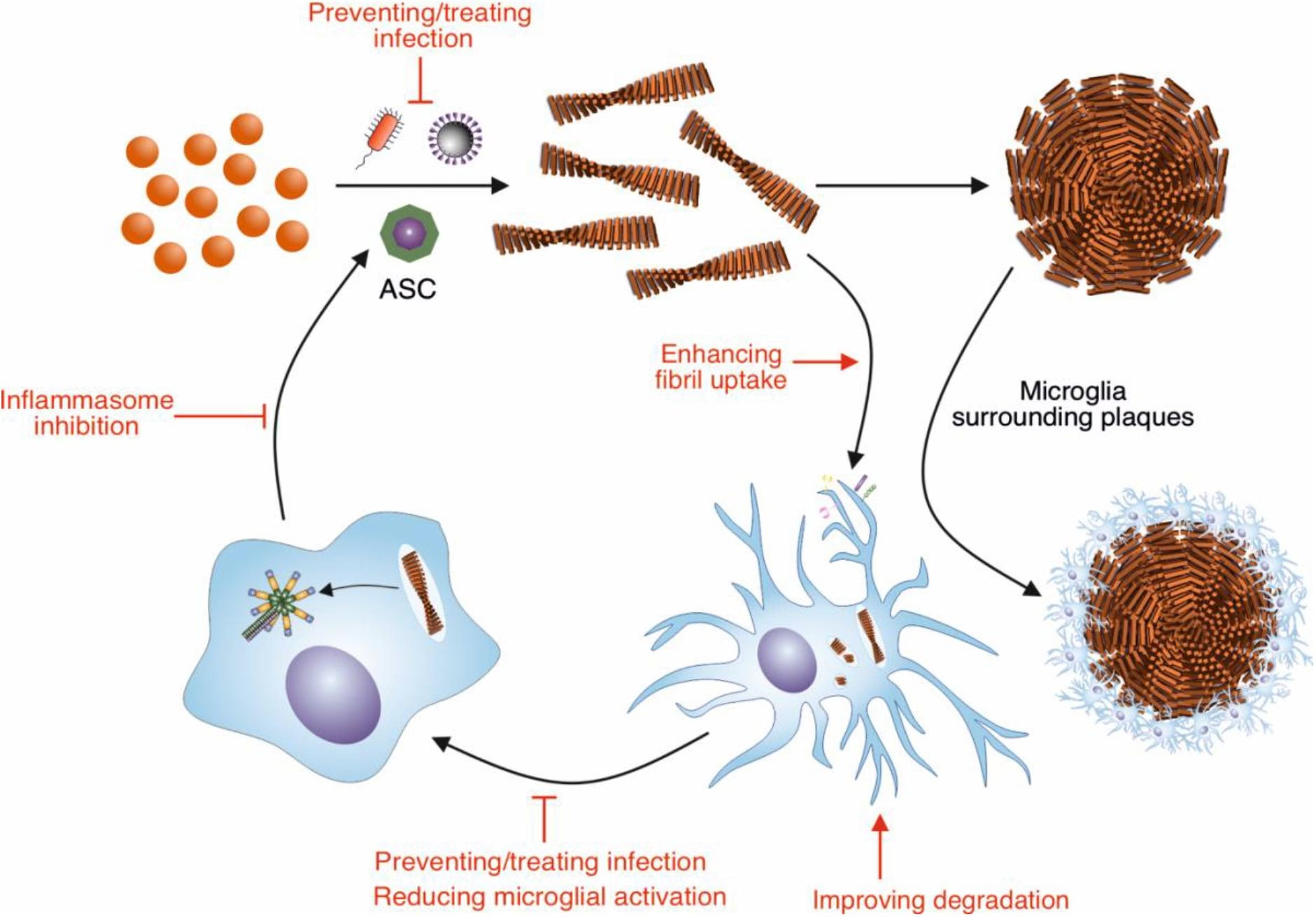
El amiloide beta es una proteína que se encuentra de forma natural en el cerebro. En condiciones normales, esta proteína se produce y se elimina sin problemas. Sin embargo, en ciertas situaciones, el amiloide beta puede plegarse de forma incorrecta y agruparse, formando placas pegajosas. Estas placas se acumulan entre las neuronas, interrumpiendo su comunicación y función. Aunque el amiloide beta es el tipo más conocido relacionado con enfermedades neurodegenerativas, otras proteínas amiloides también pueden acumularse y causar daño.
- ¿Qué son los Depósitos de Amiloide y Dónde se Acumulan?
- Angiopatía Amiloide Cerebral Hereditaria: Diversidad y Consecuencias
- El Amiloide y la Muerte Neuronal: Un Vínculo Fatal
- Cómo Placas y Ovillos Dañan el Cerebro
- ¿Se Puede Prevenir la Acumulación de Amiloide?
- Preguntas Frecuentes sobre el Amiloide Cerebral
¿Qué son los Depósitos de Amiloide y Dónde se Acumulan?
Los depósitos de amiloide son agregados anormales de proteínas mal plegadas. En el contexto de las enfermedades cerebrales, el foco principal suele estar en el péptido beta-amiloide. Este péptido se deriva de una proteína precursora amiloide (APP) más grande. En un cerebro sano, las enzimas cortan la APP en fragmentos que son eliminados. Pero cuando este proceso falla, los fragmentos de beta-amiloide se agrupan y forman oligómeros solubles, luego fibrillas insolubles y finalmente las distintivas placas amiloides que se depositan fuera de las neuronas.
Además de las placas que se forman en el tejido cerebral (parénquima), los depósitos de amiloide también pueden acumularse en las paredes de los vasos sanguíneos del cerebro. Esta acumulación se conoce como angiopatía amiloide cerebral (AAC). Cuando la AAC tiene una causa genética, se denomina angiopatía amiloide cerebral hereditaria. Esta condición es particularmente grave porque debilita los vasos sanguíneos, aumentando el riesgo de accidentes cerebrovasculares (derrames) y hemorragias cerebrales.
Angiopatía Amiloide Cerebral Hereditaria: Diversidad y Consecuencias
La angiopatía amiloide cerebral hereditaria es un grupo de trastornos genéticos caracterizados por la acumulación de depósitos de proteína amiloide en los vasos sanguíneos del cerebro. Esta acumulación provoca una enfermedad vascular que puede tener consecuencias devastadoras. Las personas afectadas a menudo experimentan una pérdida progresiva de la función intelectual, lo que lleva a la demencia, así como accidentes cerebrovasculares y otros problemas neurológicos, que generalmente comienzan en la mediana edad. Debido al deterioro neurológico, esta condición suele ser mortal, a menudo en la sexta década de vida, aunque la esperanza de vida puede variar dependiendo de la gravedad de los síntomas.
Existen varios tipos de angiopatía amiloide cerebral hereditaria, que se distinguen principalmente por su causa genética y los síntomas específicos que presentan. Estos tipos a menudo reciben el nombre de la región geográfica donde fueron diagnosticados por primera vez. Aunque todos implican depósitos de amiloide en los vasos sanguíneos, las proteínas implicadas y las manifestaciones clínicas pueden diferir.

A continuación, exploramos algunos de los tipos más conocidos:
- Tipo Holandés: Es la forma más común de AAC hereditaria. El accidente cerebrovascular es frecuentemente el primer signo y es fatal en aproximadamente un tercio de las personas con esta condición. Los supervivientes a menudo desarrollan demencia y sufren accidentes cerebrovasculares recurrentes. Alrededor de la mitad de las personas con el tipo holandés que han tenido uno o más accidentes cerebrovasculares experimentarán convulsiones recurrentes (epilepsia).
- Tipo Flamenco e Italiano: Las personas con estos tipos son propensas a sufrir accidentes cerebrovasculares recurrentes y demencia.
- Tipo Piamontés: Las personas con el tipo piamontés pueden tener uno o más accidentes cerebrovasculares y suelen experimentar movimientos alterados, entumecimiento u hormigueo (parestesias), confusión o demencia.
- Tipo Islandés: El primer signo del tipo islandés es típicamente un accidente cerebrovascular seguido de demencia. Los accidentes cerebrovasculares asociados con el tipo islandés suelen ocurrir antes que en otros tipos, generalmente en la veintena o treintena.
- Tipo Ártico: Los accidentes cerebrovasculares son raros en las personas con el tipo ártico. El primer signo suele ser la pérdida de memoria, que luego progresa a demencia severa.
- Tipo Iowa: Los accidentes cerebrovasculares también son poco comunes en las personas con el tipo Iowa. Este tipo se caracteriza por pérdida de memoria, problemas con el vocabulario y la producción del habla, cambios de personalidad y movimientos musculares involuntarios (mioclonías).
- Tipos Británico y Danés: Dos tipos conocidos como demencia familiar británica y demencia familiar danesa se caracterizan por demencia y problemas de movimiento. Los accidentes cerebrovasculares son poco comunes en estos tipos. Las personas con el tipo danés también pueden presentar opacidad del cristalino (cataratas) y sordera.
Esta diversidad de síntomas y la edad de inicio subrayan la complejidad de las angiopatías amiloides hereditarias y la necesidad de un diagnóstico genético preciso.
Tabla Comparativa de Tipos de Angiopatía Amiloide Cerebral Hereditaria
Para visualizar mejor las diferencias, presentamos una tabla comparativa de algunos de los tipos de AAC hereditaria mencionados:
| Tipo | Proteína Implicada (generalmente) | Síntomas Principales | Accidentes Cerebrovasculares | Demencia | Otros Síntomas | Edad de Inicio (generalmente) |
|---|---|---|---|---|---|---|
| Holandés | Beta-Amiloide | Accidente cerebrovascular, Demencia | Comunes, a menudo el primer signo | Común, especialmente después de ACV | Epilepsia (en sobrevivientes de ACV) | Mediana edad |
| Flamenco | Beta-Amiloide | Accidente cerebrovascular, Demencia | Recurrentes | Común | Mediana edad | |
| Italiano | Beta-Amiloide | Accidente cerebrovascular, Demencia | Recurrentes | Común | Mediana edad | |
| Piamontés | Beta-Amiloide | ACV, Demencia | Uno o más | Típica | Problemas de movimiento, Parestesias, Confusión | Mediana edad |
| Islandés | Cistatina C | Accidente cerebrovascular, Demencia | Típico, a menudo el primer signo y temprano | Típica, después de ACV | Veintena/Treintena | |
| Ártico | Beta-Amiloide | Pérdida de memoria, Demencia severa | Raros | Común, progresiva | Mediana edad | |
| Iowa | Beta-Amiloide | Pérdida de memoria, Problemas del habla, Cambios de personalidad | Poco comunes | Común | Mioclonías | Mediana edad |
| Británico | ABri (derivada de BRI2) | Demencia, Problemas de movimiento | Poco comunes | Común | Mediana edad | |
| Danés | ADan (derivada de ITM2B) | Demencia, Problemas de movimiento | Poco comunes | Común | Cataratas, Sordera | Mediana edad |
Es importante destacar que, si bien la angiopatía amiloide hereditaria es una causa específica de acumulación de amiloide vascular, la acumulación de amiloide beta en el parénquima cerebral es más comúnmente asociada con la enfermedad de Alzheimer.
El Amiloide y la Muerte Neuronal: Un Vínculo Fatal
Una de las preguntas más apremiantes en la investigación de las enfermedades neurodegenerativas ha sido cómo los depósitos proteicos como las placas de amiloide y los ovillos de tau (otra proteína que se acumula dentro de las neuronas en el Alzheimer) causan la muerte de las células cerebrales. Un estudio reciente publicado en la revista Science, liderado por el Profesor Bart De Strooper y el Dr. Sriram Balusu, ha arrojado luz sobre este proceso.
La investigación descubrió que las neuronas inician una forma de muerte celular programada, conocida como necrosis, cuando se exponen a las placas de amiloide y a los ovillos de tau. La necrosis es un tipo de muerte celular inflamatoria que difiere de la apoptosis (otra forma de muerte celular programada). Crucialmente, el equipo de investigación también fue capaz de prevenir la muerte de las neuronas y rescatarlas en el proceso. Este descubrimiento abre nuevas vías para posibles tratamientos futuros.
La enfermedad de Alzheimer es la forma más común de demencia y representa una carga significativa para los pacientes, las familias y la sociedad en general. Aunque ha habido avances recientes en tratamientos que ralentizan la progresión de la enfermedad, actualmente no existe una cura, en parte porque la causa subyacente aún no se comprende completamente.
El nuevo estudio revela algunos de los mecanismos biológicos que subyacen a la enfermedad. Sugiere que una vía conocida como necroptosis se activa en las neuronas en respuesta al amiloide y la tau, lo que lleva a su muerte. Además, los investigadores encontraron que los niveles de una molécula llamada MEG3 aumentaron significativamente en las neuronas humanas expuestas al amiloide y la tau, de manera similar a lo que se observa en pacientes con Alzheimer. Sorprendentemente, la sola presencia de MEG3 fue suficiente para desencadenar la vía de la necroptosis en neuronas humanas en un entorno de laboratorio.

Para llegar a estas conclusiones, los investigadores utilizaron un modelo innovador. Implantaron neuronas humanas sanas en los cerebros de modelos de ratón con Alzheimer. Las células humanas se degeneraron de manera similar a como lo hacen en el cerebro humano, lo que permitió a los científicos estudiarlas durante el envejecimiento cerebral y obtener una nueva perspectiva sobre los procesos subyacentes al Alzheimer. Lo notable fue que solo las neuronas humanas, y no sus contrapartes de roedores, mostraron características de la enfermedad de Alzheimer vistas en los cerebros de los pacientes, incluyendo ovillos de tau y una pérdida significativa de células neuronales. Esto sugiere que puede haber factores específicos humanos involucrados en la enfermedad de Alzheimer que los modelos de ratón estándar no pueden replicar.
El estudio también encontró que al reducir MEG3 y prevenir la necroptosis, los investigadores pudieron prevenir la muerte de las células. Se necesita más investigación para comprender exactamente cómo MEG3 desencadena la necroptosis, pero este descubrimiento representa un avance crucial en la comprensión de cómo el Alzheimer conduce a la pérdida de neuronas en el cerebro.
La necroptosis ya es un área activa de desarrollo de fármacos en el cáncer y la ELA (Esclerosis Lateral Amiotrófica). Si bien hay mucho más por explorar, estos hallazgos abren avenidas prometedoras para posibles terapias dirigidas a la enfermedad de Alzheimer, junto con enfoques tradicionales dirigidos al amiloide y la tau.
Cómo Placas y Ovillos Dañan el Cerebro
Más allá de la activación de vías de muerte celular programada como la necroptosis, las placas de amiloide y los ovillos de tau ejercen su daño a través de mecanismos más directos que interfieren con la función neuronal normal.
Las placas de amiloide, que se forman en el espacio entre las neuronas, actúan como obstáculos físicos y químicos. Interrumpen la comunicación entre las células nerviosas al interferir con las sinapsis, las uniones donde las neuronas transmiten señales. Es como si se interpusiera una barrera que dificulta que los mensajes pasen correctamente de una neurona a otra. Esta interrupción sináptica es una de las primeras etapas del daño cognitivo en la enfermedad de Alzheimer.
Por otro lado, los ovillos de tau se forman dentro de las neuronas. La proteína tau es un componente clave de los microtúbulos, que son como las vías de transporte dentro de la célula, esenciales para mover nutrientes, vesículas y otras moléculas vitales. En la enfermedad de Alzheimer, la proteína tau se fosforila de manera anormal y se agrupa en filamentos retorcidos, formando los ovillos neurofibrilares. Estos ovillos desestabilizan los microtúbulos, lo que interrumpe el transporte celular. Es como si las vías de tren dentro de la neurona se retorcieran y colapsaran, impidiendo que los suministros lleguen a donde se necesitan. Esta interrupción del transporte lleva a la disfunción y, eventualmente, a la muerte de la neurona.
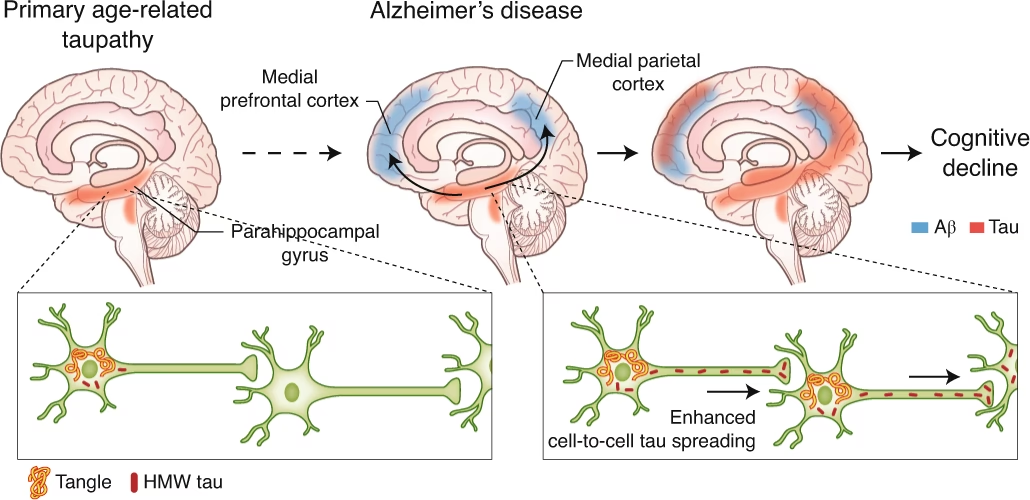
A medida que se acumulan más placas y ovillos, el daño se extiende por el cerebro, comenzando a menudo en las áreas relacionadas con la memoria (como el hipocampo) y luego afectando otras regiones. Esta propagación del daño neurodegenerativo es lo que causa la progresión de los síntomas, desde la pérdida de memoria leve en las etapas tempranas hasta la confusión severa, los problemas de lenguaje, los cambios de personalidad y la incapacidad para realizar tareas cotidianas en las etapas avanzadas.
¿Se Puede Prevenir la Acumulación de Amiloide?
Actualmente, no existe una forma definitiva de prevenir la acumulación de amiloide o curar las enfermedades que causa, como el Alzheimer o la angiopatía amiloide hereditaria. Sin embargo, la investigación sugiere que ciertos factores del estilo de vida pueden influir en el riesgo de deterioro cognitivo asociado con estas enfermedades.
Mantener el cerebro activo a través de actividades estimulantes como rompecabezas o aprender nuevas habilidades, seguir una dieta saludable rica en frutas y verduras, mantener la interacción social y gestionar condiciones de salud como la presión arterial alta y la diabetes pueden contribuir a la salud cerebral general y potencialmente mitigar el impacto de las patologías proteicas.
Es fundamental entender que estos consejos de estilo de vida son medidas de salud general del cerebro y no una cura o prevención directa de la acumulación de amiloide causada por factores genéticos o procesos patológicos específicos como los que ocurren en el Alzheimer o la AAC hereditaria. Sin embargo, un cerebro más sano podría ser más resiliente al daño causado por estas acumulaciones.
Preguntas Frecuentes sobre el Amiloide Cerebral
Aquí respondemos algunas preguntas comunes sobre los depósitos de amiloide en el cerebro:
- ¿Qué es el amiloide?
Es una proteína que se encuentra naturalmente en el cerebro. En condiciones normales, se elimina, pero en ciertas enfermedades puede agruparse y formar depósitos anormales fuera de las neuronas o en los vasos sanguíneos. - ¿Qué es la angiopatía amiloide cerebral?
Es la acumulación de proteína amiloide en las paredes de los vasos sanguíneos del cerebro, lo que los debilita y aumenta el riesgo de accidentes cerebrovasculares. Cuando es causada por factores genéticos, se llama angiopatía amiloide cerebral hereditaria. - ¿Cuántos tipos de angiopatía amiloide hereditaria hay?
Existen varios tipos, distinguidos por su causa genética y sus síntomas. Algunos ejemplos incluyen los tipos Holandés, Islandés, Ártico, Iowa, Británico y Danés, entre otros. - ¿El amiloide causa la muerte de las neuronas?
Sí, la investigación reciente sugiere que el amiloide (junto con la proteína tau) puede desencadenar una forma de muerte celular programada llamada necroptosis en las neuronas. - ¿Cómo dañan las placas y ovillos a las neuronas?
Las placas de amiloide fuera de las neuronas interrumpen la comunicación entre ellas. Los ovillos de tau dentro de las neuronas dañan las estructuras de transporte internas, lo que lleva a la disfunción y muerte celular. - ¿Se puede prevenir la acumulación de amiloide?
Actualmente no hay una prevención definitiva, especialmente para las formas genéticas. Sin embargo, mantener un estilo de vida saludable puede contribuir a la salud cerebral general.
En conclusión, la acumulación de depósitos de amiloide en el cerebro es un factor clave en el desarrollo de diversas enfermedades neurodegenerativas, desde la angiopatía amiloide cerebral hereditaria, con su impacto directo en los vasos sanguíneos y el riesgo de accidentes cerebrovasculares, hasta su papel en la compleja patología de la enfermedad de Alzheimer, donde contribuye a la formación de placas y, junto con la proteína tau, desencadena la muerte neuronal a través de mecanismos como la necroptosis. La continua investigación sobre las causas subyacentes y los mecanismos de daño del amiloide es fundamental para encontrar formas efectivas de prevenir, tratar y, en última instancia, curar estas devastadoras enfermedades.
Si quieres conocer otros artículos parecidos a Amiloide en el Cerebro: Causas y Efectos puedes visitar la categoría Neurociencia.
