El cerebro es un órgano con una demanda energética constante y elevada. Si bien su principal fuente de combustible es la glucosa que obtiene del torrente sanguíneo, también posee un mecanismo de respaldo crucial: el almacenamiento de glucógeno. Tradicionalmente considerado un reservorio energético primario de los astrocitos (células de soporte del cerebro), estudios recientes han revelado que las propias neuronas también pueden almacenar y degradar glucógeno, y que este proceso, conocido como glucogenólisis neuronal, es vital para funciones como la formación de la memoria. En este contexto emergente, la identificación de enzimas que participan en la degradación del glucógeno neuronal adquiere una importancia significativa. Una de estas enzimas, sorprendentemente, parece ser la alfa-amilasa (α-amilasa), conocida principalmente por su papel en la digestión de carbohidratos en la saliva y el páncreas. Investigaciones recientes sugieren que la presencia y función de la α-amilasa en el cerebro, particularmente en las neuronas, podrían tener implicaciones profundas para la cognición y estar vinculadas a enfermedades neurodegenerativas como el Alzheimer.
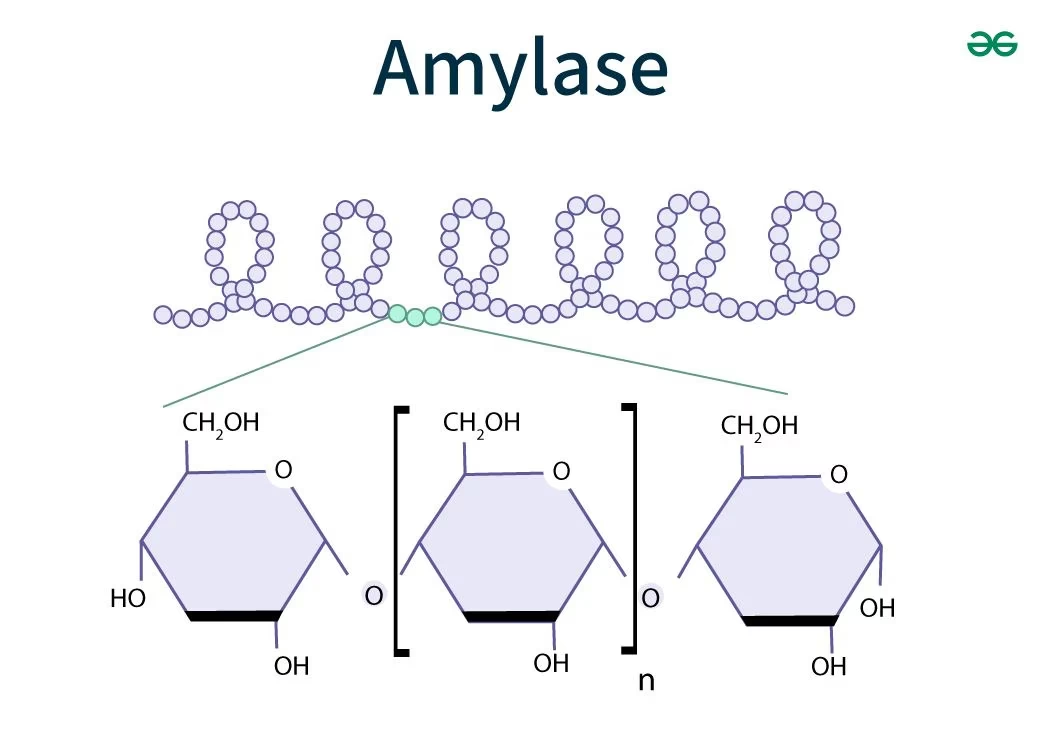
La alfa-amilasa es una enzima que rompe los enlaces glicosídicos alfa-(1-4) en polisacáridos como el almidón y el glucógeno. Aunque su expresión más conocida se da en las glándulas salivales y el páncreas para facilitar la digestión, también se ha detectado en otros órganos como el intestino, el hígado, el músculo y el pulmón. Su descubrimiento en el cerebro fue un hallazgo relativamente reciente y notable. Estudios iniciales identificaron la presencia de α-amilasa no solo en astrocitos y pericítos, sino, crucialmente, en las neuronas.
- La Amilasa Alfa en el Cerebro: Un Hallazgo Inesperado
- Localización Neuronal y Asociación con el Glucógeno
- Amilasa Alfa, Glucógeno y la Formación de la Memoria
- La Conexión con la Enfermedad de Alzheimer
- El Impacto del Beta Amiloide en la Amilasa Alfa Neuronal
- Amilasa Alfa y Actividad Neuronal
- Variaciones Genéticas y Riesgo de Alzheimer
- Consideraciones y Limitaciones
- Tabla Comparativa: Amilasa Alfa en Cerebros Sanos vs. Cerebros con Alzheimer
- Preguntas Frecuentes sobre la Amilasa Alfa y el Cerebro
La Amilasa Alfa en el Cerebro: Un Hallazgo Inesperado
La investigación ha localizado la α-amilasa en tejido post mortem del hipocampo humano, una región cerebral fundamental para la memoria. En individuos sin demencia, la inmunorreactividad de la α-amilasa se observó específicamente en estructuras que se asemejan a las espinas dendríticas en la región CA1, así como en una distribución granular en la capa molecular del hipocampo. Las espinas dendríticas son pequeñas protuberancias en las dendritas de las neuronas que son el sitio principal de la mayoría de las sinapsis excitatorias en el cerebro y son estructuras plásticas clave en el aprendizaje y la memoria. Este patrón de localización sugirió de inmediato un posible papel de la enzima en la función neuronal sináptica.
Localización Neuronal y Asociación con el Glucógeno
Para confirmar la presencia de α-amilasa en las neuronas y determinar su ubicación subcelular con mayor precisión, se realizaron estudios en neuronas primarias aisladas. Estos estudios confirmaron la inmunorreactividad de la α-amilasa en el núcleo, el citosol y los procesos neuronales. Lo más relevante fue que la α-amilasa a lo largo de los procesos neuronales aparecía punteada y se encontraba estrechamente asociada con protrusiones sinápticas positivas para marcadores de actina (faloidina) y marcadores sinápticos presinápticos (sinaptotagmina-1) y postsinápticos (CAMKII). Esta asociación con marcadores sinápticos refuerza la idea de que la α-amilasa está presente en las sinapsis. Además, la co-tinción con glucógeno reveló una asociación cercana entre la α-amilasa y algunos gránulos de glucógeno dentro del citosol y a lo largo de las dendritas. Este hallazgo es clave, ya que sugiere que la α-amilasa podría estar físicamente posicionada para interactuar con el glucógeno neuronal.
Amilasa Alfa, Glucógeno y la Formación de la Memoria
Dada la asociación física entre la α-amilasa y el glucógeno en las neuronas, y el papel conocido de la α-amilasa como enzima degradadora de polisacáridos en otros tejidos, se plantea la hipótesis de que la α-amilasa podría desempeñar una función en la glucogenólisis neuronal, es decir, la degradación del glucógeno para liberar glucosa. Para probar esta hipótesis, se realizaron experimentos en líneas celulares neuronales (SH-SY5Y). La reducción de la producción de α-amilasa mediante interferencia de ARN (siRNA) o la inhibición de su actividad con Tendamistat (un inhibidor específico de la α-amilasa) resultó en un aumento significativo en la cantidad de glucógeno por célula. Esto proporciona una fuerte evidencia de que la α-amilasa tiene propiedades degradadoras de glucógeno también en el contexto neuronal. Considerando que el glucógeno neuronal es crucial para la plasticidad sináptica a largo plazo (LTP), un proceso fundamental para la formación de la memoria, una disfunción en la degradación del glucógeno mediada por α-amilasa podría impactar negativamente la capacidad de formar recuerdos.
La Conexión con la Enfermedad de Alzheimer
La investigación sobre la α-amilasa en el cerebro adquiere una relevancia particular en el contexto de la Enfermedad de Alzheimer (EA). En pacientes con EA, se observó una reducción significativa de la inmunorreactividad de la α-amilasa en las regiones CA1 y la capa molecular del hipocampo en comparación con individuos sin demencia. Esta disminución en la α-amilasa se correlacionó negativamente con los marcadores patológicos de la EA, como la carga de beta amiloide (puntuaciones ABC) y los ovillos neurofibrilares de tau (puntuaciones de Braak). Específicamente, la tinción de α-amilasa en las estructuras tipo espinas dendríticas estaba marcadamente reducida o ausente en los cerebros con EA. Esta fuerte correlación sugiere que la pérdida de α-amilasa neuronal podría ser un factor contribuyente o un marcador de la progresión de la patología de la EA.
El Impacto del Beta Amiloide en la Amilasa Alfa Neuronal
Para investigar si la patología del beta amiloide (Aβ), una característica distintiva de la EA, podría influir directamente en los niveles de α-amilasa neuronal, se realizaron experimentos utilizando modelos celulares relevantes. En neuronas derivadas de células madre pluripotentes inducidas (hiPSC) portadoras de una mutación en el gen PSEN1 (asociada a la EA familiar y que aumenta la producción de Aβ42), los niveles de α-amilasa fueron significativamente más bajos en comparación con las células de control isogénico. De manera similar, la estimulación de células SH-SY5Y con oligómeros de Aβ42 (una forma tóxica del beta amiloide) también resultó en una reducción de la concentración de α-amilasa. Estos hallazgos sugieren que el beta amiloide puede tener un impacto negativo directo sobre la producción o los niveles de α-amilasa en las neuronas. Curiosamente, mientras que la inhibición de la α-amilasa con siRNA o Tendamistat aumentaba el glucógeno (como se esperaba de una enzima que lo degrada), las células con mutación PSEN1 y las estimuladas con Aβ42 mostraron niveles de glucógeno *reducidos* a pesar de tener menos α-amilasa. Esto indica que el Aβ no solo reduce la enzima degradadora de glucógeno (α-amilasa) sino que también impacta negativamente en la carga de glucógeno en sí misma, quizás a través de otros mecanismos (como la síntesis), lo que podría representar un doble golpe para el metabolismo del glucógeno neuronal en la EA.
Amilasa Alfa y Actividad Neuronal
Dada la posible localización sináptica de la α-amilasa y su relación con el glucógeno (importante para la energía sináptica), surge la pregunta de si la enzima es necesaria para la comunicación neuronal. Mediante técnicas de imagen de calcio en neuronas primarias de ratón, se analizó la actividad neuronal después de inhibir la actividad de la α-amilasa con Tendamistat. Si bien no hubo un cambio significativo en la frecuencia de los picos de calcio, la inhibición de la α-amilasa sí alteró otros parámetros: disminuyó la amplitud de las concentraciones intracelulares de calcio y acortó los intervalos entre picos. Esto sugiere que la α-amilasa, aunque quizás no sea esencial para la actividad neuronal *per se*, influye en los patrones de oscilación del calcio, lo que podría indicar una alteración sutil pero potencialmente patológica en la función sináptica. Se especula que esta dishomeostasis del calcio podría estar relacionada con una posible escasez de glucosa libre en las sinapsis debido a una degradación alterada del glucógeno, lo que a largo plazo podría afectar la formación de LTP dependiente de los receptores AMPA.
Variaciones Genéticas y Riesgo de Alzheimer
Un hallazgo intrigante que respalda la importancia de la α-amilasa en la función cognitiva y el riesgo de EA proviene de estudios que examinan las variaciones en el número de copias del gen de la α-amilasa salival (AMY1A). Se ha observado que los individuos con un alto número de copias de este gen (que se correlaciona con una mayor producción de α-amilasa cerebral) obtienen mejores resultados en pruebas de memoria episódica y presentan un riesgo significativamente menor de desarrollar EA. La hipótesis subyacente es que una mayor cantidad de α-amilasa, y por lo tanto una mayor capacidad para degradar el glucógeno en las sinapsis, podría proporcionar una ventaja cognitiva y una cierta protección contra la neurodegeneración asociada a la EA. Esta variación genética en poblaciones humanas, donde aquellas con dietas ricas en almidón tienden a tener más copias del gen AMY1, sugiere una selección natural que favorece una mejor digestión de carbohidratos, pero también podría tener beneficios inesperados para la salud cerebral.
Consideraciones y Limitaciones
Es importante reconocer que la investigación sobre la α-amilasa en el cerebro aún está en sus etapas iniciales y presenta ciertas limitaciones. La especificidad de los anticuerpos utilizados para detectar glucógeno neuronal ha sido objeto de debate, aunque estudios comparativos con otras técnicas sugieren una alta afinidad por el glucógeno. De manera similar, aunque el Tendamistat es un inhibidor conocido y específico de la α-amilasa, no se puede descartar por completo que tenga otros efectos celulares no relacionados con la amilasa. Además, muchos de los hallazgos provienen de modelos celulares (líneas celulares, neuronas primarias de ratón, neuronas derivadas de hiPSC), que, aunque valiosos para estudiar mecanismos específicos, no pueden replicar completamente la complejidad del cerebro humano in vivo. A pesar de estas limitaciones, los resultados convergentes de múltiples enfoques experimentales apuntan fuertemente hacia un papel de la α-amilasa en el metabolismo del glucógeno neuronal y la comunicación sináptica.
En resumen, la alfa-amilasa, una enzima tradicionalmente asociada con la digestión de alimentos, ha emergido como un actor potencial en la neurociencia. Su presencia en las neuronas, su asociación con el glucógeno y las sinapsis, su disminución en la Enfermedad de Alzheimer y su aparente impacto en la actividad neuronal sugieren un papel importante en la salud cerebral y la función cognitiva. La conexión entre la patología del beta amiloide, la reducción de la α-amilasa neuronal y las alteraciones en el metabolismo del glucógeno podría ofrecer nuevas perspectivas sobre los mecanismos subyacentes a la pérdida de memoria en la EA. Aunque se necesita más investigación para dilucidar completamente su función neuronal, la α-amilasa representa un área fascinante en la intersección del metabolismo energético, la función sináptica y las enfermedades neurodegenerativas.
Tabla Comparativa: Amilasa Alfa en Cerebros Sanos vs. Cerebros con Alzheimer
| Característica | Cerebro Sano (Control) | Cerebro con Enfermedad de Alzheimer (EA) |
|---|---|---|
| Inmunorreactividad de α-amilasa en CA1 | Alta, en estructuras tipo espinas dendríticas | Significativamente más baja, pérdida de tinción en espinas |
| Inmunorreactividad de α-amilasa en Capa Molecular | Alta, patrón granular | Significativamente más baja |
| Correlación con carga de Beta Amiloide (ABC) | No aplica (baja carga) | Correlación negativa (a menor α-amilasa, mayor carga de Aβ) |
| Correlación con Ovillos de Tau (Braak) | No aplica (bajo estadio) | Correlación negativa (a menor α-amilasa, mayor estadio de Braak) |
| Niveles de α-amilasa en modelos neuronales con patología Aβ | Normal | Reducidos (en células con mutación PSEN1 o estimuladas con Aβ42) |
| Glucógeno neuronal (en modelos neuronales) | Normal | Reducido (en células con mutación PSEN1 o estimuladas con Aβ42, a pesar de menor α-amilasa) |
Preguntas Frecuentes sobre la Amilasa Alfa y el Cerebro
¿Qué es la alfa-amilasa y por qué es sorprendente encontrarla en el cerebro?
La alfa-amilasa es una enzima conocida principalmente por digerir almidón y glucógeno en la saliva y el páncreas. Su descubrimiento en las neuronas cerebrales fue sorprendente porque se pensaba que su función estaba limitada a la digestión externa y que el glucógeno cerebral era degradado principalmente por otras enzimas (glucógeno fosforilasa y enzima desramificante).
¿Dónde se localiza exactamente la alfa-amilasa en las neuronas?
La investigación la ha encontrado en el citosol, el núcleo y, notablemente, en los procesos neuronales, asociándose estrechamente con estructuras sinápticas como las espinas dendríticas y marcadores sinápticos presinápticos y postsinápticos. También se ha observado su co-localización con gránulos de glucógeno dentro de las neuronas.
¿Cuál es la posible función de la alfa-amilasa en las neuronas?
Los estudios sugieren que la α-amilasa participa en la degradación del glucógeno neuronal (glucogenólisis). Al romper el glucógeno, podría liberar glucosa necesaria para la energía neuronal, especialmente en las sinapsis, un proceso que parece ser importante para la plasticidad sináptica y la formación de la memoria.
¿Cómo se relaciona la alfa-amilasa con la Enfermedad de Alzheimer?
Los niveles de α-amilasa están significativamente reducidos en el hipocampo de pacientes con EA, y esta reducción se correlaciona negativamente con la carga de beta amiloide y los ovillos de tau. Se plantea la hipótesis de que la pérdida de α-amilasa contribuye a la disfunción del metabolismo del glucógeno y, en consecuencia, a los déficits de memoria en la EA.
¿El beta amiloide, una de las principales patologías del Alzheimer, afecta directamente a la alfa-amilasa?
Sí, estudios en modelos celulares han demostrado que tanto las mutaciones genéticas que aumentan la producción de Aβ como la exposición directa a oligómeros de Aβ42 reducen los niveles de α-amilasa en las neuronas, sugiriendo un vínculo causal entre la patología del Aβ y la disminución de la α-amilasa.
¿Afecta la actividad de la alfa-amilasa a la comunicación neuronal?
La inhibición de la actividad de la α-amilasa altera las oscilaciones de calcio intracelular en las neuronas, lo que indica un impacto en la actividad y comunicación neuronal, aunque el mecanismo exacto y las consecuencias a largo plazo aún se están investigando.
¿Tener más copias del gen de la amilasa puede influir en el riesgo de Alzheimer?
Estudios preliminares sugieren que los individuos con un alto número de copias del gen de la α-amilasa salival (que se asocia con más α-amilasa cerebral) tienen mejores resultados en pruebas de memoria y un menor riesgo de desarrollar EA. Esto apoya la idea de que una mayor cantidad de α-amilasa neuronal podría ser beneficiosa para la salud cognitiva.
Si quieres conocer otros artículos parecidos a Amilasa Alfa: Un Actor Inesperado en el Cerebro puedes visitar la categoría Neurociencia.
