La neurociencia es un campo inmenso y en constante evolución que estudia el sistema nervioso en toda su complejidad. Dentro de este ámbito, así como en disciplinas médicas relacionadas como la traumatología, a menudo encontramos acrónimos que resumen conceptos importantes. Uno de estos acrónimos es "AIS", que, curiosamente, tiene significados muy distintos dependiendo de si hablamos de la evaluación de lesiones físicas o de la estructura y función de una neurona a nivel celular. Además de entender estas distinciones, es crucial explorar cómo las lesiones cerebrales, especialmente las traumáticas, pueden tener efectos profundos y a menudo inesperados en funciones corporales esenciales, como las reguladas por el sistema nervioso autónomo.
- AIS en Trauma: Midiendo la Severidad de las Lesiones
- El Segmento Inicial del Axón (AIS): Un Regulador Clave en la Neurona
- Arquitectura Molecular del AIS Neuronal
- Función y Dinámica del AIS Neuronal
- Ensamblaje y Alteraciones del AIS Neuronal
- Disfunción del Sistema Nervioso Autónomo tras Lesión Cerebral Traumática
- Conexión entre Ictus y Disfunción Autonómica
- Hiperactividad Simpática Paroxística (HSP)
- Manejo de la Disfunción Autonómica post-Ictus Isquémico
- Preguntas Frecuentes (FAQ)
- Tabla Comparativa: AIS en Trauma vs. AIS en Neurociencia
- Conclusión
AIS en Trauma: Midiendo la Severidad de las Lesiones
En el contexto de la traumatología y la medicina de urgencias, AIS se refiere a la AIS, o Escala Abreviada de Lesiones (Abbreviated Injury Scale). Esta escala es una herramienta estandarizada utilizada para clasificar la gravedad de una lesión individual en una escala de 1 (menor) a 6 (máxima, lesión que no tiene posibilidad de tratamiento actualmente). Desarrollada por la Association for the Advancement of Automotive Medicine (AAAM), la escala AIS es fundamental para la investigación sobre lesiones, la evaluación de la atención al trauma y la predicción de resultados. A partir de las puntuaciones AIS de lesiones individuales, se puede calcular una puntuación global de la gravedad de la lesión para un paciente, conocida como ISS (Injury Severity Score).
Regiones Corporales del ISS
El cálculo del ISS se basa en la identificación de las lesiones más graves en seis regiones corporales específicas. Aunque el diccionario AIS es más detallado anatómicamente, para el cálculo del ISS solo se utilizan estas seis regiones. La asignación de lesiones a estas regiones sigue reglas específicas:
- Cabeza o cuello: Incluye lesiones en el cerebro o la columna cervical, fracturas de cráneo o columna cervical, asfixia y/o sofocación.
- Cara: Incluye lesiones que afectan la boca, los oídos, la nariz y los huesos faciales.
- Tórax: Incluye todas las lesiones en órganos internos del tórax, ahogamiento y lesiones por inhalación. También abarca lesiones en el diafragma, la caja torácica, y la columna torácica.
- Abdomen o contenido pélvico: Incluye todas las lesiones en órganos internos abdominales y pélvicos, así como la columna lumbar.
- Extremidades o cintura pélvica: Incluye esguinces, fracturas, dislocaciones y amputaciones de brazos, piernas, hombros y pelvis.
- Lesiones externas y otras: Incluye laceraciones, contusiones, abrasiones y quemaduras, independientemente de su ubicación en la superficie corporal, excepto las quemaduras con amputación que se asignan a la región corporal apropiada. Otros eventos traumáticos asignados a esta región del ISS son: lesión eléctrica, congelación, hipotermia y lesión de cuerpo entero (tipo explosión).
Reglas de Puntuación del ISS
La puntuación del ISS es la suma de los cuadrados de los códigos AIS más altos en cada una de las tres regiones corporales más gravemente lesionadas. La puntuación del ISS varía de 1 a 75. Si una lesión individual recibe un código AIS de 6 (identificando una lesión actualmente intratable), la puntuación del ISS se asigna automáticamente como 75, independientemente de otras lesiones. Es un indicador global de la gravedad del trauma.
Ejemplo: Puntuación AIS en Lesiones de Cabeza
Para ilustrar cómo funciona la escala AIS a nivel de una región específica, consideremos las lesiones de cabeza según la escala:
- Una puntuación de 1 se asigna a lesiones menores del cuero cabelludo como abrasiones, contusiones y laceraciones superficiales.
- Las laceraciones más largas y profundas reciben una puntuación de 2, al igual que las lesiones de nervios craneales.
- Las lesiones de vasos cerebrales mayores generalmente se codifican como 3 o 4 para trombosis o formación de aneurisma traumático, o como 4 o 5 para laceración.
- Las fracturas de cráneo y base del cráneo varían de 2 para fracturas simples de la bóveda, a 3 para fracturas de base de cráneo o fracturas conminutas de bóveda, y a 4 para las fracturas abiertas más complejas con tejido cerebral expuesto o fracturas cerradas significativamente deprimidas.
- Las puntuaciones para lesiones del parénquima cerebral varían de 3 a 5. Contusiones pequeñas simples o múltiples reciben un 3, al igual que la hemorragia subaracnoidea (SAH), edema o infarto directamente relacionado con el trauma. Los hematomas se puntúan como 4 o 5, dependiendo de su tamaño.
- La destrucción masiva o las lesiones por aplastamiento reciben una puntuación de 6.
La duración de la pérdida de conciencia y la presencia de déficits neurológicos asociados también pueden utilizarse para puntuar la gravedad de la lesión si estas puntuaciones (que varían de 2 a 5) superan las puntuaciones basadas en las lesiones anatómicas. Es importante destacar que la escala de lesiones orgánicas de la American Association for the Surgery of Trauma no aborda específicamente las lesiones cerebrales, lo que resalta la importancia de escalas como la AIS para esta región.
El Segmento Inicial del Axón (AIS): Un Regulador Clave en la Neurona
Cambiando completamente de contexto dentro del ámbito de la neurociencia, AIS se refiere al Segmento Inicial del Axón (Axon Initial Segment). Esta es una región altamente especializada de la neurona, típicamente ubicada en la base del axón, justo después del cuerpo celular (soma). Funciona como el sitio principal para la iniciación del potencial de acción, el impulso eléctrico fundamental para la comunicación neuronal. Esta capacidad se debe a la altísima densidad de canales iónicos voltaje-dependientes concentrados en esta área, mucho mayor que en el soma o las dendritas. Más allá de la iniciación del potencial de acción, el AIS juega un papel crucial en el mantenimiento de la polaridad neuronal, actuando como una barrera que regula el tráfico y la distribución de proteínas y vesículas entre el soma/dendritas y el axón. Las adaptaciones en la ubicación y longitud del AIS pueden ajustar finamente la excitabilidad de las neuronas y modular la plasticidad en respuesta a la actividad.
Arquitectura Molecular del AIS Neuronal
La estructura y función del AIS dependen de un complejo andamiaje molecular. La proteína clave, considerada el organizador maestro del AIS, es la Ankyrin G (AnkG). AnkG es una proteína citoesquelética submembrana que se acumula selectivamente en el AIS y los Nodos de Ranvier (brechas en la vaina de mielina a lo largo del axón). Su presencia es indispensable para el ensamblaje, la estabilidad y la organización espacial de la mayoría de los componentes del AIS. La pérdida de AnkG puede hacer que el axón adquiera características dendríticas, subrayando su papel en la polaridad.
Proteínas Andamiaje y Canales Iónicos
La AnkG recluta y ancla una alta densidad de canales iónicos voltaje-dependientes a la membrana plasmática del AIS. Los canales de sodio (Nav1.1, Nav1.2, Nav1.6) son particularmente abundantes (entre 5 y 50 veces más concentrados que en otras áreas) y cruciales para la iniciación del potencial de acción, ya que reducen el umbral de potencial de membrana requerido. Se unen a AnkG a través de un motivo de direccionamiento específico en su dominio citoplasmático. La fosforilación de ciertos residuos en este dominio por la proteína quinasa CK2 aumenta la afinidad de AnkG por los canales de sodio, regulando su densidad en el AIS. Los canales de potasio, como Kv7.2 y Kv7.3 (KCNQ2/3), también se acumulan en el AIS interactuando con AnkG y son importantes para modular el potencial de acción. Otros canales de potasio, como Kv1.1 y Kv1.2, se localizan en la parte distal del AIS, y aunque se ha sugerido que PSD93 podría estar implicado en su anclaje, los mecanismos exactos no están completamente claros. Aunque estudios electrofisiológicos sugieren la presencia de canales de calcio en el AIS, poco se sabe sobre sus mecanismos moleculares de localización y función específica en esta región.
Moléculas de Adhesión Celular (CAMs)
Varias moléculas de adhesión celular (CAMs) también se localizan en el AIS, contribuyendo a su estructura y función. Las L1 CAMs interactúan con AnkG. NF186 es otra CAM importante que no solo interactúa con AnkG sino que también recluta moléculas de la matriz extracelular (ECM) al AIS, como agrecán y brevican, creando un vínculo entre el citoesqueleto submembrana y la ECM. Esto podría tener roles en la estabilización de sinapsis o la plasticidad. Otras CAMs como ADAM22, Caspr2 y Tag-1 se localizan en el AIS distal, y se cree que interactúan con PSD93. Las funciones precisas y los compañeros de unión extracelular de la mayoría de estas CAMs del AIS aún no se comprenden completamente.
El Citoesqueleto Submembrana
Inmediatamente debajo de la membrana del AIS, un citoesqueleto denso formado por la Ankyrin G, Spectrina βIV y αII spectrin, junto con actina, proporciona soporte estructural y organiza los componentes. La Spectrina βIV se une a AnkG y a la actina, mientras que la αII spectrin interactúa con Spectrina βIV. La microscopía de superresolución ha revelado que este citoesqueleto de actina/spectrina/ankirina forma una estructura periódica de anillos espaciados aproximadamente 190 nm. Esta red citoesquelética es esencial para la estabilidad del AIS y la organización de sus componentes. Los microtúbulos en el AIS también tienen una disposición particular (fasciculada) y están vinculados a la AnkG a través de proteínas de unión a microtúbulos como EB1 y EB3, lo que puede estabilizar los microtúbulos y facilitar el tráfico axonal. La proteína TRIM46 está enriquecida en el AIS proximal e interactúa con microtúbulos, siendo necesaria para su fasciculación.
Función y Dinámica del AIS Neuronal
Más allá de la iniciación del potencial de acción, el AIS actúa como una barrera funcional que ayuda a mantener la polaridad neuronal al restringir el tráfico y la distribución de proteínas y vesículas. La pérdida de Ankyrin G, por ejemplo, permite que las proteínas somatodendríticas invadan el axón, haciendo que este adquiera características dendríticas. Se ha propuesto que parches dinámicos de actina en el AIS podrían funcionar como "puntos de control" que regulan el tráfico de vesículas, permitiendo el paso de cargas axonales pero deteniendo y redirigiendo las cargas somatodendríticas hacia el soma/dendritas. Aunque la existencia y el mecanismo preciso de estos puntos de control de actina son temas de investigación activa, la evidencia sugiere que el AIS regula activamente el transporte intracelular para mantener la identidad de los compartimentos neuronales.
Ensamblaje y Alteraciones del AIS Neuronal
El ensamblaje del AIS durante el desarrollo neuronal es un proceso dinámico. La investigación sugiere que un límite intra-axonal formado por un citoesqueleto de AnkB/αII/βII spectrin se establece en el axón distal y avanza hacia el soma, restringiendo así la acumulación de AnkG/βIV spectrin al segmento proximal. Este límite actúa como una barrera física que define la ubicación del AIS. Alteraciones en este proceso o la pérdida de componentes clave del citoesqueleto distal, como la αII spectrin o βII spectrin, pueden llevar a un AIS fragmentado o disperso a lo largo del axón, comprometiendo su función.

Además de los defectos genéticos en los componentes del AIS, las lesiones neuronales pueden impactar su estructura y función. Por ejemplo, la isquemia (falta de flujo sanguíneo) puede causar la pérdida de canales de sodio del AIS, afectando la excitabilidad neuronal. Mutaciones en genes que codifican componentes del AIS (como ankirinas, canales iónicos y spectrinas) se han asociado con diversos trastornos neurológicos. Entender cómo las lesiones y las mutaciones afectan el AIS es crucial para comprender la fisiopatología de estas enfermedades.
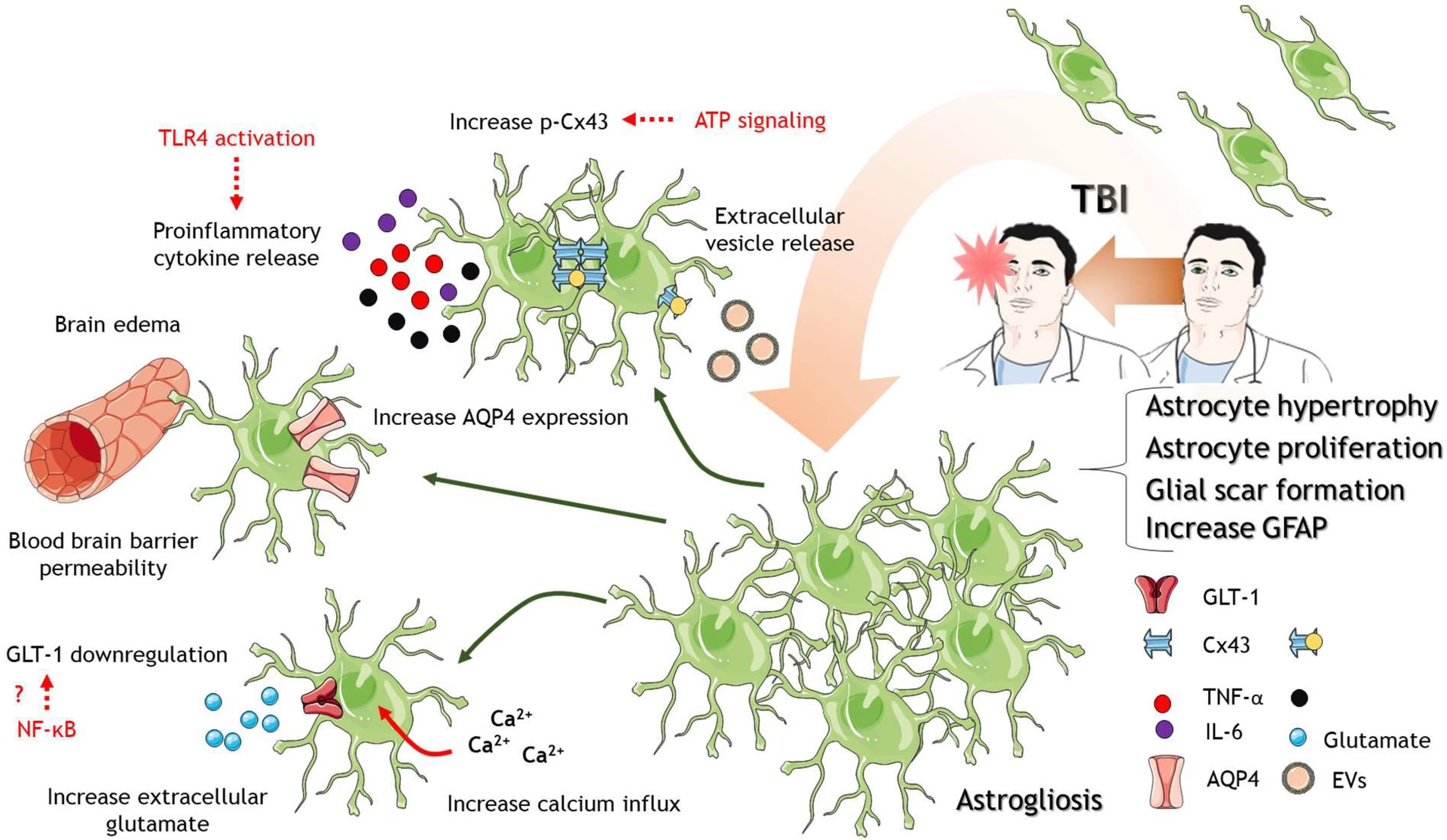
Disfunción del Sistema Nervioso Autónomo tras Lesión Cerebral Traumática
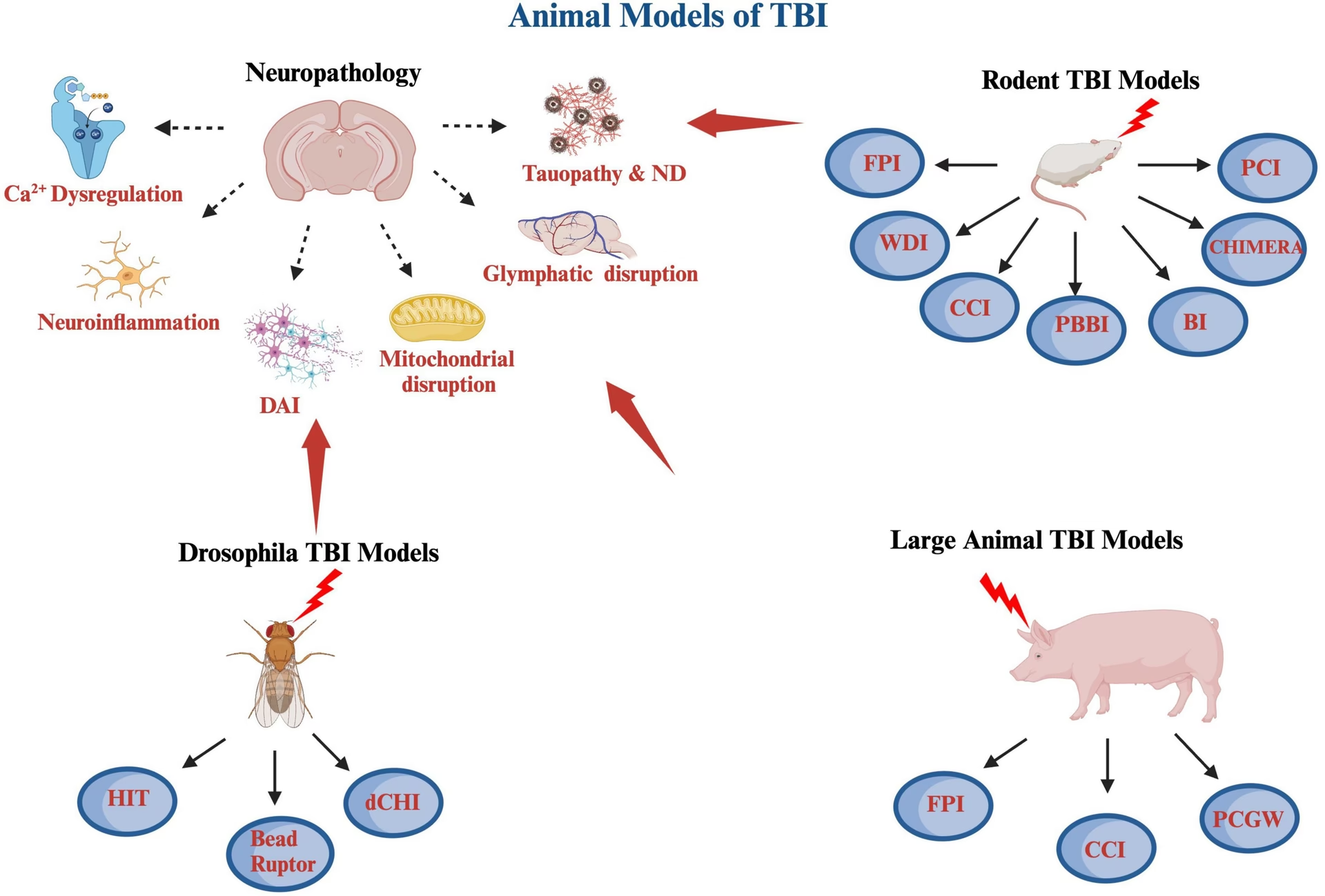
La Lesión Cerebral Traumática (LCT), especialmente en casos severos, puede tener consecuencias de largo alcance que afectan no solo las funciones cognitivas y motoras, sino también el control de procesos corporales involuntarios regulados por el Sistema Nervioso Autónomo (SNA). El daño difuso, focal o hipóxico resultante de una LCT puede afectar tanto los mecanismos corticales como subcorticales que controlan el SNA. Esto, a su vez, ayuda a revelar las complejas conexiones de la Red Autonómica Central (CAN).
La mezcla única de lesiones en cada paciente que sobrevive a una LCT tiene el potencial de producir patrones específicos de control autónomo alterado. Esta disfunción autónoma puede manifestarse de diversas maneras, desde alteraciones en la frecuencia cardíaca y la presión arterial hasta problemas respiratorios y de termorregulación, y tener un impacto significativo en el pronóstico y la recuperación del paciente.
Conexión entre Ictus y Disfunción Autonómica
Existe evidencia convincente de que los ictus isquémicos, particularmente aquellos que afectan la corteza insular, pueden resultar en una desregulación autonómica, con consecuencias cardíacas notables. Estudios post-mortem han encontrado hemorragias subendocárdicas e infarto de miocardio en pacientes con ictus isquémico, incluso en ausencia de aterosclerosis coronaria o enfermedad cardíaca previa. Esto sugiere un vínculo directo entre el daño cerebral y la salud cardíaca.
La corteza insular, una región cortical profunda, parece desempeñar un papel crucial en el control autónomo. Algunos estudios, incluyendo investigaciones en animales y datos de estimulación intraoperatoria en humanos, sugieren una lateralización en el control autónomo: la ínsula izquierda podría estar más involucrada en el control parasimpático (asociada a bradicardia e hipotensión), mientras que la ínsula derecha podría tener un papel predominante en el control simpático (asociada a taquicardia e hipertensión). Sin embargo, otros estudios, como los que miden la variabilidad de la frecuencia cardíaca (un indicador de la actividad del SNA), encuentran disfunción autónoma independientemente de la lateralidad del ictus, lo que sugiere que el control autonómico central es más complejo y no estrictamente lateralizado. No obstante, niveles aumentados de norepinefrina y la presencia de lesiones insulares se han asociado consistentemente con peores resultados funcionales después de un ictus, lo que subraya la importancia de esta área cerebral en la recuperación.

La hipótesis prevalente, respaldada por datos epidemiológicos, estudios en animales y datos retrospectivos, sugiere que el lado derecho del cerebro controla la salida simpática, mientras que el lado izquierdo controla la salida parasimpática, con una entrada cortical superior significativa, particularmente de la ínsula bilateral, que juega un papel clave en la regulación autonómica central.
Hiperactividad Simpática Paroxística (HSP)
Un ejemplo clínico llamativo de disfunción de la CAN es la Hiperactividad Simpática Paroxística (HSP), también conocida por otros nombres como tormenta autonómica o disautonomía. Este síndrome se observa con mayor frecuencia en pacientes con Lesión Cerebral Traumática severa. Los pacientes con HSP típicamente muestran episodios paroxísticos de signos vitales exagerados, como taquicardia (frecuencia cardíaca elevada), taquipnea (respiración rápida) e hipertensión (presión arterial alta), a menudo acompañados de sudoración excesiva, fiebre y posturas distónicas (movimientos musculares involuntarios y sostenidos). Se cree que la HSP es el resultado de daño axonal difuso severo y/o lesiones focales en el tronco cerebral que funcionalmente desconectan las vías de control inhibitorio descendente desde las estructuras de control superior de la CAN hacia la médula espinal, dejando la médula en un estado de excitación simpática desinhibida.
Manejo de la Disfunción Autonómica post-Ictus Isquémico
Actualmente, no existen intervenciones preventivas o terapéuticas definitivas para las complicaciones cardíacas que surgen directamente de la disfunción autonómica en pacientes con ictus isquémico. La mayoría de los pacientes con ictus isquémico no desarrollan arritmias graves o potencialmente mortales. El tratamiento se centra en el soporte y manejo de los síntomas y factores de riesgo. Las siguientes son sugerencias basadas en la práctica clínica:
- Monitoreo de telemetría: Dado que es no invasivo, indoloro y ampliamente disponible en la mayoría de los hospitales, debe considerarse seriamente para pacientes con ictus isquémico, especialmente en las primeras etapas. Ayuda a identificar ritmos cardíacos anormales (arritmias) y permite una intervención rápida si es necesario.
- Revisión de medicación: La prolongación del intervalo QT en el electrocardiograma ha sido identificada en varios estudios como un factor de riesgo para arritmias cardíacas en pacientes con ictus. Al prescribir medicamentos que tradicionalmente pueden prolongar el QT (por ejemplo, algunos antipsicóticos o antibióticos), es apropiado que el clínico considere cuidadosamente alternativas primero. Cualquier medicamento con capacidad de prolongar el QT debe administrarse por el menor período posible.
- Manejo agresivo de electrolitos: La corrección de desequilibrios electrolíticos como la hipokalemia (niveles bajos de potasio) y la hipomagnesemia (niveles bajos de magnesio) puede reducir los eventos cardíacos sintomáticos. Corregir estos desequilibrios es fácilmente facilitado en el entorno hospitalario y suele ser bien tolerado.
Estas medidas buscan mitigar los riesgos asociados a la disfunción autonómica, aunque la investigación continúa para encontrar terapias más dirigidas.
Preguntas Frecuentes (FAQ)
- ¿Qué significa el acrónimo AIS?
- AIS puede significar Escala Abreviada de Lesiones (Abbreviated Injury Scale) en el contexto del trauma para clasificar la gravedad de las lesiones, o Segmento Inicial del Axón (Axon Initial Segment) en el contexto de la neurociencia celular para describir una parte clave de la neurona.
- ¿Cómo se calcula el ISS?
- El Índice de Severidad de la Lesión (ISS) se calcula sumando los cuadrados de las puntuaciones AIS más altas obtenidas por el paciente en cada una de las tres regiones corporales más gravemente lesionadas de las seis definidas por el sistema ISS.
- ¿Qué es el AIS en neurociencia?
- Es el Segmento Inicial del Axón, una región especializada en la base del axón neuronal donde se inician los potenciales de acción y que es fundamental para mantener la polaridad y la función de la neurona.
- ¿Cuál es la proteína principal que organiza el AIS neuronal?
- La proteína organizadora maestra es la Ankyrin G (AnkG), que actúa como un andamiaje para reclutar y anclar otros componentes esenciales como los canales iónicos y las moléculas de adhesión.
- ¿Puede una lesión cerebral traumática afectar el corazón?
- Sí, una Lesión Cerebral Traumática (LCT) severa puede dañar los centros de control del Sistema Nervioso Autónomo en el cerebro, lo que puede llevar a disfunciones que afectan órganos como el corazón, manifestándose en alteraciones de la frecuencia cardíaca, la presión arterial o incluso daños miocárdicos.
- ¿Qué es la HSP?
- HSP significa Hiperactividad Simpática Paroxística, un síndrome de disfunción autonómica que se observa a menudo después de una LCT severa, caracterizado por episodios de aumento extremo de la actividad simpática (taquicardia, hipertensión, sudoración) y posturas anormales.
Tabla Comparativa: AIS en Trauma vs. AIS en Neurociencia
| Concepto | AIS (Trauma) | AIS (Neurociencia) |
|---|---|---|
| Campo Principal | Traumatología, Evaluación de Lesiones | Neurobiología Celular, Fisiología Neuronal |
| Función/Uso Principal | Clasificar la gravedad de lesiones anatómicas específicas (escala 1-6). Utilizado para calcular el ISS global. | Sitio de iniciación del potencial de acción neuronal. Mantenimiento de la polaridad axón-dendrita. |
| Componente Clave | Es una escala de puntuación basada en evaluación médica. | Una estructura subcelular compuesta por proteínas como Ankyrin G, spectrinas y canales iónicos. |
| Relación con Severidad | Indica la gravedad de una lesión específica; puntuaciones más altas significan lesiones más graves. | La integridad estructural y funcional del AIS es vital para la función neuronal normal. Alteraciones se asocian con disfunción neurológica. |
Conclusión
El acrónimo AIS es un claro ejemplo de cómo un mismo conjunto de letras puede representar conceptos fundamentales en áreas distintas de la ciencia biomédica. En el trauma, la AIS nos permite cuantificar y comparar la severidad de las lesiones, siendo una herramienta vital para la investigación, la evaluación clínica y el desarrollo de estrategias de prevención y tratamiento. En la neurociencia, el AIS, como Segmento Inicial del Axón, es una estructura subcelular fascinante, esencial para la comunicación neuronal y el mantenimiento de la identidad polarizada de la neurona, dependiente de un complejo andamiaje molecular organizado por proteínas clave como la Ankyrin G y la Spectrina βIV.
Además, hemos explorado cómo eventos como una Lesión Cerebral Traumática o un ictus pueden tener un impacto profundo en el control del cuerpo a través del Sistema Nervioso Autónomo. La disfunción autonómica post-LCT o post-ictus es una complicación seria que subraya la intrincada conexión entre el cerebro y los sistemas fisiológicos vitales, con implicaciones significativas para el manejo y la recuperación del paciente. Comprender estas distinciones y conexiones es fundamental para una visión completa de la salud y la enfermedad en el sistema nervioso y sus interacciones con el resto del organismo.
Si quieres conocer otros artículos parecidos a AIS: Trauma vs. Neurociencia y LCT puedes visitar la categoría Neurociencia.
