En el vasto y complejo universo de la biología, la capacidad de observar y manipular estructuras a escalas diminutas es fundamental para desentrañar sus misterios. Durante mucho tiempo, técnicas como la microscopía óptica y electrónica han sido pilares en esta exploración. Sin embargo, el advenimiento de la microscopía de fuerza atómica (AFM) ha revolucionado nuestra capacidad para estudiar materiales biológicos, permitiéndonos ir más allá de la simple visualización y adentrarnos en sus propiedades físicas a nivel nanométrico, incluso en su entorno nativo.

- ¿Qué es la Microscopía de Fuerza Atómica (AFM)?
- Principios de Funcionamiento del AFM
- Modos de Operación Principales: Contacto y Tapping
- ¿Qué Información Nos Proporciona el AFM?
- AFM vs. Otras Técnicas de Microscopía
- Aplicaciones del AFM en Ciencias de la Visión
- Espectroscopía de Fuerza y Medición del Módulo Elástico
- Combinación de AFM con Otras Técnicas
- Selección de Puntas y Voladizos
- Preguntas Frecuentes sobre AFM
- Conclusión
¿Qué es la Microscopía de Fuerza Atómica (AFM)?
La AFM es una técnica de microscopía de sonda de barrido que permite obtener imágenes de la superficie de casi cualquier tipo de material, sin necesidad de que sea conductor. A diferencia de los microscopios ópticos, cuya resolución está limitada por la difracción de la luz, o los microscopios electrónicos, que a menudo requieren preparación de muestras invasivas y operan en vacío, la AFM puede funcionar en aire o líquido, lo que la hace ideal para muestras biológicas delicadas.
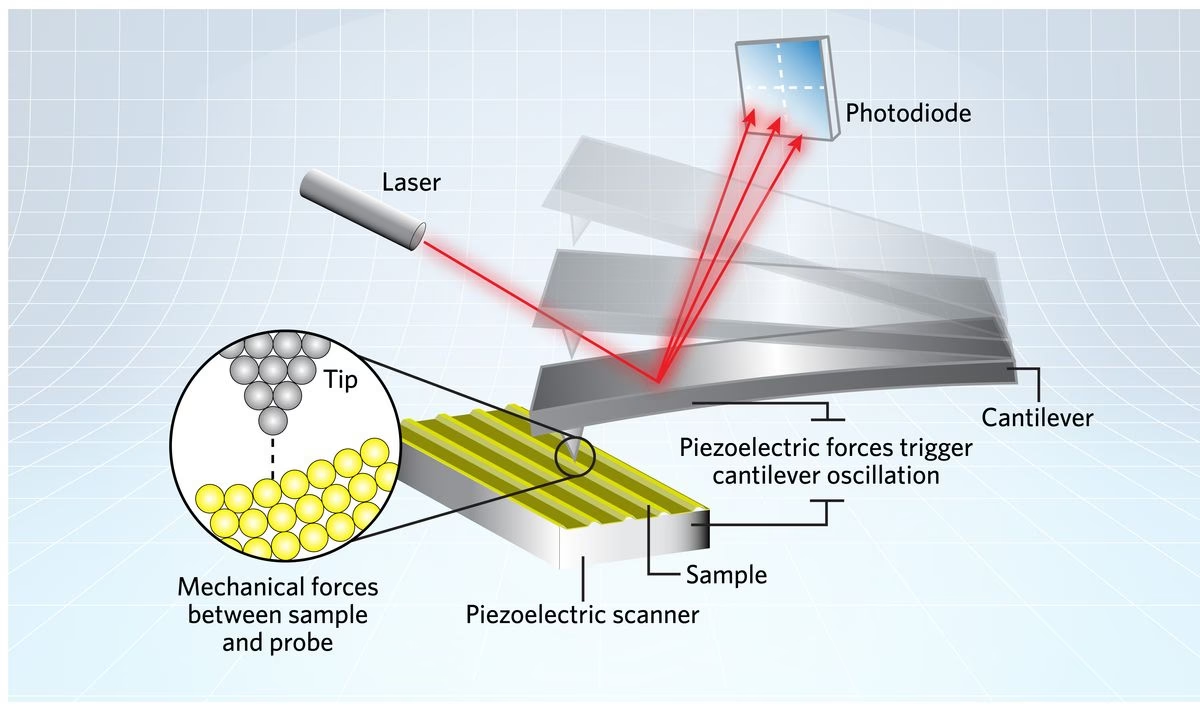
El corazón del AFM es una sonda extremadamente afilada, con un diámetro de punta de apenas unos pocos nanómetros (típicamente de 10 a 20 nm), unida al extremo de un pequeño voladizo (cantilever). Este voladizo actúa como un resorte sensible a las fuerzas. La interacción entre la punta y la superficie de la muestra provoca una deflexión o vibración del voladizo, que es detectada con alta precisión.
Principios de Funcionamiento del AFM
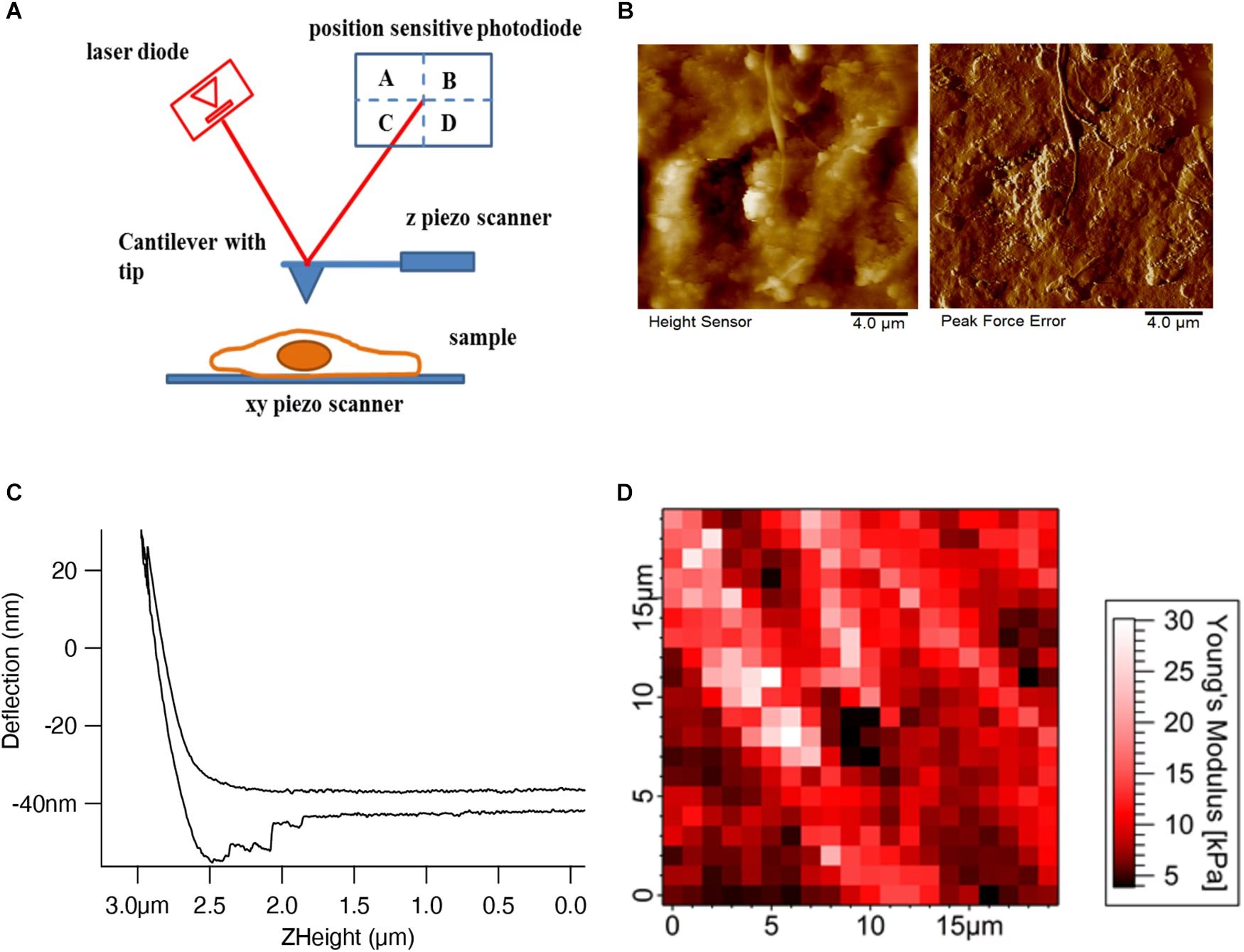
El funcionamiento básico del AFM implica escanear la punta o la muestra a través de la superficie mientras se monitorea la respuesta del voladizo. Un sistema óptico, generalmente compuesto por un láser que incide en la parte posterior del voladizo y un fotodetector sensible a la posición, mide los pequeños cambios en la deflexión del voladizo. Estos cambios se traducen en información sobre la altura de la superficie, permitiendo construir un perfil tridimensional de la muestra.
La resolución lateral del AFM está limitada principalmente por el tamaño y la forma de la punta, pudiendo alcanzar resoluciones de pocos nanómetros. La resolución vertical (en el eje Z) es notablemente alta, llegando a ser de aproximadamente 1 Å (sub-angstrom), limitada solo por el ruido electrónico y térmico del sistema.
Modos de Operación Principales: Contacto y Tapping
El AFM se puede operar en diferentes modos, siendo los más comunes el modo de contacto y el modo de tapping (o vibración).
- Modo de Contacto: En este modo, la punta del AFM permanece en contacto constante con la superficie de la muestra mientras se escanea. Se monitorea y mantiene constante la deflexión del voladizo mediante un sistema de retroalimentación, ajustando la altura del escáner para seguir la topografía de la superficie. Es adecuado para muestras duras, pero puede causar daño o deformación en muestras biológicas blandas debido a las fuerzas laterales.
- Modo de Tapping (o Vibración): Este modo es más suave y ampliamente utilizado para muestras biológicas. El voladizo se hace vibrar cerca de su frecuencia de resonancia, y la punta "golpea" intermitentemente la superficie de la muestra. La interacción punta-superficie reduce la amplitud de la vibración del voladizo. El sistema de retroalimentación mantiene constante esta amplitud de vibración ajustando la altura del escáner. Al minimizar las fuerzas laterales, el modo de tapping reduce significativamente el daño a la muestra.
¿Qué Información Nos Proporciona el AFM?
El AFM no solo nos da una imagen de la superficie, sino que es una herramienta multifacética que puede medir diversas propiedades físicas y químicas a escala nanométrica.
Topografía de Alta Resolución
La función más básica del AFM es la obtención de imágenes topográficas tridimensionales de la superficie. Esta capacidad permite visualizar características moleculares o ultraestructurales en el entorno nativo de la muestra y en tiempo real. Comparar imágenes de estados normales y patológicos puede revelar reorganizaciones moleculares que no son observables con otras técnicas.
Propiedades Mecánicas y Mediciones de Fuerza
Una de las capacidades más poderosas del AFM es su habilidad para ejercer y medir fuerzas en el rango de los piconewtons. Esto permite investigar las propiedades mecánicas de los materiales biológicos, como el módulo elástico local (una medida de la rigidez), la variación del módulo a través de una superficie (mapas de fuerza), y las interacciones específicas ligando-receptor.
La capacidad de explorar las propiedades mecánicas en el estado nativo es crucial para comprender cómo las señales biofísicas, como la rigidez del sustrato, influyen en el comportamiento celular (migración, proliferación, diferenciación, etc.). Se ha demostrado que las células responden activamente a la rigidez del entorno que las rodea, y los cambios en esta rigidez pueden estar implicados en el desarrollo de diversas enfermedades.
Las mediciones de fuerza se realizan típicamente adquiriendo curvas de fuerza-distancia en puntos específicos de la superficie. Una curva de fuerza traza la deflexión del voladizo (relacionada con la fuerza) en función de la distancia a medida que la punta se acerca y se retira de la superficie. Analizando estas curvas, se puede determinar el módulo elástico, fuerzas de adhesión, o incluso desenrollar moléculas individuales.
Otras Propiedades
Además de la topografía y las propiedades mecánicas, el AFM y sus variantes pueden medir:
- Fricción (Microscopía de Fuerza Lateral - LFM).
- Diferencias de dureza y viscoelasticidad (Imagen de Fase).
- Propiedades eléctricas, magnéticas, térmicas, etc. (con puntas especializadas).
AFM vs. Otras Técnicas de Microscopía
El AFM presenta ventajas significativas sobre técnicas establecidas como la microscopía electrónica (ME) y la microscopía óptica (MO) para el estudio de materiales biológicos:
| Característica | AFM | Microscopía Electrónica (ME) | Microscopía Óptica (MO) |
|---|---|---|---|
| Entorno de Imagen | Aire, Líquido, Vacío | Alto Vacío (principalmente) | Aire, Líquido |
| Preparación de Muestra | Mínima (sin fijación, tinción, recubrimiento metálico) | Extensiva (fijación, deshidratación, tinción, recubrimiento) | Variable (puede requerir tinción) |
| Resolución Lateral | Pocos nm (limitada por la punta) | Sub-nm (TEM), pocos nm (SEM) | ~200 nm (limitada por difracción) |
| Resolución Vertical (Z) | Sub-Å | Limitada (principalmente 2D o sección) | Limitada |
| Tipo de Imagen | Perfil 3D de la Superficie | Proyección 2D (TEM), Imagen 2D con profundidad de campo (SEM) | Imagen 2D |
| Medición de Propiedades | Topografía, Propiedades Mecánicas (rigidez, adhesión), Fuerza, Fricción, Eléctricas, Magnéticas, etc. | Topografía (SEM), Estructura interna (TEM), Composición química (SEM con EDS) | Imagen, Fluorescencia, etc. |
| Daño a la Muestra | Mínimo (especialmente en modo de tapping) | Puede ser significativo (preparación, haz de electrones) | Generalmente bajo |
Aunque el AFM tiene una ventaja en resolución y versatilidad de entorno sobre la MO, y en preparación de muestra y capacidad 3D sobre la ME, su área de imagen es significativamente menor que la de un SEM (máximo ~150x150 µm vs mm x mm).
Aplicaciones del AFM en Ciencias de la Visión
A pesar de su enorme potencial, el AFM ha estado subutilizado en comparación con otras áreas de la biología y la ciencia de materiales. Sin embargo, su aplicación en las ciencias de la visión ha ido en aumento, abordando preguntas fundamentales sobre la estructura y función de los tejidos oculares a nivel nanométrico.
Superficie Ocular
El AFM se ha utilizado para caracterizar la topografía de la superficie ocular en diversas especies. Por ejemplo, combinado con espectroscopía Raman, ha revelado diferencias topográficas y químicas en la superficie de los omatidios de ojos compuestos de insectos, lo que podría estar relacionado con funciones como la antirreflexión o la humectación de la superficie.
Mucinas
En el estudio de las mucinas oculares, el AFM ha sido invaluable. Permite distinguir mucinas individuales y caracterizar su heterogeneidad conformacional. Las mediciones de fuerza con puntas recubiertas de mucina han proporcionado información detallada sobre las interacciones mucina-superficie y mucina-mucina, relevantes para comprender la lubricación y adhesión en la superficie del ojo.
Córnea
El AFM ha permitido visualizar fibrillas de colágeno corneales con alta resolución, incluso en su estado nativo sin los artefactos de la preparación de muestra de la ME. También se ha utilizado para caracterizar la topografía de las células epiteliales y endoteliales corneales. Crucialmente, el AFM es la técnica ideal para medir las propiedades mecánicas locales de capas delgadas dentro de la córnea, como las membranas basales anterior y de Descemet. Se ha encontrado que estas membranas tienen rigideces significativamente diferentes, una distinción importante para el diseño de prótesis o sustratos biomiméticos para ingeniería de tejidos corneales. El AFM también ha evaluado los cambios topográficos en la superficie corneal después de la fotoablación con láser excimer.
Malla Trabecular y Glaucoma
Investigaciones recientes utilizando AFM han revelado un aumento dramático en la rigidez de la malla trabecular en ojos glaucomatosos en comparación con ojos sanos. La malla trabecular es responsable de regular la salida del humor acuoso, y su endurecimiento podría contribuir al aumento de la presión intraocular, un factor clave en el glaucoma. El AFM es una herramienta única para medir esta propiedad mecánica a nivel local.
Cristalino
El AFM ha medido el módulo elástico del cristalino intacto y ha investigado la topografía de las fibras del cristalino. Estudios fascinantes han utilizado AFM de alta resolución para examinar la organización de la acuaporina 0 en las membranas de las fibras del cristalino, revelando diferencias entre cristalinos normales y cataratosos que sugieren una alteración en la comunicación intercelular.
Rodopsina y Bacteriorrodopsina
El AFM ha proporcionado la primera evidencia experimental de la estructura dimérica de la rodopsina en membranas discales de bastones. La espectroscopía de fuerza de molécula única con AFM ha permitido estudiar la estabilidad de la rodopsina y desenrollar segmentos individuales. De manera similar, el AFM de alta resolución ha caracterizado la estructura y los cambios conformacionales inducidos por la luz en la bacteriorrodopsina, un protón bomba modelo.

Membrana de Bruch
El AFM ha visualizado las fibras de colágeno de la membrana de Bruch y estudiado la adsorción de péptidos. La espectroscopía de fuerza con mapeo de fuerza ha permitido caracterizar las propiedades de adhesión de la superficie de la membrana de Bruch, lo cual es relevante para comprender la adhesión de células del epitelio pigmentario retiniano en tratamientos para la degeneración macular.
Células Retinianas
El AFM se ha utilizado para caracterizar las propiedades mecánicas de los melanosomas del epitelio pigmentario retiniano, revelando posibles cambios relacionados con la edad. También se ha empleado para cuantificar la rugosidad nanométrica de sustratos sintéticos para ingeniería de tejidos retinianos, ya que la topografía del sustrato influye en el comportamiento celular.
Membrana Limitante Interna (MLI)
Las propiedades mecánicas y el grosor de la MLI retiniana durante el desarrollo se han estudiado con AFM, mostrando cambios estructurales significativos a lo largo del tiempo.
Espectroscopía de Fuerza y Medición del Módulo Elástico
La capacidad del AFM para medir fuerzas permite determinar las propiedades mecánicas de los materiales a través de la espectroscopía de fuerza. La medición del módulo elástico, un indicador de la rigidez de un material, es una aplicación clave.
Se realiza obteniendo curvas de fuerza-distancia. Al presionar la punta contra la superficie, la curva de aproximación muestra cómo el voladizo se deflecta a medida que la punta indenta la muestra. La profundidad de indentación se calcula a partir del desplazamiento del piezocerámico y la deflexión del voladizo.
Para calcular el módulo elástico (E), se ajusta la curva de fuerza de aproximación a un modelo teórico apropiado. El modelo de Hertz es el más común para materiales biológicos, asumiendo que la muestra es elástica lineal, homogénea, infinitamente gruesa y sin adhesión. Aunque los materiales biológicos son a menudo viscoelásticos, a tasas de indentación típicas de AFM (<100 nm de profundidad a 2 µm/s), pueden comportarse de manera elástica lineal.
El modelo de Hertz relaciona la fuerza de carga (F) con la profundidad de indentación (δ) y la geometría de la punta (cono o esfera). Para una punta cónica, la ecuación es F ∝ E * δ², y para una punta esférica, F ∝ E * δ³. Conociendo la constante del resorte del voladizo (k), la deflexión (d) y la posición del piezocerámico (z), se puede calcular F = k * (d - d₀) y δ = z - z₀ - d, donde d₀ y z₀ son los valores en el punto de contacto inicial. Ajustando la curva experimental a estas ecuaciones, se puede obtener el valor de E.
Es crucial considerar las suposiciones del modelo de Hertz. Si la muestra es muy delgada o muestra viscoelasticidad significativa (histéresis en las curvas de carga/descarga), el modelo de Hertz puede no ser apropiado o requerir modificaciones. El AFM mide un módulo local en la superficie, que puede diferir del módulo medido por otras técnicas (como pruebas de tracción) que promedian las propiedades mecánicas de todo el volumen de la muestra o aplican la tensión en una dirección diferente.
Combinación de AFM con Otras Técnicas
Para obtener una comprensión más completa de las muestras, el AFM se integra a menudo con técnicas ópticas o espectroscópicas como microscopía de fluorescencia, confocal o Raman. Esta combinación permite correlacionar la topografía de alta resolución del AFM con información química o molecular específica obtenida por las otras técnicas. Por ejemplo, se pueden mapear la distribución de receptores fluorescentes en la superficie celular y correlacionarlos con la estructura celular visualizada por AFM.
Selección de Puntas y Voladizos
La elección adecuada del voladizo y la punta es esencial. Para imágenes de muestras biológicas blandas, especialmente en modo de contacto en líquido, se requieren voladizos con constantes de resorte bajas (<0.2 N/m) para minimizar el daño. En modo de tapping en líquido también se usan voladizos blandos, mientras que en aire se necesitan voladizos más rígidos (~45 N/m). Las constantes de resorte bajas también son necesarias para medir fuerzas intermoleculares.
La geometría de la punta afecta la resolución de la imagen y el análisis de las mediciones de fuerza. Puntas afiladas (~20-30 nm de radio) dan mayor resolución de imagen, pero pueden dañar muestras blandas. Esferas (~µm de radio) unidas al voladizo se usan a menudo para mediciones de propiedades mecánicas (nanoindentación), ya que su geometría bien definida simplifica el análisis con modelos como el de Hertz e incluyen un área de muestra más grande.
Las puntas también pueden ser funcionalizadas con moléculas específicas (ligandos, proteínas, células) para estudiar interacciones con la superficie de interés mediante mediciones de fuerza.
Preguntas Frecuentes sobre AFM
Aquí respondemos algunas preguntas comunes sobre la microscopía de fuerza atómica:
¿Cuál es la diferencia entre AFM y SEM?
Aunque ambos son microscopios de barrido, el SEM utiliza electrones y opera en vacío, proporcionando imágenes 2D con gran profundidad de campo y puede analizar composición química. El AFM utiliza una punta física, puede operar en aire, líquido o vacío, proporciona perfiles 3D de la superficie con mayor resolución vertical y permite medir propiedades físicas como rigidez y fuerza.
¿Qué tan alta es la resolución del AFM?
La resolución lateral puede ser de pocos nanómetros, limitada por el tamaño de la punta. La resolución vertical (en altura) es excepcionalmente alta, de aproximadamente 1 Å.
¿Es difícil operar un AFM?
Aprender a operar un AFM requiere entrenamiento, comparable al de aprender a conducir un coche. Las operaciones básicas se pueden dominar en pocas horas, pero obtener imágenes de muy alta resolución o realizar mediciones de fuerza avanzadas requiere más práctica y conocimiento de los parámetros de control y calibración.
¿Cuánto tiempo dura una punta de AFM?
La vida útil de una punta varía. Un operador principiante puede usar una punta por día. Un operador experimentado para aplicaciones rutinarias puede usar una punta durante una semana o dos. Las puntas pueden romperse durante el acercamiento a la muestra si hay un "choque" o durante el escaneo si los parámetros de control no están optimizados.
Conclusión
La microscopía de fuerza atómica es una técnica extraordinariamente poderosa que ofrece capacidades únicas para la exploración del nanomundo biológico. Su habilidad para obtener imágenes de alta resolución y medir propiedades mecánicas y fuerzas en el entorno nativo de las muestras la convierte en una herramienta invaluable, especialmente en campos como las ciencias de la visión. A medida que la investigación avanza y las preguntas se vuelven más sofisticadas, la integración del AFM con otras técnicas y el desarrollo de nuevas aplicaciones seguirán expandiendo nuestro conocimiento de la biología a escalas fundamentales. Se espera que su uso continúe creciendo, estimulando a más investigadores a incorporarla en sus estudios para abordar desafíos complejos en biología celular, ingeniería de tejidos y comprensión de enfermedades.
Si quieres conocer otros artículos parecidos a AFM: Explorando el Nanomundo Biológico puedes visitar la categoría Neurociencia.
