La Activina es una proteína fascinante que pertenece a la superfamilia del factor de crecimiento transformante beta (TGF-β). Junto con su contraparte, la Inhibina, desempeña roles fundamentales en una amplia gama de procesos biológicos, actuando a menudo de manera antagónica. Mientras que la Inhibina es conocida principalmente por su capacidad para suprimir la liberación de la hormona foliculoestimulante (FSH), la Activina ejerce el efecto opuesto, estimulando su secreción. Esta interacción dinámica entre Activina e Inhibina es vital para la regulación de sistemas como el reproductivo, pero las funciones de la Activina se extienden mucho más allá, influyendo en el crecimiento muscular, la adhesión celular y la proliferación, entre otros.
Para comprender completamente el impacto de la Activina, es crucial examinar su estructura molecular, sus diversos mecanismos de acción, los tipos de Receptores con los que interactúa y las funciones específicas que desempeña en diferentes tejidos y procesos celulares, tal como se desprende de la investigación.
Estructura Molecular de la Activina
Tanto los complejos proteicos de Activina como los de Inhibina presentan una estructura dimérica, lo que significa que están compuestos por dos subunidades. En cada complejo, las dos subunidades monoméricas están unidas entre sí por un único enlace disulfuro. Aunque ambos complejos derivan de la misma familia de genes y proteínas relacionados, difieren en la composición de sus subunidades.
Las Activinas son dímeros compuestos por subunidades beta, específicamente βA o βB. Existen tres variaciones comunes de Activina basadas en la combinación de estas subunidades:
- Activina A: Compuesta por dos subunidades βA (βAβA).
- Activina B: Compuesta por dos subunidades βB (βBβB).
- Activina AB: Compuesta por una subunidad βA y una subunidad βB (βAβB).
En mamíferos, se han descrito cuatro subunidades beta: activina βA, activina βB, activina βC y activina βE. Las subunidades βA y βB son idénticas a las dos subunidades beta de la Inhibina. Una quinta subunidad, activina βD, ha sido descrita en Xenopus laevis. Es importante destacar que la subunidad βC puede formar heterodímeros de activina con las subunidades βA o βB, pero no puede dimerizarse con la subunidad alfa de la Inhibina. Aunque teóricamente son posibles muchas combinaciones de heterodímeros, no todas se han descrito.
Las subunidades alfa (α) y beta (β) comparten aproximadamente un 25% de similitud de secuencia, mientras que la similitud entre las subunidades beta es considerablemente mayor, alrededor del 65%. Esta diferencia estructural subyace a las distintas actividades biológicas de Activina e Inhibina.
Funciones Principales de la Activina
Como miembros de la familia TGF-β, las Activinas participan en una multitud de procesos biológicos. Una de sus funciones más reconocidas es la regulación de la secreción de la hormona foliculoestimulante (FSH) por la hipófisis anterior. Mientras que la Inhibina suprime esta secreción, la Activina la estimula activamente. Este control dual es fundamental para el ciclo reproductivo.
Sin embargo, las Activinas tienen múltiples tejidos diana y funciones que van más allá de la reproducción. Se sabe que regulan el crecimiento muscular, actuando a través de sus Receptores de tipo 2. La miostatina, otro miembro de la superfamilia TGF-β, es un regulador negativo del crecimiento muscular que también se une a los Receptores de activina (principalmente ACVR2B y en menor medida ACVR2A).
En el sistema reproductivo, los Receptores de activina están presentes en los testículos durante su desarrollo. Se localizan principalmente en los gonocitos y las células de Sertoli. Estas células responden a la señalización autocrina y paracrina de la activina B, que controla su proliferación. Los Receptores ACVR2A también se encuentran en las células del epidídimo, mientras que los ACVR2B se localizan en la rete testis.
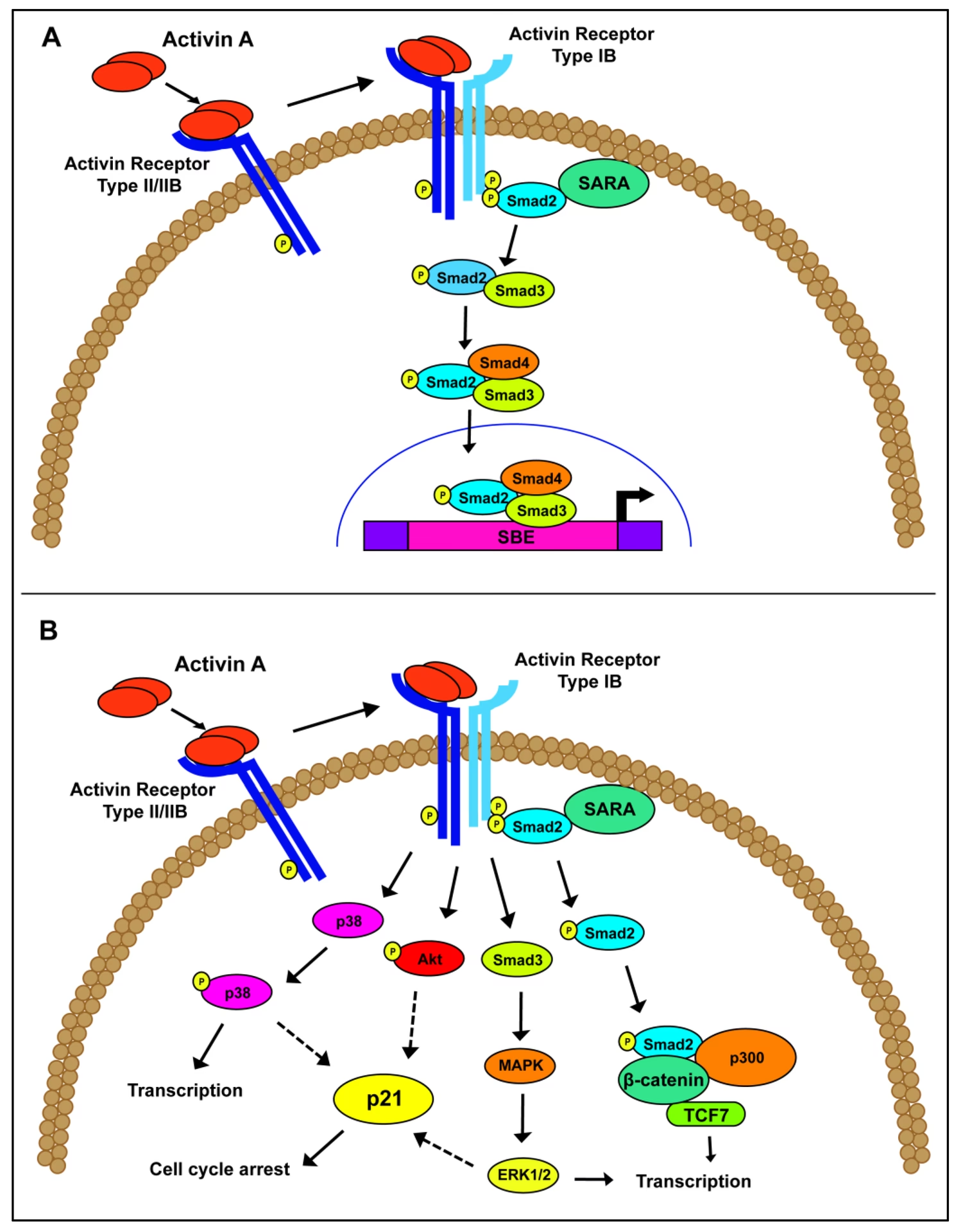
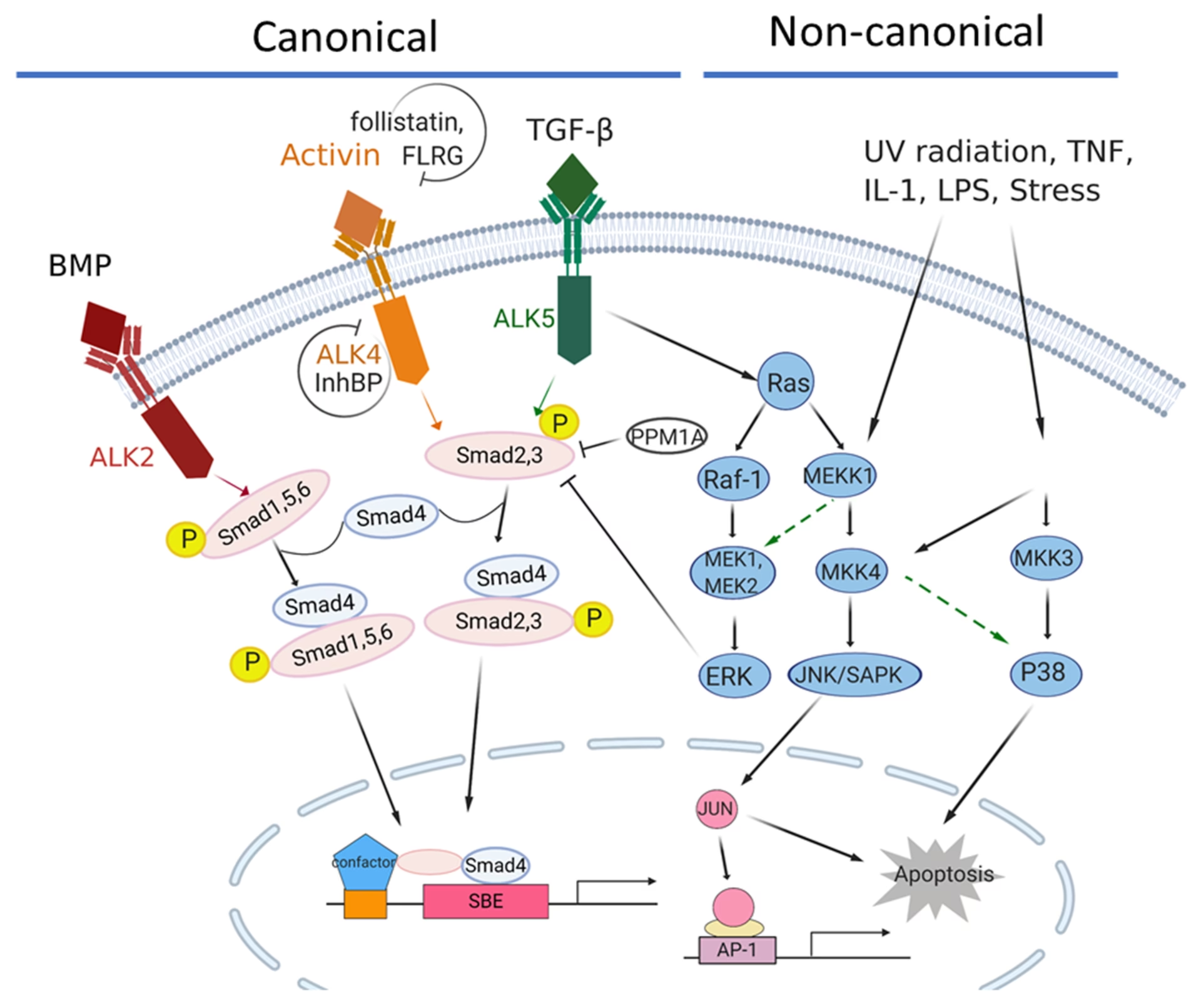
Mecanismo de Acción de la Activina
El sistema de señalización utilizado por las Activinas sigue el patrón establecido por la familia TGF-β. Las Activinas transmiten sus señales uniéndose a Receptores de serina/treonina quinasa de tipo II, como ActRII o ActRIIB. Esta unión provoca la fosforilación de Receptores de serina/treonina quinasa de tipo I (principalmente ALK4) de manera canónica. La activación de ALK4 conduce a la activación de las proteínas Smad, lo que a su vez inicia la expresión de genes específicos.
La Inhibina, por otro lado, ejerce su antagonismo de varias maneras. También se une a los Receptores de tipo II (ActRII), lo que proporciona un medio de regulación por señalización competitiva. Sin embargo, a diferencia de la Activina, la Inhibina no se une a ALK4. Esto podría representar otro nivel de regulación del flujo de información. El análisis mutacional de la subunidad βA de la activina ha permitido identificar residuos necesarios para la unión al receptor, la actividad y la inhibición de su función por la Inhibina a través de sus propios Receptores.
Además, la betaglicano (TGF-β RIII), un proteoglicano de la superficie celular, actúa como un corregulador de alta afinidad para la Inhibina. La unión de la Inhibina al betaglicano aumenta considerablemente su afinidad por los Receptores de activina. A través de esta intervención del betaglicano, la Inhibina puede interrumpir la interacción de la Activina con sus propios Receptores y la interacción de los Receptores de activina con otros miembros de la familia TGF-β.
Existen otros factores que pueden modular la señalización de la Activina. La folistatina, una glicoproteína, se une a la Activina con alta afinidad. La folistatina inhibe la producción de FSH, y este efecto supresor se atribuye a su capacidad para unirse y secuestrar la Activina. La disponibilidad de Activina es, por tanto, un determinante importante de la secreción de FSH por la hipófisis.
Otro factor es Cripto, que media la señalización de Nodal. Cripto puede unirse a la Activina y a ActRII/IIB. Cuando Cripto está involucrado en la señalización de Nodal, es capaz de inhibir la señalización de la Activina, lo que podría tener consecuencias potenciales para la función de la Inhibina.
El Papel Específico de la Activina A
Estudios experimentales han investigado el papel específico de la Activina A en diversos procesos celulares. Utilizando líneas celulares como MHSteCs (células estelares hepáticas murinas), se ha evaluado el impacto de la Activina A en la proliferación, adhesión, migración y otras funciones celulares.
- Proliferación Celular: Mediante ensayos como el CCK-8 y el análisis en tiempo real RTCA, se ha demostrado que la Activina A influye en la tasa de proliferación celular. Diferentes concentraciones de Activina A (por ejemplo, 5, 10 y 20 ng/mL) pueden afectar la viabilidad y el crecimiento de las células a lo largo del tiempo (24, 48, 72 horas).
- Adhesión Celular: La Activina A también afecta la capacidad de las células para adherirse a la matriz extracelular (ECM). Ensayos de adhesión a ECM (como fibronectina) y estudios de adhesión en tiempo real (RTCA) han mostrado que la presencia de Activina A puede modificar la adhesión celular.
- Cicatrización de Heridas (Wound Healing): Mediante ensayos de rascado (wound scratch assay), se ha observado que la Activina A puede influir en la capacidad de las células para migrar y cerrar una "herida" en una monocapa celular, indicando un papel en los procesos de reparación tisular.
- Migración Celular: Los ensayos de migración, como el Transwell y los ensayos basados en microfluídica, han revelado que la Activina A puede actuar como un factor quimiotáctico, influyendo en la dirección y la velocidad del movimiento celular. Se ha observado que las células migran hacia gradientes de concentración de Activina A.
- Flujo de Calcio: La Activina A puede afectar los niveles de calcio intracelular. Mediante el uso de colorantes sensibles al calcio como Fluo-4 y citometría de flujo, se ha observado que la adición de Activina A puede inducir cambios en la señal de fluorescencia, lo que indica alteraciones en el flujo de calcio.
Estos hallazgos experimentales, obtenidos mediante técnicas como RT-PCR, qPCR, Western Blotting y ensayos funcionales, subrayan la versatilidad funcional de la Activina A a nivel celular, mostrando su implicación en procesos dinámicos como la proliferación, la adhesión y la migración.

Los Receptores de Activina
Las Activinas ejercen sus efectos biológicos uniéndose a Receptores específicos en la superficie celular. Los principales Receptores de tipo II para la Activina son ACVR2A y ACVR2B. Estos Receptores son cruciales para transmitir la señal de la Activina dentro de la célula.
Varios ligandos que señalan a través de los Receptores de activina de tipo 2 regulan el crecimiento muscular. Como se mencionó anteriormente, la miostatina se une a ACVR2B y en menor medida a ACVR2A. Estudios en ratones con mutaciones nulas (knockout) para ACVR2A o ACVR2B han mostrado un aumento en el tamaño de varios grupos musculares, lo que refuerza el papel de estos Receptores en la regulación negativa del crecimiento muscular (mediada por miostatina y posiblemente otras señales).
En el sistema reproductivo, los Receptores ACVR2A y ACVR2B son particularmente importantes. Se encuentran localizados principalmente en los gonocitos y las células de Sertoli en los testículos en desarrollo, donde median la señalización de activina B para controlar la proliferación celular. Los Receptores ACVR2A también están presentes en las células del epidídimo, y los ACVR2B en la rete testis.
Implicaciones Clínicas de los Receptores de Activina
La importancia de los Receptores de activina no se limita a la biología básica; también tienen relevancia clínica, particularmente en el contexto del cáncer. Se ha encontrado que el gen ACVR2 (que codifica para el receptor de tipo II ACVR2A) a menudo está inactivado en el cáncer de próstata y en tumores que presentan inestabilidad de microsatélites (MSI).
En el cáncer colorrectal con alta inestabilidad de microsatélites (MSI-H), el gen ACVR2A se encuentra mutado en un porcentaje significativo de casos (58.1%). Estas mutaciones, a menudo truncadas, pueden causar una reducción significativa en la señalización mediada por activina en el laboratorio. El gen ACVR2A también parece desempeñar un papel en algunos cánceres colorrectales que no son MSI-H. Estos hallazgos sugieren que las alteraciones en la vía de señalización de la Activina a través de sus Receptores pueden contribuir al desarrollo y la progresión de ciertos tipos de cáncer.
Activina vs. Inhibina: Un Dúo Antagónico
La relación entre Activina e Inhibina es un ejemplo clásico de regulación biológica mediante proteínas relacionadas pero con funciones opuestas. Ambas son glicoproteínas heterodiméricas de la familia TGF-β, pero sus diferencias estructurales y funcionales son clave:
- Estructura: La Activina está compuesta por dos subunidades beta (βAβA, βBβB, βAβB). La Inhibina está compuesta por una subunidad alfa (α) y una subunidad beta (α/βA para Inhibina A, α/βB para Inhibina B).
- Producción: Las subunidades beta de la Inhibina y las Activinas se producen en muchos tejidos. Sin embargo, las dímeros de Inhibina procesados y la subunidad alfa se producen exclusivamente en las células de la granulosa del ovario.
- Tejidos Diana Principales: La Inhibina tiene dos focos principales de función: la gonadotropina hipofisaria y el ovario. Las Activinas tienen múltiples tejidos diana en todo el cuerpo.
- Efecto sobre la FSH: Esta es la diferencia funcional más destacada. La Activina estimula la biosíntesis y secreción de FSH desde la hipófisis anterior, mientras que la Inhibina bloquea estos procesos.
- Mecanismo de Señalización: Ambas se unen a Receptores de tipo II (ActRII). Sin embargo, la Activina también activa Receptores de tipo I (ALK4) para iniciar la vía Smad, algo que la Inhibina no hace. La Inhibina utiliza correguladores como el betaglicano para potenciar su unión a ActRII y competir con la Activina.
Esta compleja interacción y antagonismo permiten un control fino de procesos biológicos cruciales, especialmente en el sistema reproductivo, donde la regulación de la FSH es fundamental para el desarrollo folicular y la producción de gametos y hormonas.
Preguntas Frecuentes (FAQ)
Aquí respondemos algunas preguntas comunes sobre la Activina:
¿Qué es la Activina?
La Activina es una proteína dimérica que pertenece a la superfamilia del factor de crecimiento transformante beta (TGF-β). Está compuesta por dos subunidades beta unidas por un enlace disulfuro y desempeña roles importantes en la regulación celular y del desarrollo.

¿Cuál es la función principal de la Activina?
Una de sus funciones principales es estimular la producción y liberación de la hormona foliculoestimulante (FSH) por la glándula hipófisis. También está involucrada en la regulación del crecimiento muscular, la reproducción, la proliferación, adhesión y migración celular.
¿Cómo se diferencia la Activina de la Inhibina?
Aunque relacionadas y a menudo actúan de forma antagónica, la Activina y la Inhibina difieren en su estructura de subunidades (Activina tiene dos subunidades beta; Inhibina tiene una alfa y una beta) y en su efecto principal sobre la FSH (Activina la estimula, Inhibina la inhibe).
¿Dónde se produce la Activina en el cuerpo?
Las subunidades beta de la Activina y las Activinas en sí se producen en muchos tejidos del cuerpo, a diferencia de la Inhibina, cuya subunidad alfa y dímeros procesados se producen principalmente en las células de la granulosa del ovario.
¿Cómo funciona la señalización de la Activina a nivel celular?
La Activina se une a Receptores específicos en la superficie celular (tipo II como ActRII/IIB y tipo I como ALK4), lo que desencadena una cascada de eventos intracelulares que involucran proteínas Smad y culmina en la regulación de la expresión génica.
¿Los Receptores de Activina están relacionados con alguna enfermedad?
Sí, se ha encontrado que los genes que codifican los Receptores de activina, como ACVR2A, a menudo están mutados o inactivados en ciertos tipos de cáncer, como el cáncer de próstata y el cáncer colorrectal con inestabilidad de microsatélites.
En resumen, la Activina es un regulador multifacético con un papel crucial en la homeostasis y el desarrollo a través de su compleja interacción con Receptores específicos y su antagonismo con la Inhibina. Su influencia en procesos que van desde la reproducción hasta el crecimiento muscular y su implicación en patologías como el cáncer la convierten en un sujeto de estudio continuo en biología y medicina.
Si quieres conocer otros artículos parecidos a La Activina: Función, Estructura y Receptores puedes visitar la categoría Neurociencia.
