Los vectores de virus adenoasociados (AAV) se han posicionado como una plataforma fundamental para la transferencia génica in vivo en ensayos clínicos. Su perfil de seguridad favorable y su alta eficiencia para transducir una amplia gama de tejidos, incluyendo aquellos relevantes en neurociencia, los hacen atractivos. La tecnología AAV ha mostrado éxito clínico en diversas afecciones, como trastornos de la coagulación, ceguera hereditaria y enfermedades neurodegenerativas. Sin embargo, el camino desde la investigación básica hasta la aplicación clínica es largo e implica abordar desafíos complejos que surgen durante el desarrollo. A pesar de los logros, han aparecido varios obstáculos tanto en estudios preclínicos como en ensayos clínicos. Superar estos problemas es crucial para expandir el alcance de la transferencia génica con AAV como modalidad terapéutica para una variedad de enfermedades humanas.
La Naturaleza de los Vectores AAV
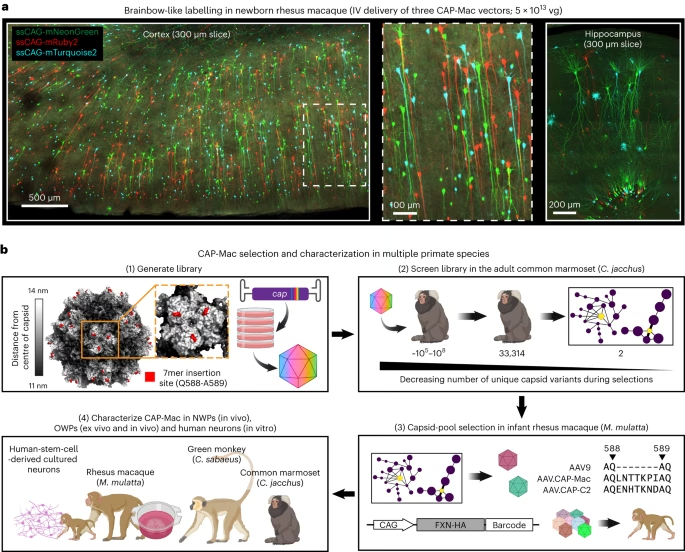
El virus adenoasociado (AAV) es un virus pequeño, de aproximadamente 25 nm, perteneciente a la familia Parvoviridae. Posee una cápside icosaédrica no envuelta que encapsula un genoma de ADN lineal de cadena simple de alrededor de 4.7 kb. Este genoma codifica proteínas virales esenciales para su ciclo de vida, flanqueadas por repeticiones terminales invertidas (ITRs) palindrómicas específicas de AAV. Los virus AAV naturales infectan células tanto en división como no en división y permanecen latentes en el ADN del huésped, generalmente integrándose en sitios cromosómicos específicos (AAVS), a menos que un virus auxiliar induzca su replicación. La exposición humana al AAV salvaje es común en la infancia y no se asocia con enfermedades conocidas. Esta exposición temprana define la respuesta inmunológica del huésped a los vectores AAV recombinantes.
En la terapia génica, se utilizan vectores AAV recombinantes donde las secuencias virales (excepto las dos ITRs, que son señales de empaquetamiento) son reemplazadas por el ADN exógeno de interés, conocido como el “casete de expresión del transgén”. La infección y transducción celular implican varios pasos: interacción de la cápside con receptores celulares, internalización por endocitosis, tráfico intracelular, escape endosomal, importación nuclear, desencapsidación y conversión del ADN viral de cadena simple a doble cadena. A diferencia del virus salvaje, el genoma de los vectores AAV recombinantes no se integra preferentemente en sitios específicos, sino que permanece principalmente de forma episomal en el núcleo, con una baja frecuencia de integración aleatoria (0.1%–1%).
Se han identificado al menos 12 serotipos de AAV y más de 100 aislados. La versatilidad del sistema de producción permite crear vectores híbridos combinando ITRs de un serotipo (comúnmente AAV2) con cápsides de otros serotipos (pseudotipado, AAV2/n). Dado que la cápside determina el tropismo celular y la cinética de expresión, seleccionar la cápside adecuada es crucial. Recientemente, se identificó un receptor universal (AAVR), pero co-receptores y otros factores explican el diverso tropismo. Además de los serotipos naturales, la ingeniería de cápsides mediante diseño racional o evolución dirigida ha expandido el repertorio de vectores AAV.
La fabricación de vectores AAV implica métodos como la transfección transitoria triple de células mamíferas (común en investigación y clínica), infección de células de empaquetamiento, entre otros. La purificación es vital para eliminar contaminantes celulares y cápsides vacías, que pueden influir en los resultados. Mejorar los procesos de fabricación para aumentar el rendimiento y la pureza es un área de enfoque.
Principales Limitaciones de los Vectores AAV
A pesar de su promesa, los vectores AAV presentan varias limitaciones significativas que deben abordarse para su aplicación generalizada y segura en terapia génica.
Inmunogenicidad del Vector
Los vectores AAV, compuestos por una cápside proteica y un genoma de ADN, pueden desencadenar respuestas inmunes en el huésped. Dado que la cápside es similar al virus salvaje al que los humanos están expuestos, las respuestas inmunes pueden ser parecidas a las de una infección natural, aunque la dosis y vía de administración influyen.
- Respuesta de Células T: La inmunidad celular mediada por células T CD8+ dirigidas contra la cápside AAV es crítica para la seguridad y eficacia. Se observó por primera vez en ensayos clínicos de terapia génica hepática para la hemofilia B, donde un aumento transitorio de enzimas hepáticas y pérdida de expresión del transgén coincidieron con la expansión de células T CD8+ específicas de la cápside. Estas células probablemente causaron el rechazo de los hepatocitos transducidos. La respuesta parece ser dosis-dependiente; por encima de cierto umbral, la activación de células T puede llevar a hepatotoxicidad y pérdida de expresión. La variabilidad individual (tipo HLA, exposición previa) influye en el resultado. La administración oportuna de inmunosupresión (como corticosteroides) ha sido clave para mitigar este efecto, aunque el momento y la necesidad varían. La influencia de la fabricación (por ejemplo, la proporción de cápsides vacías) en la inmunogenicidad de las células T está bajo investigación.
- Inmunidad Humoral (Anticuerpos Neutralizantes): Una proporción significativa de individuos desarrolla inmunidad humoral contra la cápside AAV tras la exposición natural, generalmente a partir de los 2 años. Estos anticuerpos neutralizantes (NAbs) pueden tener un impacto profundo en la eficacia de la transferencia génica, bloqueando la transducción celular. La alta prevalencia de NAbs y su reactividad cruzada entre serotipos son un obstáculo importante, especialmente para la administración intravenosa. Títulos bajos de NAbs pueden ser suficientes para impedir la eficacia terapéutica. La presencia de NAbs preexistentes es un criterio de exclusión común en ensayos clínicos, limitando el número de pacientes elegibles y dificultando la re-administración del vector.
Potencia y Eficacia
El objetivo es lograr una expresión estable y duradera del transgén a niveles terapéuticos. Los ensayos clínicos iniciales mostraron que los niveles terapéuticos se alcanzan de manera dosis-dependiente. Sin embargo, dosis más altas se correlacionan positivamente con respuestas inmunes no deseadas, lo que puede disminuir o anular la expresión del transgén. Además, la fabricación de vectores AAV es compleja y costosa. Maximizar la potencia del vector es crucial para disminuir la relación dosis/respuesta y reducir el riesgo de efectos adversos relacionados con la dosis y la inmunogenicidad.
La potencia puede mejorarse optimizando el diseño del vector (cápside/genoma) y el casete de expresión. Esto busca aumentar la infección/transducción celular o los niveles/actividad del transgén. El serotipo AAV8 ha mostrado ser eficiente para la transducción hepática sistémica. La ingeniería de cápsides (mutaciones en residuos específicos, diseño racional, evolución dirigida) busca mejorar el tropismo, la evasión de la degradación proteasomal y la evitación de la inmunidad preexistente. Los modelos humanizados (hígados quiméricos ratón-humano) son herramientas valiosas para evaluar la transducción en hepatocitos humanos.
Capacidad de Empaquetamiento Limitada
Una limitación inherente de los vectores AAV es su capacidad limitada para empaquetar ADN, que es de aproximadamente 4.7 kb. Esto impide la entrega de genes grandes o el uso de elementos reguladores extensos necesarios para una expresión génica óptima. Se han desarrollado varias estrategias para superar esta limitación:
- Vectores scAAV (Auto-complementarios): Estos vectores empaquetan un genoma de doble cadena listo para la expresión, lo que resulta en un inicio más rápido y niveles más altos de expresión del transgén. Sin embargo, debido a su formato de doble cadena, solo pueden empaquetar transgenes de hasta ~2.4 kb, reduciendo su aplicabilidad para genes más grandes.
- Vectores AAV Oversized (Sobredimensionados): Intentan empaquetar genomas más grandes (>4.7 kb), pero esto a menudo resulta en preparaciones heterogéneas y genomas truncados, limitando la eficiencia de transducción y el desarrollo clínico.
- Vectores AAV Duales: Dividen un casete de expresión grande en dos mitades, cada una empaquetada en un vector AAV separado. La re-ensamblaje del casete completo ocurre tras la co-infección de la misma célula. Esto puede suceder por recombinación homóloga (vectores superpuestos) o concatenación mediada por ITRs (vectores trans-splicing), o una combinación (vectores híbridos). Aunque han demostrado eficacia en modelos animales, su eficiencia es generalmente menor que la de los vectores AAV simples, requiriendo dosis más altas.
- Estrategias de Re-ensamblaje Proteico: Implican el uso de vectores AAV separados para entregar secuencias que codifican dominios polipeptídicos que se re-ensamblan dentro de la célula para formar una proteína funcional completa.
Genotoxicidad
Aunque la integración del genoma del vector AAV en el ADN del huésped es un evento raro, el riesgo de genotoxicidad asociada es una preocupación. La integración aleatoria puede causar mutaciones por pérdida o ganancia de función, alterando la funcionalidad celular. Estudios en ratones neonatales han reportado que la administración sistémica de AAV los predispone al carcinoma hepatocelular (HCC) debido a la inserción de genomas virales cerca de loci específicos (como Rian en ratones) que regulan genes implicados en el desarrollo tumoral. La preferencia por ciertos sitios de inserción parece favorecer loci transcripcionalmente activos. Además, la fuerza del promotor en el casete de expresión influye en la disfunción génica inducida por la inserción. La presencia de elementos trans-activadores hepáticos en el genoma del AAV salvaje también se ha relacionado con la inserción clonal en HCC humanos. Sin embargo, estudios a largo plazo en modelos animales grandes (perros, primates no humanos) y datos preliminares en humanos no han mostrado preocupaciones significativas sobre la genotoxicidad. El riesgo parece mayor en tejidos en proliferación o en animales con susceptibilidad tumoral preexistente.
Persistencia en Tejidos en Proliferación
Los genomas de AAV recombinantes persisten principalmente de forma episomal (extra-cromosómica) en el núcleo de las células transducidas. En tejidos con alta tasa de proliferación, como el hígado en crecimiento de neonatos o en ciertas enfermedades metabólicas que causan recambio celular, estos genomas episomales pueden diluirse con cada división celular. Esto lleva a una pérdida de expresión del transgén con el tiempo, limitando la eficacia terapéutica, especialmente si el tratamiento se realiza en la infancia. En contraste, en tejidos adultos post-mitóticos o de lenta replicación, los genomas de AAV muestran una persistencia mucho mayor y una expresión estable del transgén durante años.
Para abordar la pérdida de genomas en tejidos en división, se han explorado estrategias para promover la integración del genoma del vector en el ADN del huésped. Esto incluye el uso de secuencias de homología para dirigir la integración a loci específicos (como el locus de la Albúmina en la estrategia "gene-ride") o el uso de nucleasas (como ZFNs o CRISPR/Cas9) para inducir rupturas de doble cadena y potenciar la recombinación homóloga. Estas estrategias buscan lograr una integración estable que se mantenga a través de las divisiones celulares. Sin embargo, la eficiencia de integración sigue siendo baja en la mayoría de los enfoques, requiriendo altas dosis de vector, y la evaluación cuidadosa del riesgo de integración fuera del objetivo y sus efectos genotóxicos es crucial.
Estrategias para Superar las Limitaciones
La investigación activa busca mitigar estas limitaciones:
- Ingeniería de Vectores: Desarrollo de nuevas cápsides con tropismo mejorado, menor inmunogenicidad o mayor capacidad de empaquetamiento. Optimización de genomas vectoriales, incluyendo el diseño de vectores scAAV mejorados o duales más eficientes.
- Optimización del Casete de Expresión: Diseño de promotores, enhancers y otros elementos reguladores específicos del tejido para maximizar la expresión del transgén solo en las células deseadas y evitar su expresión en células presentadoras de antígenos. Optimización de codones y uso de variantes proteicas mejoradas (mayor actividad, secreción).
- Modulación de la Respuesta Inmune: Uso de regímenes de inmunosupresión transitoria para mitigar la respuesta de células T anti-cápside. Desarrollo de estrategias para inducir tolerancia inmune al transgén (como la expresión hepática). Uso de señuelos de cápside o vectores exo-AAV para evadir los anticuerpos neutralizantes.
- Mejora de la Entrega: Optimización de las vías y métodos de administración (por ejemplo, entrega regional) y el uso de fármacos que potencien la transducción celular al proteger las partículas virales de la degradación.
- Promoción de la Integración: Estrategias de edición genómica (CRISPR/Cas9, ZFNs) combinadas con vectores AAV para lograr una integración dirigida y estable en tejidos en proliferación, aunque se necesita investigación adicional sobre seguridad y eficiencia.
- Estrategias de Re-administración: Desarrollo de enfoques para permitir la re-administración de vectores AAV en pacientes que han desarrollado anticuerpos, como el cambio de serotipo de cápside o el uso de terapias para reducir los niveles de anticuerpos.
Comparativa de Estrategias para Superar la Capacidad Limitada
| Estrategia | Descripción | Capacidad de Empaquetamiento | Ventajas | Desventajas |
|---|---|---|---|---|
| ssAAV (Cadena Simple) | Vector AAV estándar con genoma de cadena simple. | ~4.7 kb | Históricamente usado, buena capacidad relativa. | Expresión lenta (requiere síntesis de 2da cadena), menor potencia que scAAV en algunos tejidos. |
| scAAV (Auto-complementario) | Genoma diseñado para formar una estructura de doble cadena. | ~2.4 kb | Expresión rápida y alta, mayor potencia. | Capacidad de empaquetamiento muy limitada. |
| AAV Dual (Superpuesto/Trans-splicing/Híbrido) | Divide el transgén grande en dos vectores AAV separados que se re-ensamblan en la célula. | Hasta ~10 kb (depende del re-ensamblaje) | Permite la entrega de transgenes muy grandes. | Menor eficiencia que AAV simple, requiere co-infección, complejidad en el diseño. |
| AAV Oversized | Intenta empaquetar genomas más grandes de lo normal. | >4.7 kb (parcial) | Potencial para genes grandes. | Ineficiente, preparaciones heterogéneas, genomas truncados. |
| Re-ensamblaje Proteico | Entrega subunidades proteicas separadas que se re-ensamblan en la célula. | Múltiples genes pequeños | Permite la expresión de proteínas muy grandes. | Requiere que la proteína sea funcional como subunidades, eficiencia de re-ensamblaje variable. |
Preguntas Frecuentes sobre las Limitaciones de AAV
¿Se puede usar la terapia génica con AAV en pacientes que ya han sido expuestos al virus AAV salvaje?
Sí, pero la exposición previa al AAV salvaje a menudo resulta en la presencia de anticuerpos neutralizantes (NAbs) contra la cápside. Estos NAbs pueden bloquear la transducción del vector, reduciendo drásticamente la eficacia. Los ensayos clínicos a menudo excluyen a pacientes con títulos altos de NAbs. Se están investigando estrategias para superar esta limitación, como usar serotipos menos prevalentes, diseñar cápsides que evadan los NAbs o emplear técnicas como la plasmaféresis para reducir los niveles de anticuerpos antes del tratamiento.
¿Es segura a largo plazo la terapia génica con AAV, especialmente en niños?
Los datos a largo plazo en modelos animales grandes y los datos preliminares en humanos (más de 7 años en algunos casos) son generalmente tranquilizadores en cuanto a la genotoxicidad en tejidos adultos. Sin embargo, estudios en ratones neonatales sugieren un riesgo potencial de inserción genómica y desarrollo de tumores en tejidos en rápida proliferación. La persistencia del genoma del vector en el hígado en crecimiento de niños también es una preocupación, ya que los genomas episomales pueden diluirse. Se necesitan más datos a largo plazo, especialmente en pacientes pediátricos, para comprender completamente la seguridad y persistencia en esta población.
¿Por qué se necesitan dosis tan altas de vectores AAV?
La necesidad de dosis altas se debe a varios factores, incluyendo la eficiencia de entrega y transducción del vector al tejido objetivo, la respuesta inmune del huésped que puede neutralizar el vector o eliminar las células transducidas, y la potencia del casete de expresión para generar suficiente proteína terapéutica. Además, una proporción de las partículas virales en las preparaciones pueden ser cápsides vacías o genomas defectuosos. La alta dosis, a su vez, puede exacerbar la respuesta inmune. La investigación busca aumentar la potencia del vector y mejorar la fabricación para reducir la dosis necesaria.
¿Puede la respuesta inmune del paciente eliminar las células tratadas con terapia génica AAV?
Sí, la respuesta inmune mediada por células T CD8+ contra los antígenos de la cápside AAV presentados por las células transducidas puede llevar a la eliminación de estas células y a la pérdida de la expresión del transgén. Esto se ha observado en ensayos clínicos, particularmente en terapia génica hepática. La administración de inmunosupresores es una estrategia para mitigar esta respuesta, pero no siempre es completamente efectiva y su uso conlleva riesgos. Comprender mejor los factores que desencadenan esta respuesta y desarrollar estrategias más específicas para controlarla son áreas de investigación activa.
¿Qué pasa si el gen que necesito entregar es más grande que la capacidad de empaquetamiento del AAV?
La capacidad limitada de ~4.7 kb es un obstáculo para muchos genes terapéuticos. Para genes grandes, se están desarrollando estrategias como los vectores AAV duales, donde el gen se divide en dos partes empaquetadas en vectores separados que se re-ensamblan en la célula objetivo. Otras estrategias implican el re-ensamblaje de proteínas a partir de subunidades más pequeñas entregadas por vectores AAV separados. Aunque prometedoras, estas estrategias suelen ser menos eficientes que el uso de un único vector AAV con un transgén pequeño.
Conclusión
Los vectores AAV representan una herramienta poderosa y cada vez más utilizada en el campo de la terapia génica, con aplicaciones que se extienden a diversas enfermedades, incluidas las neurológicas. Su historial de seguridad favorable y su capacidad para transducir eficazmente diversos tejidos los han convertido en la plataforma de elección para muchas aplicaciones in vivo. Sin embargo, persisten desafíos importantes relacionados con la inmunogenicidad del vector y del transgén, la capacidad limitada de empaquetamiento, el riesgo, aunque bajo, de genotoxicidad por integración y la persistencia limitada en tejidos en proliferación.
La investigación continua está generando enfoques innovadores para superar estas barreras, desde la ingeniería avanzada de cápsides y genomas hasta la optimización de los casetes de expresión, pasando por estrategias de modulación inmune y métodos de entrega mejorados. Las lecciones aprendidas en ensayos clínicos, particularmente en áreas como la terapia génica hepática para la hemofilia, están informando el diseño de futuras terapias y la gestión de la respuesta del huésped. A medida que se perfeccionan estas tecnologías y se obtienen más datos a largo plazo, especialmente en poblaciones pediátricas y en aplicaciones para enfermedades complejas como las neurodegenerativas, el potencial terapéutico de los vectores AAV seguirá expandiéndose, acercándonos a tratamientos efectivos y duraderos para una amplia gama de afecciones.
Si quieres conocer otros artículos parecidos a Retos en Terapia Génica con Vectores AAV puedes visitar la categoría Neurociencia.
