La investigación en neurociencia busca comprender la complejidad intrincada del cerebro y el sistema nervioso. Para ello, es fundamental poder identificar y localizar componentes específicos dentro de las células y tejidos. Aquí es donde entra en juego una técnica poderosa y fundamental: la Inmunohistoquímica, comúnmente conocida como IHC.
La Inmunohistoquímica (IHC) constituye la base del análisis histológico y patológico, siendo una herramienta indispensable para la detección y caracterización de proteínas en una amplia variedad de tejidos orgánicos, y de manera crucial, en los tejidos cerebrales. Esta técnica permite a los científicos 'ver' dónde se encuentran proteínas específicas dentro de una muestra de tejido, proporcionando información vital sobre su función y distribución en condiciones normales y patológicas.
- ¿Qué es la Inmunohistoquímica (IHC)?
- La Importancia de la IHC en la Investigación del Cerebro
- Preparación del Tejido: El Rol del FFPE
- Métodos de Visualización en IHC
- Comparación de Métodos de Visualización
- El Proceso Estándar de IHC en Secciones de Cerebro
- Automatización en IHC
- Aplicaciones Avanzadas y Consideraciones
- Preguntas Frecuentes sobre IHC en Neurociencia
- Conclusión
¿Qué es la Inmunohistoquímica (IHC)?
En esencia, la IHC es una técnica basada en la interacción altamente específica entre un anticuerpo y su antígeno (la proteína diana). Se utiliza un anticuerpo marcado (directamente o indirectamente) que se une específicamente a la proteína que nos interesa dentro de una muestra de tejido. Una vez que el anticuerpo se ha unido a la proteína, se utiliza un método de detección para visualizar esta unión, revelando así la ubicación de la proteína en el tejido.
La IHC es fundamental porque las proteínas son los caballos de batalla de las células; realizan la mayoría de las funciones celulares y son esenciales para la estructura, función y regulación de los tejidos. Conocer la localización precisa de una proteína puede proporcionar información crucial sobre su papel biológico. Por ejemplo, si una proteína se encuentra predominantemente en el núcleo de una neurona, es probable que esté involucrada en la regulación génica. Si se encuentra en las sinapsis, probablemente juegue un papel en la comunicación neuronal.
La Importancia de la IHC en la Investigación del Cerebro
El cerebro es un órgano increíblemente complejo con una vasta diversidad de tipos celulares y estructuras interconectadas. La capacidad de localizar proteínas específicas en este entorno es vital para desentrañar sus misterios. La IHC es un método clave que proporciona un análisis más preciso de la localización y función de:
- Neuronas: Permite identificar diferentes tipos de neuronas basándose en las proteínas que expresan, estudiar su morfología y seguir sus proyecciones.
- Células Neuroendocrinas: Facilita la detección de hormonas y neuropéptidos producidos por estas células en el sistema nervioso central.
- Células Madre Neurales: Ayuda a rastrear su ubicación, diferenciación y migración durante el desarrollo y en el cerebro adulto.
- Células Gliales: Incluyendo astrocitos, oligodendrocitos y microglía, la IHC permite estudiar su distribución, activación y papel en el soporte neuronal, la mielinización y la respuesta inmune del cerebro.
- Unidades Neurovasculares: Facilita el estudio de la interacción entre las neuronas, las células gliales y los vasos sanguíneos, crucial para comprender la barrera hematoencefálica y las enfermedades cerebrovasculares.
En resumen, la IHC permite a los neurocientíficos mapear la arquitectura molecular del cerebro, identificar poblaciones celulares específicas y estudiar cómo la expresión y localización de proteínas cambian durante el desarrollo, el aprendizaje, el envejecimiento y en diversas patologías neurológicas como el Alzheimer, el Parkinson o los accidentes cerebrovasculares.
Preparación del Tejido: El Rol del FFPE
Para realizar IHC, el tejido debe ser preservado adecuadamente para mantener su estructura y la integridad de las proteínas. Un método de preparación de tejido muy común y ampliamente utilizado es la fijación en formalina y el posterior embebimiento en parafina (FFPE, por sus siglas en inglés: Formalin-Fixed Paraffin-Embedded).
Los tejidos FFPE son populares por varias razones:
- Almacenamiento Sencillo: Los bloques de parafina con tejido embebido pueden almacenarse a temperatura ambiente durante años o incluso décadas, creando archivos valiosos para la investigación retrospectiva.
- Versatilidad: Permiten cortar secciones muy finas (típicamente de 3 a 10 micrómetros) que son ideales para la microscopía.
- Preservación Morfológica: La fijación con formalina preserva muy bien la estructura celular y tisular.
Aunque los tejidos FFPE son convenientes, el proceso de fijación con formalina puede crear enlaces cruzados entre proteínas que a veces enmascaran los sitios de unión del anticuerpo (epítopos). Por ello, a menudo es necesario realizar un paso adicional llamado 'recuperación antigénica' antes de la tinción con anticuerpos para 'desenmascarar' estos epítopos y permitir que el anticuerpo se una eficazmente.
Otros métodos de preparación de tejido incluyen el tejido fresco congelado, que a menudo preserva mejor la antigenicidad de algunas proteínas, pero requiere almacenamiento a temperaturas muy bajas y las secciones suelen ser más frágiles.
Métodos de Visualización en IHC
La visualización de las interacciones anticuerpo-antígeno, una vez que los anticuerpos se han unido a las proteínas diana, se realiza principalmente de dos maneras:
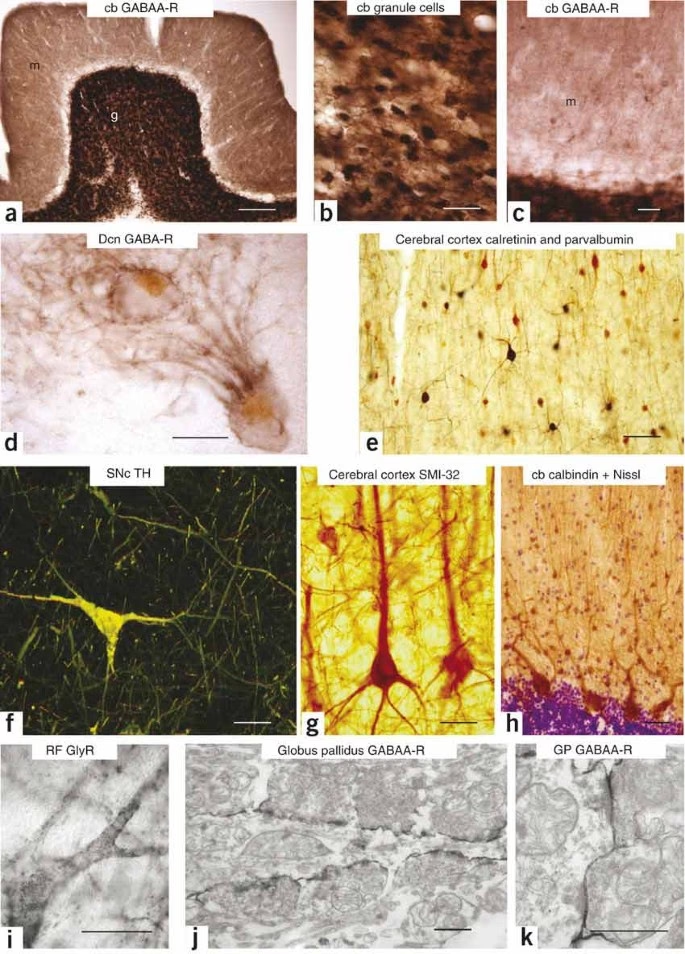
1. IHC con Tinción Cromogénica
En la IHC con tinción cromogénica, un anticuerpo (generalmente el secundario, que se une al anticuerpo primario que se une a la proteína diana) está conjugado químicamente a una enzima. Las enzimas más comunes son la Peroxidasa de Rábano Picante (HRP) o la Fosfatasa Alcalina (AP).
Después de que los anticuerpos se han unido a la proteína diana y se ha aplicado la enzima conjugada, se añade un sustrato adecuado. La enzima cataliza una reacción que convierte el sustrato incoloro en un producto coloreado e insoluble que precipita en el sitio de la reacción (donde la proteína diana se encuentra). Este colorante se puede ver con un microscopio óptico estándar. Un cromógeno común para HRP es el DAB (diaminobencidina), que produce un precipitado marrón.
La ventaja principal de este método es que no requiere equipos de microscopía especializados y la tinción es permanente, lo que facilita el archivo de las muestras. Sin embargo, generalmente solo permite visualizar una o dos proteínas por muestra de tejido debido a la superposición de colores.
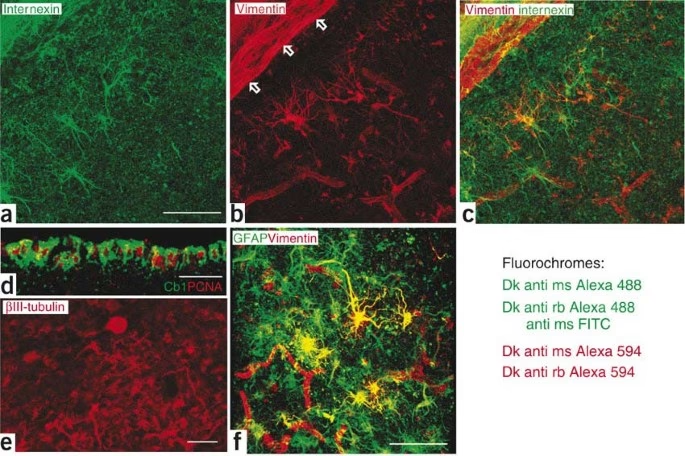
2. IHC con Tinción Fluorescente
En la IHC con tinción fluorescente (a menudo llamada Inmunofluorescencia, IF), los anticuerpos están marcados con compuestos fluorescentes, conocidos como fluorocromos. Ejemplos comunes de fluorocromos incluyen el Isotiocianato de Fluoresceína (FITC), la Rodamina, el Alexa Fluor, etc.
Cuando los fluorocromos son excitados por luz de una longitud de onda específica, emiten luz en una longitud de onda diferente. Esta luz emitida se detecta utilizando un microscopio de fluorescencia. La señal fluorescente aparece como puntos brillantes o patrones en las áreas donde la proteína diana está presente.
Una ventaja significativa de la IHC fluorescente es la capacidad de realizar tinciones múltiples (multiplexing), donde se detectan simultáneamente varias proteínas en la misma sección de tejido utilizando anticuerpos marcados con diferentes fluorocromos que emiten luz en distintos colores. Esto es increíblemente útil en neurociencia para estudiar la colocalización de proteínas o identificar diferentes tipos celulares en un mismo campo de visión.
Sin embargo, la fluorescencia puede desvanecerse con el tiempo (fotoblanqueo) y requiere un microscopio de fluorescencia, que es más costoso que un microscopio óptico estándar.
Comparación de Métodos de Visualización
| Característica | IHC Cromogénica | IHC Fluorescente |
|---|---|---|
| Detección | Enzima + Sustrato (color) | Fluorocromo (luz) |
| Microscopio | Óptico estándar | Fluorescencia |
| Señal | Precipitado coloreado, permanente | Fluorescencia, puede desvanecerse |
| Multiplexing (múltiples proteínas) | Limitado (1-2) | Alto potencial (múltiples colores) |
| Costo del equipo | Menor | Mayor |
| Fotoblanqueo | No aplica | Sí |
El Proceso Estándar de IHC en Secciones de Cerebro
Si bien los protocolos específicos pueden variar, un flujo de trabajo estándar para la IHC en secciones de tejido cerebral FFPE típicamente incluye los siguientes pasos:
- Fijación y Procesamiento: El tejido cerebral se fija (ej. con formalina) y se procesa para ser embebido en parafina.
- Corte de Secciones: Se obtienen secciones finas (ej. 5-10 µm) utilizando un micrótomo.
- Montaje y Secado: Las secciones se montan en portaobjetos de vidrio y se secan.
- Desparafinación e Hidratación: Las secciones se pasan por solventes (ej. xileno) para eliminar la parafina y luego por alcoholes de concentración decreciente para rehidratar el tejido.
- Recuperación Antigénica: Se aplica calor o enzimas para desenmascarar los epítopos de las proteínas que pudieron haber sido alterados por la fijación.
- Bloqueo: Se incuba la sección con una solución de bloqueo (ej. suero normal o albúmina) para reducir la unión no específica de anticuerpos.
- Incubación con Anticuerpo Primario: El anticuerpo primario, específico para la proteína diana, se incuba con la sección.
- Lavados: Se lava para eliminar el anticuerpo primario no unido.
- Incubación con Anticuerpo Secundario (si es indirecta): Si se usa un método indirecto, se incuba un anticuerpo secundario (dirigido contra el anticuerpo primario) conjugado a una enzima o fluorocromo.
- Lavados: Se lava para eliminar el anticuerpo secundario no unido.
- Detección (si es cromogénica): Se añade el sustrato para la enzima, produciendo un precipitado de color en el sitio de la proteína diana.
- Contratinción: A menudo se tiñe el núcleo celular con otro color (ej. Hematoxilina para IHC cromogénica, DAPI para IHC fluorescente) para proporcionar contexto morfológico.
- Montaje y Cubreobjetos: La sección se monta con un medio de montaje y se cubre con un cubreobjetos.
- Visualización: Se examina la sección bajo el microscopio apropiado.
Automatización en IHC
Para laboratorios con alto rendimiento o que buscan una mayor estandarización y reproducibilidad, los autoestimadores de inmunotinción representan una opción valiosa. Estos sistemas automatizan la mayoría de los pasos del protocolo de IHC, desde la desparafinación y recuperación antigénica hasta la incubación con anticuerpos y la detección. La automatización ayuda a reducir la variabilidad asociada con los protocolos manuales, ahorra tiempo y reactivos, y permite procesar múltiples muestras simultáneamente.
Aplicaciones Avanzadas y Consideraciones
Más allá de la detección básica, la IHC se puede adaptar para aplicaciones más complejas. La inmunofluorescencia multiplex es cada vez más utilizada en neurociencia para estudiar la interacción de múltiples poblaciones celulares o la expresión de varias proteínas dentro de un mismo microambiente tisular. Técnicas como el CLARITY o la inmunotinción de tejidos completos (whole-mount immunostaining) combinan la IHC con métodos de aclaramiento de tejido para visualizar estructuras y redes neuronales en volúmenes de tejido más grandes sin necesidad de seccionar finamente, lo cual es revolucionario para estudiar la conectividad cerebral.
Es crucial considerar la especificidad y validación de los anticuerpos utilizados en IHC. Un anticuerpo debe unirse específicamente a su proteína diana y no a otras proteínas, para asegurar que la señal detectada sea precisa. Los controles negativos (omitiendo el anticuerpo primario) y positivos (usando tejido conocido por expresar la proteína) son esenciales para validar los resultados.
Preguntas Frecuentes sobre IHC en Neurociencia
¿Qué tipo de proteínas se pueden detectar con IHC en el cerebro?
Prácticamente cualquier proteína para la que exista un anticuerpo específico y validado puede detectarse, incluyendo proteínas estructurales (ej. citoesqueleto), enzimas, receptores, canales iónicos, neurotransmisores, factores de transcripción, marcadores de tipos celulares específicos (ej. NeuN para neuronas, GFAP para astrocitos), y proteínas asociadas a enfermedades (ej. placas de beta-amiloide, ovillos de tau fosforilada).
¿Es la IHC una técnica cuantitativa?
La IHC es principalmente una técnica cualitativa o semicuantitativa. Permite determinar la presencia y localización de una proteína, y a menudo se puede estimar visualmente la intensidad de la tinción o el número de células positivas. Sin embargo, para una cuantificación precisa de los niveles de proteína, se suelen preferir técnicas como Western blot o ELISA, aunque la IHC proporciona la crucial información espacial que estas últimas no ofrecen.
¿Puedo ver múltiples proteínas en la misma sección de tejido cerebral?
Sí, especialmente utilizando la IHC fluorescente (inmunofluorescencia multiplex). Al usar anticuerpos primarios de diferentes especies o isótipos, o anticuerpos secundarios conjugados a fluorocromos con diferentes espectros de emisión, se pueden visualizar varias proteínas simultáneamente en la misma muestra, cada una con un color distinto.
¿Cuál es la diferencia entre IHC e Inmunofluorescencia (IF)?
La Inmunofluorescencia (IF) es un tipo específico de Inmunohistoquímica (IHC) que utiliza fluorocromos para la detección, en lugar de reacciones enzimáticas que producen un color visible en microscopía óptica. IF es IHC fluorescente.
Conclusión
La Inmunohistoquímica es una piedra angular de la investigación en neurociencia. Su capacidad para visualizar la distribución espacial de proteínas dentro del intrincado paisaje del tejido cerebral ha proporcionado y sigue proporcionando conocimientos fundamentales sobre la estructura, función y patología del sistema nervioso. Ya sea utilizando métodos cromogénicos para una visualización sencilla o técnicas fluorescentes multiplex para desentrañar complejas interacciones moleculares, la IHC sigue siendo una herramienta indispensable en el arsenal del neurocientífico, ayudando a desvelar los secretos ocultos en las proteínas del cerebro.
Si quieres conocer otros artículos parecidos a IHC: Desvelando Proteínas en el Cerebro puedes visitar la categoría Neurociencia.