Durante décadas, la genética fue vista como el destino inmutable de nuestra biología. Sin embargo, la neurociencia moderna nos revela una imagen mucho más dinámica del cerebro, una donde los genes no son la única historia. Ha emergido un campo fascinante que está revolucionando nuestra comprensión: la epigenética.
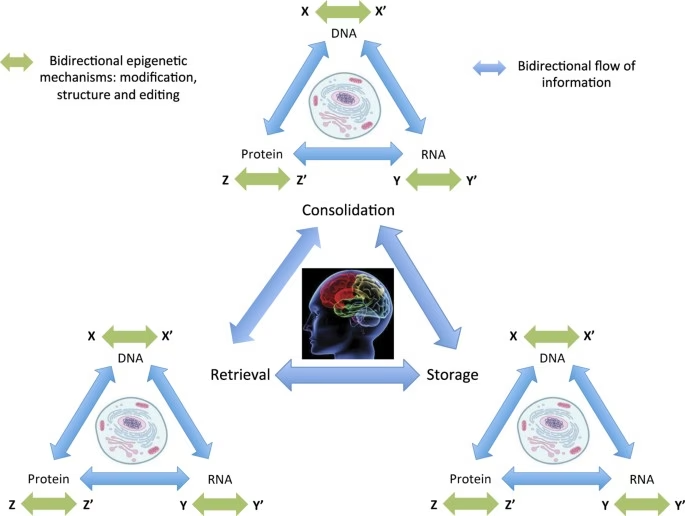
Definida de forma sencilla, la epigenética se refiere a los cambios en la expresión génica que ocurren sin alterar la secuencia subyacente del ADN. Piensa en ello como la 'narración' que el cuerpo lee del 'libro' de ADN. La secuencia de letras del libro (el genoma) no cambia, pero la forma en que se lee esa historia (la expresión génica) sí puede variar drásticamente, influenciada por múltiples factores. En el contexto del cerebro, esta capacidad de modificar la expresión génica a largo plazo, a menudo de forma heredable, ha abierto un abanico de nuevas posibilidades para entender desde el desarrollo hasta las enfermedades complejas.
- ¿Qué Implica la Epigenética en el Cerebro?
- Epigenética y Neuroplasticidad: Una Alianza Dinámica
- El Papel de la Epigenética en el Desarrollo Neuronal
- La Epigenética en las Enfermedades Neurológicas y Psiquiátricas
- Factores Ambientales y Estilo de Vida: Moldeando el Epigenoma Cerebral
- Implicaciones Clínicas: Diagnóstico, Tratamiento y Prevención
- Moduladores Epigenéticos Naturales
- Preguntas Frecuentes sobre Epigenética y Neurociencia
- Conclusión
¿Qué Implica la Epigenética en el Cerebro?
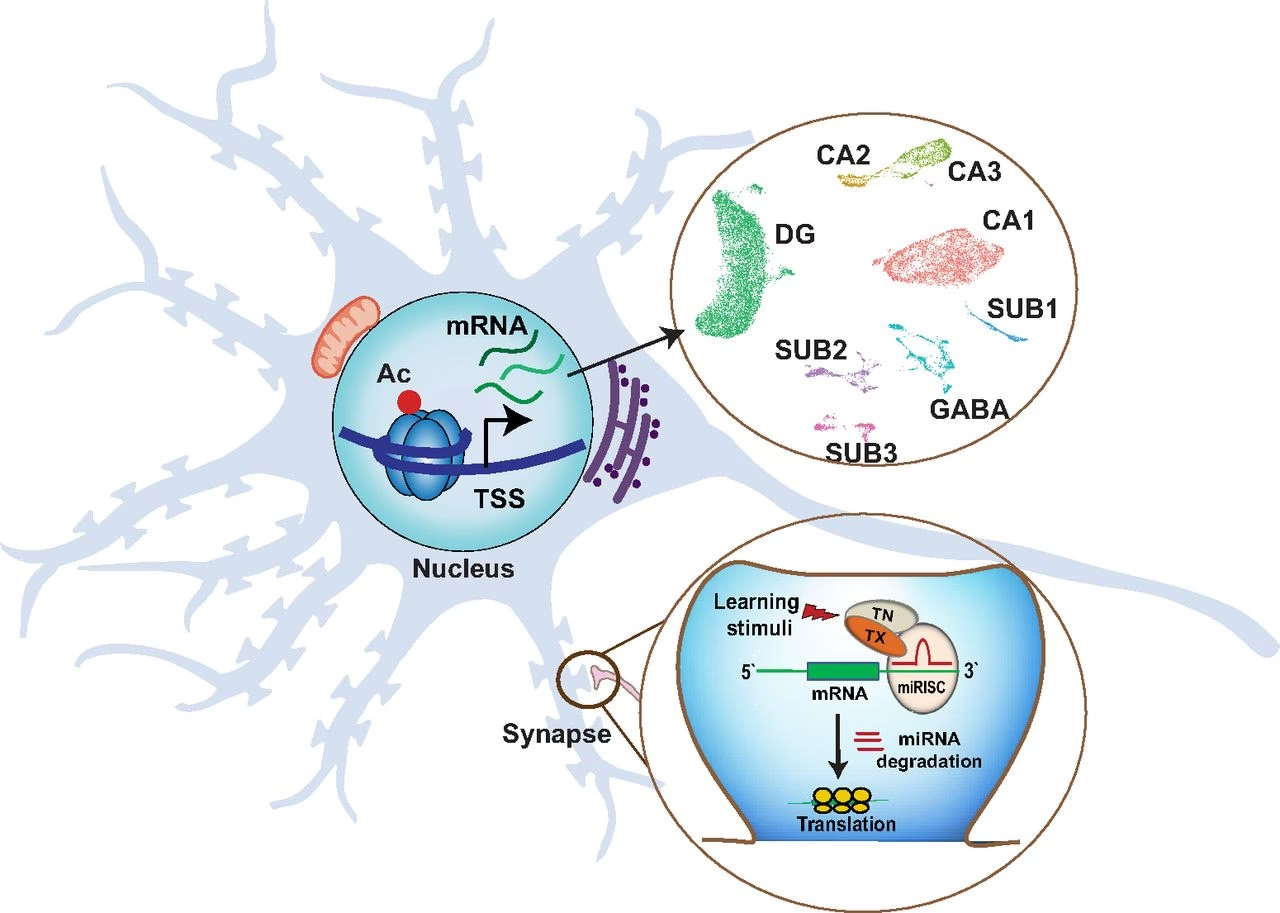
Los mecanismos epigenéticos son procesos bioquímicos que actúan como interruptores o reguladores de la actividad génica. Los principales actores en el cerebro incluyen:
- Metilación del ADN: La adición de un grupo metilo a la base citosina del ADN, usualmente en regiones promotoras de genes. Generalmente, la metilación en promotores tiende a silenciar la expresión génica.
- Modificaciones de Histonas: El ADN se enrolla alrededor de proteínas llamadas histonas. Las modificaciones químicas en estas histonas (como acetilación, metilación, fosforilación) pueden alterar la estructura de la cromatina (el complejo de ADN y proteínas), haciendo que los genes sean más o menos accesibles para la maquinaria de transcripción. La acetilación de histonas, por ejemplo, tiende a abrir la cromatina y facilitar la expresión génica, mientras que ciertas metilaciones pueden reprimirla.
- ARN No Codificantes (ncRNAs): Moléculas de ARN que no se traducen en proteínas pero que desempeñan roles regulatorios cruciales, incluyendo la modulación de la estabilidad del ARNm o el silenciamiento génico (como los microARNs o miRNAs).
Estos mecanismos no son estáticos; son dinámicos y sensibles al entorno. En el cerebro, regulan procesos fundamentales como el desarrollo neuronal, la formación y el refinamiento de las conexiones sinápticas (plasticidad sináptica) y la consolidación de la memoria. La interrupción de este delicado equilibrio epigenético puede tener consecuencias profundas para la función cerebral y está implicada en una amplia gama de trastornos neurológicos y psiquiátricos.
Epigenética y Neuroplasticidad: Una Alianza Dinámica
La neuroplasticidad es la asombrosa capacidad del cerebro para reorganizarse a lo largo de la vida, formando nuevas conexiones neuronales en respuesta a la experiencia, el aprendizaje o una lesión. No es un órgano fijo, sino que se adapta constantemente. Esta plasticidad ocurre a diferentes niveles, desde cambios en la fuerza de las sinapsis individuales (plasticidad sináptica) hasta la generación de nuevas neuronas (neurogénesis).
La epigenética no es lo mismo que la neuroplasticidad, pero es un mecanismo fundamental que la impulsa y la regula. Los factores ambientales y las experiencias de vida actúan como 'factores epigenéticos' que influyen en la estructura y función cerebral a través de modificaciones epigenéticas. Por ejemplo, la acetilación de histonas y la metilación/desmetilación del ADN son mecanismos epigenéticos de primera línea detrás de la neuroplasticidad.
Moléculas específicas, a menudo llamadas 'moléculas de firma epigenética', desempeñan papeles cruciales en esta reprogramación. Proteínas como MeCP2 (proteína de unión a CpG metilado 2), HATs (histona acetiltransferasas), HDACs (histona deacetilasas), BDNF (factor neurotrófico derivado del cerebro), REST (factor de transcripción silenciador de elementos represores) y TETs (translocaciones diez-once) son actores clave en la modulación epigenética que subyace a la plasticidad. El BDNF, por ejemplo, es esencial para el crecimiento y la supervivencia neuronal, el aprendizaje y la memoria, y su expresión está influenciada por mecanismos epigenéticos como la metilación del ADN. MeCP2 es otro modulador neuronal importante cuya función está ligada a síndromes neurológicos con componentes epigenéticos, como el Síndrome de Rett.
La investigación en neuroepigenética está desentrañando cómo la interacción compleja y dinámica entre las neuronas, la plasticidad neuronal y los mecanismos epigenómicos permite que el cerebro se adapte, aprenda y forme recuerdos. Comprender estos mecanismos es vital para abordar las disfunciones sinápticas y neuronales que subyacen a muchas enfermedades.
El Papel de la Epigenética en el Desarrollo Neuronal
El desarrollo del cerebro, desde las etapas embrionarias hasta la edad adulta, es un proceso finamente orquestado que depende críticamente de la regulación epigenética.

Neurogénesis Embrionaria
Durante el desarrollo embrionario, las células madre neurales generan neuronas siguiendo una secuencia precisa. La metilación del ADN y las modificaciones de histonas dirigen este proceso. Por ejemplo, la metilación del ADN por enzimas como DNMT3b y DNMT1 es esencial para el desarrollo temprano del tubo neural. DNMT3a, aunque no es crucial para la supervivencia embrionaria, es vital para la formación adecuada de la corteza cerebral después del nacimiento, regulando la transición entre el destino de neurona y el de célula glial al metilar genes gliogénicos como Sox9.
Las enzimas TET juegan un papel dinámico al oxidar la 5-metilcitosina (desmetilación), permitiendo la expresión de genes cruciales en el desarrollo. Los microARNs, como miR-124 y miR-9, también son reguladores clave, afinando la expresión génica para controlar la diferenciación y migración neuronal. miR-124, abundante en el SNC, promueve la diferenciación neuronal, mientras que miR-9 regula tanto la diferenciación como la autorrenovación.
Neurogénesis Adulta
Contrariamente a la creencia antigua, el cerebro adulto continúa generando nuevas neuronas en nichos especializados como el giro dentado del hipocampo y la zona subventricular. La metilación del ADN dependiente de DNMT3a, junto con la actividad de miR-124, mantiene el equilibrio entre la quiescencia y la activación de las células madre neurales.
Un área fascinante de la neurogénesis adulta es la reprogramación de astrocitos. Las células gliales como los astrocitos pueden alterar su destino celular bajo ciertas condiciones. La expresión de genes como Mash1, NeuroG1 y NeuroG2 puede reprogramar astrocitos en neuronas, un proceso facilitado por el aumento de la acetilación de histonas (H3K9 y H3K14) cerca de estos genes. Silenciar los mecanismos de metilación del ADN previene que las células progenitoras de astrocitos se rediferencien a su destino glial original, manteniendo un estado más plástico.
La Epigenética en las Enfermedades Neurológicas y Psiquiátricas
La disfunción epigenética, es decir, las alteraciones en la maquinaria epigenómica, está fuertemente asociada con la etiología y progresión de una amplia gama de trastornos cerebrales. A medida que envejecemos, se producen cambios epigenéticos naturales (como la reducción de la heterocromatina global, cambios en las marcas de histonas y la metilación del ADN) que pueden aumentar la susceptibilidad a enfermedades. La regulación epigenética de las regiones potenciadoras (enhancers) en las neuronas también se ha relacionado con enfermedades neurodegenerativas.
Neurodegeneración
- Enfermedad de Alzheimer: Se han identificado cambios epigenéticos específicos, incluyendo alteraciones en la metilación del ADN y modificaciones de histonas. La expresión de microARNs está desregulada (miR-9 y miR-128 aumentados, miR-15a disminuido). El Factor Neurotrófico Derivado del Cerebro (BDNF), crucial para la supervivencia neuronal y la función sináptica, a menudo se reprime a través de la metilación del ADN en pacientes con Alzheimer. El gen APP, responsable de la formación de placas amiloides, tiene una región promotora rica en GC altamente susceptible a la metilación, que disminuye con el envejecimiento. La exposición a toxinas ambientales como el plomo puede causar una sobreexpresión de APP al interferir con su metilación. La teoría de la 'deriva epigenética' relacionada con la edad sugiere que cambios acumulativos contribuyen a la enfermedad esporádica. Los inhibidores de HDAC muestran potencial preclínico para mejorar la función cognitiva al aumentar la plasticidad sináptica.
- Enfermedad de Parkinson: El análisis de la metilación del ADN revela una desregulación significativa en las islas CpG y en genes de riesgo para la enfermedad. La metilación del ADN mitocondrial también fluctúa con la edad y el estrés oxidativo, factores implicados en la disfunción mitocondrial en el Parkinson. Se han observado aumentos en la acetilación de histonas (H2A, H3, H4) en neuronas dopaminérgicas de pacientes con Parkinson. Los niveles de HDAC disminuyen, posiblemente debido a su degradación. Los microARNs también contribuyen; miR-205 parece regular negativamente LRRK2, un gen implicado en el Parkinson. La inhibición de HDAC6 y Sirt2, que regulan la respuesta al estrés celular y la estabilidad citoesquelética, se propone como estrategia neuroprotectora.
- Enfermedad de Huntington: La acetilación de histonas disminuye en loci génicos específicos (Drd2, Penk1, Actb, Grin1), sugiriendo que la mutación del gen HTT interfiere con la actividad de las HATs. Los inhibidores de HDAC (como SAHA, TSA, fenilbutirato) han mostrado efectos beneficiosos en modelos murinos, aunque no restauran la expresión normal de genes de identidad neuronal. La investigación actual también apunta a efectos no dependientes de histonas, como la promoción de la degradación de agregados de HTT mutante.
Trastornos Psiquiátricos
- Depresión y Trastorno de Estrés Postraumático (TEPT): Se han identificado cambios distintivos en la metilación del ADN. En el TEPT, estos cambios varían si ha habido abuso infantil. Se han encontrado regiones diferencialmente metiladas en gemelos con trastorno depresivo mayor. El estrés temprano en la vida, como el abuso infantil o el estrés prenatal (identificado a través de biomarcadores placentarios), puede dejar marcas epigenéticas duraderas que aumentan el riesgo de depresión, ansiedad y TEPT.
- Trastorno Bipolar: Es un trastorno complejo y altamente heredable con componentes epigenéticos. La metilación del ADN (genes como PPIEL, SLC6A4, KCNQ3), la hidrometilación del ADN y las modificaciones de histonas contribuyen. El maltrato infantil en la niñez influye en el estado de metilación de genes como 5-hidroxitriptamina 3A, alterando cómo el maltrato afecta el trastorno bipolar. Los inhibidores de DNMT y HDAC muestran efectos antidepresivos en modelos preclínicos.
- Esquizofrenia: Se han observado patrones de metilación del ADN en genes involucrados en el desarrollo neuronal y la neurotransmisión.
- Adicción: La epigenética juega un papel significativo, especialmente en respuesta a drogas de abuso como la cocaína. Se han demostrado cambios en la acetilación de histonas (inhibidores de HDAC aumentan la sensibilidad a la cocaína) y la metilación del ADN, así como la implicación de microARNs.
- Síndrome de Rett: Un trastorno grave del neurodesarrollo causado por mutaciones en MECP2, un regulador epigenético clave.
Factores Ambientales y Estilo de Vida: Moldeando el Epigenoma Cerebral
La comprensión de los trastornos neurológicos y psiquiátricos se ha profundizado al reconocer la intrincada interacción entre factores genéticos, epigenéticos y ambientales. Nuestros estilos de vida y las exposiciones a lo largo de la vida no son meros acompañamientos; son fuerzas activas que moldean nuestro epigenoma.
Los factores de estilo de vida como la dieta, el ejercicio, el abuso de sustancias y el estrés influyen significativamente en el paisaje epigenético. Los desequilibrios nutricionales pueden alterar los patrones de metilación del ADN, contribuyendo a trastornos. La actividad física regular modifica marcadores epigenéticos relacionados con la salud cerebral. El abuso de sustancias induce cambios epigenéticos que afectan las vías neurales implicadas en la adicción y las comorbilidades psiquiátricas. El estrés crónico se relaciona con modificaciones epigenéticas en genes que regulan la respuesta al estrés.
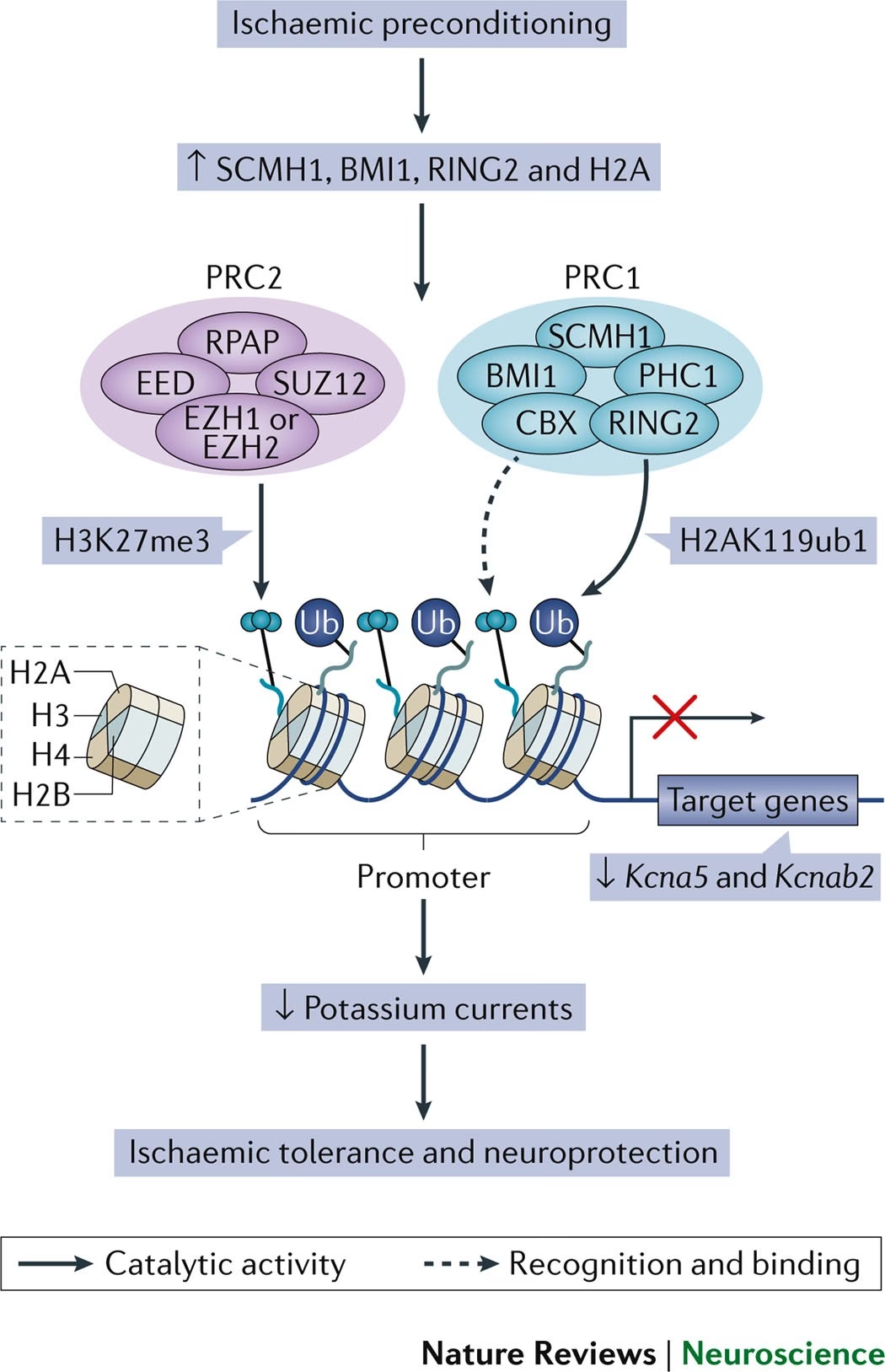
Las exposiciones tempranas en la vida son particularmente influyentes. El estrés materno, la desnutrición o la exposición a toxinas durante el embarazo pueden inducir cambios epigenéticos duraderos que afectan el neurodesarrollo y aumentan el riesgo de trastornos en la vida adulta. El trauma infantil también causa alteraciones epigenéticas a largo plazo que incrementan el riesgo de trastornos. Las toxinas ambientales como el plomo o la contaminación del aire durante períodos críticos del desarrollo pueden alterar el epigenoma, contribuyendo a trastornos neurodesarrollales.
Implicaciones Clínicas: Diagnóstico, Tratamiento y Prevención
La epigenética no es solo un campo de investigación fascinante; tiene un potencial transformador para la práctica clínica.
Diagnóstico
Las modificaciones epigenéticas pueden servir como biomarcadores para diversas enfermedades. Patrones específicos de metilación del ADN se proponen como herramientas de diagnóstico temprano para el Alzheimer. La metilación del ADN en células sanguíneas periféricas podría ofrecer una lectura fácil de eventos epigenéticos cerebrales, útil para el diagnóstico de TEPT. Los biomarcadores epigenéticos en la placenta pueden indicar la exposición materna al estrés y el riesgo futuro para el niño. Esta identificación de biomarcadores permite la detección temprana e intervenciones más oportunas, así como un enfoque más personalizado al reconocer el paisaje epigenético único de cada individuo.
Tratamiento
El potencial terapéutico de la epigenética radica en la naturaleza reversible de las modificaciones epigenéticas. Se están desarrollando terapias dirigidas a enzimas o procesos epigenéticos específicos:
- Inhibidores de HDAC: Sustancias que promueven la acetilación de histonas. Algunos ya están aprobados para otras indicaciones (como el ácido valproico para epilepsia y manía bipolar) o en oncología (vorinostat, romidepsin). En modelos animales, inhibidores específicos (HDAC2, HDAC3, HDAC6) han demostrado mejorar la memoria en el Alzheimer.
- Inhibidores de la Metilación del ADN: Sustancias como 5-azacitidina o RG108 buscan revertir la hipermetilación patológica.
- Terapias Basadas en microARNs: Uso de 'mimics' para restaurar miRNAs deficientes o 'antagomirs' para suprimir miRNAs sobreexpresados (ej. mimics de miR-132 para Alzheimer, moduladores de miR-137 para esquizofrenia).
Estas terapias buscan normalizar la expresión génica alterada en las enfermedades. El desafío principal es lograr una especificidad suficiente para dirigirse solo a las modificaciones aberrantes relevantes para la enfermedad sin causar efectos generalizados no deseados. La personalización del tratamiento basada en el perfil epigenético individual es una promesa clave.
Prevención
La epigenética abre nuevas vías para la prevención, permitiendo identificar individuos en riesgo basándose en marcadores epigenéticos y aplicar intervenciones tempranas. Promover estilos de vida saludables (dieta, ejercicio, manejo del estrés) puede influir positivamente en el epigenoma y mitigar el riesgo. A nivel de salud pública, comprender cómo factores ambientales (toxinas) o sociales (trauma) moldean el epigenoma puede informar políticas y programas comunitarios dirigidos a reducir la exposición a riesgos y promover el bienestar mental.
Moduladores Epigenéticos Naturales
La investigación también explora el potencial de compuestos naturales, a menudo encontrados en la dieta, como moduladores epigenéticos. Conceptos como la "dieta epigenética" o "epidrogas" de origen natural ganan terreno. Compuestos como la curcumina (del cúrcuma), el epigalocatequina-3-galato (EGCG) (del té verde) o el resveratrol (de las uvas) han mostrado capacidad para influir en procesos epigenéticos (como la actividad de DNMTs o HDACs) y ejercer efectos neuroprotectores en diversos modelos de trastornos neurológicos. Si bien gran parte de la investigación se centra en el estrés oxidativo y la inflamación, el vínculo epigenético subyacente a sus efectos en la neuroplasticidad es un área activa de estudio.
| Compuesto Natural | Categoría | Fuente | Trastornos Neurológicos (Ejemplos) | Mecanismos/Efectos (Relacionados con Epigenética o Plasticidad) |
|---|---|---|---|---|
| Curcumina | Fenólico | Cúrcuma | Alzheimer, Parkinson, Depresión, Ictus, Esclerosis Múltiple, Rett, Huntington | Aumenta BDNF, modula actividad HDACs y DNMTs, remodelación de cromatina. |
| Epigalocatequina-3-galato (EGCG) | Flavonol | Té verde | Alzheimer, Parkinson, Depresión, Ictus, Esclerosis Múltiple, Rett, Huntington | Reduce estrés oxidativo (relacionado con mecanismos epigenéticos), aumenta neurogénesis hipocampal. |
| Resveratrol | Polifenol | Uvas, cacahuates | Alzheimer, Parkinson, Depresión, Ictus, Esclerosis Múltiple, Rett, Huntington | Induce activación de SIRT1 (una deacetilasa de histonas), afecta vías de señalización relacionadas con plasticidad. |
| Quercetina | Flavonol | Uvas, manzanas, bayas | Alzheimer, Parkinson, Depresión, Ictus, Esclerosis Múltiple, Rett, Huntington | Aumenta BDNF, aumenta proliferación de células madre neurales vía vías de señalización. |
Si bien estos estudios son prometedores, se necesita más investigación para establecer claramente el vínculo epigenético específico de estos compuestos y su impacto en la neuroplasticidad en el contexto de las enfermedades.
Preguntas Frecuentes sobre Epigenética y Neurociencia
¿Qué enfermedades neurológicas están relacionadas con la epigenética?
Una amplia gama de trastornos neurológicos y psiquiátricos tienen componentes epigenéticos. Estos incluyen enfermedades neurodegenerativas como el Alzheimer, Parkinson y Huntington, trastornos psiquiátricos como la depresión, TEPT, trastorno bipolar, esquizofrenia y adicción, así como trastornos del neurodesarrollo como el Síndrome de Rett y los trastornos del espectro autista. Las disfunciones epigenéticas contribuyen a su etiología y progresión.
¿Es la epigenética lo mismo que la neuroplasticidad?
No, no son lo mismo. La neuroplasticidad es la capacidad del cerebro para cambiar y reorganizarse (sus estructuras y funciones) en respuesta a la experiencia. La epigenética se refiere a los mecanismos moleculares que regulan la expresión génica sin cambiar la secuencia del ADN. La epigenética es uno de los mecanismos fundamentales que subyacen, impulsan y permiten la neuroplasticidad. Es decir, la epigenética es una herramienta que el cerebro utiliza para lograr su plasticidad.
¿Qué sugiere la teoría epigenética del desarrollo neuronal?
Sugiere que los mecanismos epigenéticos (como la metilación del ADN, las modificaciones de histonas y los microARNs) son esenciales para orquestar el desarrollo preciso del cerebro, desde la formación de las capas corticales embrionarias hasta la generación continua de neuronas en la edad adulta. Estos mecanismos regulan cuándo y dónde se expresan los genes clave, dirigiendo la diferenciación celular, la migración neuronal y la formación de sinapsis. La disrupción de estos procesos epigenéticos durante el desarrollo puede tener consecuencias duraderas y contribuir a trastornos neurodesarrollales.
¿Se pueden tratar las enfermedades neurológicas con terapias epigenéticas?
Existe un gran potencial. Las terapias dirigidas a las enzimas y procesos epigenéticos (como inhibidores de HDAC, inhibidores de DNMT y terapias basadas en microARNs) están siendo investigadas como tratamientos para normalizar la expresión génica aberrante que causa enfermedades. Aunque los desafíos en la especificidad y la entrega de fármacos persisten, los estudios preclínicos y algunos ensayos clínicos tempranos son prometedores, ofreciendo nuevas vías para el tratamiento de trastornos como el Alzheimer, Parkinson, Huntington y diversos trastornos psiquiátricos.
Conclusión
La epigenética ha pasado de ser un concepto de nicho a una fuerza central en la investigación neurocientífica. Nos muestra que el cerebro es un órgano increíblemente adaptable, cuya función y disfunción están intrínsecamente ligadas a cómo nuestro entorno y experiencias de vida interactúan con nuestro genoma a nivel molecular. Los mecanismos epigenéticos no solo son cruciales para el desarrollo y la plasticidad cerebral a lo largo de la vida, sino que su desregulación es un factor clave en la patogénesis de una vasta gama de enfermedades neurológicas y psiquiátricas.
La promesa de la epigenética para el futuro de la atención médica es inmensa. Desde la identificación de biomarcadores para el diagnóstico temprano y personalizado, hasta el desarrollo de nuevas terapias dirigidas a corregir las marcas epigenéticas aberrantes, e incluso estrategias de prevención basadas en la modificación del estilo de vida y las exposiciones ambientales, la neuroepigenética está abriendo caminos sin precedentes para comprender, tratar y potencialmente prevenir los trastornos cerebrales. A medida que nuestra comprensión de este campo dinámico continúa creciendo, también lo hace la esperanza de mejorar la vida de millones de personas afectadas por estas desafiantes condiciones.
Si quieres conocer otros artículos parecidos a Epigenética: La Nueva Frontera Cerebral puedes visitar la categoría Neurociencia.