La regeneración neurológica es un campo de estudio crucial en la neurociencia que busca comprender y promover la reparación de las células nerviosas dañadas o perdidas. A diferencia de otros tejidos del cuerpo que pueden regenerarse con facilidad, el sistema nervioso, especialmente el central, presenta desafíos significativos para la recuperación completa tras una lesión. Sin embargo, la investigación en este ámbito está abriendo nuevas vías para restaurar la función y mejorar la calidad de vida de los pacientes afectados por traumas, enfermedades neurodegenerativas y otras afecciones neurológicas.
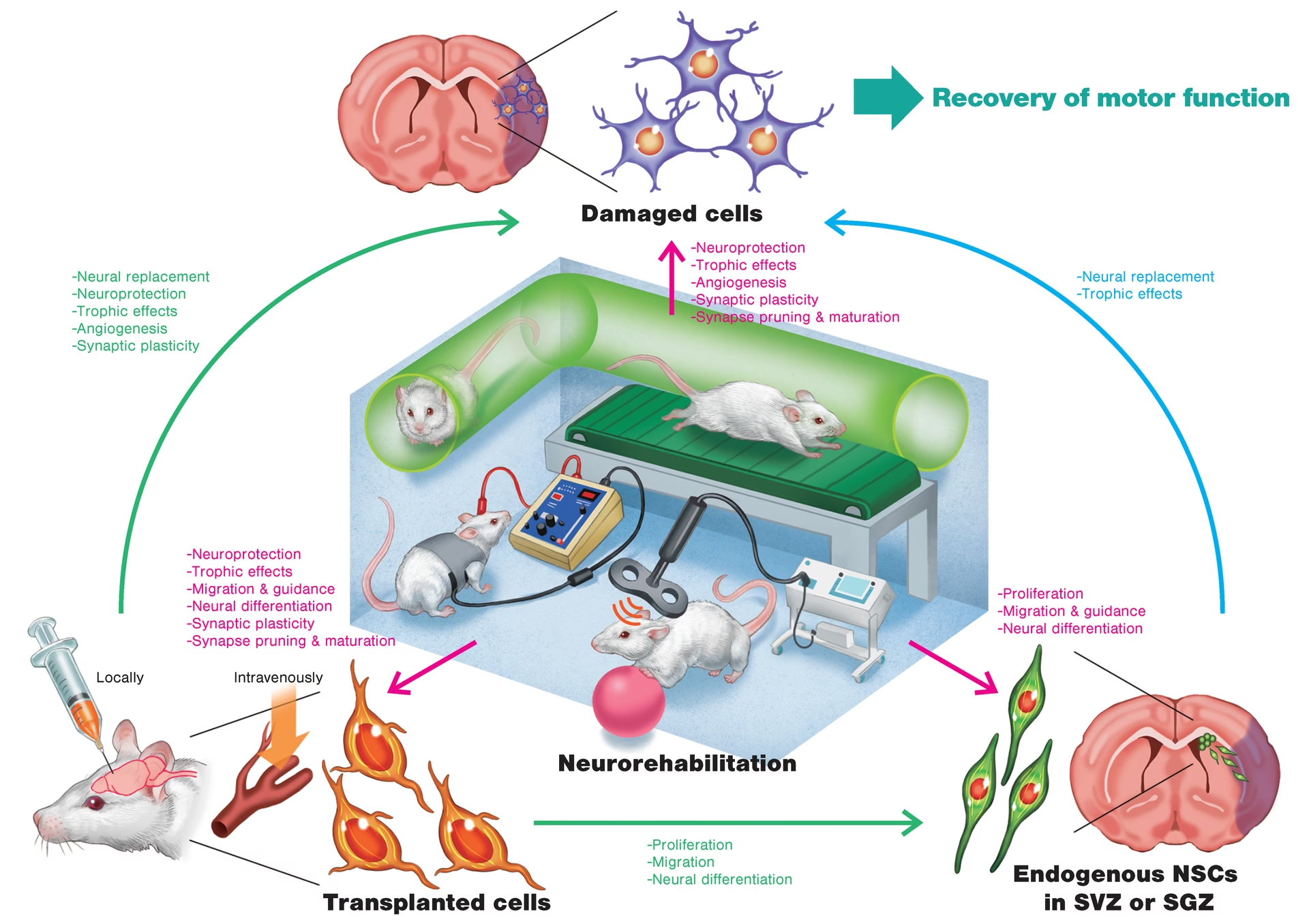
- La Notoria Capacidad de Regeneración del Sistema Nervioso Periférico (SNP)
- Los Grandes Obstáculos en la Regeneración del Sistema Nervioso Central (SNC)
- Comparación Clave: Regeneración en SNP vs. SNC
- Terapias Regenerativas: Explorando Nuevas Vías para la Reparación Neurológica y el Dolor
- Preguntas Frecuentes sobre Regeneración Neurológica
- ¿Puede el cerebro o la médula espinal regenerarse después de una lesión?
- ¿Qué tan rápido crecen los nervios?
- ¿Qué son las cicatrices gliales y por qué impiden la regeneración?
- ¿Qué tipos de terapias regenerativas se están explorando para problemas neurológicos o dolor asociado?
- ¿Son seguras las terapias regenerativas como el PRP o las células madre?
- ¿La viscosuplementación y la proloterapia regeneran nervios?
La Notoria Capacidad de Regeneración del Sistema Nervioso Periférico (SNP)
Cuando un nervio periférico sufre una lesión, por ejemplo, un corte, el cuerpo pone en marcha un proceso de reparación sorprendentemente efectivo. La regeneración en el sistema nervioso periférico ocurre en un grado significativo. Tras el daño al axón (la prolongación larga de la neurona que transmite señales), las neuronas periféricas activan una variedad de vías de señalización que activan genes promotores del crecimiento. Esto lleva a la reformación de un cono de crecimiento funcional, una estructura especializada en el extremo del axón que guía su elongación.
El crecimiento de estos axones también está influenciado por factores quimiotácticos secretados por las Células de Schwann, que son las células gliales (de soporte) del SNP. Inmediatamente después de la lesión, hay una migración de fagocitos, Células de Schwann y macrófagos al sitio lesionado. Su función principal es limpiar los restos celulares y el tejido dañado, que de otra manera inhibirían la regeneración. Este proceso de limpieza es crucial para preparar el terreno para el crecimiento del nuevo axón.
Cuando un axón nervioso es seccionado, el extremo que permanece unido al cuerpo celular se llama segmento proximal, y el otro extremo es el segmento distal. Después de la lesión, el extremo proximal se hincha y experimenta cierta degeneración retrógrada. Sin embargo, una vez que se eliminan los restos, comienza a brotar axones y se detecta la presencia de conos de crecimiento. Los axones proximales pueden volver a crecer siempre que el cuerpo celular esté intacto y hayan hecho contacto con las Células de Schwann dentro del endoneuro (también conocido como tubo o canal endoneurial). El endoneuro es una vaina de tejido conectivo que rodea cada fibra nerviosa. En las etapas posteriores de la regeneración, este tubo endoneurial restante actúa como un conducto que guía el crecimiento del axón de regreso hacia sus dianas correctas.
Mientras tanto, el segmento distal experimenta lo que se conoce como degeneración Walleriana, que ocurre a las pocas horas de la lesión. Los axones y la mielina (la capa aislante que recubre los axones) degeneran rápidamente, pero la estructura del endoneuro permanece. Durante la degeneración Walleriana, las Células de Schwann proliferan y crecen en columnas ordenadas a lo largo del tubo endoneurial, formando una estructura llamada Banda de Büngner. Esta banda protege y preserva el canal endoneurial, facilitando la guía del axón en crecimiento. Además, tanto los macrófagos como las Células de Schwann liberan factores neurotróficos (sustancias que promueven la supervivencia y el crecimiento neuronal) que mejoran el rebrote. Las tasas de crecimiento de los axones humanos en el SNP pueden alcanzar los 2 mm por día en nervios pequeños y hasta 5 mm por día en nervios más grandes, un testimonio de la notable capacidad regenerativa de este sistema.
Los Grandes Obstáculos en la Regeneración del Sistema Nervioso Central (SNC)
A diferencia del sistema nervioso periférico, la lesión en el SNC (que incluye el cerebro y la médula espinal) no suele ir seguida de una regeneración extensa. Esta limitación se debe principalmente a las influencias inhibitorias del entorno glial y extracelular. El entorno hostil, que no permite el crecimiento, es creado en parte por la migración de inhibidores asociados a la mielina, astrocitos, oligodendrocitos (las células gliales que producen mielina en el SNC), precursores de oligodendrocitos y microglía (las células inmunes residentes del SNC).
El entorno dentro del SNC, especialmente después de un trauma, contrarresta activamente la reparación de la mielina y las neuronas. A diferencia del SNP, los factores de crecimiento no se expresan o re-expresan de manera efectiva. Por ejemplo, la matriz extracelular del SNC carece de lamininas, que son importantes para el crecimiento axonal. Además, las cicatrices gliales se forman rápidamente. Estas cicatrices son creadas principalmente por astrocitos reactivos y otras células gliales que proliferan en el sitio de la lesión. Lo que es peor, estas células gliales en la cicatriz producen factores que inhiben activamente la remielinización y la reparación axonal, como NOGO y NI-35, que son potentes inhibidores del crecimiento axonal.
Otro factor que contribuye a la falta de regeneración en el SNC es que los propios axones centrales parecen perder parte de su potencial de crecimiento con la edad, lo que se relaciona con una disminución en la expresión de proteínas como GAP43, que son importantes para el crecimiento axonal. Además, la degeneración del segmento distal de un axón lesionado en el SNC es mucho más lenta que la degeneración Walleriana rápida que ocurre en el SNP. Esta degeneración más lenta contribuye al entorno inhibitorio porque los restos de mielina y axones, que contienen inhibidores, no se eliminan tan rápidamente como en el SNP.
Todos estos factores (la presencia de inhibidores, la falta de factores de crecimiento, la formación de la cicatriz glial y la degeneración lenta de los restos) contribuyen a la formación de la cicatriz glial. Los axones simplemente no pueden crecer a través de esta barrera inhibitoria. Aunque el segmento proximal intenta regenerarse después de una lesión, su crecimiento se ve gravemente obstaculizado por este entorno hostil. Es importante destacar que se ha demostrado que los axones del SNC pueden volver a crecer en entornos permisivos, lo que sugiere que el problema principal para la regeneración axonal en el SNC es superar o eliminar el sitio de la lesión inhibitoria. Además, la morfología y las propiedades funcionales de las neuronas del SNC son extremadamente complejas, lo que significa que una neurona funcionalmente idéntica no puede ser simplemente reemplazada por una de otro tipo (lo que se conoce como la ley de Llinás), haciendo la recuperación funcional aún más desafiante.
Comparación Clave: Regeneración en SNP vs. SNC
Para resumir las diferencias fundamentales en la capacidad regenerativa de ambos sistemas, podemos observar la siguiente tabla comparativa:
| Característica | Sistema Nervioso Periférico (SNP) | Sistema Nervioso Central (SNC) |
|---|---|---|
| Capacidad Regenerativa | Significativa | Limitada / Mínima |
| Degeneración Distal | Rápida (Degeneración Walleriana) | Lenta |
| Eliminación de Restos | Rápida y eficiente (Macrófagos, Células de Schwann) | Lenta e incompleta |
| Entorno Glial | Permisivo, soporta el crecimiento (Células de Schwann, Endoneuro) | Inhibitorio (Astrocitos, Oligodendrocitos, Microglía) |
| Formación de Cicatriz | Mínima o ausente | Prominente (Cicatriz Glial) |
| Factores de Crecimiento | Liberados y re-expresados (Neurotróficos) | Ausentes o no re-expresados eficazmente |
| Estructuras de Guía | Endoneuro, Banda de Büngner | Ausentes |
| Inhibidores del Crecimiento | Baja presencia | Alta presencia (NOGO, NI-35, etc.) |
Terapias Regenerativas: Explorando Nuevas Vías para la Reparación Neurológica y el Dolor
La medicina regenerativa, un campo más amplio, busca restaurar la función de tejidos u órganos enfermos mediante la entrega de células o productos celulares. Aunque gran parte de la investigación y aplicación actual se centra en tejidos musculoesqueléticos, la neurociencia regenerativa se beneficia de los avances en estas terapias, buscando aplicarlas para superar los desafíos del SNC y mejorar la recuperación del SNP.
Dentro de la medicina regenerativa, existen diversas vías terapéuticas. Aunque el texto proporcionado las describe principalmente en el contexto del manejo del dolor crónico (a menudo relacionado con problemas articulares o musculares, pero con componentes neurológicos en el dolor), algunas tienen un potencial directo o indirecto para la reparación neurológica:
- Viscosuplementación: Implica la inyección de ácido hialurónico en las articulaciones. Si bien se enfoca en restaurar la lubricación y amortiguación en la osteoartritis, no tiene un efecto directo en la regeneración nerviosa.
- Proloterapia: Involucra la inyección de una solución (a menudo dextrosa hipertónica) para inducir una respuesta inflamatoria controlada que promueva la curación de tejidos conectivos como ligamentos y tendones. Aunque se centra en la estabilidad articular, al mejorar el entorno tisular, podría tener efectos indirectos en nervios circundantes, pero no es una terapia de regeneración nerviosa directa.
- Plasma Rico en Plaquetas (PRP): Se obtiene de la sangre del propio paciente y contiene una alta concentración de plaquetas. Las plaquetas liberan factores de crecimiento y citoquinas que estimulan la cicatrización, tienen propiedades analgésicas y antiinflamatorias. El PRP se utiliza para tratar lesiones musculares, tendinosas y articulares, y también se está explorando para trastornos de la columna vertebral. Dado que las plaquetas contienen más de 300 factores de crecimiento, la entrega de PRP a un sitio de lesión nerviosa podría teóricamente proporcionar un entorno más favorable para la supervivencia y el crecimiento axonal, aunque su aplicación directa en la reparación nerviosa requiere más investigación. El texto menciona su uso potencial en dolor de espalda relacionado con la degeneración discal y la osteoartritis facetaria, condiciones que implican el sistema nervioso.
- Células Madre Mesenquimales (CMM): Estas son células madre multipotentes que pueden diferenciarse en varios tipos de células, como osteoblastos (hueso), condroblastos (cartílago) y adipocitos (grasa). Se pueden obtener de varias fuentes (médula ósea, tejido adiposo, cordón umbilical, etc.). Las CMM no solo tienen la capacidad de diferenciarse, sino que también secretan una gran cantidad de factores tróficos y inmunomoduladores que pueden promover la reparación tisular, reducir la inflamación y proteger las células existentes. Su uso se está explorando activamente en neurología regenerativa. Si bien el texto se centra en su uso para tratar problemas musculoesqueléticos como la osteonecrosis o la tendinopatía, las CMM tienen un enorme potencial para la reparación del SNC y SNP. Pueden potencialmente reemplazar neuronas perdidas (aunque esto es más complejo), pero más prometedoramente, pueden crear un entorno más favorable para la regeneración axonal al liberar factores neurotróficos, reducir la cicatrización glial y modular la respuesta inflamatoria. El texto menciona su uso para trastornos musculoesqueléticos del hombro, rodilla, tobillo y columna, lo que subraya su potencial en áreas anatómicas cercanas al sistema nervioso.
La investigación en regeneración neurológica se enfoca en encontrar formas de replicar las condiciones permisivas del SNP en el SNC, utilizando enfoques como la inhibición de los factores inhibitorios (como NOGO), la entrega de factores de crecimiento, el uso de andamios biomateriales para guiar el crecimiento axonal y, de manera muy importante, el uso de terapias celulares como las células madre para crear un entorno más propicio para la reparación.
Preguntas Frecuentes sobre Regeneración Neurológica
¿Puede el cerebro o la médula espinal regenerarse después de una lesión?
La regeneración espontánea en el sistema nervioso central (SNC), que incluye el cerebro y la médula espinal, es muy limitada en comparación con el sistema nervioso periférico. Esto se debe a un entorno interno que inhibe el crecimiento axonal y a la formación de cicatrices gliales. Sin embargo, la investigación activa busca desarrollar terapias que puedan promover la regeneración en el SNC.
¿Qué tan rápido crecen los nervios?
En el sistema nervioso periférico, los axones lesionados pueden regenerarse a una velocidad de aproximadamente 2 mm por día en nervios pequeños y hasta 5 mm por día en nervios grandes, siempre que el cuerpo celular esté intacto y el entorno sea favorable.
¿Qué son las cicatrices gliales y por qué impiden la regeneración?
Las cicatrices gliales son formaciones de tejido que aparecen en el sitio de una lesión en el SNC. Están compuestas principalmente por astrocitos reactivos y otras células gliales. Estas cicatrices actúan como una barrera física y química, liberando moléculas que inhiben el crecimiento de los axones, lo que impide que las neuronas lesionadas se reconecten.
¿Qué tipos de terapias regenerativas se están explorando para problemas neurológicos o dolor asociado?
Se están investigando diversas terapias. Aunque muchas se aplican actualmente a lesiones musculoesqueléticas, su potencial se extiende a la neurología. Incluyen el uso de Plasma Rico en Plaquetas (PRP), que aporta factores de crecimiento, y especialmente las Células Madre Mesenquimales (CMM), que pueden secretar factores neurotróficos, reducir la inflamación y modular el entorno de la lesión. La investigación también se centra en superar los inhibidores del crecimiento y utilizar biomateriales para guiar la regeneración.
¿Son seguras las terapias regenerativas como el PRP o las células madre?
Generalmente, estas terapias, especialmente cuando usan material autólogo (del propio paciente), son bien toleradas. Los efectos secundarios más comunes son dolor o hinchazón en el sitio de la inyección. Las complicaciones graves son raras, pero como con cualquier procedimiento médico, existen riesgos que deben evaluarse individualmente. Las contraindicaciones varían según la terapia específica, incluyendo infecciones activas, problemas de coagulación o ciertos tipos de cáncer.
¿La viscosuplementación y la proloterapia regeneran nervios?
Según la información proporcionada, la viscosuplementación y la proloterapia se centran principalmente en mejorar el entorno articular y del tejido conectivo (ligamentos, tendones) para tratar el dolor musculoesquelético. No están diseñadas para promover la regeneración directa de los nervios.
En conclusión, mientras que el sistema nervioso periférico posee una notable capacidad intrínseca para repararse, el sistema nervioso central enfrenta barreras significativas para la regeneración. La neurociencia regenerativa, apoyada por avances en la medicina regenerativa más amplia, continúa explorando y desarrollando estrategias prometedoras para superar estos obstáculos y restaurar la función en pacientes con daño neurológico, ofreciendo esperanza para el futuro.
Si quieres conocer otros artículos parecidos a Regeneración Neurológica: Reparando el Cerebro puedes visitar la categoría Neurociencia.
