El monofosfato de guanosina 3’,5’-cíclico, conocido comúnmente como GMP cíclico o cGMP, es una molécula de señalización intracelular fundamental, clasificada como un segundo mensajero. Este compuesto desempeña un papel crucial en la modulación de una amplia gama de efectos celulares y fisiológicos, incluyendo procesos tan diversos como la vasodilatación, la fototransducción en la retina, la homeostasis del calcio y, de manera muy relevante para este artículo, la neurotransmisión. El cGMP ejerce su influencia principalmente a través de la activación y alteración de canales iónicos específicos, su asociación con proteínas quinasas dependientes de cGMP (PKG) y su interacción con enzimas llamadas fosfodiesterasas (PDEs). Comprender la compleja red de señalización del cGMP es esencial para desentrañar los mecanismos subyacentes de numerosas funciones biológicas y patologías.
- Fundamentos y Síntesis del cGMP
- Mecanismos de Acción: Canales Iónicos, Quinasas y Fosfodiesterasas
- Funciones Diversas del cGMP en el Organismo
- El cGMP en el Sistema Nervioso: Plasticidad y Más Allá
- El Rol del cGMP en la Visión: Fototransducción
- Importancia Clínica y Dianas Terapéuticas
- Preguntas Frecuentes sobre el cGMP
Fundamentos y Síntesis del cGMP
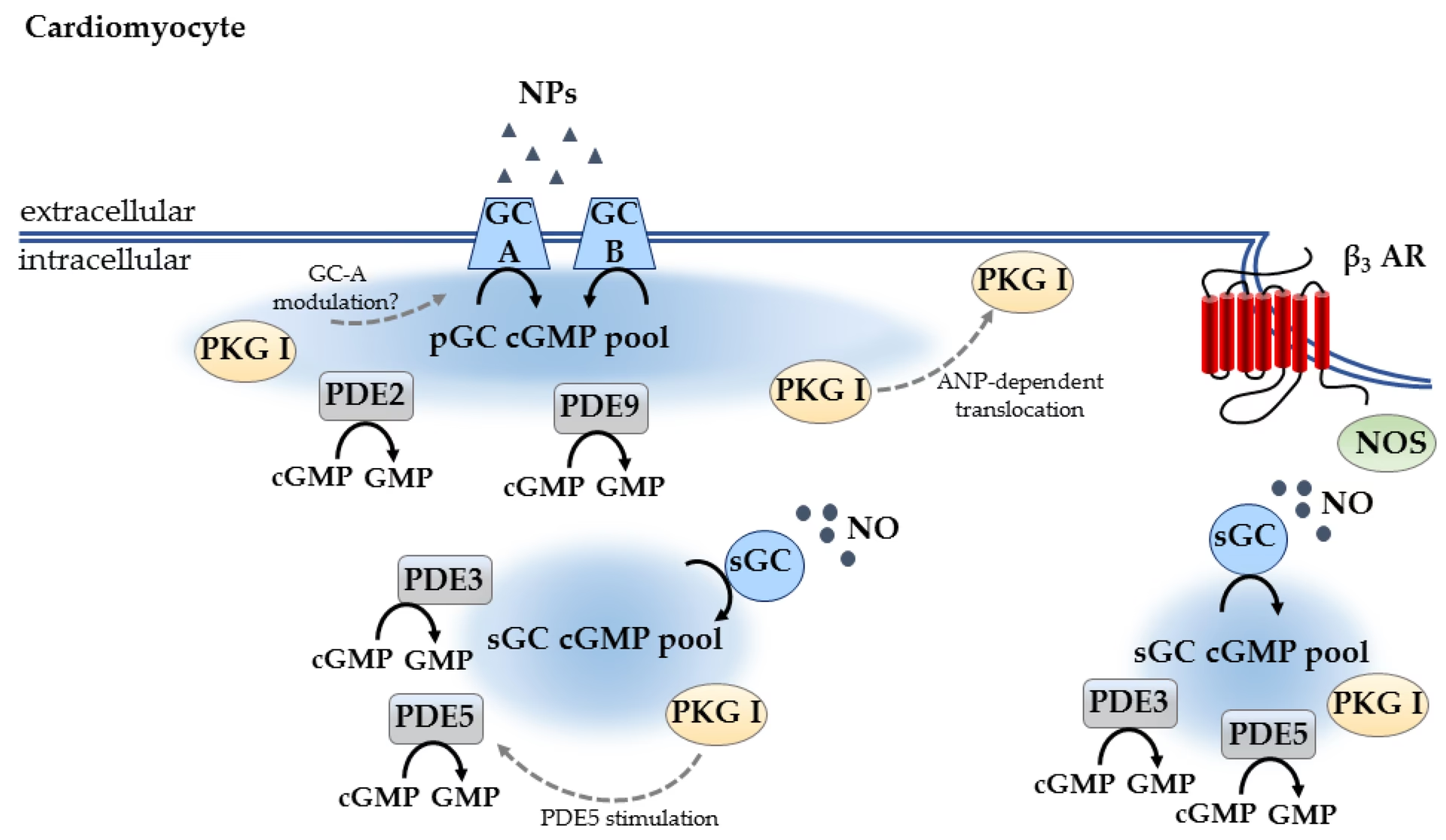
La síntesis de cGMP es catalizada por una enzima liasa conocida como guanilato ciclasa (GC). Existen dos formas principales de esta enzima: la guanilato ciclasa soluble (sGC) y la guanilato ciclasa particulada (pGC), asociada a la membrana. La sGC es notable por ser activada por el óxido nítrico (NO), una molécula gaseosa. De hecho, el cGMP es el único segundo mensajero conocido que es activado por un gas. El NO se une a la sGC y aumenta enormemente su actividad catalítica, potenciando la conversión de guanosina-5'-trifosfato (GTP) en cGMP. Este mecanismo es particularmente importante en el sistema cardiovascular y nervioso.
Por otro lado, la pGC es típicamente activada por la unión de péptidos natriuréticos (PN), como el péptido natriurético auricular (ANP), a receptores específicos en la membrana celular. Estos péptidos activan la pGC, que también convierte GTP en cGMP. La guanilato ciclasa también puede interactuar con la cascada de proteínas G, activada por bajos niveles de calcio, lo que lleva a la conversión de GTP en cGMP en respuesta a este ion. La regulación de los niveles de cGMP es un equilibrio delicado entre su síntesis por las GC y su degradación por las fosfodiesterasas (PDEs), que lo hidrolizan a 5'-GMP, finalizando así su actividad.
Mecanismos de Acción: Canales Iónicos, Quinasas y Fosfodiesterasas
El cGMP ejerce sus efectos biológicos a través de tres vías principales:
- Canales Iónicos Activados por Nucleótidos Cíclicos (CNG): Estos canales se activan directamente por la unión de nucleótidos cíclicos. Los canales CNG son canales catiónicos no selectivos que principalmente promueven la entrada de iones sodio y calcio. Han sido mejor caracterizados en los fotorreceptores retinianos, pero también se encuentran en neuronas sensoriales olfativas y la glándula pineal. Los canales CNG de bastones y conos son selectivos para cGMP, mientras que otros pueden ser activados por cAMP. Los canales HCN (Hyperpolarization-activated and Cyclic Nucleotide-gated), un subtipo de canales CNG, también pueden ser activados por cGMP, aunque están principalmente regulados por cAMP. Estos canales a menudo actúan como marcapasos en el corazón y el cerebro, estableciendo actividad rítmica coordinada.
- Proteínas Quinasas Dependientes de cGMP (PKG): Son enzimas serina/treonina proteína quinasa activadas principalmente por la unión de cGMP. Se han identificado dos subclases principales, PKGI y PKGII, que difieren en su distribución tisular y sus dianas de fosforilación. La activación de PKG por cGMP es un proceso donde la unión del cGMP a las subunidades reguladoras de la PKG induce un cambio conformacional que activa las subunidades catalíticas, permitiéndoles fosforilar proteínas sustrato. A diferencia de otras quinasas como la PKA, las subunidades de PKG generalmente no se disocian al activarse. El cGMP también puede activar la proteína quinasa A (PKA), aunque es un agonista más débil que el cAMP.
- Interacción con Fosfodiesterasas (PDEs): La superfamilia de PDEs consta de 11 miembros, diferenciados por su especificidad de sustrato (cAMP/cGMP), cinética, activación e inhibición. El cGMP es el único sustrato de las PDEs 5, 6 y 9, y es un sustrato dual (junto con cAMP) de las PDEs 1, 2, 3, 10 y 11. Esta dualidad permite que el cGMP influya en los niveles de cAMP al unirse a ciertas PDEs (como la PDE3), bloqueando la degradación de cAMP y elevando sus niveles, lo que media efectos posteriores. Las PDEs son cruciales para finalizar la señalización del cGMP y también son dianas terapéuticas importantes.
Funciones Diversas del cGMP en el Organismo
El cGMP participa en una amplia gama de procesos fisiológicos en distintos tipos celulares. La regulación al alza del cGMP intracelular por el óxido nítrico (NO) se ha relacionado con numerosos efectos, mediado principalmente por PKGI. Estos incluyen la relajación del músculo liso gastrointestinal y vascular, la inhibición de la agregación plaquetaria, la mejora de la función cognitiva y la cardioprotección.
PKGI modula la función del músculo liso en el intestino y la vasculatura; ratones sin esta proteína mostraron una motilidad intestinal marcadamente ralentizada y presión arterial elevada (hipotetizado por falta de respuesta al NO). Además, PKGI probablemente modula la plasticidad neuronal, la función eréctil, la función del tracto urinario inferior y la permeabilidad endotelial. Otras funciones mediadas por PKG pueden incluir la disminución de los niveles intracelulares de calcio, la regulación del metabolismo óseo, la alteración de la absorción renal, la producción de melanocitos en respuesta a la radiación ultravioleta y la reducción de los niveles de cGMP a través de la activación de PDE.
La unión directa del cGMP a los canales CNG es necesaria para abrirlos y promover el flujo de corriente máxima. En fotorreceptores y neuronas olfativas, la amplificación de la estimulación lumínica u olfativa por el cGMP contribuye a la alta discriminación visual y olfativa en humanos. El cGMP y los canales CNG también están involucrados en la homeostasis del calcio; bajos niveles intracelulares de calcio pueden activar proteínas activadoras de GC, lo que lleva a un aumento de cGMP y a la entrada de calcio a través de los canales CNG abiertos.
La superfamilia de PDEs se expresa heterogéneamente en todo el cuerpo. Las miembros con afinidad por cGMP tienen roles específicos:
| PDE | Especificidad | Ubicación/Rol Principal |
|---|---|---|
| PDE1 | Dual (cAMP/cGMP) | Neuronas, función cerebral, modulación sináptica |
| PDE2 | Dual (cAMP/cGMP) | Cambios y función vascular |
| PDE3 | Dual (cAMP/cGMP) | Meiosis en ovocitos, sensibilidad a la insulina, metabolismo |
| PDE5 | cGMP específica | Tono vasomotor, presión arterial, función eréctil |
| PDE6 | cGMP específica | Retina, transducción visual |
| PDE9 | cGMP específica | Cerebro (ampliamente expresada), comportamiento, aprendizaje |
| PDE10 | Dual (cAMP/cGMP) | Cerebro, enfermedades neurodegenerativas (Huntington) |
| PDE11 | Dual (cAMP/cGMP) | Próstata, testículos, función reproductiva |
La homeostasis metabólica es otra área potencial de interés para la investigación del cGMP. Generalmente, el cGMP induce cambios positivos en el gasto energético. En el tejido adiposo marrón, donde el NO induce cGMP, aumenta la cantidad, tamaño y actividad de las mitocondrias. El cGMP también puede inducir el pardeamiento de células adiposas blancas y mejorar la sensibilidad a la insulina. Además, puede regular la liberación de glucagón en el páncreas, ejercer efectos antioxidantes y antiinflamatorios en el hígado, y regular la ingesta de alimentos y agua a través de interacciones hipotalámicas.
El cGMP en el Sistema Nervioso: Plasticidad y Más Allá
El cGMP juega un papel significativo en la función neurológica, especialmente en lo que respecta a la plasticidad sináptica, la formación y la recuperación de la memoria. En las sinapsis del hipocampo, la estimulación de los receptores NMDA postsinápticos puede llevar a la liberación de NO en la hendidura sináptica. Este NO se une a la sGC en la neurona presináptica, lo que resulta en la producción de cGMP.
El cGMP parece aumentar la actividad de PKGI en la neurona presináptica, lo que potencia la potenciación a largo plazo (LTP) de la sinapsis. Esto es crucial para el aprendizaje y la memoria. Apoyando este hallazgo, la inyección directa de cGMP en neuronas presinápticas mejora la LTP, mientras que la inyección de un inhibidor de PKG la bloquea. En general, el cGMP puede ayudar a facilitar tanto la formación como la recuperación de la memoria a través de sus efectos sobre la LTP en el hipocampo.
La actividad del cGMP también se ha relacionado con cambios sinápticos en otras regiones cerebrales. En la amígdala, la actividad mediada por cGMP puede contribuir a la LTP asociada a la formación de la memoria del miedo. Por el contrario, en las células de Purkinje del cerebelo, el cGMP ha sido implicado en la depresión a largo plazo (LTD) sináptica, que subyace al aprendizaje motor. Menos comprendidos son los efectos del cGMP en otras regiones cerebrales. El cGMP puede mediar la cognición, la psicosis, la depresión y la neurodegeneración, probablemente a través de la actividad de las PDEs.
A través de modulaciones presinápticas y postsinápticas y efectos sobre la expresión génica neuronal, el cGMP potencialmente modula múltiples funciones conductuales y de aprendizaje en el sistema nervioso central. La PDE1, presente principalmente en neuronas, media la función y actividad cerebral a través de la modulación sináptica. La PDE9, ampliamente expresada en el cerebro, puede modular el comportamiento y el aprendizaje. La PDE10 está asociada con la actividad cerebral y puede desempeñar un papel en enfermedades neurodegenerativas como la enfermedad de Huntington.

El Rol del cGMP en la Visión: Fototransducción
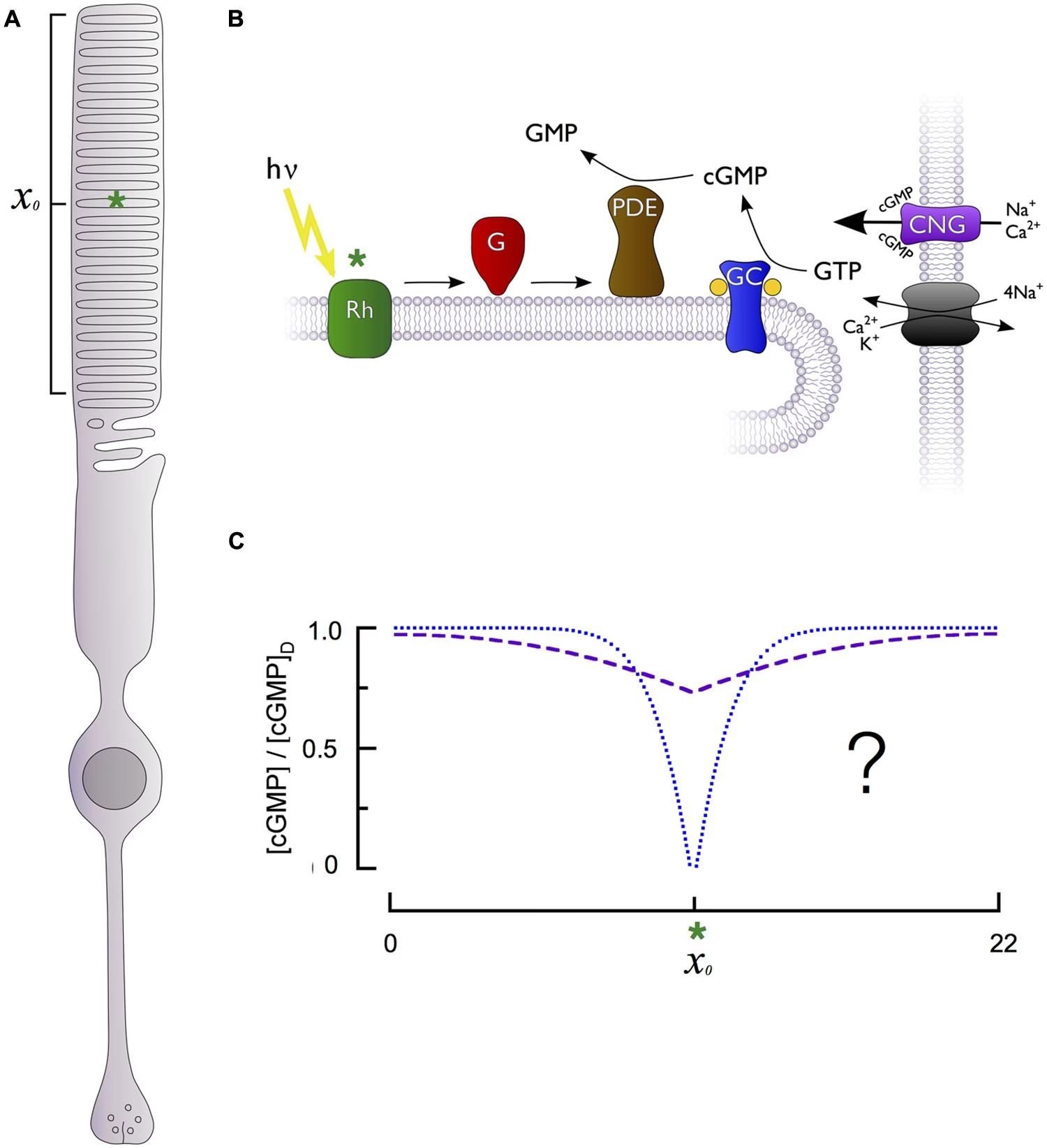
En el ojo, el cGMP desempeña un papel fundamental en el proceso de fototransducción, la conversión de la luz en señales eléctricas. En los fotorreceptores (bastones y conos) de la retina, el cGMP está presente en altas concentraciones en la oscuridad, manteniendo abiertos los canales catiónicos CNG en la membrana plasmática. Esto permite la entrada de iones sodio y calcio, manteniendo el fotorreceptor despolarizado en la oscuridad.
Cuando la luz incide en los pigmentos visuales (rodopsina en bastones, opsinas en conos), se desencadena una cascada metabólica que activa la enzima fosfodiesterasa (PDE) específica de cGMP, principalmente la PDE6 en los fotorreceptores. La PDE6 activada hidroliza rápidamente el cGMP a 5'-GMP. La disminución resultante en la concentración de cGMP intracelular provoca el cierre de los canales CNG. Este cierre reduce el flujo de iones positivos, lo que lleva a la hiperpolarización de la membrana del fotorreceptor. Este cambio en el potencial de membrana es la señal eléctrica que se transmite a las neuronas bipolares y otras células retinianas, iniciando el procesamiento de la información visual que finalmente llega al cerebro.
Estudios en ojos humanos con desprendimiento de retina han mostrado una disminución significativa en los niveles de cGMP tanto en el humor vítreo como en el fluido subretiniano en comparación con ojos control. El desprendimiento de retina separa los fotorreceptores del epitelio pigmentario de la retina, privándolos de oxígeno y glucosa. Se cree que la hipoxia e isquemia resultantes dañan los fotorreceptores y otras células retinianas, lo que lleva a una menor producción y liberación de cGMP por parte de estas células degeneradas. La disminución de los niveles de cGMP en el fluido subretiniano se correlacionó inversamente con la duración del desprendimiento, sugiriendo que cuanto más tiempo permanece desprendida la retina, menores son los niveles de cGMP, lo que podría reflejar el daño celular progresivo. No se detectó actividad de PDE en las muestras de fluido extracelular, lo que sugiere que la disminución de cGMP no se debe a un aumento de la degradación extracelular, sino probablemente a una menor producción intracelular.
Importancia Clínica y Dianas Terapéuticas
Dada su participación en tantos procesos fisiológicos, el cGMP y las enzimas que regulan sus niveles son importantes dianas terapéuticas. Estrategias farmacológicas comunes para aumentar los niveles de cGMP en células diana incluyen la estimulación de la guanilato ciclasa y la inhibición de las fosfodiesterasas (PDEs).
Los estimuladores de la sGC están siendo investigados como terapia potencial para tratar la hipertensión pulmonar, ya que pueden aumentar la síntesis de cGMP incluso en ausencia de NO. Los inhibidores de la PDE5, como el sildenafil (Viagra), son bien conocidos por su uso en el tratamiento de la disfunción eréctil, donde potencian el efecto vasodilatador del cGMP en el cuerpo cavernoso al inhibir la degradación de cGMP por la PDE5. Sin embargo, el sildenafil también se está estudiando por sus efectos cardioprotectores. La elevación del cGMP miocárdico se asocia con una mejora del tono vascular pulmonar y la función ventricular derecha en la insuficiencia cardíaca diastólica.

Las terapias dirigidas a los niveles de cGMP también han demostrado resultados prometedores para tratar el dolor visceral. En el síndrome del intestino irritable con estreñimiento (SII-E), el dolor y la incomodidad abdominal son factores significativos. Los agonistas de la guanilato ciclasa parecen reducir el dolor visceral al disminuir la hipersensibilidad de los nociceptores crónicamente estimulados y al elevar el cGMP extracelular en el colon.
A través de la activación de PKG1, la modulación de los niveles de cGMP podría ser un tratamiento efectivo para la enfermedad renal. Los inhibidores de la PDE5 han demostrado mejorar la función renal, específicamente en la inhibición de la fibrosis renal, contrarrestando la trombosis a través de la regulación de la agregación plaquetaria y con propiedades antitumorales promoviendo la apoptosis de células tumorales.
Aunque asociado con muchos resultados positivos, el aumento de los niveles de cGMP también puede tener un efecto citotóxico en algunas circunstancias. Los niveles elevados de cGMP se correlacionan con la degeneración retiniana acelerada en modelos de distrofia retiniana. La entrada incontrolada de calcio a través de canales CNG constitutivamente abiertos y la sobreactivación de PKGI pueden ser parcialmente responsables de la muerte celular retiniana.
Algunos medicamentos utilizados para tratar la hipertensión, como la hidralazina, el nitroprusiato y otros nitratos, actúan aumentando la actividad del cGMP, lo que lleva a la relajación del músculo liso vascular y la consiguiente vasodilatación.
Preguntas Frecuentes sobre el cGMP
- ¿Qué es un segundo mensajero? Es una molécula intracelular que transmite señales desde receptores en la superficie celular a dianas dentro de la célula, amplificando la señal inicial y coordinando las respuestas celulares. El cGMP es uno de ellos, junto con el cAMP, el calcio y el IP3.
- ¿Cómo se produce el cGMP? Es sintetizado por enzimas llamadas guanilato ciclasas (GC) a partir de la molécula GTP. Las GC pueden ser activadas por diversas señales, como el óxido nítrico (NO) o péptidos natriuréticos (PN).
- ¿Cómo se elimina el cGMP? Es degradado por enzimas llamadas fosfodiesterasas (PDEs), que lo convierten en 5'-GMP inactivo. Existen varios tipos de PDEs con diferentes especificidades y localizaciones.
- ¿Cuál es el papel del cGMP en el cerebro? El cGMP es crucial para la plasticidad sináptica, que es fundamental para el aprendizaje y la memoria. Participa en la potenciación a largo plazo (LTP) en el hipocampo y la amígdala, y en la depresión a largo plazo (LTD) en el cerebelo. También está involucrado en la función de neuronas olfativas y en la retina.
- ¿Cómo afecta el cGMP la visión? En los fotorreceptores, el cGMP mantiene abiertos los canales iónicos en la oscuridad. La luz activa una enzima (PDE6) que degrada el cGMP, cerrando los canales y generando una señal eléctrica (hiperpolarización) que inicia la visión.
- ¿Por qué el cGMP es importante en la medicina? El cGMP es una diana para varios medicamentos. Por ejemplo, los inhibidores de la PDE5 se usan para la disfunción eréctil y se investigan para enfermedades cardiovasculares. Otros fármacos que afectan la vía del cGMP se usan para la hipertensión y se estudian para el dolor y enfermedades renales.
En conclusión, el cGMP es una molécula señalizadora de notable versatilidad, con roles que abarcan desde la regulación vascular y metabólica hasta procesos neuronales complejos como la plasticidad sináptica, el aprendizaje y la memoria. Su participación en la fototransducción visual subraya su importancia en funciones sensoriales clave. La intrincada red de síntesis, degradación y acción del cGMP, mediada por GC, PKG y PDEs, lo convierte en un actor esencial en la fisiología celular y un objetivo prometedor para el desarrollo de terapias dirigidas a una amplia gama de condiciones, incluidas las que afectan al sistema nervioso.
Si quieres conocer otros artículos parecidos a cGMP: El Mensajero Molecular del Cerebro puedes visitar la categoría Neurociencia.
