El cerebro, el centro de mando de nuestro cuerpo, requiere un entorno excepcionalmente estable y protegido para funcionar correctamente. A diferencia de otros órganos, que interactúan más libremente con el torrente sanguíneo, el sistema nervioso central (SNC) posee un sofisticado mecanismo de defensa que regula estrictamente el paso de sustancias desde la sangre hacia su delicado tejido. Este guardián, conocido como la Barrera Hematoencefálica (BHE), es una membrana selectiva semipermeable que actúa como una interfaz crucial entre los vasos sanguíneos cerebrales y el intersticio del cerebro.

La BHE no es simplemente un filtro pasivo. Es una estructura dinámica y compleja compuesta por varios elementos celulares que trabajan en conjunto para mantener la homeostasis cerebral, proteger contra toxinas y patógenos, y asegurar el suministro adecuado de nutrientes. Su existencia es fundamental para la salud neuronal, y su disfunción está implicada en numerosas enfermedades neurológicas. Comprender la BHE es adentrarse en uno de los aspectos más fascinantes de la neurociencia.
- Estructura y Composición del Guardián Cerebral
- Funciones Vitales de la Barrera Hematoencefálica
- Excepciones a la Regla: Los Órganos Circumventriculares
- El Desarrollo de la Barrera Hematoencefálica: Un Proceso Complejo
- La BHE en la Enfermedad: Cuando el Guardián Fallo
- Cruzando la Barrera: Desafíos y Estrategias para la Administración de Fármacos
- Tabla Comparativa: Sustancias y su Capacidad de Cruce
- Preguntas Frecuentes sobre la Barrera Hematoencefálica
Estructura y Composición del Guardián Cerebral
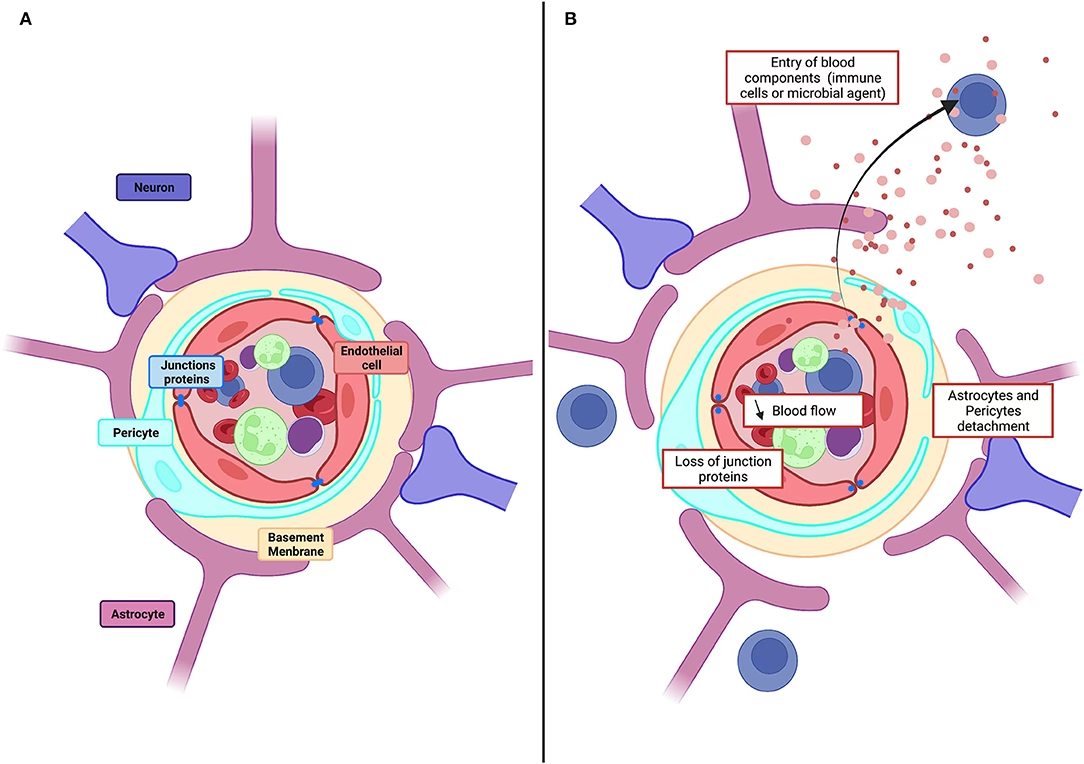
La Barrera Hematoencefálica está formada por una unidad neurovascular (UNV) altamente organizada. Los componentes principales incluyen:
- Células Endoteliales (CE): Forman el revestimiento interno de los capilares cerebrales. A diferencia de las células endoteliales en el resto del cuerpo, las CE de la BHE carecen de fenestraciones (poros) y están unidas por extensas uniones estrechas.
- Uniones Estrechas (UE): Son complejos proteicos localizados entre las células endoteliales adyacentes. Estas uniones actúan como una barrera física que sella el espacio paracelular, impidiendo el paso libre de la mayoría de las sustancias hidrofílicas (solubles en agua) y proteínas desde la sangre hacia el cerebro. Son el componente clave de la impermeabilidad de la BHE.
- Membrana Basal Capilar: Una capa de matriz extracelular que rodea los capilares.
- Pericitos (PC): Células embebidas dentro de la membrana basal. Los pericitos desempeñan un papel crucial en la integridad estructural de los microvasos, la angiogenesis y la inducción y mantenimiento de las uniones estrechas entre las células endoteliales.
- Pies Terminales de Astrocitos: Extensiones de células gliales llamadas astrocitos que envuelven casi por completo la pared de los vasos sanguíneos cerebrales. Aunque no forman parte directa de la barrera física en sí misma, los astrocitos y sus pies terminales son esenciales para la inducción y el mantenimiento de las propiedades de barrera de las células endoteliales, influyendo en la expresión de las proteínas de unión estrecha y los transportadores.
La interacción entre estos elementos celulares y la matriz extracelular circundante crea un entorno único que permite a la BHE llevar a cabo sus funciones vitales.
Funciones Vitales de la Barrera Hematoencefálica
La BHE desempeña múltiples funciones esenciales para la salud y el funcionamiento del SNC:
- Protección: Actúa como un escudo contra sustancias tóxicas, patógenos (bacterias, virus) y células inmunes circulantes que podrían dañar el tejido cerebral.
- Mantenimiento de la Homeostasis: Regula de manera precisa la composición del fluido intersticial cerebral, controlando las concentraciones de iones, neurotransmisores y otros metabolitos. Esta estabilidad es vital para la actividad neuronal adecuada.
- Transporte Selectivo: Permite el paso de nutrientes esenciales (como glucosa y aminoácidos) desde la sangre al cerebro a través de mecanismos de transporte específicos.
- Transporte de Eflujo: Bombea activamente sustancias no deseadas, incluyendo muchos fármacos hidrofóbicos, desde el cerebro de regreso al torrente sanguíneo, limitando su acumulación en el SNC.
- Regulación del Tráfico Celular: Bajo condiciones normales, limita la migración de células sanguíneas (como leucocitos) al cerebro.
Estas funciones se logran a través de cuatro mecanismos principales:
- Prevención de la difusión paracelular de compuestos hidrofílicos (gracias a las uniones estrechas).
- Mediación del transporte activo de nutrientes hacia el cerebro (a través de transportadores específicos).
- Activación del transporte de eflujo de moléculas hidrofóbicas y fármacos desde el cerebro hacia la sangre (mediante bombas de eflujo).
- Regulación de la migración transendotelial de células sanguíneas circulantes y patógenos.
Excepciones a la Regla: Los Órganos Circumventriculares
Aunque la BHE está presente en la mayor parte del cerebro, existen ciertas regiones que carecen de ella o tienen una barrera modificada. Estas áreas se conocen como Órganos Circumventriculares (OCV) y están localizadas alrededor del tercer y cuarto ventrículos cerebrales. Los vasos sanguíneos en los OCV tienen fenestraciones, lo que permite una mayor difusión de moléculas sanguíneas.
La ausencia de una BHE estricta en estas regiones es funcionalmente relevante, ya que permite que estas áreas detecten y respondan a señales químicas en la sangre, como hormonas y osmolalidad, que regulan funciones autonómicas y endocrinas. Los OCV incluyen:
- La glándula pineal
- La eminencia media
- El órgano subcomisural
- La neurohipófisis
- El órgano subfornical
- El área postrema
- El órgano vasculoso de la lámina terminalis
Estas regiones actúan como puntos de comunicación entre el torrente sanguíneo y el cerebro, permitiendo que el cerebro monitorice el estado del cuerpo y ajuste sus respuestas.
El Desarrollo de la Barrera Hematoencefálica: Un Proceso Complejo
La formación de la BHE durante el desarrollo embrionario es un proceso finamente orquestado que ocurre en varias etapas:
- Angiogénesis: Comienza temprano en la gestación con la invasión de vasos preexistentes, guiados por factores como el Factor de Crecimiento Endotelial Vascular (VEGF), en el neuroectodermo en desarrollo. Estos vasos tempranos ya muestran algunas propiedades de la BHE.
- Diferenciación: Señales anti-angiogénicas inducen la estructuración adecuada de la BHE. Es en esta etapa donde se reclutan astrocitos y pericitos a los vasos recién formados.
- Maduración: Se completa el sellado de las uniones estrechas y se establece la unidad neurovascular estabilizada. La integridad de la BHE se mantiene a través del contacto cercano entre células endoteliales, astrocitos y pericitos.
Moléculas señalizadoras como Wnt, GPR124 y Sonic Hedgehog (SHH) desempeñan roles críticos en la inducción y maduración de las propiedades de barrera. Alteraciones en este desarrollo pueden tener consecuencias a largo plazo, aumentando la susceptibilidad a enfermedades metabólicas y neurológicas.

La BHE en la Enfermedad: Cuando el Guardián Fallo
Bajo condiciones fisiológicas normales, la BHE es altamente impermeable. Sin embargo, en estados patológicos, su integridad puede verse comprometida, permitiendo el paso de sustancias que normalmente serían bloqueadas. La disfunción de la BHE es un factor clave o una consecuencia en muchas enfermedades neurológicas.
Mediadores de la Disrupción de la BHE
Diversos mediadores químicos liberados en condiciones patológicas pueden aumentar la permeabilidad de la BHE, incluyendo glutamato, aspartato, taurina, ATP, endotelina-1, óxido nítrico (NO), TNF-alfa e IL-beta (producidos por astrocitos), así como bradicinina, histamina, trombina, y radicales libres, entre otros.
Enfermedades Asociadas a la Disfunción de la BHE
- Tumores Cerebrales: Especialmente los gliomas de alto grado, secretan VEGF, que induce la ruptura de la arquitectura de la BHE existente y el crecimiento de vasos anormales y más permeables.
- Encefalopatía Hipóxico-Isquémica (EHI): La falta de flujo sanguíneo y oxígeno daña directamente las uniones estrechas endoteliales, aumentando la permeabilidad de la BHE y permitiendo la entrada de factores pro-inflamatorios.
- VIH: El virus o sus proteínas Tat y gp120 alteran la expresión de proteínas de unión estrecha y aumentan la migración de monocitos a través de la BHE, contribuyendo a disfunciones neurocognitivas.
- Esclerosis Múltiple (EM): Una enfermedad autoinmune caracterizada por la desmielinización. La disrupción de la BHE y la migración de leucocitos activados son eventos tempranos en la patogénesis de la EM.
- Enfermedad de Alzheimer (EA): La disfunción de la BHE contribuye a la acumulación de proteína A-beta en el cerebro al fallar su transporte de eflujo. Los cambios en los componentes estructurales de la BHE se asocian con un mayor riesgo de EA, creando un ciclo vicioso entre la patología A-beta y el daño de la BHE.
- Edema Vasogénico: Acumulación de fluido extracelular debido a la disrupción de la BHE y la extravasación de proteínas séricas. Esto aumenta el volumen cerebral y la presión intracraneal.
- Encefalopatía Hepática: La acumulación de toxinas como el amoníaco, debido a una enfermedad hepática, altera la expresión y función de los transportadores de eflujo en la BHE, permitiendo que estas toxinas entren al cerebro.
- Neuromielitis Óptica: Asociada a anticuerpos contra la acuaporina-4, una proteína presente en los pies terminales de astrocitos que rodean los vasos sanguíneos y contribuyen al mantenimiento de la BHE.
- Hemorragia Intraventricular (HIV) en Neonatos Prematuros: Causada por la inmadurez de la BHE en la matriz germinal, con uniones estrechas deficientes y escasa cobertura por pericitos y pies terminales de astrocitos.
- Estrés Oxidativo y Neuroinflamación: En condiciones como el accidente cerebrovascular isquémico o la Esclerosis Lateral Amiotrófica (ELA), el estrés oxidativo y la inflamación pueden dañar las uniones estrechas y otros componentes de la BHE.
- Epilepsia: La disfunción de la BHE puede alterar el equilibrio iónico y de neurotransmisores en el cerebro, contribuyendo a la hiperexcitabilidad neuronal y las convulsiones.
La investigación continúa desentrañando los complejos mecanismos por los cuales la BHE se ve afectada en estas y otras condiciones neurológicas.
Cruzando la Barrera: Desafíos y Estrategias para la Administración de Fármacos
La misma selectividad que hace que la BHE sea un guardián eficaz del cerebro representa un gran desafío para la administración de fármacos al SNC. Se estima que más del 90% de los fármacos de molécula pequeña y casi el 100% de las terapias más grandes no pueden cruzar la BHE.
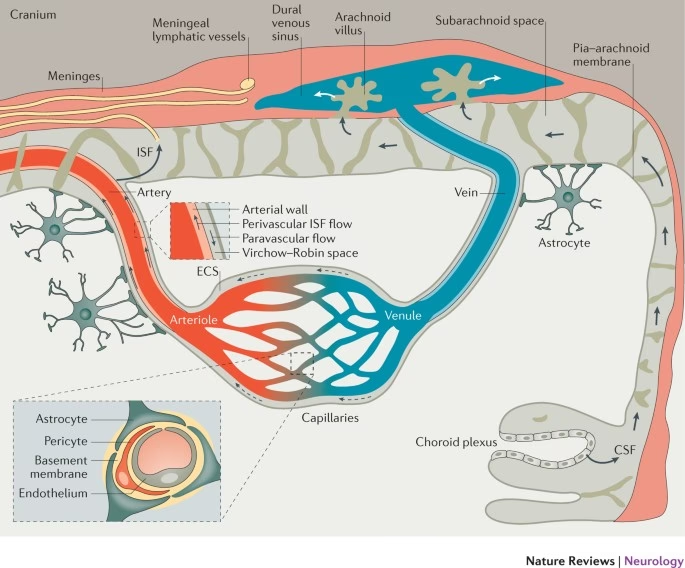
Generalmente, solo las moléculas lipofílicas (solubles en lípidos), con carga positiva y bajo peso molecular (menos de 400-600 Dalton) pueden cruzar la BHE por difusión pasiva. Para otras moléculas, existen rutas de transporte específicas:
- Difusión: Permite el paso de agua, iones pequeños (Na, K, Cl) y moléculas lipofílicas pequeñas (O2, CO2, anestésicos, barbitúricos, etanol, nicotina, cafeína).
- Transporte Mediado por Membrana: Incluye:
- Bombas de Eflujo (como la P-glicoproteína) que expulsan fármacos del cerebro.
- Transcitosis Mediada por Receptor (para insulina, leptina, IgG, transferrina).
- Transcitosis Mediada por Adsorción (para albúmina, histonas).
- Transporte Mediado por Portador (para glucosa, creatina, lactato, piruvato, aminoácidos grandes neutros).
Dada la dificultad para que los fármacos accedan al cerebro, se están desarrollando diversas estrategias para superar la BHE y lograr la entrega terapéutica en el SNC. Estas técnicas se clasifican generalmente en invasivas y no invasivas:
Técnicas Invasivas
Implican la administración directa o la interrupción temporal de la barrera:
- Infusiones o inyecciones intracerebroventriculares e intratecales: Entrega directa de fármacos en el líquido cefalorraquídeo (LCR).
- Disrupción transitoria de la BHE: Utilizando ultrasonido focalizado, agentes nocivos o soluciones hiperosmolares para abrir temporalmente las uniones estrechas.
Aunque efectivas, estas técnicas tienen limitaciones, como la insatisfacción del paciente y el riesgo de comprometer la integridad de la BHE, permitiendo la entrada de sustancias no deseadas.
Técnicas No Invasivas o Misceláneas
Buscan aprovechar o modificar las rutas de transporte existentes o crear nuevas:
- Administración intranasal: Permite el transporte directo al LCR a través de vías neuronales que conectan la mucosa nasal con el cerebro.
- Uso de sistemas de transporte/portadores: Acoplar el fármaco a una molécula transportable (enfoque de 'caballo de Troya').
- Tecnologías basadas en nanopartículas: Nanopartículas lipídicas o poliméricas que encapsulan y protegen el fármaco, facilitando su paso y liberación controlada.
- Modificación química: Convertir moléculas hidrosolubles en liposolubles.
- Proteínas de fusión con anticuerpos monoclonales (por ejemplo, fusiones IgG).
- Inhibición de transportadores de eflujo: Bloquear las bombas que expulsan los fármacos del cerebro.
- Péptidos quiméricos: Acoplar un fármaco a un péptido vector transportable a través de la BHE.
- Proteínas genéticamente modificadas: Diseñadas para ser transportadas por receptores endógenos.
La investigación en este campo es muy activa, buscando formas seguras y efectivas de llevar los tratamientos al cerebro.
Tabla Comparativa: Sustancias y su Capacidad de Cruce
| Sustancia/Molécula | Capacidad de Cruce de la BHE | Mecanismo Principal |
|---|---|---|
| Glucosa | Sí | Transporte mediado por portador (GLUT1) |
| Aminoácidos esenciales | Sí | Transporte mediado por portador |
| Oxígeno (O2) | Sí | Difusión pasiva |
| Dióxido de Carbono (CO2) | Sí | Difusión pasiva |
| Agua | Sí | Difusión pasiva (y acuaporinas) |
| Iones pequeños (Na+, K+, Cl-) | Limitado | Canales iónicos, difusión limitada, bombas |
| Albúmina sérica | No (normalmente) / Sí (en disfunción) | Difusión paracelular limitada / Aumento en disfunción |
| Patógenos (Bacterias, Virus) | No (normalmente) / Sí (en infección) | Bloqueo físico / Transcitosis inducida por patógenos |
| Fármacos lipofílicos pequeños | Sí | Difusión pasiva |
| Fármacos hidrofílicos pequeños | No (normalmente) / Sí (en disrupción) | Bloqueo por uniones estrechas / Paso paracelular en disrupción |
| La mayoría de los fármacos de molécula grande | No | Tamaño, hidrofília, bombas de eflujo |
| Insulina, Leptina, Transferrina | Sí | Transcitosis mediada por receptor |
| Proteína A-beta | Transporte de eflujo (fallo en EA) | Transporte mediado (LRP1) |
Preguntas Frecuentes sobre la Barrera Hematoencefálica
¿Qué significa BHE en neurociencia?
BHE significa Barrera Hematoencefálica. Es una interfaz especializada entre la sangre y el cerebro que regula el paso de sustancias para proteger el tejido nervioso y mantener su entorno estable.
¿Cuál es la función principal de la Barrera Hematoencefálica?
Su función principal es proteger el cerebro de sustancias dañinas y patógenos en la sangre, mantener la homeostasis del fluido cerebral y facilitar el transporte selectivo de nutrientes esenciales.

¿Qué sustancias pueden cruzar la BHE fácilmente?
Generalmente, las sustancias lipofílicas (solubles en grasa) de bajo peso molecular y algunos gases como el oxígeno y el dióxido de carbono pueden cruzar la BHE por difusión pasiva. Los nutrientes esenciales como la glucosa cruzan mediante transportadores específicos.
¿Qué ocurre cuando la Barrera Hematoencefálica se daña?
Cuando la BHE se daña, su permeabilidad aumenta, permitiendo que sustancias tóxicas, patógenos y células inmunes entren al cerebro. Esto puede causar neuroinflamación, edema, disfunción neuronal y contribuir a la progresión de enfermedades neurológicas.
¿Es posible administrar fármacos al cerebro si la BHE es tan restrictiva?
Sí, es posible, pero es un gran desafío. Se están investigando y utilizando diversas estrategias, tanto invasivas (como la inyección directa) como no invasivas (como el uso de nanopartículas o el acoplamiento a transportadores), para facilitar el paso de los fármacos a través o alrededor de la BHE.
En resumen, la Barrera Hematoencefálica es un componente crítico del sistema nervioso central. Su estructura única y sus múltiples funciones son esenciales para la salud cerebral. La investigación continua sobre su biología y su papel en las enfermedades ofrece la esperanza de nuevas estrategias terapéuticas para trastornos neurológicos que actualmente son difíciles de tratar debido a esta formidable barrera.
Si quieres conocer otros artículos parecidos a La Barrera Hematoencefálica: Guardián del Cerebro puedes visitar la categoría Neurociencia.
