El cerebro, con su intrincada red de miles de millones de neuronas interconectadas, representa uno de los desafíos más complejos y fascinantes para la ciencia moderna. Comprender cómo funcionan estos circuitos neuronales y desarrollar formas de repararlos cuando fallan es la vanguardia de la neurociencia y la terapia génica. En esta búsqueda, una herramienta viral inesperada ha surgido como protagonista: el Virus Adenoasociado, o AAV por sus siglas en inglés.
El AAV es un virus pequeño, no envuelto, que pertenece a la familia de los parvovirus. Curiosamente, es defectuoso para la replicación, lo que significa que necesita la ayuda de otros virus (como el adenovirus) para poder multiplicarse activamente. Una característica fundamental y muy ventajosa del AAV es que no causa enfermedades conocidas en humanos y solo induce una respuesta inmunitaria muy leve. Estas propiedades lo convierten en un candidato ideal para ser modificado y utilizado como vector, un vehículo para entregar material genético en células específicas.
¿Qué es Exactamente un Virus Adenoasociado (AAV)?
Como mencionamos, AAV significa Adeno-Associated Virus. Es un virus con un genoma pequeño de ADN monocatenario de aproximadamente 4.7 kilobases (kb). Su estructura es simple: una cápside proteica (la cubierta exterior) que protege el material genético interno. Esta cápside está compuesta por tres proteínas principales (VP1, VP2, VP3) y juega un papel crucial en la interacción del virus con las células huésped y la determinación de su tropismo, es decir, su preferencia por infectar ciertos tipos de células o tejidos.
Existen al menos 11 serotipos naturales de AAV humanos identificados, cada uno con diferentes propiedades de tropismo y transducción (la capacidad de infectar una célula y entregar su carga genética). Además de los serotipos naturales, los científicos han desarrollado virus adenoasociados recombinantes (rAAVs). Estos rAAVs son la forma utilizada en investigación y terapia, ya que se les puede reemplazar casi todo el genoma viral (aproximadamente el 96% de sus genes) con ADN foráneo, como genes terapéuticos o secuencias que codifican proteínas fluorescentes, sin que el virus mantenga su capacidad de replicación salvaje. El genoma modificado, flanqueado por secuencias llamadas repeticiones terminales invertidas (ITRs), se empaqueta dentro de la cápside del AAV.
Una vez que un rAAV infecta una célula, el material genético que lleva se transporta al núcleo. En ausencia de un virus ayudante, este ADN generalmente permanece en el núcleo como una molécula circular (episoma) en lugar de integrarse en el genoma de la célula huésped de manera eficiente. Esta característica es ventajosa para la seguridad en terapia génica, aunque los episomas pueden diluirse con el tiempo en células que se dividen rápidamente.
AAV como Herramienta para Mapear y Manipular Circuitos Neuronales
La complejidad del cerebro radica en la organización de las neuronas en circuitos funcionales. Identificar y clasificar estos circuitos es fundamental. Los circuitos neuronales se definen por múltiples factores: ubicación de las neuronas, sus conexiones (dónde se originan y terminan sus axones), el tipo de célula (basado en morfología, electrofisiología o neurotransmisores que liberan, como serotonina o glutamato). Un nodo dentro de un circuito podría ser un grupo de neuronas en una ubicación específica, y los 'bordes' son sus conexiones con otros nodos.
Tradicionalmente, estudiar estos circuitos ha sido un desafío. Sin embargo, las propiedades únicas de los AAVs, especialmente su capacidad para dirigirse a poblaciones neuronales específicas, los convierten en una herramienta excelente para este fin. Para analizar anatómicamente los nodos y las conexiones de los circuitos, un objetivo común es introducir un vector viral que infecte las neuronas de interés y haga que expresen una proteína fluorescente. Esto permite visualizar las neuronas y sus proyecciones bajo el microscopio.
Dado que los AAVs son defectuosos para la replicación y no se propagan eficientemente entre neuronas conectadas sin modificaciones (es decir, no saltan fácilmente a través de las sinapsis), son útiles para etiquetar y estudiar un único nodo o una población neuronal específica dentro de un circuito más grande. Esto minimiza la preocupación de que el virus se extienda incontroladamente y etiquete neuronas vecinas que no son el objetivo primario.
Aunque algunos serotipos naturales de AAV pueden tener un tropismo bajo para ciertos tipos de neuronas, los rAAVs han demostrado ser una solución eficaz. Al modificar la cápside (un proceso llamado pseudotipado), se pueden crear rAAVs con mayor eficiencia de transducción y tropismo mejorado para tipos celulares específicos. Por ejemplo, el serotipo AAV2 es el más estudiado y tiene un tropismo natural por las neuronas. Vectores basados en AAV2 que expresan proteínas fluorescentes han sido fundamentales para mapear la conectividad entre regiones cerebrales en modelos animales, como el proyecto Allen Mouse Brain Connectivity Atlas.
Sin embargo, AAV2 no infecta ampliamente todos los tipos neuronales, lo que puede ser una desventaja si se busca una transducción global en un nodo, pero una ventaja si se desea etiquetar un subconjunto pequeño de neuronas. Los diferentes serotipos de AAV tienen variados tropismos. Por ejemplo, AAVs 1, 6, y 7 muestran mayor especificidad por neuronas sobre células gliales in vitro, mientras que in vivo, AAVs 1, 2, 5, 7, 8, y 9 muestran una fuerte preferencia por neuronas en muchas regiones cerebrales.

Transporte de AAV en las Neuronas
Una propiedad clave de muchos rAAVs es su capacidad de ser transportados dentro de la neurona. La mayoría muestran transporte anterógrado: si se inyectan cerca del soma (cuerpo celular), el virus infecta la célula, y el material genético entregado puede ser transportado a lo largo del axón hasta los terminales nerviosos. Esto es útil para mapear proyecciones neuronales.
Algunos AAVs también tienen la capacidad natural de transporte retrógrado: si se inyectan en una región donde terminan los axones, el virus puede ser captado por los terminales, transportado hacia atrás a lo largo del axón hasta el soma, y luego infectar la célula en su origen. Aunque la mayoría de los AAVs naturales facilitan mal el transporte retrógrado, se han desarrollado rAAVs diseñados para mejorarlo, como el rAAV2-retro. El transporte (anterógrado, retrógrado, bidireccional) depende del serotipo y la concentración.
Además, ciertos serotipos como AAV1 y AAV9 son capaces de migrar de forma transináptica. Esto significa que, después de llegar a un terminal nervioso, pueden cruzar la sinapsis e infectar las neuronas postsinápticas conectadas. Esta propiedad es invaluable para etiquetar y manipular redes de circuitos neuronales más allá de la simple conectividad directa.
Dirigiendo AAVs a Tipos Neuronales Específicos
Más allá de la especificidad innata de los serotipos, los rAAVs permiten una focalización aún más precisa mediante enfoques de genética interseccional. Esto significa que se puede diseñar un AAV para que solo infecte o exprese su carga genética en células que expresan un marcador genético particular.
Una estrategia es modificar el genoma del AAV para que la expresión del gen de interés esté bajo el control de un promotor específico de un tipo celular (ej. promotores de CamKIIa para neuronas excitadoras, GFAP para astrocitos). Alternativamente, se pueden usar sistemas de recombinación como Cre-loxP. Se diseña un AAV con un elemento DIO (doblemente flanqueado e invertido) que contiene el gen de interés. Este gen solo se expresará si la enzima Cre recombinasa está presente en la célula. Combinando este AAV-DIO con animales modelo que expresan Cre en tipos celulares definidos, o co-inyectando un segundo AAV que expresa Cre bajo un promotor específico, se logra una transducción altamente selectiva.
Estos enfoques multiplexados, a menudo combinando AAVs con otras herramientas como virus de la rabia modificados, permiten a los investigadores mapear con una precisión sin precedentes las entradas a regiones cerebrales específicas o manipular subpoblaciones neuronales muy definidas.
Entrega de AAV en el Cerebro: Superando la Barrera Hematoencefálica
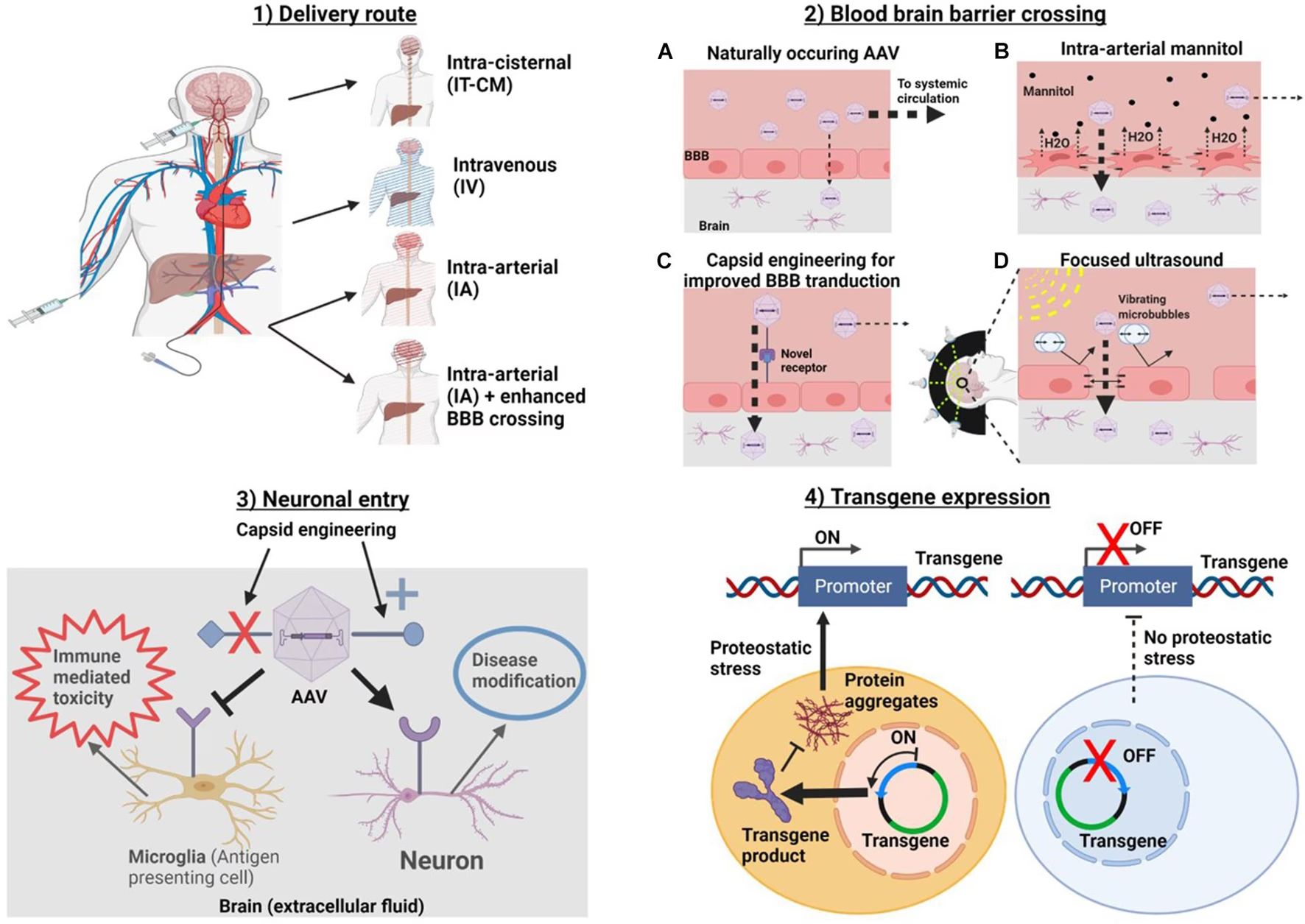
El uso de AAVs para estudiar y tratar enfermedades neurológicas a menudo requiere que el virus llegue al cerebro. Sin embargo, la Barrera Hematoencefálica (BHE) es un obstáculo importante. Esta barrera limita el paso de muchas sustancias del torrente sanguíneo al tejido cerebral, protegiendo el cerebro de patógenos y toxinas, pero dificultando la entrega de terapias.
Existen varias estrategias para entregar AAVs al cerebro:
- Inyección Directa: Consiste en inyectar el AAV directamente en el parénquima cerebral (el tejido nervioso) o en el líquido cefalorraquídeo (LCR), ya sea en los ventrículos (intracerebroventricular) o en el espacio intratecal (espinal). Esta es la forma más común de asegurar que el virus llegue a la región deseada, pero es invasiva y limita la distribución a un área específica.
- Inyección Intravenosa: Administrar el AAV en el torrente sanguíneo es mucho menos invasivo, pero la BHE limita la cantidad de virus que llega al cerebro. Sin embargo, se han desarrollado variantes de AAV diseñadas para cruzar la BHE de manera más eficiente, como AAV9, y más recientemente, AAV-PHP.eB y AAV-PHP.S, que muestran un tropismo mejorado por el sistema nervioso central (SNC) y periférico (SNP) respectivamente tras inyección intravenosa.
- Entrega Intranasal: En algunos casos, la administración por vía nasal puede permitir que pequeñas cantidades de virus lleguen al SNC a través de vías neuronales.
- Ultrasonido Focalizado: Una tecnología emergente utiliza ultrasonido focalizado para abrir temporalmente la BHE en una región específica, permitiendo que los AAVs administrados por vía intravenosa entren al tejido cerebral.
La elección de la estrategia de entrega depende de la enfermedad, la región cerebral objetivo y el serotipo de AAV utilizado.
AAV en la Terapia Génica para Enfermedades Neurológicas
Dada su seguridad, eficiencia y capacidad para transduir neuronas, los rAAVs son vectores muy prometedores para la terapia génica de enfermedades neurológicas. Muchas de estas enfermedades son causadas por mutaciones en un solo gen (enfermedades monogénicas), donde la terapia génica busca reemplazar el gen defectuoso o aumentar la expresión de un gen funcional.

Numerosos ensayos clínicos están utilizando AAVs para tratar una variedad de trastornos neurológicos, incluyendo:
- Enfermedad de Batten (CLN2, LINCL)
- Enfermedad de Canavan
- Mucopolisacaridosis (MPS) tipos IIIA y IIIB
- Atrofia Muscular Espinal (AME)
- Enfermedad de Parkinson
- Enfermedad de Alzheimer
- Neuropatías ópticas hereditarias (LHON)
- Retinosquisis ligada al X
- Achromatopsia
Las estrategias varían desde la inyección directa en regiones cerebrales específicas (como en la Enfermedad de Parkinson o algunas MPS) hasta la administración intratecal en el LCR (para enfermedades con afectación más amplia como la AME) o la inyección intravenosa con serotipos que cruzan la BHE.
Aunque los resultados preclínicos son a menudo prometedores, la traducción a humanos no siempre es predecible. Superar la Barrera Hematoencefálica de manera segura y eficiente para lograr una distribución terapéutica adecuada sigue siendo un desafío clave en la terapia génica del SNC.
Ventajas y Desafíos del Uso de AAV
El AAV ofrece varias ventajas significativas como vector de entrega génica:
- Seguridad: Es un virus no patógeno y poco inmunogénico en comparación con otros vectores virales. Los rAAVs carecen de genes virales activos.
- Eficiencia: Puede infectar tanto células que se dividen como las que no se dividen, incluyendo las neuronas postmitóticas del cerebro.
- Versatilidad: La ingeniería de la cápside permite modificar el tropismo para dirigirse a diferentes tipos celulares y tejidos. La capacidad de dirigir el transporte dentro de las neuronas (anterógrado, retrógrado) es invaluable para la investigación de circuitos.
- Persistencia: El genoma entregado puede persistir como episoma en el núcleo de células que no se dividen durante largos períodos, lo que es ideal para terapias de dosis única en tejidos como el músculo o el cerebro.
Sin embargo, también existen desafíos:
- Capacidad de Carga Limitada: El tamaño máximo del ADN que puede empaquetarse en un AAV es de aproximadamente 5 kb (o 3.3 kb para AAVs autocomplementarios), lo que limita su uso para genes muy grandes.
- Inmunogenicidad: Aunque baja, la cápside del AAV y, en algunos casos, la proteína expresada por el transgén, pueden desencadenar una respuesta inmunitaria adaptativa y humoral. La preexistencia de anticuerpos neutralizantes en pacientes debido a una exposición previa al virus natural es un obstáculo importante para la eficacia, especialmente con la administración sistémica.
- Entrega al SNC: La Barrera Hematoencefálica sigue siendo un desafío para lograr una distribución amplia y eficiente en el cerebro mediante administración sistémica.
- Fabricación: La producción a gran escala de rAAVs de alta calidad para uso clínico es compleja y costosa. Asegurar la pureza y la proporción adecuada de partículas 'llenas' (con el transgén) frente a partículas 'vacías' es crucial.
Preguntas Frecuentes
¿Qué significa AAV?
Significa Adeno-Associated Virus, o Virus Adenoasociado.
¿Es seguro el AAV?
El AAV natural no causa enfermedades conocidas en humanos y solo induce una respuesta inmune leve. Los vectores de terapia génica basados en rAAV se modifican para ser defectuosos para la replicación y se consideran generalmente muy seguros, aunque la respuesta inmune a la cápside o al transgén es una consideración clínica.
¿Cómo se usa el AAV en neurociencia?
Se utiliza principalmente como un vector para entregar genes en neuronas y otras células del sistema nervioso. Esto permite a los investigadores expresar proteínas fluorescentes para visualizar circuitos neuronales, introducir herramientas genéticas para manipular la actividad neuronal o entregar genes terapéuticos para tratar enfermedades neurológicas.
¿Puede el AAV cruzar la Barrera Hematoencefálica?
Algunos serotipos de AAV, notablemente AAV9 y variantes diseñadas como AAV-PHP.eB, tienen la capacidad de cruzar la Barrera Hematoencefálica después de la inyección intravenosa, permitiendo la entrega al sistema nervioso central sin necesidad de inyección directa en el cerebro.
¿Qué son los serotipos de AAV?
Los serotipos son variantes naturales del virus AAV que tienen diferencias en la composición de su cápside. Estas diferencias confieren a cada serotipo un tropismo distinto, es decir, una preferencia por infectar ciertos tipos de células o tejidos.
El campo de los AAVs para la neurociencia y la terapia génica está en constante evolución. El desarrollo de nuevos serotipos, estrategias de ingeniería de cápsides y métodos de entrega más eficientes y seguros promete expandir aún más el potencial de esta notable herramienta viral para desentrañar los misterios del cerebro y abordar enfermedades neurológicas devastadoras.
Si quieres conocer otros artículos parecidos a AAV en Neurociencia y Terapia Génica puedes visitar la categoría Neurociencia.
