La neurociencia, en su incansable búsqueda por desentrañar los misterios del cerebro, recurre a una diversidad de modelos animales. Si bien los roedores han dominado históricamente el campo, un humilde habitante de acuario, el pez cebra (Danio rerio), ha emergido como un protagonista inesperado y excepcionalmente valioso. Su creciente prominencia no es casualidad; una combinación única de características biológicas lo convierte en una herramienta poderosa para explorar desde el desarrollo neuronal más temprano hasta los complejos mecanismos de las enfermedades neurodegenerativas.

Inicialmente reconocido por sus virtudes en genética, farmacología y toxicología, el pez cebra ha extendido su influencia al ámbito de la neurociencia conductual. Aunque a veces se le etiqueta como un modelo 'alternativo' a los mamíferos, una perspectiva más precisa lo considera un modelo 'complementario'. Ciertas preguntas, especialmente aquellas ligadas a estructuras corticales o del hipocampo prominentes en mamíferos, no pueden abordarse directamente en peces. Sin embargo, sus atributos distintivos abren puertas a investigaciones que son difíciles o imposibles en otros modelos.
- ¿Por qué el Pez Cebra es un Modelo Valioso?
- Neurodesarrollo y Regeneración sin Precedentes
- Explorando el Comportamiento Neuronal
- Modelando Enfermedades Neurodegenerativas Humanas
- Herramientas Experimentales y Avances
- El Pez Cebra vs. Otros Modelos: Una Comparativa
- Limitaciones y la Promesa del Futuro
- Preguntas Frecuentes sobre el Pez Cebra en Neurociencia
¿Por qué el Pez Cebra es un Modelo Valioso?
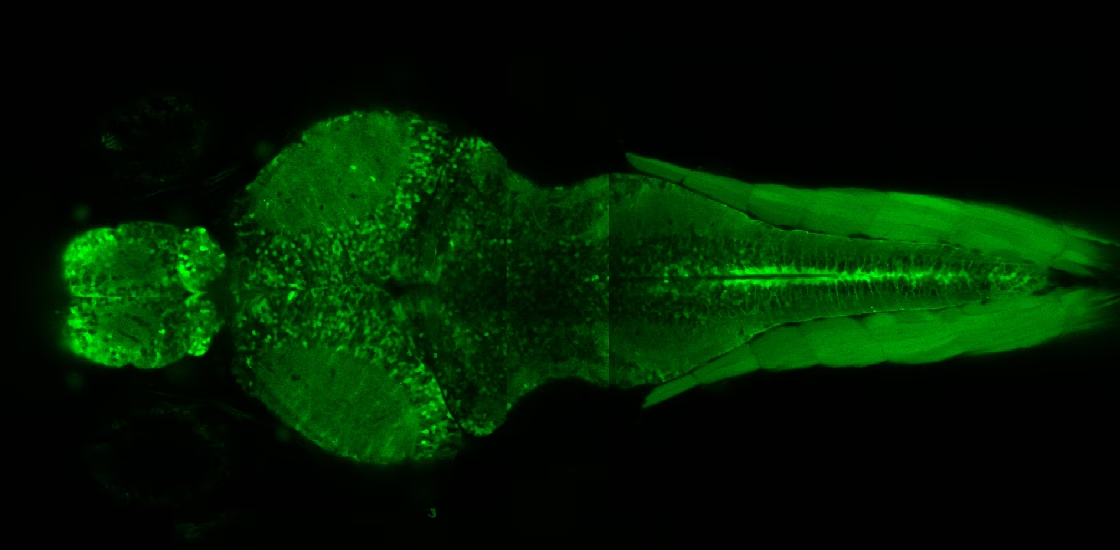
Las razones detrás del éxito del pez cebra en neurociencia son múltiples y convincentes. Una de las más destacadas es la transparencia de sus embriones y larvas, especialmente en ciertas cepas mutantes. Esta claridad óptica permite la visualización continua y no invasiva del neurodesarrollo en tiempo real, observando cómo las células neurales proliferan, se diferencian, migran y establecen proyecciones. Sistemas reporteros fluorescentes pueden marcar poblaciones neuronales específicas, facilitando su seguimiento.
Otro factor crucial es su ciclo de vida. El pez cebra se reproduce en grandes cantidades y se desarrolla con asombrosa rapidez. Los aspectos clave del neurodesarrollo ocurren en cuestión de días, no semanas o meses como en mamíferos. Esta combinación de prolificidad y desarrollo veloz reduce drásticamente los costos experimentales y permite un alto rendimiento en la investigación, posibilitando la realización de más experimentos en menos tiempo.
La facilidad para la manipulación genética es una ventaja fundamental. Se dispone de una gran cantidad de mutantes que ayudan a evaluar mecanismos moleculares a lo largo de la vida. Técnicas como la morfolina permiten la supresión genética reversible durante el desarrollo temprano, revelando la importancia de mecanismos moleculares específicos. Más recientemente, la llegada de herramientas de edición genética como CRISPR/Cas9 ha revolucionado la capacidad de crear modelos genéticos precisos, superando algunas limitaciones de las morfolinas.
Además, el pez cebra exhibe una amplia gama de comportamientos que son análogos a los de especies terrestres. Esto incluye comportamientos sociales complejos, navegación espacial, aprendizaje no asociativo (habituación), condicionamiento pavloviano y operante, y respuestas sensoriales sofisticadas como visión a color, electrorrecepción (en algunas especies) y detección de movimientos del agua mediante la línea lateral. Esta riqueza conductual, combinada con la accesibilidad de sus circuitos neuronales, lo convierte en un excelente modelo para la neurociencia conductual.
Neurodesarrollo y Regeneración sin Precedentes
El pez cebra se ha convertido rápidamente en un modelo prominente para estudiar las bases moleculares del neurodesarrollo de vertebrados. Su capacidad para visualizar continuamente la neuroanatomía en desarrollo y su susceptibilidad al análisis genético lo hacen ideal para estudios mecanicistas.
Quizás una de las capacidades más fascinantes del pez cebra, y que lo distingue radicalmente de los mamíferos, es su impresionante habilidad para la regeneración de tejidos y órganos, incluido el sistema nervioso central. Pueden regenerar el cerebro, la médula espinal, la retina, el corazón y las aletas con una capacidad limitada o ausente de cicatrización glial persistente. Este fenómeno está estrechamente ligado a la activación de células madre neurales y a una respuesta inmune peculiar.

Tras una lesión cerebral, el pez cebra moviliza microglía y otras células inmunes de manera aguda y controlada. A diferencia de los mamíferos, donde la inflamación crónica contribuye a la formación de cicatrices gliales que inhiben la regeneración axonal y la migración neuronal, la respuesta inflamatoria en el pez cebra es transitoria y parece desempeñar un papel positivo en la activación de las células gliales radiales (que actúan como células madre neurales en el telencéfalo adulto). Estas células proliferan y generan nuevas neuronas y oligodendrocitos que repueblan el sitio lesionado, restaurando la estructura y función del tejido dañado sin dejar cicatrices visibles tras unos meses. Este contraste en la respuesta inmune y la formación de cicatrices es un área clave de investigación para entender cómo potenciar la regeneración en mamíferos.
La retina del pez cebra, estructuralmente similar a la de los mamíferos, también exhibe una notable capacidad regenerativa. Las células de Müller, un tipo de glía, pueden desdiferenciarse y reprogramarse para generar todos los tipos celulares perdidos en la retina dañada. Esta capacidad lo convierte en un modelo invaluable para estudiar enfermedades retinianas degenerativas y buscar estrategias para restaurar la visión.
Explorando el Comportamiento Neuronal
La investigación conductual en peces no es nueva, con etólogos y psicólogos comparativos estudiando la evolución del aprendizaje y la cognición. Sin embargo, el pez cebra ha permitido llevar estos estudios a un nivel molecular y genético. Para ello, se han adaptado o desarrollado diversas pruebas conductuales:
- Laberinto en T Acuático: Usado para estudiar discriminación (ej. color), navegación y efectos de manipulaciones genéticas.
- Tambor Giratorio: Evalúa reflejos de escape visualmente guiados.
- Pruebas de Exploración de Novedad: Similar a las pruebas de ansiedad en roedores, evalúa la respuesta a estímulos nuevos y la habituación.
- Procedimiento de Preferencia de Lugar: Utilizado para medir el condicionamiento apetitivo o aversivo a estímulos asociados a recompensas o castigos (ej. drogas).
- Caja de Lanzadera (Shuttle Box): Permite estudiar el condicionamiento pavloviano y operante, donde el pez aprende a evitar un estímulo aversivo nadando a otro compartimento.
- Laberinto de Tres Cámaras: Una simplificación del laberinto en T para evaluar aprendizaje espacial y no espacial, así como memoria.
Estas pruebas, combinadas con la capacidad de manipular genéticamente o tratar farmacológicamente a los peces, permiten investigar los mecanismos neuronales subyacentes a una amplia gama de comportamientos.
Modelando Enfermedades Neurodegenerativas Humanas
El pez cebra se está consolidando como un modelo relevante para la investigación traslacional de la neuropatología humana. A pesar de las diferencias anatómicas, su cerebro comparte similitudes fundamentales en vías neuroanatómicas y neuroquímicas con los humanos. Además, pueden recapitular sellos distintivos de la patología humana, como la agregación de proteínas, la degeneración neuronal y la activación glial.
Enfermedad de Parkinson (EP)
La EP, caracterizada por la pérdida de neuronas dopaminérgicas y la acumulación de α-sinucleína, ha sido ampliamente modelada en pez cebra. Se han generado modelos genéticos mediante la sobreexpresión de α-sinucleína humana o el silenciamiento (inicialmente con morfolinas, ahora con CRISPR) de genes implicados en la EP familiar (PINK1, Parkin, LRRK2, DJ-1, FBXO7). Estos modelos recapitulan aspectos como la pérdida de neuronas dopaminérgicas (principalmente en el tubercúlo posterior, homólogo de la sustancia negra), neuroinflamación y déficits motores. También se han usado modelos inducidos químicamente con neurotoxinas como MPTP. El pez cebra permite estudiar la formación de agregados, las consecuencias de mutaciones o exposición a pesticidas, y evaluar fármacos. La observación de efectos similares de la nicotina en la memoria en pez cebra y mamíferos subraya la relevancia del modelo para estudiar vías conservadas.
Enfermedad de Alzheimer (EA)
Modelar la EA en pez cebra ha sido más desafiante, pero se han logrado avances significativos. Se han creado modelos que expresan la proteína amiloide-β (Aβ) o la proteína tau humana mutante. Si bien la agregación de Aβ o la formación de ovillos neurofibrilares de tau pueden inducirse (a veces mediante inyección directa o tratamiento químico), los fenotipos no siempre replican completamente la progresión clínica humana (ej. la neurogénesis puede aumentar en lugar de disminuir). Sin embargo, el pez cebra es muy útil para cribados de fármacos a alto rendimiento dirigidos a reducir la agregación de proteínas o mitigar la neurotoxicidad, aprovechando su capacidad para absorber compuestos disueltos en el agua.
Esclerosis Lateral Amiotrófica (ELA)
La ELA, una enfermedad de las motoneuronas, se beneficia enormemente de la transparencia de las larvas de pez cebra, que permite visualizar las motoneuronas, sus axones y las uniones neuromusculares en tiempo real. Se han modelado mutaciones en genes clave de la ELA (SOD1, TARDBP/TDP-43, C9orf72, FUS). Estos modelos recapitulan características de la ELA como atrofia muscular, anormalidades axónicas, pérdida de motoneuronas y déficits motores. Estudios en pez cebra han proporcionado información valiosa sobre mecanismos moleculares, por ejemplo, el papel de Filamin C en la patogénesis mediada por TDP-43 o la función de FUS en el empalme de ARN.

Enfermedad de Huntington (EH)
Aunque menos estudiada que otras enfermedades neurodegenerativas en este modelo, el pez cebra también ha aportado insights sobre la EH. La sobreexpresión de huntingtina mutante (mHTT) o el silenciamiento de HTT han mostrado un aumento de la apoptosis neuronal y defectos en el neurodesarrollo. A diferencia de los ratones, los peces cebra sin HTT son viables, lo que permite estudiar su función durante el desarrollo. Se han utilizado para identificar compuestos que inhiben la agregación de la proteína mutante y para investigar el papel de HTT en el metabolismo del hierro o en la interacción entre células neuroepiteliales.
Herramientas Experimentales y Avances
La manipulación genética en pez cebra ha evolucionado significativamente. Inicialmente, las morfolinas (MO) fueron la herramienta principal para silenciar la expresión génica de forma transitoria. Si bien fueron útiles, presentaban limitaciones como efectos fuera del objetivo y su transitoriedad. La llegada de la edición genética mediante CRISPR/Cas9 ha permitido la creación de mutantes estables con deleciones o mutaciones precisas, lo que proporciona modelos más fiables y permanentes.
La transparencia de las larvas, combinada con la disponibilidad de líneas transgénicas que expresan proteínas fluorescentes en tipos celulares específicos (neuronas, glía, microglía), facilita la obtención de imágenes *in vivo* de alta resolución. Esto permite seguir el desarrollo, la migración celular, la formación de circuitos, la agregación de proteínas o la muerte neuronal en tiempo real.
La capacidad de mantener grandes poblaciones de peces a bajo costo y la administración de fármacos en el agua hacen del pez cebra un modelo ideal para cribados farmacológicos a alto rendimiento. Sistemas automatizados permiten testear cientos o miles de compuestos en larvas simultáneamente, acelerando la búsqueda de potenciales terapias.
El Pez Cebra vs. Otros Modelos: Una Comparativa
Para comprender mejor el nicho que ocupa el pez cebra en la investigación neurocientífica, es útil compararlo con modelos más tradicionales como los roedores:
| Característica | Pez Cebra (Danio rerio) | Modelos Mamíferos (ej. Ratón/Rata) |
|---|---|---|
| Costo y Mantenimiento | Bajo, alta capacidad de reproducción, muchos individuos | Alto, mantenimiento más complejo |
| Velocidad de Desarrollo | Rápido (días para etapas clave) | Lento (semanas/meses para madurez) |
| Transparencia (Etapa Larva) | Alta, permite visualización *in vivo* continua | Baja o nula, requiere métodos invasivos o especiales |
| Capacidad de Regeneración | Alta (cerebro, retina, médula espinal, etc.) sin cicatrización | Muy limitada en SNC (generalmente con cicatrización) |
| Manipulación Genética | Relativamente fácil (mutantes, transgenia, CRISPR) | Más compleja, aunque bien establecida |
| Estructura Cerebral | Más simple, carece de algunas estructuras mamíferas (corteza frontal, hipocampo) | Compleja, similar a humanos |
| Rendimiento Experimental | Alto rendimiento (muchos individuos, desarrollo rápido) | Menor rendimiento por experimento |
Esta tabla ilustra cómo el pez cebra complementa a los modelos mamíferos, destacando en áreas como la visualización del desarrollo, la regeneración y los cribados a gran escala, mientras que los mamíferos son insustituibles para estudiar funciones que dependen de estructuras cerebrales más complejas y específicas.
Limitaciones y la Promesa del Futuro
A pesar de sus múltiples ventajas, el pez cebra no está exento de limitaciones. La principal es, quizás, la ausencia de ciertas estructuras cerebrales complejas presentes en mamíferos, lo que restringe el estudio de funciones cognitivas altamente dependientes de ellas. Aunque se pueden modelar aspectos de enfermedades neurodegenerativas que suelen tener inicio en la edad adulta, el uso de larvas jóvenes puede no replicar completamente la patología de inicio tardío, aunque sí puede ofrecer pistas sobre predisposiciones o etapas pre-manifestación.

La interpretación de los ensayos conductuales en peces puede ser diferente a la de mamíferos, y se necesita más trabajo para desarrollar pruebas que capturen la sutileza de ciertos déficits motores o psiquiátricos observados en pacientes humanos. La administración de fármacos en el agua, aunque conveniente para cribados, dificulta la determinación precisa de la dosis absorbida y no siempre refleja la farmacocinética en mamíferos.
Sin embargo, la investigación continúa abordando estas limitaciones. El desarrollo de mutantes pigmentados permite el estudio en peces adultos. Las herramientas de edición genética mejoran la fiabilidad de los modelos genéticos. El diseño de nuevos ensayos conductuales busca una mayor relevancia traslacional. Además, el pez cebra se está utilizando para estudiar barreras como la hematoencefálica y probar nuevas estrategias de entrega de fármacos, como la nanotecnología.
Preguntas Frecuentes sobre el Pez Cebra en Neurociencia
¿Puede el pez cebra regenerar el cerebro?
Sí, el pez cebra tiene una notable capacidad para regenerar varias regiones de su cerebro, incluido el telencéfalo. Tras una lesión, las células madre neurales (células gliales radiales) en el cerebro adulto se activan, proliferan y generan nuevas neuronas y células gliales que migran al sitio dañado y lo repueblan, restaurando la estructura sin formar una cicatriz glial permanente como ocurre en mamíferos.
¿Cómo es un modelo para enfermedades neurodegenerativas?
El pez cebra es un modelo para enfermedades neurodegenerativas porque comparte una alta conservación genética con los humanos, incluyendo muchos genes implicados en enfermedades como el Parkinson, Alzheimer, ELA y Huntington. Se pueden crear modelos genéticos (mutantes, transgénicos) o tóxicos que recapitulan características clave de estas enfermedades a nivel celular (agregación de proteínas, degeneración neuronal, neuroinflamación) y conductual (déficits motores). Su uso permite estudiar los mecanismos subyacentes a la enfermedad y realizar cribados de fármacos a gran escala.
¿Puede el pez cebra regenerar los ojos?
Sí, el pez cebra puede regenerar su retina, que es la parte del ojo responsable de detectar la luz. Las células de Müller en la retina del pez cebra actúan como células madre, activándose y proliferando después de una lesión para reemplazar las células retinianas dañadas o perdidas, incluidos los fotorreceptores. Esta capacidad lo hace un modelo excelente para estudiar la regeneración de la retina y buscar terapias para enfermedades oculares degenerativas.
En resumen, el pez cebra ha pasado de ser un modelo de nicho a una herramienta esencial y versátil en la neurociencia moderna. Sus características únicas, desde la transparencia de sus larvas hasta su excepcional capacidad regenerativa y la facilidad para la manipulación genética y el cribado de fármacos, lo posicionan como un complemento indispensable a los modelos mamíferos. A medida que las tecnologías experimentales sigan avanzando, el pez cebra sin duda continuará desempeñando un papel crucial en la profundización de nuestra comprensión del cerebro y en la búsqueda de tratamientos para sus patologías.
Si quieres conocer otros artículos parecidos a El Pez Cebra en la Neurociencia puedes visitar la categoría Neurociencia.
