Durante mucho tiempo, el sistema nervioso se ha considerado principalmente el centro de nuestras funciones cognitivas, sensoriales y motoras. Sin embargo, investigaciones recientes han revelado una faceta sorprendente y fundamental: su profunda implicación en el desarrollo y la progresión del cáncer. Esta intersección emergente ha dado origen a un campo de estudio completamente nuevo, la Neurociencia del Cáncer, que está redefiniendo nuestra comprensión de esta compleja enfermedad y abriendo vías insospechadas para su tratamiento.

El sistema nervioso, tanto el central (cerebro y médula espinal) como el periférico (nervios que se extienden por todo el cuerpo), no solo regula procesos fisiológicos vitales como el desarrollo de órganos, la homeostasis y la plasticidad a lo largo de la vida, sino que también desempeña un papel paralelo, y a menudo promotor, en la regulación de los tumores. Esta influencia es bidireccional: mientras que el sistema nervioso puede impulsar el cáncer, el cáncer y sus tratamientos también pueden alterar drásticamente la función neural, causando problemas neurológicos significativos.
- La Influencia del Sistema Nervioso en el Inicio y Crecimiento del Cáncer
- El Cáncer Secuestra Mecanismos Neurobiológicos
- Neuro-Inmuno-Oncología: La Triple Alianza
- El Impacto del Cáncer y sus Terapias en el Sistema Nervioso
- Hacia Terapias Basadas en la Neurociencia del Cáncer
- El Futuro de la Neurociencia del Cáncer
- Preguntas Frecuentes sobre Neurociencia y Cáncer
- ¿Qué es la Neurociencia del Cáncer?
- ¿Cómo interactúan las neuronas con las células tumorales?
- ¿Pueden los medicamentos utilizados para tratar trastornos neurológicos ayudar a tratar el cáncer?
- ¿Afecta el cáncer o su tratamiento a mi sistema nervioso?
- ¿Es este campo de estudio relevante para todos los tipos de cáncer?
- Mecanismos de Interacción Sistema Nervioso-Cáncer
La Influencia del Sistema Nervioso en el Inicio y Crecimiento del Cáncer
La idea de que las neuronas podrían ser actores clave en la biología tumoral no es del todo nueva, con observaciones histológicas que datan de hace más de un siglo. Sin embargo, las herramientas de la neurociencia moderna han permitido dilucidar los complejos mecanismos detrás de esta interacción. Se ha demostrado que la actividad del sistema nervioso puede impulsar la iniciación, el crecimiento, la invasión y la diseminación metastásica de los tumores, tanto en el cerebro como en órganos periféricos.
Comunicación Directa: Sinapsis y Señalización Paracrina
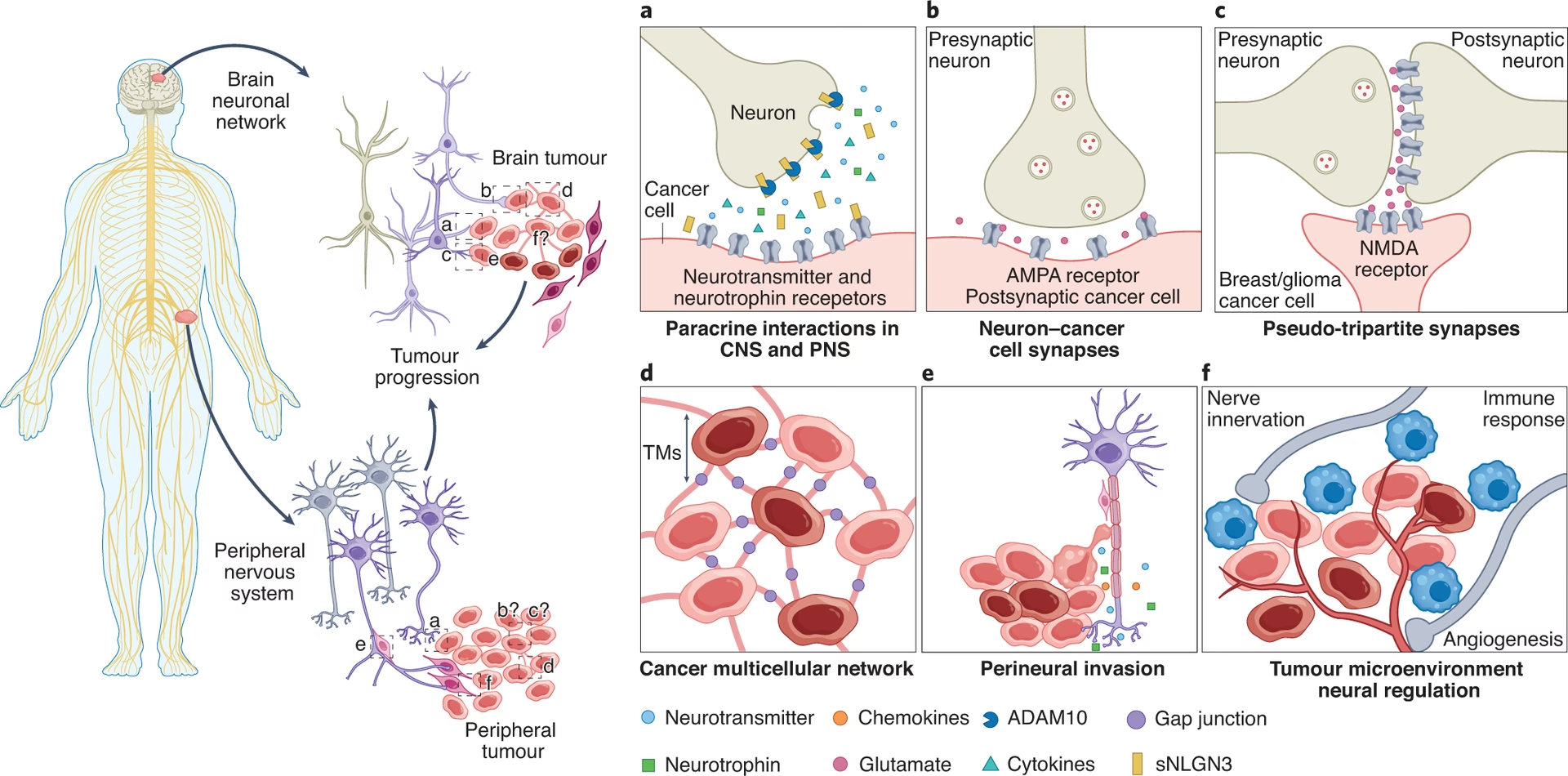
Una de las revelaciones más asombrosas es la existencia de una comunicación directa entre las neuronas y las células cancerosas, especialmente en tumores cerebrales como los gliomas. Las células de glioma pueden formar sinapsis funcionales con las neuronas, recibiendo entradas excitatorias mediadas principalmente por receptores AMPA (AMPAR). Esta actividad sináptica neuronal no solo despolariza las células de glioma, sino que también impulsa su proliferación e invasión. Fármacos antiepilépticos que bloquean los AMPAR, como el perampanel, han mostrado potencial para reducir el crecimiento del glioma en modelos preclínicos.
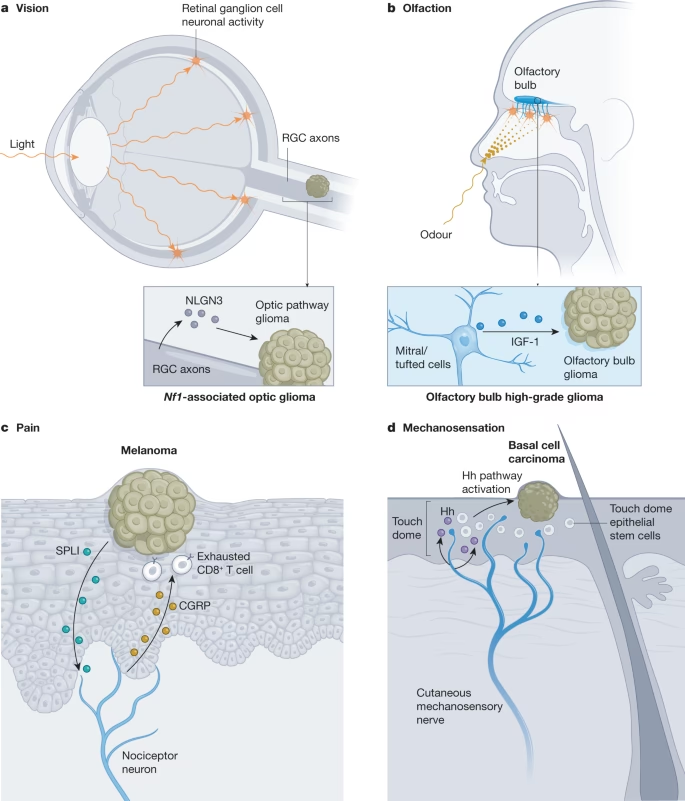
Además de las sinapsis directas, existe una señalización paracrina crucial. La actividad neuronal puede liberar factores como neuroligina-3 (NLGN3), BDNF (factor neurotrófico derivado del cerebro) o GRP78, que actúan sobre las células tumorales estimulando su crecimiento. Por ejemplo, la actividad neuronal dependiente de la experiencia visual puede impulsar la iniciación de gliomas ópticos a través de la secreción de NLGN3. Inhibir la enzima que libera NLGN3 (ADAM10) ha mostrado efectos prometedores en modelos de ratón.
Interacciones Indirectas y el Microambiente Tumoral
La influencia neural también se ejerce de manera indirecta, a través de su impacto en otras células del microambiente tumoral, como células inmunes y vasos sanguíneos. El sistema nervioso autónomo, con sus ramas simpática y parasimpática, inerva la mayoría de los órganos y puede modular el microambiente local. Por ejemplo, en cánceres periféricos como el de mama, ovario o próstata, la señalización adrenérgica (simpática) a menudo promueve el crecimiento tumoral y la metástasis, mientras que la señalización colinérgica (parasimpática) puede tener efectos variables, a veces promotores (cáncer gástrico) o inhibidores (cáncer de páncreas).
Los nervios sensoriales también participan, como se ve en los carcinomas de células basales, que requieren señales de nervios mecanosensoriales cutáneos para formarse, o en el cáncer de páncreas, donde la ablación de neuronas sensoriales ralentiza el crecimiento. La invasión perineural (PNI), donde las células cancerosas rodean o invaden los tractos nerviosos, es una manifestación histológica de esta interacción, asociada a menudo con un peor pronóstico en muchos cánceres periféricos (páncreas, próstata, mama).
Las células tumorales, a su vez, pueden secretar factores neurotróficos (como NGF, GDNF, ARTN) que no solo fomentan el crecimiento de los nervios (axonogénesis) y la inervación del tumor, sino que también actúan directamente sobre las células cancerosas promoviendo su supervivencia y crecimiento, creando un círculo vicioso.
El Cáncer Secuestra Mecanismos Neurobiológicos
Sorprendentemente, las células cancerosas, especialmente en el cerebro, parecen secuestrar y reutilizar mecanismos celulares y de red que normalmente están asociados con el neurodesarrollo y la plasticidad neural. Esto les confiere ventajas para el crecimiento, la invasión y la resistencia al tratamiento.
Microtúbulos Tumorales y Redes Funcionales
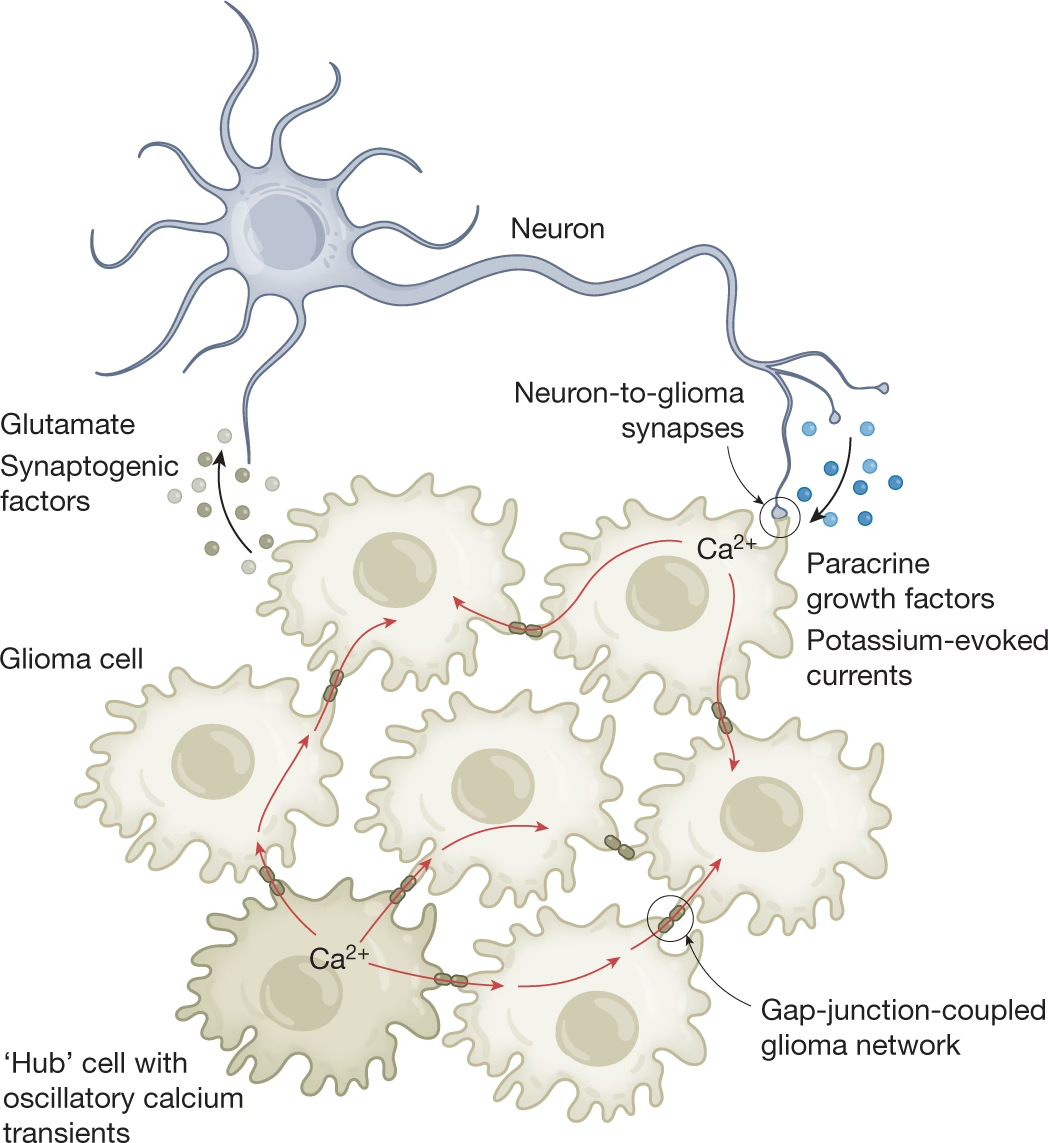
Las células de glioma pueden extender largas protuberancias membranosas similares a neuritas, llamadas Microtúbulos Tumorales (TMs). Los TMs permiten a las células escanear el microambiente cerebral, invadir y colonizar nuevas áreas. Lo más notable es que los TMs conectan células de glioma entre sí, a menudo a través de uniones gap (conexina 43), formando una red funcional multicelular. Esta red no solo facilita la comunicación intercelular (por ejemplo, ondas de calcio), sino que también confiere resistencia a terapias citotóxicas como la radioterapia y la quimioterapia estándar. Las células integradas en la red son más resilientes, mientras que las células menos conectadas parecen ser las principales impulsoras de la invasión.
Esta red tumoral muestra similitudes con las redes de astrocitos en el cerebro sano, que también usan uniones gap para la comunicación y el soporte metabólico. Incluso se ha observado que las células de glioma pueden conectarse a la red de astrocitos del cerebro huésped, lo que también contribuye a la supervivencia de las células cancerosas.
Además, algunas células de glioma actúan como "marcapasos" dentro de estas redes, generando actividad rítmica autónoma que impulsa la actividad de toda la red y es crucial para el crecimiento y la supervivencia del tumor. Este fenómeno recuerda a la actividad rítmica espontánea de células neuronales marcapasos durante el neurodesarrollo temprano.
Características Neurales Intrínsecas
Más allá de la formación de redes, las propias células cancerosas pueden exhibir características moleculares y funcionales típicamente neurales. Esto incluye la expresión de canales iónicos que regulan la excitabilidad o la migración, o la producción autocrina de neurotrofinas. Por ejemplo, cambios en la expresión de canales de potasio o del canal iónico NALCN se han relacionado con la progresión metastásica en varios cánceres.
En el síndrome de predisposición al cáncer NF1, los tumores benignos de vaina nerviosa (neurofibromas) están íntimamente asociados con los nervios. Se ha descubierto que las neuronas sensoriales de ganglios de la raíz dorsal mutantes para NF1 son hiperexcitables y secretan colágeno 1a2, que actúa como mitógeno para las células de Schwann deficientes en NF1 que dan origen a los tumores. Inhibir la excitabilidad neuronal o la producción de colágeno reduce el crecimiento tumoral en modelos de ratón.
Neuro-Inmuno-Oncología: La Triple Alianza
La interconexión entre el sistema nervioso, el sistema inmune y el cáncer representa una capa adicional de complejidad y oportunidad. El sistema nervioso regula potentemente las respuestas inmunes. Fibras aferentes (por ejemplo, del nervio vago) informan al cerebro sobre desafíos inmunes periféricos, y vías eferentes (vago, simpático) modulan la respuesta inmune, por ejemplo, suprimiendo la liberación de citoquinas proinflamatorias o controlando el tráfico de células inmunes.
En el contexto del cáncer, esta interacción triangular (neurona-célula inmune-célula cancerosa) es crítica. La señalización neural, como la adrenérgica (norepinefrina) a través de receptores beta2 (B2AR) en células inmunes, puede tener efectos inmunosupresores, limitando la inmunidad antitumoral y promoviendo la inflamación pro-tumoral. Los nervios sensoriales también pueden inducir agotamiento de las células T en tumores sólidos, un efecto que podría revertirse inhibiendo el neuropéptido CGRP.
Además, las células inmunes pueden usar moléculas de señalización neural. Los linfocitos B pueden sintetizar GABA, y en modelos de cáncer de colon, este GABA puede unirse a receptores en linfocitos T CD8+ para reducir la inmunidad antitumoral. La serotonina, secretada por plaquetas, puede aumentar la expresión de PD-L1 en células cancerosas, un mecanismo relevante para la respuesta a la inmunoterapia.
La Neuro-Inmuno-Oncología busca entender cómo la modulación neural podría mejorar las estrategias de inmunoterapia, por ejemplo, alterando el microambiente inmune tumoral o ralentizando el crecimiento tumoral para permitir que la respuesta inmune sea más efectiva.
El Impacto del Cáncer y sus Terapias en el Sistema Nervioso
La relación es bidireccional. Así como el sistema nervioso influye en el cáncer, el cáncer y, sobre todo, sus tratamientos tienen un impacto significativo en la función neural.
Neurotoxicidad Inducida por el Tratamiento
Una consecuencia común y debilitante de la quimioterapia y la radioterapia es la neurotoxicidad. Esto se manifiesta en dos formas principales:
- Disfunción Cognitiva: Conocida popularmente como "quimio-cerebro", afecta la atención, la memoria, la velocidad de procesamiento y las funciones ejecutivas. Se relaciona con daño a células madre neurales, neurogénesis hipocampal alterada, disrupción de la mielina y cambios en la conectividad sináptica.
- Neuropatía Periférica: Afecta los nervios periféricos, causando síntomas sensoriales (entumecimiento, hormigueo, dolor), motores (debilidad) y autonómicos (problemas digestivos, cardiovasculares).
Estos efectos adversos, aunque a menudo inevitables con las terapias actuales, impactan significativamente la calidad de vida de los pacientes. Irónicamente, las terapias dañan los mismos mecanismos neurales (plasticidad, regeneración, función de células madre) que el cáncer secuestra para crecer. Comprender esto podría llevar a terapias más específicas y menos tóxicas.
Efectos Directos del Cáncer
El propio cáncer también puede afectar el sistema nervioso. Tumores en órganos periféricos pueden alterar la función cerebral a distancia, impactando el sueño o el metabolismo. A nivel local, la interacción entre células tumorales y nervios periféricos contribuye al dolor asociado al cáncer, a menudo impulsando la hipersensibilidad y el crecimiento nervioso en la zona tumoral.
Hacia Terapias Basadas en la Neurociencia del Cáncer
El campo de la Neurociencia del Cáncer ofrece un gran potencial terapéutico. La idea es modular las interacciones neurales-tumorales para frenar el crecimiento, la invasión y la metástasis, e incluso mejorar la respuesta a otras terapias como la inmunoterapia.
Dianas Terapéuticas y Reutilización de Fármacos
Dado que el sistema nervioso es una fuente rica en dianas terapéuticas, y que ya existen numerosos fármacos aprobados para trastornos neurológicos o psiquiátricos, la reutilización de fármacos existentes es una vía prometedora para una rápida traslación clínica. Ejemplos incluyen:
- Inhibidores de AMPAR (ej. perampanel) para gliomas con sinapsis neuronales.
- Beta-bloqueantes para modular la señalización simpática en cánceres periféricos.
- Inhibidores de canales iónicos (ej. lamotrigina para HCN1) o factores específicos (ej. inhibidores de ADAM10) en tumores con características neurales o dependientes de actividad neuronal.
- Estrategias para desconectar las redes de células tumorales, como la inhibición de uniones gap (ej. meclofenamato).
La clave será identificar las dianas terapéuticas más relevantes para cada tipo de cáncer y etapa, y encontrar la ventana terapéutica adecuada para afectar selectivamente a las células tumorales sin causar neurotoxicidad inaceptable en el tejido neural sano. La denervación quirúrgica en algunos cánceres periféricos también es una opción terapéutica en estudio.
Ensayo Clínicos y Biomarcadores
La traslación de estos hallazgos a la clínica ya está en marcha con ensayos clínicos en fase temprana evaluando fármacos que modulan la interacción neural-tumoral. Para que estos ensayos tengan éxito, es crucial desarrollar biomarcadores que permitan:
- Identificar a los pacientes con tumores que dependen de la señalización neural.
- Evaluar si el fármaco está alcanzando su diana y modulando la interacción neural-tumoral deseada.
- Monitorizar los posibles efectos en el sistema nervioso del paciente.
Se necesitan nuevas tecnologías de imagen, electrofisiología y multi-ómicas (genómica, transcriptómica, proteómica) aplicadas a muestras tumorales y fluidos corporales (LCR, sangre) para caracterizar estas interacciones a múltiples escalas.
Terapias de Combinación
Es probable que las terapias dirigidas a la interacción neural-tumoral funcionen mejor en combinación con tratamientos estándar (quimioterapia, radioterapia) o con inmunoterapias. Por ejemplo, desconectar las redes tumorales podría sensibilizar las células a la quimioterapia, o modular el microambiente inmune vía nerviosa podría potenciar la inmunoterapia.
El Futuro de la Neurociencia del Cáncer
El campo de la Neurociencia del Cáncer está en auge. Las pruebas de la influencia, tanto directa como indirecta, del sistema nervioso en el cáncer son cada vez más sólidas y se extienden a un número creciente de tipos tumorales. La pregunta de si las interacciones sistema nervioso-cáncer se convertirán en un principio general de la patogénesis del cáncer parece cada vez más plausible.
Los desafíos son claros: necesitamos mapear con mayor detalle el "conectoma" neural-tumoral, comprender la heterogeneidad espacial y temporal de estas interacciones, y dilucidar completamente el papel de las células gliales del sistema nervioso (Schwann, astrocitos, microglia/macrófagos) en este proceso. Esto requiere una colaboración interdisciplinaria intensa entre neurocientíficos, oncólogos, inmunólogos, patólogos y desarrolladores de tecnología.
La innovación tecnológica en áreas como la microscopía avanzada, la electrofisiología de alta resolución y las técnicas multi-ómicas espaciales será fundamental para avanzar. Estas herramientas nos permitirán visualizar y cuantificar la actividad neural en tiempo real dentro de los tumores, analizar la comunicación sináptica y paracrina a nivel celular y subcelular, y correlacionar estos hallazgos funcionales con perfiles moleculares.
La promesa es inmensa. La Neurociencia del Cáncer no solo profundiza nuestra comprensión fundamental de la enfermedad, sino que también ofrece un nuevo pilar potencial para el tratamiento del cáncer, con el objetivo de frenar el crecimiento tumoral, prevenir la metástasis y, al mismo tiempo, preservar o restaurar la función neurológica y mejorar la calidad de vida de los pacientes. Al igual que la inmunología transformó la oncología, la neurociencia tiene el potencial de ser la próxima gran frontera en la lucha contra el cáncer.
Preguntas Frecuentes sobre Neurociencia y Cáncer
¿Qué es la Neurociencia del Cáncer?
Es un campo científico emergente que estudia la compleja interacción bidireccional entre el sistema nervioso (cerebro, médula espinal, nervios periféricos) y el cáncer. Investiga cómo la actividad neural y los nervios influyen en el inicio, crecimiento, invasión, metástasis y resistencia al tratamiento de los tumores, y cómo el cáncer afecta al sistema nervioso.
¿Cómo interactúan las neuronas con las células tumorales?
Las interacciones pueden ser directas, como la formación de sinapsis entre neuronas y células de glioma que transmiten señales eléctricas que estimulan el crecimiento tumoral. También hay comunicación paracrina, donde las neuronas o las células tumorales secretan moléculas (neurotransmisores, neurotrofinas) que afectan a las células vecinas. Indirectamente, el sistema nervioso influye en el microambiente tumoral, incluyendo células inmunes y vasos sanguíneos.
¿Pueden los medicamentos utilizados para tratar trastornos neurológicos ayudar a tratar el cáncer?
Es una posibilidad terapéutica clave en la Neurociencia del Cáncer. Muchos fármacos neurológicos o psiquiátricos modulan la señalización neural. Si se identifica que un tipo de cáncer depende de una vía de señalización neural específica (por ejemplo, receptores de neurotransmisores, canales iónicos), un medicamento ya aprobado que actúe sobre esa vía podría ser reutilizado como terapia contra el cáncer, a menudo en combinación con otros tratamientos.
¿Afecta el cáncer o su tratamiento a mi sistema nervioso?
Sí. El cáncer mismo puede afectar la función neurológica (por ejemplo, causando dolor, alterando el sueño o el metabolismo). Además, muchas terapias contra el cáncer, como la quimioterapia y la radioterapia, son neurotóxicas y pueden causar problemas cognitivos (quimio-cerebro) y daños a los nervios periféricos (neuropatía).
¿Es este campo de estudio relevante para todos los tipos de cáncer?
La investigación ha encontrado evidencia creciente de la influencia del sistema nervioso en una amplia gama de cánceres, incluyendo tumores cerebrales (gliomas) y cánceres periféricos (mama, próstata, páncreas, gástrico, etc.). Aunque los mecanismos específicos pueden variar entre tipos de cáncer y órganos, parece ser un principio general de la biología tumoral.
Mecanismos de Interacción Sistema Nervioso-Cáncer
| Tipo de Interacción | Descripción | Ejemplos (Cáncer) |
|---|---|---|
| Paracrina | Neuronas/nervios secretan moléculas (neurotransmisores, neurotrofinas, etc.) que afectan células tumorales o microambiente. | NLGN3, BDNF, GRP78 (gliomas), NGF, GDNF (periféricos). |
| Electroquímica/Sináptica | Comunicación directa (sinapsis) o indirecta vía actividad eléctrica neuronal, despolarización celular. | Sinapsis neurona-glioma (mediada por AMPAR), despolarización de células tumorales. |
| Vía Inmune | El sistema nervioso regula la respuesta inmune, que a su vez influye en el tumor. | Sistema nervioso autónomo modulando células inmunes, neuropéptidos (CGRP) afectando células T. |
| Vía del Microambiente | Efectos neurales en vasos sanguíneos, estroma, suministro metabólico. | Regulación del flujo sanguíneo (neurovascular coupling), soporte metabólico tumoral, inervación de vasos. |
| Intrínseca Tumoral | Células tumorales adoptan características neurales (morfología, redes, señalización). | Microtúbulos tumorales, redes celulares (uniones gap), actividad rítmica intrínseca. |
En conclusión, la Neurociencia del Cáncer representa una frontera emocionante en la investigación oncológica. Al desentrañar las intrincadas conversaciones entre las células tumorales y el sistema nervioso, estamos abriendo la puerta a nuevas estrategias terapéuticas que podrían mejorar drásticamente los resultados para los pacientes con cáncer.
Si quieres conocer otros artículos parecidos a Neurociencia y Cáncer: La Conexión Inesperada puedes visitar la categoría Neurociencia.