El desarrollo del sistema nervioso central es uno de los procesos más complejos y finamente orquestados en la embriogénesis de los vertebrados. Un evento fundamental en esta etapa es la neurulación, donde la placa neural, una capa engrosada del ectodermo, se pliega y se cierra para formar el tubo neural, el precursor del cerebro y la médula espinal. Si bien el proceso general comparte similitudes entre especies, existen variaciones significativas, especialmente en la región anterior que dará origen al cerebro. El pez cebra (Danio rerio) se ha convertido en un modelo excepcionalmente valioso para estudiar estos eventos debido a su transparencia embrionaria y rápido desarrollo externo.
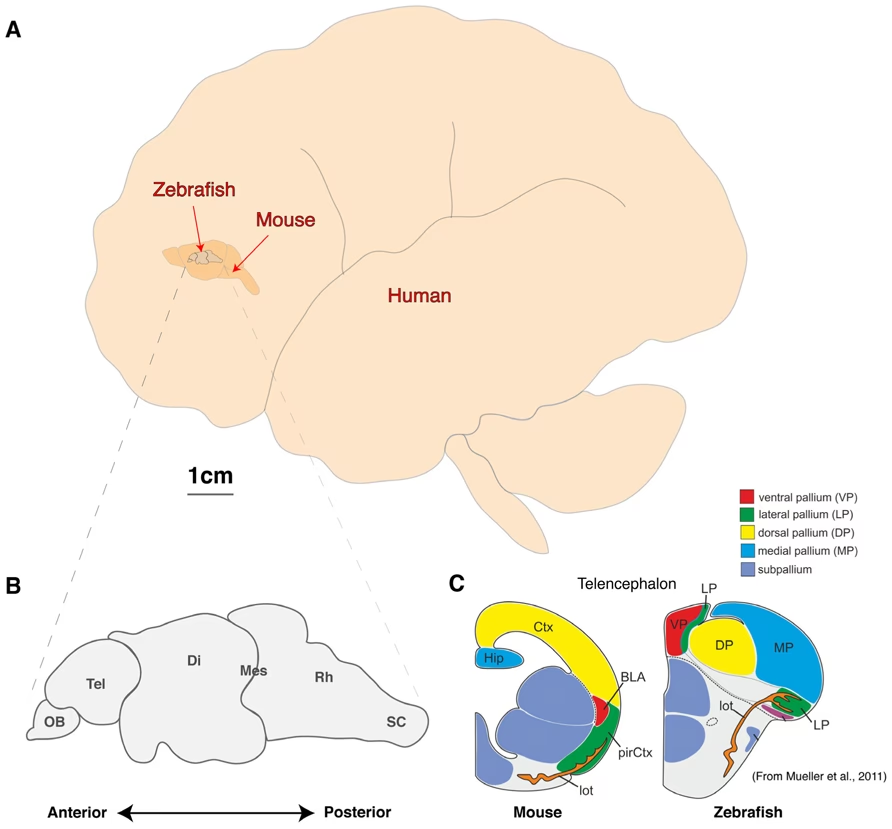
La formación del tubo neural en el pez cebra, particularmente en su región anterior que forma el prosencéfalo (cerebro anterior), presenta características distintivas en comparación con otros modelos como los mamíferos. Una de estas particularidades es la epitelialización precoz de la Placa Neural Anterior (ANP, por sus siglas en inglés). Esta epitelialización, que ocurre antes que en regiones más posteriores, parece estar asociada con el proceso de plegamiento de esta estructura.
- Morfología y Destino de la Placa Neural Anterior (ANP)
- Puntos de Bisagra y Pliegues Neurales: Estructuras Transitorias
- Cambios en la Forma Celular: La Morfogénesis a Nivel Celular
- Dinámica de la Fusión de los Pliegues Neurales
- Sincronización de Eventos y Distinciones Moleculares
- El Papel Crucial de la Miosina No Muscular II
- El Pez Cebra como Modelo para Estudiar el Desarrollo Neural
Morfología y Destino de la Placa Neural Anterior (ANP)
La morfología de la ANP en el pez cebra evoluciona rápidamente durante las primeras etapas del desarrollo embrionario. Inicialmente, en estadios de 2 a 5 somitas, la ANP presenta una forma de 'V' característica, marcada por un surco neural medial. Este surco está flanqueado por los bordes laterales elevados de la ANP, que recuerdan a los pliegues neurales observados en otras especies. Sin embargo, para el estadio de 7 somitas, el surco medial ya no es visible. En su lugar, los bordes elevados de la ANP se han fusionado medialmente, formando un abultamiento dorsal. Esta secuencia de eventos sugiere que la ANP se pliega en la línea media, y este plegamiento se correlaciona directamente con la elevación de sus bordes laterales.
El destino de las diferentes regiones de la ANP está bien definido. La parte central de la ANP está destinada a formar los ojos, mientras que sus bordes laterales darán origen al telencéfalo, una estructura que se posicionará dorsalmente en el cerebro. La región más ventral de la ANP, por otro lado, se diferenciará en el hipotálamo. Las células precursoras del telencéfalo, identificadas mediante marcadores como Emx3, se localizan en los bordes laterales de la ANP. Estas células se elevan, migran sobre el campo ocular y finalmente se fusionan en la línea media alrededor del estadio de 7 somitas para formar el telencéfalo. Notablemente, para este mismo estadio de 7 somitas, la ANP, que inicialmente es un tejido multicapa con un núcleo superficial mesenquimal y una capa profunda marginal, se resuelve en un neuroectodermo con una única capa celular epitelial.
Puntos de Bisagra y Pliegues Neurales: Estructuras Transitorias
La neurulación en muchos vertebrados involucra la formación de puntos de bisagra (regiones de células que se constriñen apicalmente) y pliegues neurales que se elevan y convergen. En el pez cebra anterior, se ha observado la presencia de estructuras que parecen ser los equivalentes funcionales de estos puntos, aunque con algunas particularidades.
Se identifican puntos de bisagra transitorios en la ANP. Un punto de bisagra medial (MHP) se forma en la región medial/superficial, mientras que dos puntos de bisagra dorsolaterales (DLHPs) aparecen en cúmulos celulares en la capa profunda marginal. Estos puntos de bisagra se caracterizan por la constricción apical de las células y el enriquecimiento de actina filamentosa (F-actina) en su polo apical. A diferencia de los amniotas, donde el MHP se forma en la capa profunda, en el pez cebra, el MHP se forma en la capa superficial, posicionándose más dorsalmente.
Los bordes laterales de la ANP, que se elevan, tienen una organización bilaminar en el estadio de 5 somitas. Consisten en una capa de células neuroectodérmicas cubierta por una capa de ectodermo no neural. Esta estructura bilaminar es indicativa de un pliegue neural. Las células neuroectodérmicas de la punta del pliegue neural dan origen al telencéfalo. Estos pliegues neurales, al igual que los puntos de bisagra, son transitorios y ya no se observan claramente en embriones de 7 somitas, momento en el que sus puntas han convergido y fusionado medialmente para formar el telencéfalo.
Cambios en la Forma Celular: La Morfogénesis a Nivel Celular
Los cambios en la forma de las células son impulsores clave de los movimientos tisulares durante la morfogénesis. En la ANP del pez cebra, se observan cambios celulares específicos tanto en los puntos de bisagra como en los pliegues neurales.
En la capa profunda dorsolateral, las células que forman los DLHPs experimentan constricción apical y expansión basal. Estos cambios de forma les confieren una apariencia de cuña y parecen iniciar el abultamiento de las vesículas ópticas (los precursores de los ojos). Las células neuroectodérmicas dentro de los pliegues neurales, por su parte, se alargan y sus polos basales se constriñen, dando la impresión de que se abren en abanico desde un punto focal en la membrana basal. Sus membranas plasmáticas presentan actividad protrusiva.
Las células del MHP, localizadas en la capa superficial medial, también experimentan constricción apical. Entre los estadios de 2 y 5 somitas, estas células se vuelven más densamente empaquetadas, se orientan hacia la línea media y se desplazan ventralmente. Adquieren una forma de cuña con una constricción apical pronunciada y se alargan significativamente. Curiosamente, la posición del núcleo dentro de estas células no cambia drásticamente, lo que sugiere que no contribuye a su acuñamiento como se observa en algunos otros modelos.
La constricción apical de las células del MHP no es un proceso lineal sino que ocurre mediante constricciones oscilatorias. Las áreas de superficie apical de estas células se reducen progresivamente a través de ciclos de constricción y re-expansión, con una amplitud decreciente. Este comportamiento oscilatorio parece proceder en una dirección posterior a anterior.
Dinámica de la Fusión de los Pliegues Neurales
La fusión de los pliegues neurales es el paso final en la formación del tubo neural. En el pez cebra anterior, este proceso también muestra una dinámica particular.
Los pliegues neurales anteriores forman un arco con el vértice posicionado anteriormente. La fusión de estos pliegues no ocurre simultáneamente a lo largo de todo el arco. Se inicia cerca del vértice del arco y avanza en dirección anterior a posterior por una distancia inicial. Este punto de inicio se define como el punto de cierre uno (C1). Posteriormente, se forma un segundo punto de cierre (C2) más caudalmente. Estos dos puntos de cierre delimitan una abertura transitoria en forma de ojo.
El proceso de fusión posterior se asemeja a una cremallera que avanza desde ambos puntos de cierre (C1 y C2) hacia el centro de la abertura en forma de ojo. A nivel celular, las células neuroectodérmicas de los pliegues neurales utilizan prolongaciones dinámicas llamadas filopodios para establecer contacto con las células del pliegue contralateral a través de la línea media. Además, los cuerpos celulares pueden extenderse más allá de la línea media, sugiriendo un proceso de interdigitación entre las células de los pliegues opuestos antes de que la línea media se defina claramente tras la epitelialización.
Sincronización de Eventos y Distinciones Moleculares
Un aspecto interesante del desarrollo de la ANP en el pez cebra es la sincronización de los eventos morfogenéticos clave. A diferencia de los amniotas, donde la formación del MHP generalmente precede a la de los DLHPs y la elevación de los pliegues, en el pez cebra, los cambios en el ángulo del surco neural (reflejando la constricción del MHP), el ángulo de la vesícula óptica (reflejando la constricción/elongación de los DLHPs) y el ángulo basal del pliegue neural (reflejando el plegamiento epitelial) ocurren concurrentemente y se correlacionan temporalmente con la elevación y convergencia de los pliegues neurales. Las tasas de estos movimientos (elevación y convergencia de pliegues, cambios en ángulos) son relativamente constantes a lo largo del tiempo.
A nivel molecular, tanto el MHP como los DLHPs muestran signos de epitelialización temprana y acumulan marcadores de polaridad apical como Pard3-GFP, ZO-1 y N-cadherina, que colocalizan con F-actina en el polo apical. Sin embargo, existe una distinción molecular importante: la acumulación de miosina de cadena ligera fosforilada II (P-MLC), un componente clave de la maquinaria contráctil de actomiosina, se observa apicalmente en las células del MHP donde se superpone con F-actina, pero no se enriquece apicalmente en los DLHPs. La P-MLC sí se acumula en la corteza celular de las células neuroectodérmicas de los pliegues neurales y en la superficie basal de la capa envolvente (EVL).
El Papel Crucial de la Miosina No Muscular II
La maquinaria contráctil de actomiosina, impulsada por la miosina no muscular II (NMII), es fundamental para la constricción apical en muchos procesos morfogenéticos. Los estudios en pez cebra han confirmado su papel crucial en la formación del MHP y la convergencia de los pliegues neurales anteriores.
El bloqueo de la NMII, ya sea mediante tratamiento farmacológico con blebbistatina o el uso de morfolinos para silenciar NMIIb, tiene efectos significativos en la ANP. En embriones tratados, las células del MHP no se constriñen apicalmente ni se alargan adecuadamente, adoptando una forma más redondeada. Esto se correlaciona con la ausencia de un MHP claramente definido. En contraste, aunque la longitud de las células de los DLHPs también se reduce con el tratamiento, estas células conservan su forma de cuña y su ratio apical-basal es consistente con la constricción apical. Esta diferencia en la respuesta a la inhibición de NMII es consistente con la observación de que la P-MLC se acumula apicalmente en el MHP pero no en los DLHPs.
A nivel tisular, la inhibición de NMII altera la convergencia de los pliegues neurales anteriores. Los embriones tratados con blebbistatina muestran un dominio telencefálico significativamente más ancho en comparación con los controles, lo que indica un fallo en la fusión completa de los pliegues. Esto subraya que la contractilidad de la miosina es esencial para la correcta neurulación anterior en el pez cebra, y la incapacidad de las células del MHP para constreñirse apicalmente probablemente contribuye de manera importante a este fenotipo.
El Pez Cebra como Modelo para Estudiar el Desarrollo Neural
El pez cebra es un gnatostomado (vertebrado con mandíbulas) que pertenece al grupo de los teleósteos. Evolutivamente, se separó del linaje que condujo a los mamíferos hace unos 350 millones de años, experimentando una duplicación del genoma completo hace unos 200 millones de años que contribuyó a su diversificación. Aunque comparte muchas características generales con otros vertebrados, como la organización básica del sistema nervioso y los órganos sensoriales, también posee rasgos derivados únicos (como el aparato de Weber para la audición). Es importante reconocer que el pez cebra no es un vertebrado primitivo, sino que ha evolucionado por separado y presenta tanto características conservadas como novedades propias, al igual que otros modelos como Xenopus o el ratón.
A pesar de estas diferencias evolutivas, muchos de los mecanismos fundamentales del desarrollo neural, incluida la neurulación, están conservados. Las particularidades observadas en la neurulación anterior del pez cebra, como la epitelialización precoz, la formación de puntos de bisagra transitorios con localizaciones y propiedades moleculares ligeramente diferentes, y la dinámica específica de la fusión de los pliegues, lo convierten en un modelo complementario valioso. Permite identificar principios generales de la morfogénesis neural y, al mismo tiempo, explorar cómo las variaciones en estos mecanismos básicos pueden conducir a la diversidad de formas cerebrales observadas en los vertebrados.
Tabla Comparativa: Neurulación Anterior (ANP)
| Característica | Pez Cebra (ANP) | Amniotas (Prosencéfalo) |
|---|---|---|
| Epitelialización | Precoz en la ANP | Generalmente ocurre más tarde |
| Puntos de Bisagra Medial (MHP) | Superficial, más dorsal | Profundo, más ventral |
| Puntos de Bisagra Dorsolaterales (DLHPs) | En capa profunda, no enriquece P-MLC apical | Presentes, enriquecen P-MLC apical |
| Sincronización de Eventos | MHP, DLHP, plegamiento NF concurrentes | MHP precede a DLHPs y elevación NF |
| Fusión de Pliegues Neurales | Iniciada en múltiples puntos de cierre (C1, C2), proceso de cremallera | Varía, a menudo con puntos de cierre específicos |
| Papel de la Miosina II | Esencial para MHP y convergencia NF | Esencial para constricción apical y cierre NT |
Preguntas Frecuentes sobre la Neurulación en Pez Cebra
¿Qué es la neurulación?
La neurulación es el proceso temprano en el desarrollo embrionario de los vertebrados en el que la placa neural, una región especializada del ectodermo, se pliega y se cierra para formar el tubo neural, el precursor del sistema nervioso central.
¿Qué son los somitas y por qué se usan como referencia?
Los somitas son bloques segmentados de mesodermo que se forman a lo largo del eje anteroposterior del embrión durante el desarrollo temprano. Su número aumenta de manera secuencial y predecible, lo que los convierte en un marcador temporal conveniente y preciso para seguir las etapas del desarrollo embrionario en especies como el pez cebra.
¿Qué son los puntos de bisagra?
Los puntos de bisagra son regiones del neuroectodermo donde las células experimentan cambios de forma, típicamente constricción apical y expansión basal, adquiriendo una forma de cuña. Estos cambios celulares inducen el plegamiento del tejido y son esenciales para dar forma al tubo neural.
¿Qué son los pliegues neurales?
Los pliegues neurales son los bordes elevados de la placa neural que se forman durante la neurulación. Se elevan, se mueven hacia la línea media dorsal y finalmente se fusionan para cerrar el tubo neural.
¿Cómo se diferencia la neurulación anterior del pez cebra de la de los mamíferos?
Aunque los principios generales son similares, la neurulación anterior del pez cebra presenta diferencias como la epitelialización precoz de la ANP, la localización superficial del MHP, la ausencia de enriquecimiento apical de P-MLC en los DLHPs y una sincronización concurrente de los eventos clave de plegamiento y convergencia, a diferencia de la secuencia más escalonada observada en mamíferos. Además, la dinámica de fusión de los pliegues neurales con múltiples puntos de cierre y un proceso de cremallera es una particularidad notoria.
En conclusión, el estudio detallado de la neurulación anterior en el pez cebra revela un proceso altamente dinámico que involucra complejos cambios en la forma celular, la formación transitoria de puntos de bisagra y pliegues neurales, y la acción coordinada de la maquinaria molecular, especialmente la miosina. Las particularidades de este proceso en el pez cebra, en comparación con otros vertebrados, no solo enriquecen nuestra comprensión de la diversidad evolutiva del desarrollo neural, sino que también destacan la conservación de mecanismos moleculares y celulares fundamentales. El pez cebra continúa siendo una poderosa herramienta para desentrañar los intrincados pasos que llevan a la formación del cerebro y para comprender las bases del desarrollo neurológico y sus posibles alteraciones.
Si quieres conocer otros artículos parecidos a Neurulación en el Pez Cebra: Placa Neural Anterior puedes visitar la categoría Neurociencia.